Слайд 2Биосферное значение фотосинтеза
Обеспечение постоянства содержания СО2 в воздухе.
Препятствие
развитию парникового эффекта.
Накопление кислорода в атмосфере. Ежегодно растения и
другие фотосинтезирующие организмы поставляют в атмосферу примерно 120 млрд. тонн кислорода.
Озоновый экран.
Накопление органической массы.
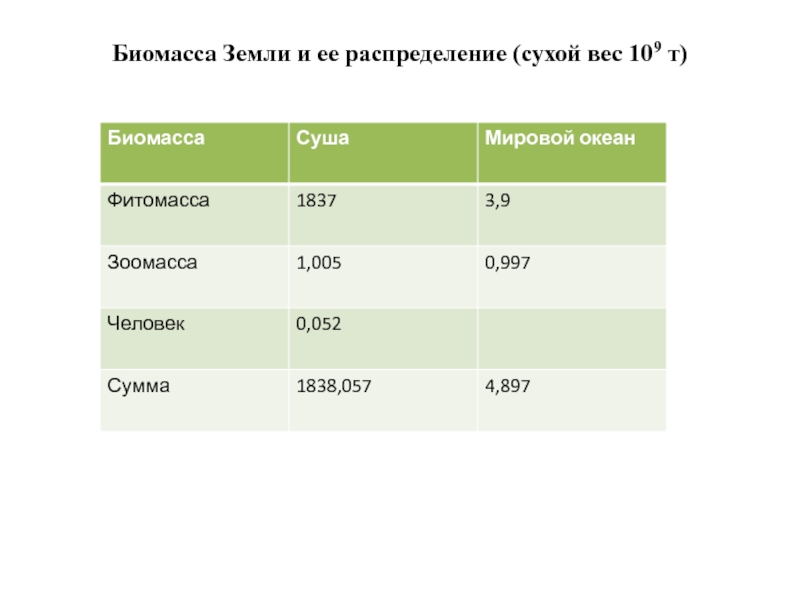
Слайд 3Биомасса Земли и ее распределение (сухой вес 109 т)
Слайд 5История развития представлений о фотосинтезе
XVII в. фламандский врач Ван Гельмонт
- материал, из которого образовалось дерево произошел из воды.
1777
г. английский ботаник Стивен Хейлс - в качестве питательного вещества, необходимого для роста, растения используют главным образом воздух;
1770-1780-е гг - первые опыты по фотосинтезу английский химик Джозеф Пристли - растения выделяют кислород, который необходим для дыхания и горения.
Слайд 6Голландский врач Ингенхауз обнаружил, что растения окисляют кислород лишь на солнечном
свету и что только их зеленые части обеспечивают выделение кислорода.
1817 г. французские химики, П. Ж. Пельтье и Ж. Кавенту, выделили из листьев зеленое вещество и назвали его хлорофиллом.
Разделить пигменты и изучить их по отдельности удалось М. С. Цвету с помощью созданного им метода хроматографии.
1845 г. немецкий физик Роберт Майер - зеленые растения преобразуют энергию, солнечного света в химическую энергию.
1877 г. В. Пфеффер назвал этот процесс фотосинтезом.
Слайд 7К середине 19 в. было установлено, что фотосинтез является процессом,
как бы обратным дыхательному.
Французский ученый Жан Батист Буссенго (1802-1887)
- в процессе фотосинтеза происходит выделение кислорода из углекислого газа.
К. А. Тимирязев – изучение спектров поглощения хлорофилла.
Корнелис ван Ниль - окислительно-восстановительная сущность и общее уравнение фотосинтеза.
Это означало что кислород в фотосинтезе образуется полностью из воды, что экспериментально подтвердил в 1941 А. П. Виноградов в опытах с изотопной меткой.
Слайд 8 1941 г. - американский биохимик Мелвин Калвин - процесс
фотосинтеза заключается в фотолизе молекул воды, в результате чего образуются
кислород, выделяющийся в атмосферу, и водород, идущий на восстановление диоксида углерода до органических веществ.
1961 г. Нобелевская премия по химии.
В 1937 г. Роберт Хилл установил что процесс окисления воды (и выделения кислорода), а также ассимиляции CO2 можно разобщить.
В 1954—1958 Д. Арнон - механизм световых стадий фотосинтеза
Слайд 10Хлоропласты – органеллы фотосинтеза
Слайд 11Химический состав хлоропластов (на сухую массу):
белок — 35—55 %;
липиды — 20—30 %;
углеводы — 10 %;
РНК —
2—3 %;
ДНК — до 0,5 %;
хлорофиллы — 9 %;
каротиноиды — 4,5 %.
Слайд 14Схема взаимопревращения
пластид (по Р.Г. Херрманну)
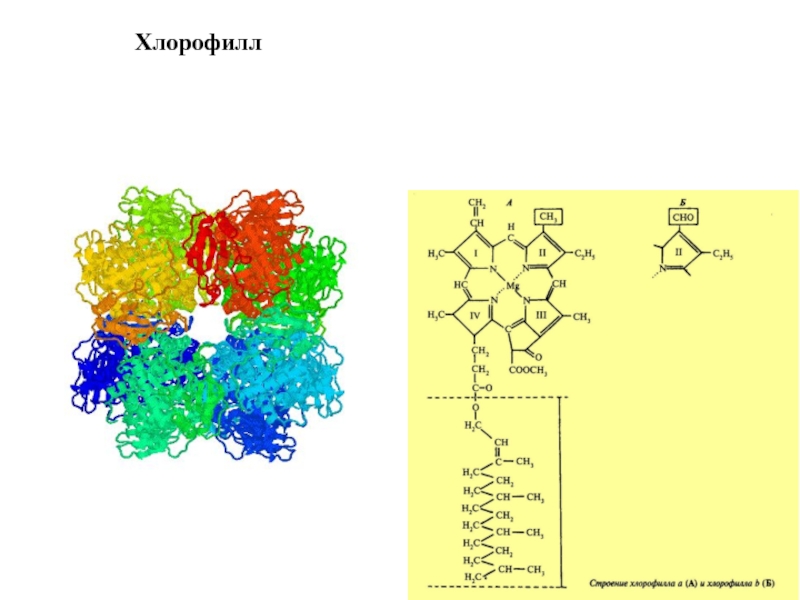
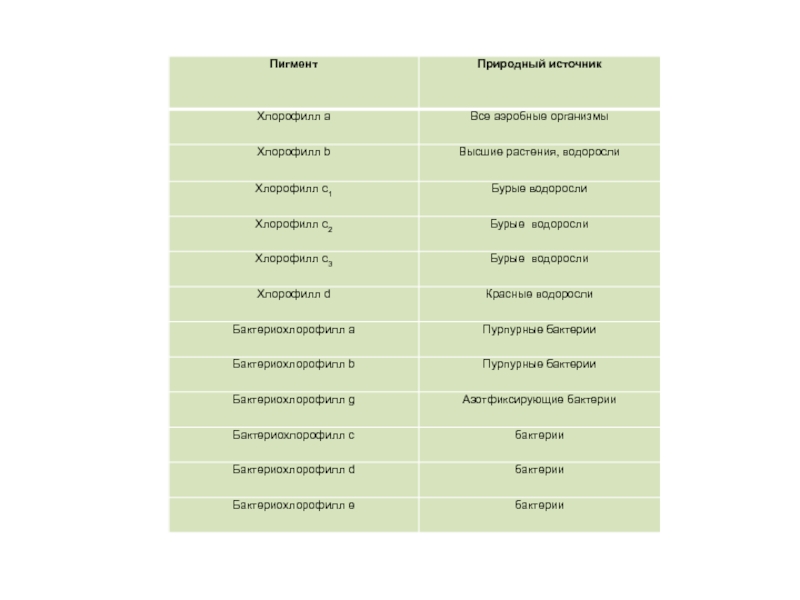
Слайд 16Основные классы фотосинтетических пигментов
Хлорофиллы
Каротиноиды
Фикобилины
Слайд 20 Каротиноиды -
полиизопреноиды
Виды: каротины (ненасыщенные углеводороды) – оранжевые, красные
ксантофиллы (содержат кислород)
– желтые.
Функции:
Антенная
Защитная
Фотопротекторная (защита от фотоокисления)
Слайд 21Фикобилины - открытые тетрапиррольные структуры
Цианеи, красные водоросли
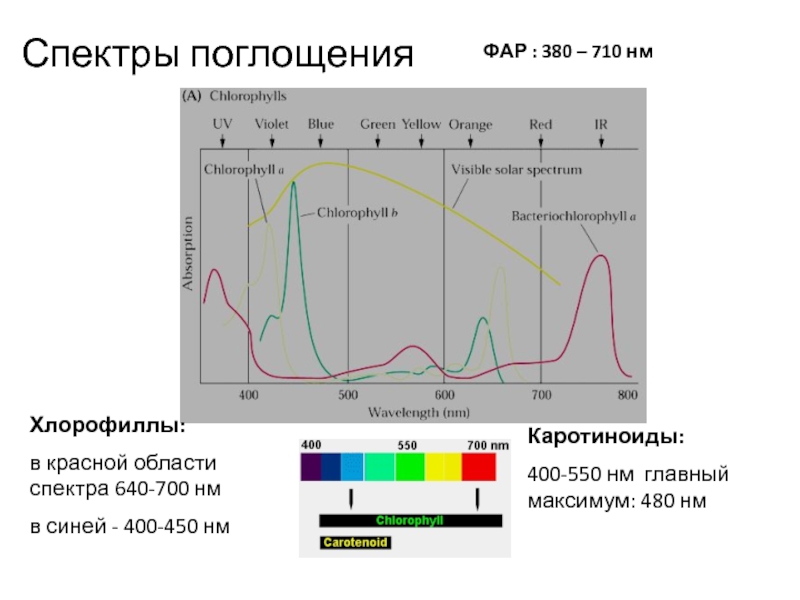
Слайд 22Спектры поглощения
ФАР : 380 – 710 нм
Каротиноиды:
400-550 нм главный
максимум: 480 нм
Хлорофиллы:
в красной области спектра 640-700 нм
в
синей - 400-450 нм
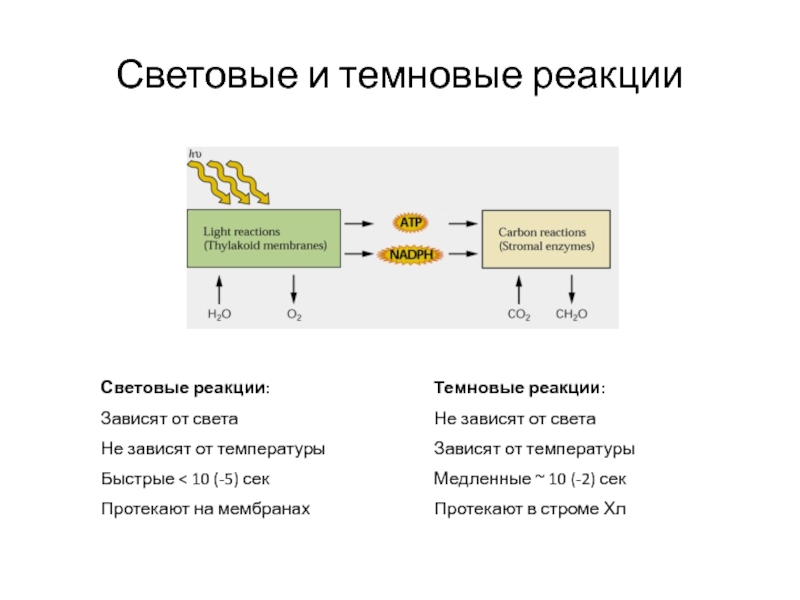
Слайд 23Световые и темновые реакции
Световые реакции:
Зависят от света
Не зависят от температуры
Быстрые
< 10 (-5) сек
Протекают на мембранах
Темновые реакции:
Не зависят от света
Зависят
от температуры
Медленные ~ 10 (-2) сек
Протекают в строме Хл
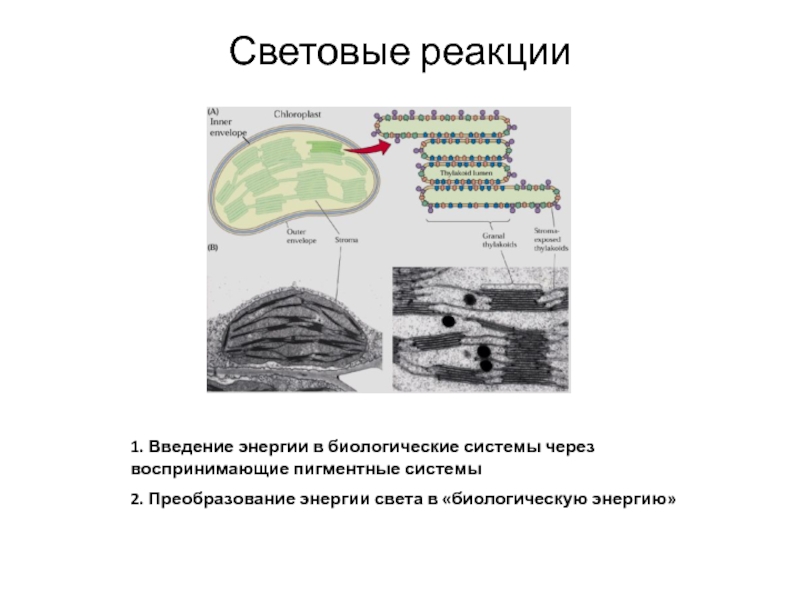
Слайд 24Световые реакции
1. Введение энергии в биологические системы через воспринимающие пигментные
системы
2. Преобразование энергии света в «биологическую энергию»
Слайд 25Хлорофилл способен к окислительно-восстановительным превращениям «реакция Красновского»
1 – флуоресценция
2 –
миграция энергии
3 – химическая энергия
4 - фосфоресценция
S*1
S 0
430
680
T
1
2 3
4 3
S*2
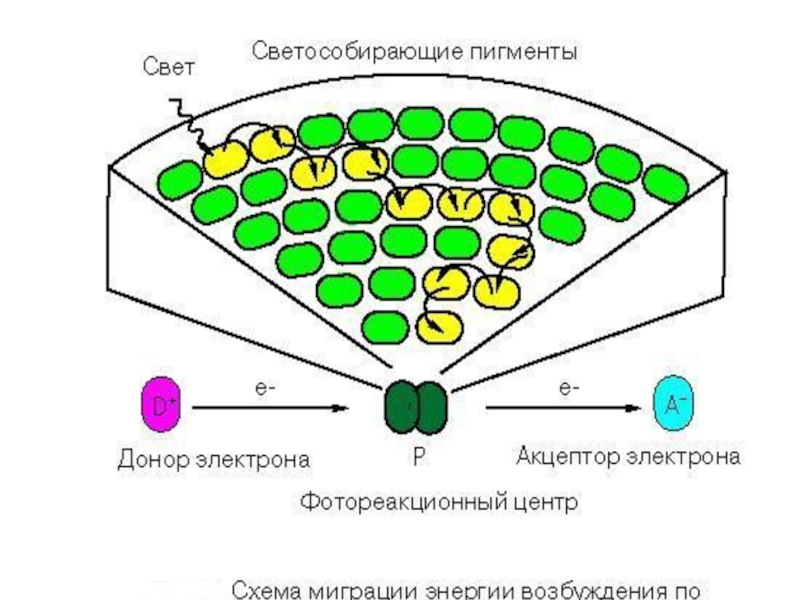
Слайд 26 Фотосистема (ФС):
антенный комплекс (светособирающий комплекс);
фотохимический реакционный центр
– хлорофилл-белковый комплекс (димер Хл а 680 или 700);
переносчики
электронов.
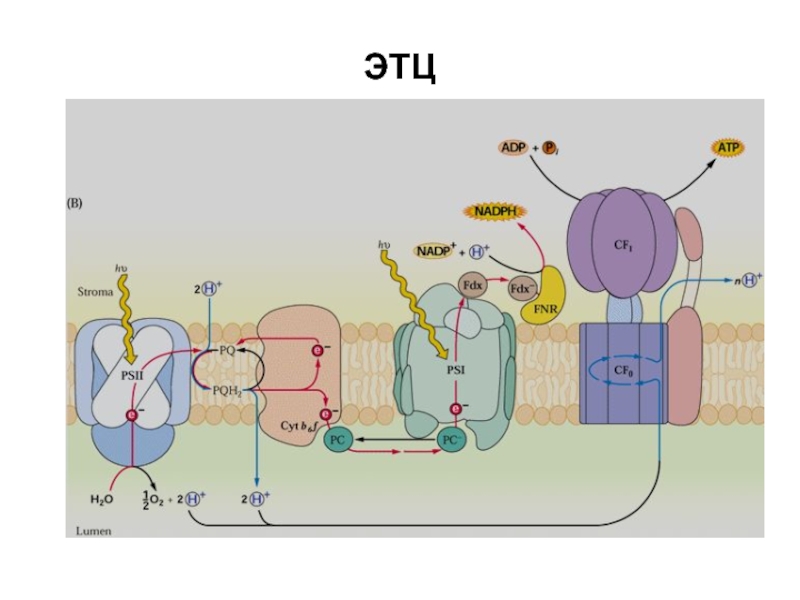
Хл а2 Хл а2+. + е-
ФС I: донор е – пластоцианин, акцептор – филлохинон;
ФС II : донор е – водорасщепляющий комплекс, акцептор – феофитин
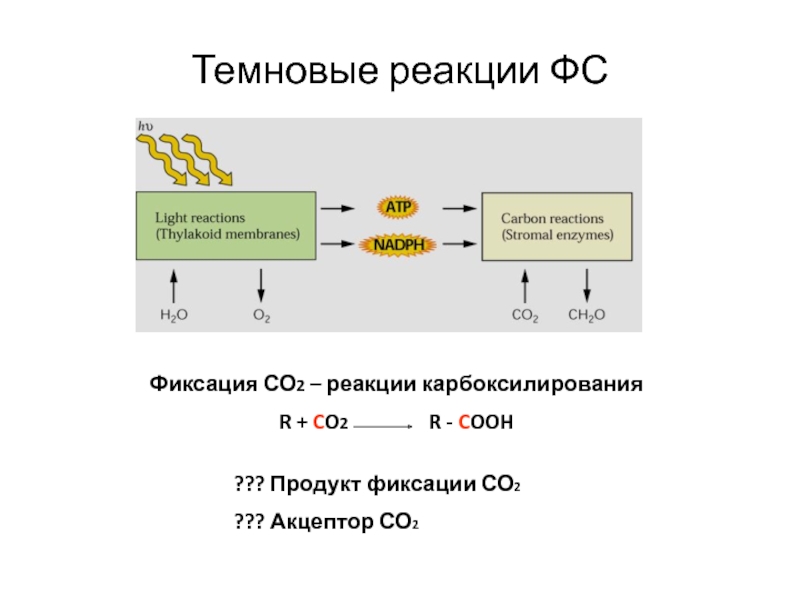
Слайд 32Темновые реакции ФС
Фиксация СО2 – реакции карбоксилирования
R + CO2
R - COOH
??? Продукт
фиксации СО2
??? Акцептор СО2
Слайд 33Лоуренсовская лаборатория (Калифорния, США)
1946 – 1956
Мелвин Кальвин
Объект: Chlorella
Методы:
С(14), P(32),
Двумерная
хроматография
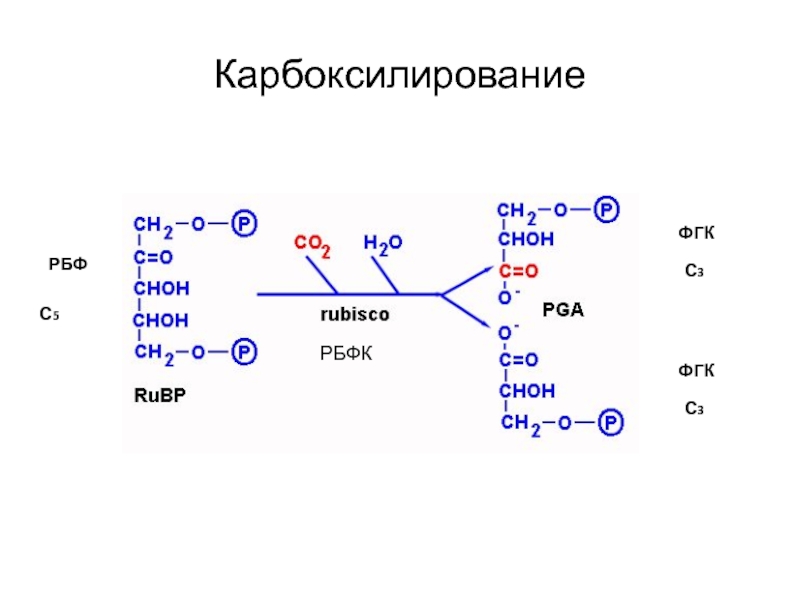
Слайд 34Карбоксилирование
ФГК
РБФ
ФГК
С5
С3
С3
РБФК
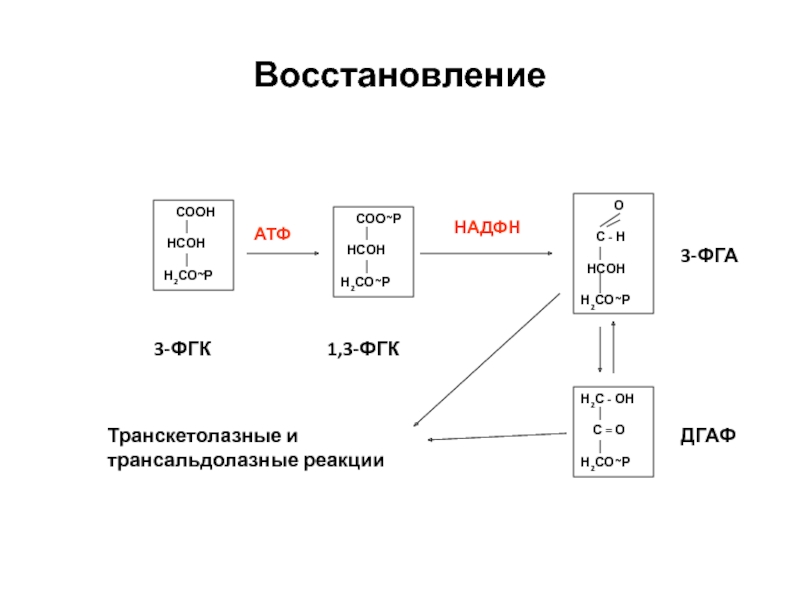
Слайд 35Восстановление
СООН
НСОН
Н2СОР
СООР
НСОН
Н2СОР
О
С - Н
НСОН
Н2СОР
АТФ
НАДФН
Н2С - ОН
С = О
Н2СОР
3-ФГК
1,3-ФГК
3-ФГА
ДГАФ
Транскетолазные и трансальдолазные реакции
С - Н
НСОН
Н2СОР
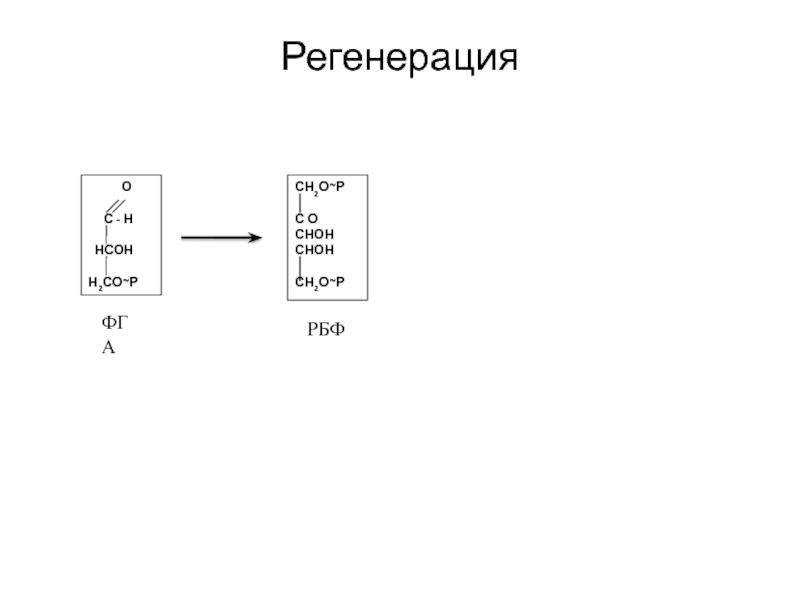
ФГА
СН2ОР
С
О
СНОН
СНОН
СН2ОР
РБФ
Слайд 38РБФК (Рубиско)
Optimum pH = 7,8 – 8,0 (рН стромы на
свету)
Субстраты: СО2 и РБФ
Регуляторный центр: E - CO2
– Mg
Зависит от доступности АТФ
Аллостерическая регуляция (+Фр6Ф, -Фр1,6Ф)
Зависит от доступности СО2
Зависит от концентрации О2 (фотодыхание)
Регуляторная роль света (тиоредоксин, РБФК активаза, экспрессия гена малой субьединицы через фитохром)
Слайд 39Цикл Хэтча – Слэка - Карпилова
Незговорова Л.А. 1956 – 1957
Карпилов
Ю.С. (кукуруза) 1960
Тарчевский И.А. 1963
М.Д. Хэтч и К.Р. Слэк (сах.
Тростник) 1966
Продукт фиксации
С4 – малат (ЩУК), аспартат
Акцептор
С3 – ФЕП
Слайд 42С4 растения различаются по способам декарбоксилирования
Карбоксилирование у всех одинаково: в
цитозоле клеток мезофилла
ФЕПК - фосфоенолпируват карбоксилаза
Пути декарбоксилирования
1. НАД-малатдегидрогеназный
2. НАДФ-маликэнзимный
3. ФЕП-карбоксикиназный
Слайд 43ФЕПК
Локализована в цитозоле кл. мезофилла
Субстрат НСО3
Оптимум рН = 8
Не
ингибируется О2
Аллостерическая регуляция (ЩУК, малат)
Фоторегуляция: активация светом ФЕПК-киназы
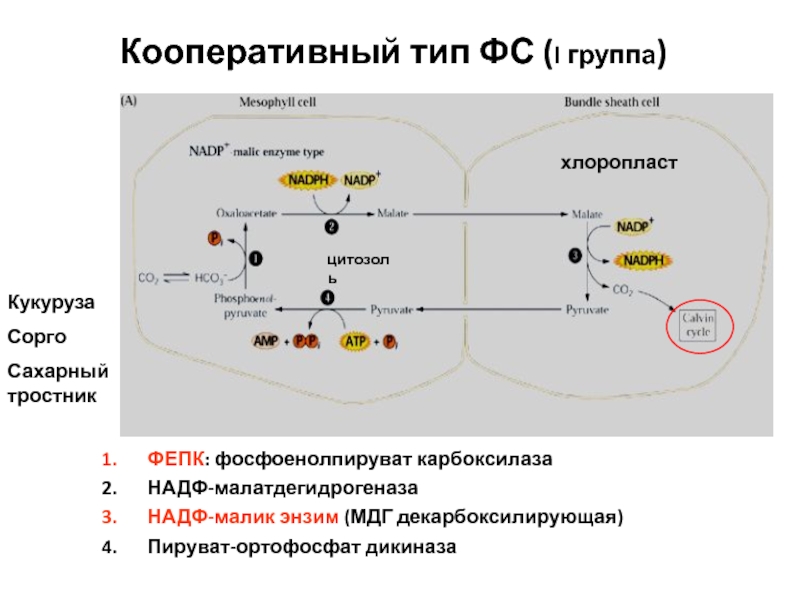
Слайд 44Кооперативный тип ФС (I группа)
ФЕПК: фосфоенолпируват карбоксилаза
НАДФ-малатдегидрогеназа
НАДФ-малик энзим (МДГ
декарбоксилирующая)
Пируват-ортофосфат дикиназа
Кукуруза
Сорго
Сахарный тростник
хлоропласт
цитозоль
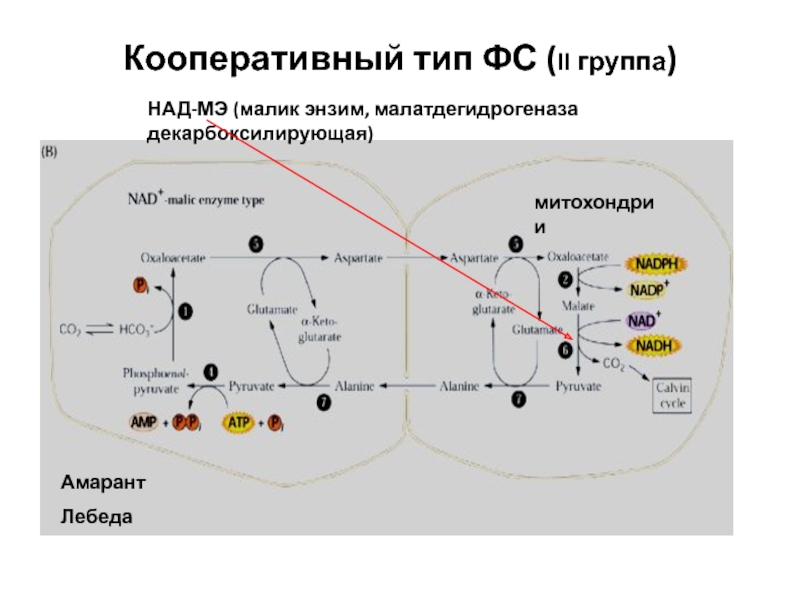
Слайд 45Кооперативный тип ФС (II группа)
Амарант
Лебеда
митохондрии
НАД-МЭ (малик энзим, малатдегидрогеназа декарбоксилирующая)
Слайд 46Кооперативный тип ФС (III группа)
Просо
хлорис
ФЕПКК: фосфоенолпируват карбоксикиназный тип
цитозоль
Слайд 47Кооперативный тип фотосинтеза
! Морфологические особенности
! Биохимические особенности
Фермент декарбоксилирования
НАДФ-МЭ
НАД-МЭ
ФЕП-КК
Продукт фиксации СО2
малат
аспартат
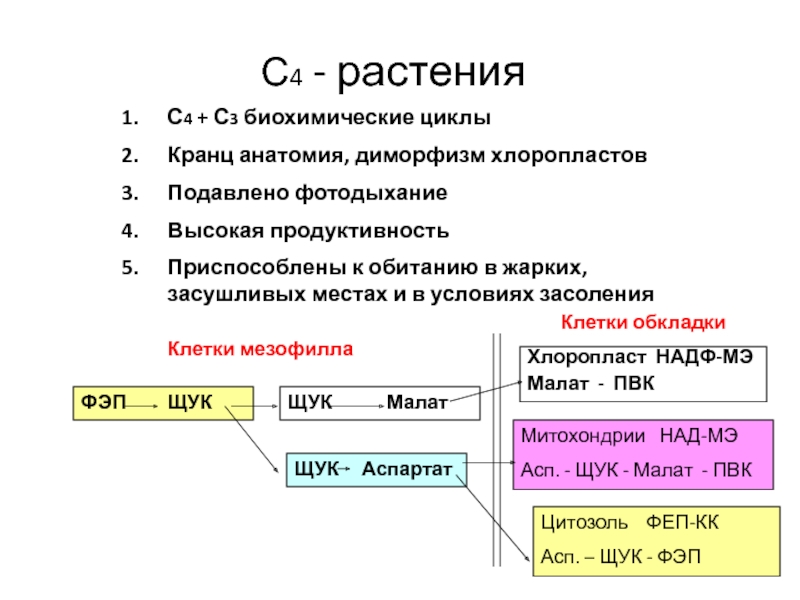
Слайд 48С4 - растения
С4 + С3 биохимические циклы
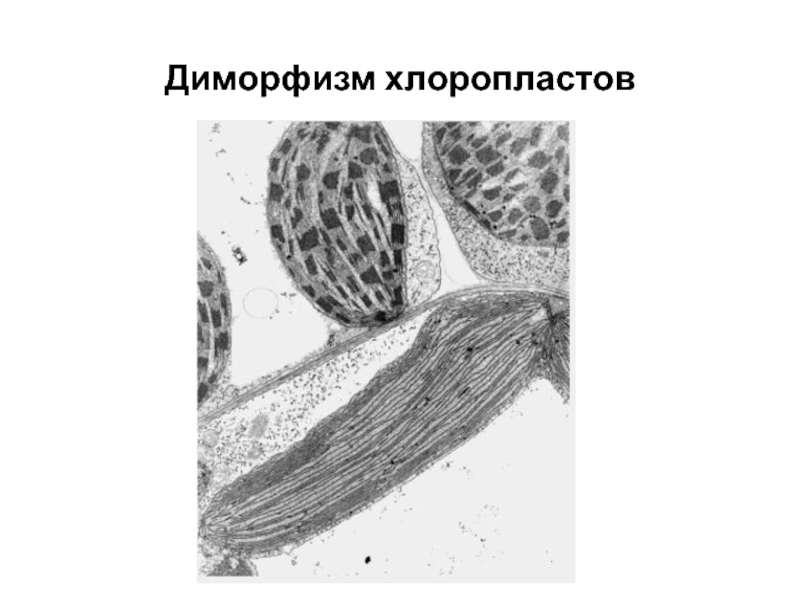
Кранц анатомия, диморфизм хлоропластов
Подавлено
фотодыхание
Высокая продуктивность
Приспособлены к обитанию в жарких, засушливых местах и в
условиях засоления
ФЭП ЩУК
ЩУК Малат
Клетки обкладки
Хлоропласт НАДФ-МЭ
Малат - ПВК
Митохондрии НАД-МЭ
Асп. - ЩУК - Малат - ПВК
Цитозоль ФЕП-КК
Асп. – ЩУК - ФЭП
Клетки мезофилла
ЩУК Аспартат
Слайд 49Злаки:
3 типа кранц анатомии, 3 энзиматические группы
Маревые:
4 типа
кранц анатомии, 3 энзиматические группы
C4 – растения: 18 семейств
90%
видов в двух семействах
Poaceae (1000) и Chenopodiaceae (250)
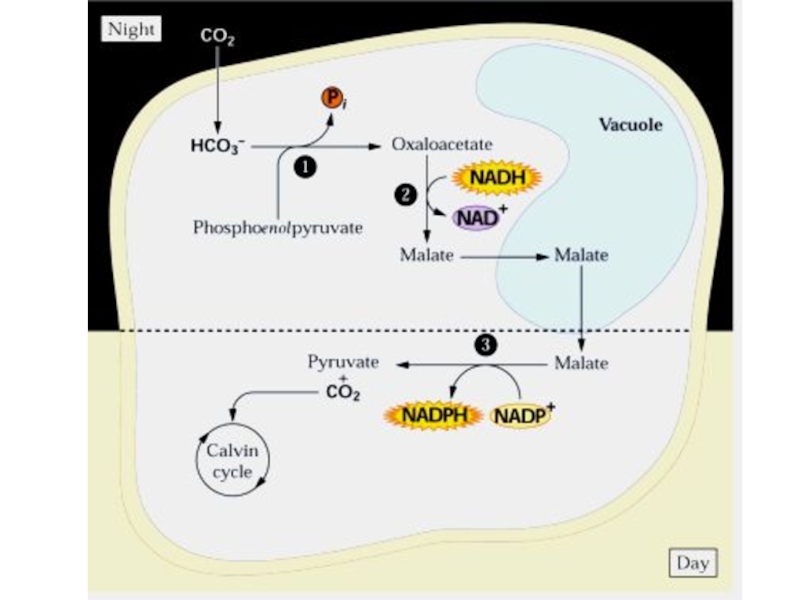
Слайд 50САМ (Сrassulaceae Acid Metabolism)
особый тип фотосинтеза
Характерен для суккулентов (каланхоэ, очитки,
толстянковые, агавовые, бромелиевые, орхидные, кактусовые, портулаковые) – около 300 видов
Слайд 52САМ
С3
С4
СО2 (день)
НСО3- (день)
СО2 (ночь)
Клетки мезофилла
Клетки мезофилла
Клетки обкладки
Цикл Кальвина
Рубиско
Схема ассимиляции СО2
у растений с разным типом ФС
НСО3- (день)
Клетки мезофилла
Клетки мезофилла
СО2 (день)
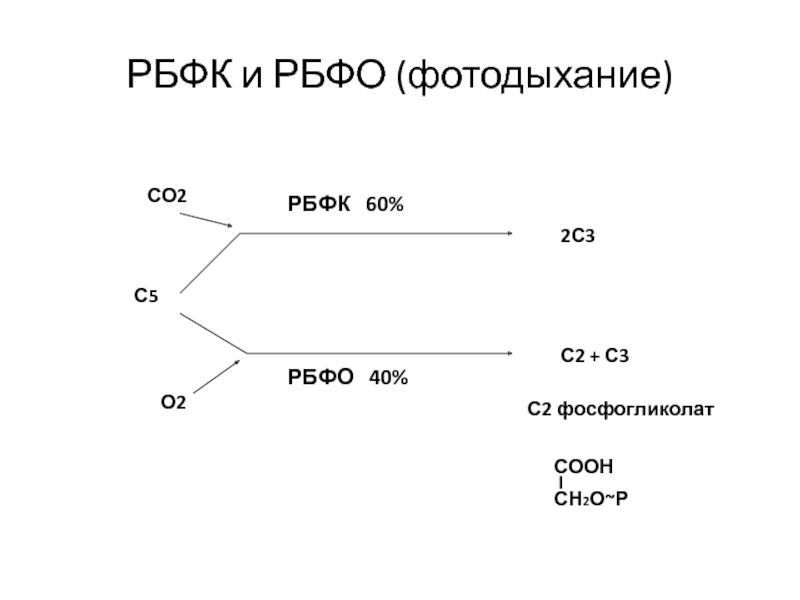
Слайд 53РБФК и РБФО (фотодыхание)
С5
СО2
О2
2С3
С2 + С3
РБФК 60%
РБФО 40%
С2
фосфогликолат
СООН
I
СН2О~Р
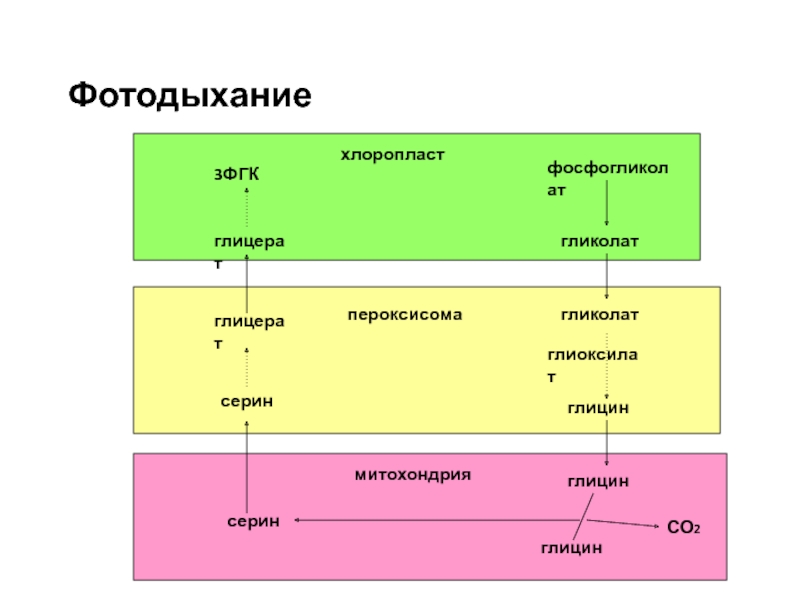
Слайд 54Фотодыхание
фосфогликолат
гликолат
глиоксилат
гликолат
глицин
глицин
глицин
серин
СО2
серин
глицерат
глицерат
3ФГК
хлоропласт
пероксисома
митохондрия
Слайд 55Зависимость интенсивности ФС
от факторов среды
Интенсивность света
Концентрация СО2
Температура
Слайд 56Световая кривая ФС
Интенсивность света
II
I
СКП
I - лимитируются световыми реакциями
II –
лимитируются темновыми реакциями
ФС [mkmol CO2/m2 * sec]
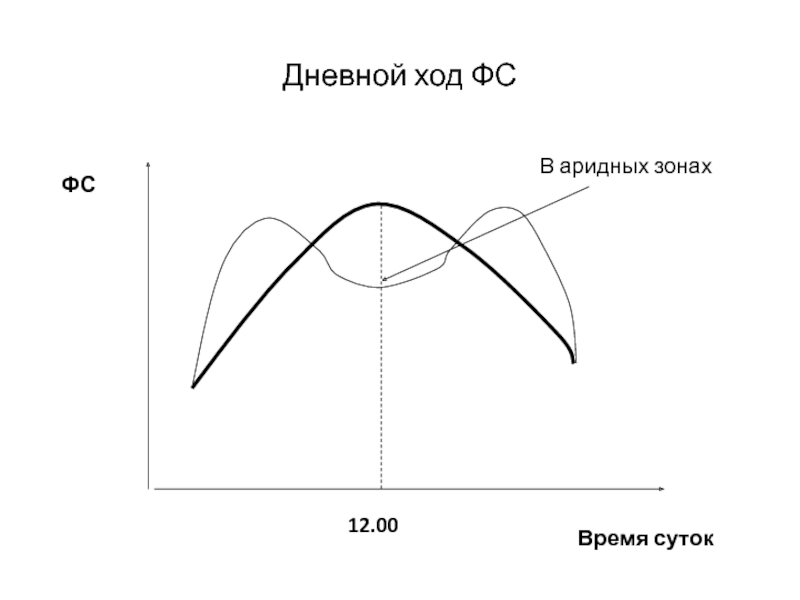
Слайд 57Дневной ход ФС
Время суток
ФС
12.00
В аридных зонах


































![Фотосинтез Световая кривая ФСИнтенсивность светаIIIСКП I - лимитируются световыми реакциямиII – лимитируются Световая кривая ФСИнтенсивность светаIIIСКП I - лимитируются световыми реакциямиII – лимитируются темновыми реакциямиФС [mkmol CO2/m2 * sec]](/img/thumbs/68f12dc21872a84abb7ccb75ea9e8f9c-800x.jpg)