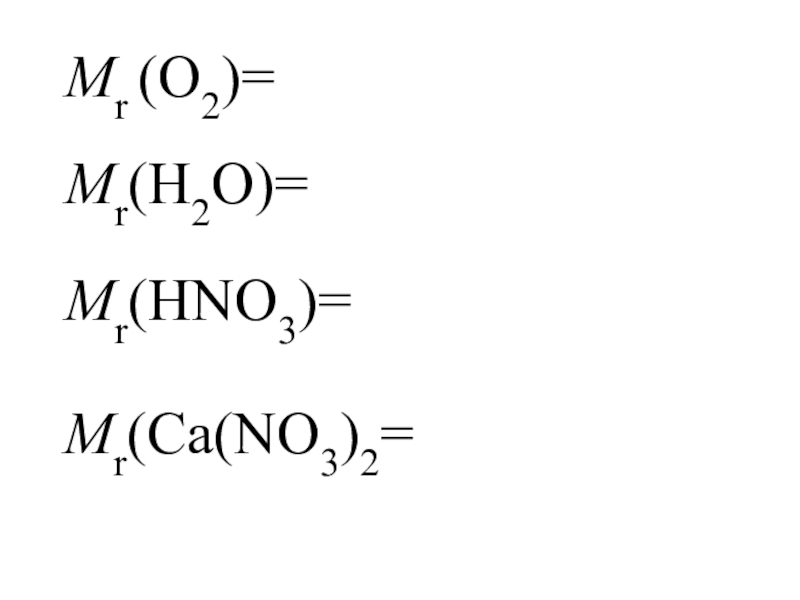Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические формулы. Относительная атомная и молекулярная масса. Нахождение
Содержание
- 1. Химические формулы. Относительная атомная и молекулярная масса. Нахождение
- 2. Слайд 2
- 3. Поваренная соль (ионный кристалл)Чем могут быть образованы
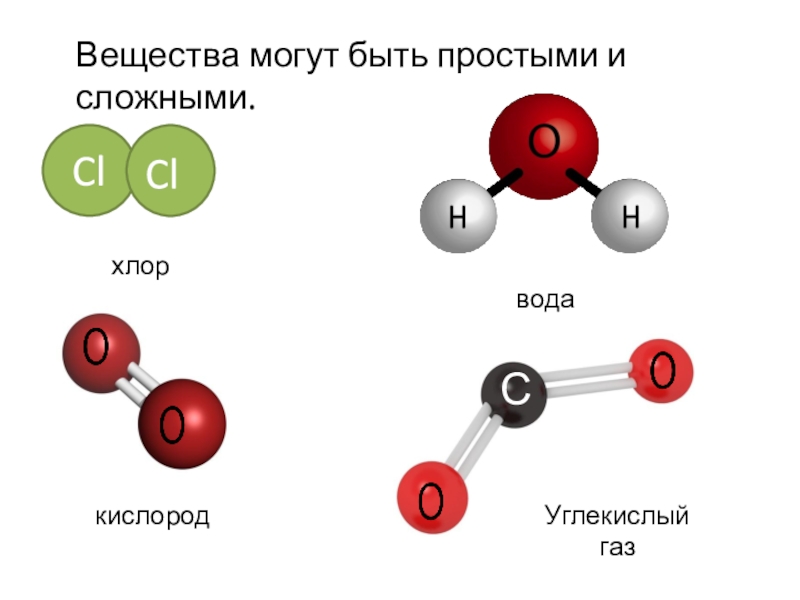
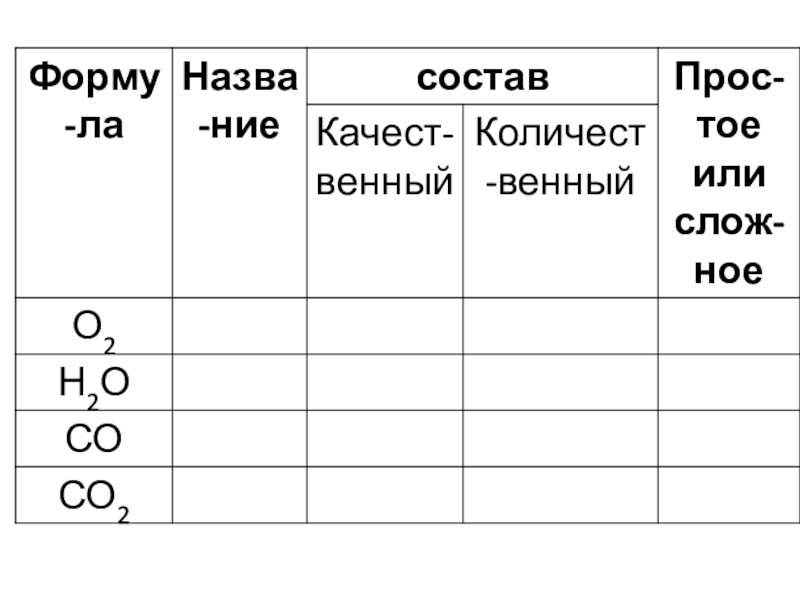
- 4. O2кислородводаН2ОCl2хлорClClВещества могут быть простыми и сложными.Углекислый газС
- 5. Вещества могут иметь постоянный и переменный состав.Химическая
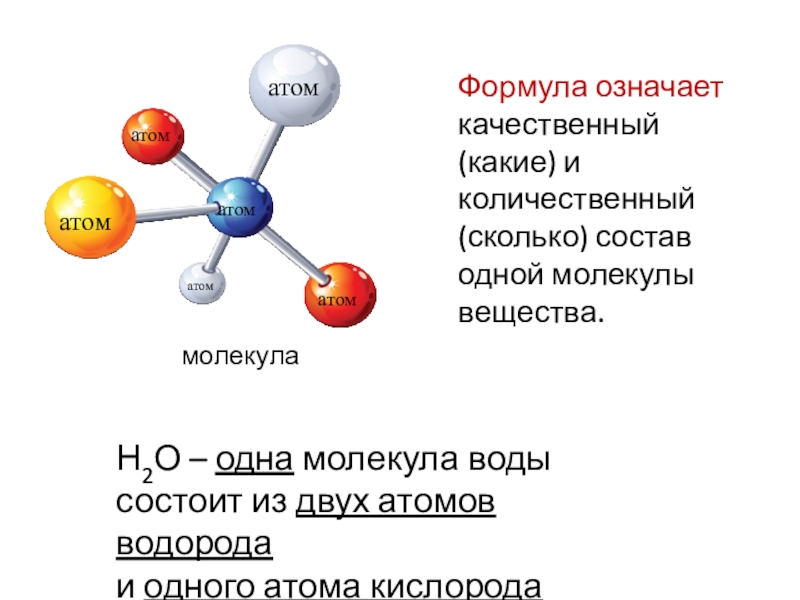
- 6. Формула означаеткачественный (какие) и количественный (сколько) состав
- 7. CO2Индексы — цифры, которые стоят внизу справа
- 8. Слайд 8
- 9. Относительная атомная массапоказывает, во сколько раз масса
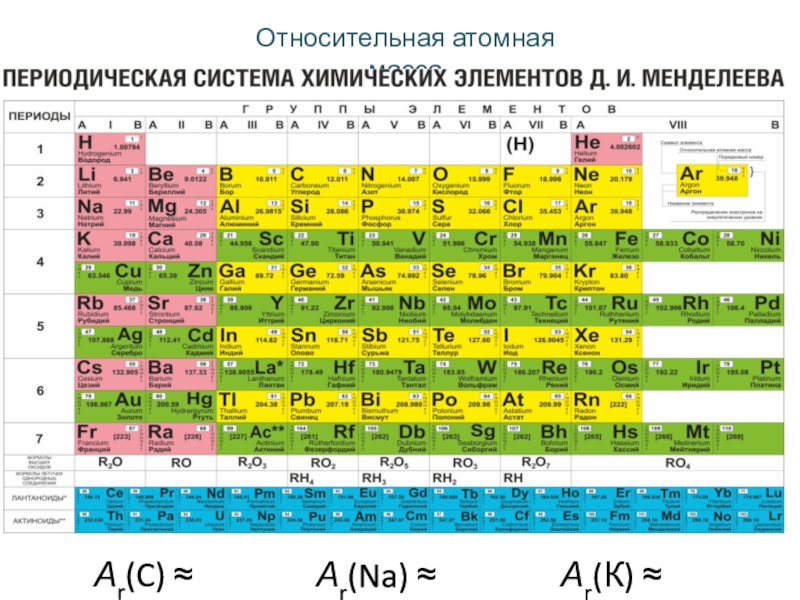
- 10. Относительная атомная массаАr(К) ≈ 39Аr(Na) ≈ 23Аr(C) ≈ 12
- 11. MrОтносительная молекулярная массаЗная относительные атомные массы,
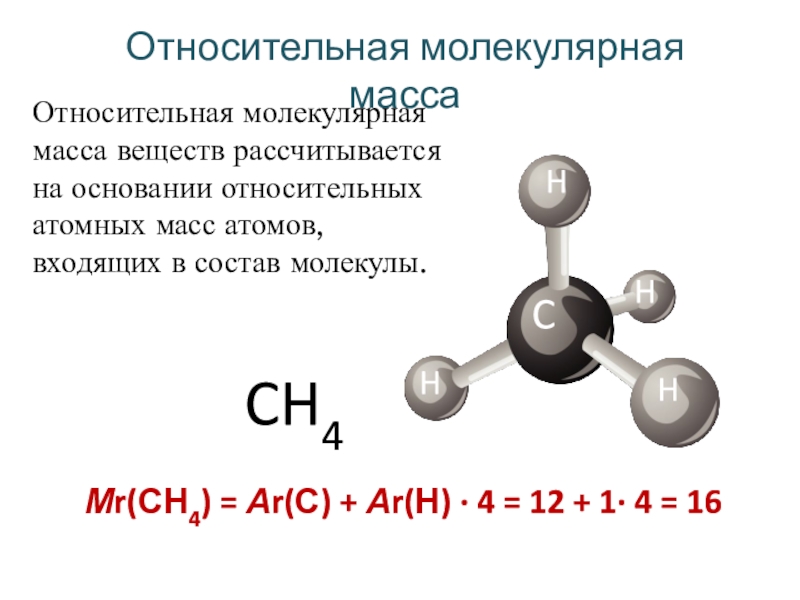
- 12. Относительная молекулярная массаCH4CHHHHМr(СН4) = Аr(С) + Аr(Н)
- 13. Mr (О2)=Mr(Н2О)=Mr(HNО3)=Mr(Ca(NО3)2=
- 14. Домашнее задание:§ 6, упр. 1,2,4 письменно
- 15. Скачать презентанцию
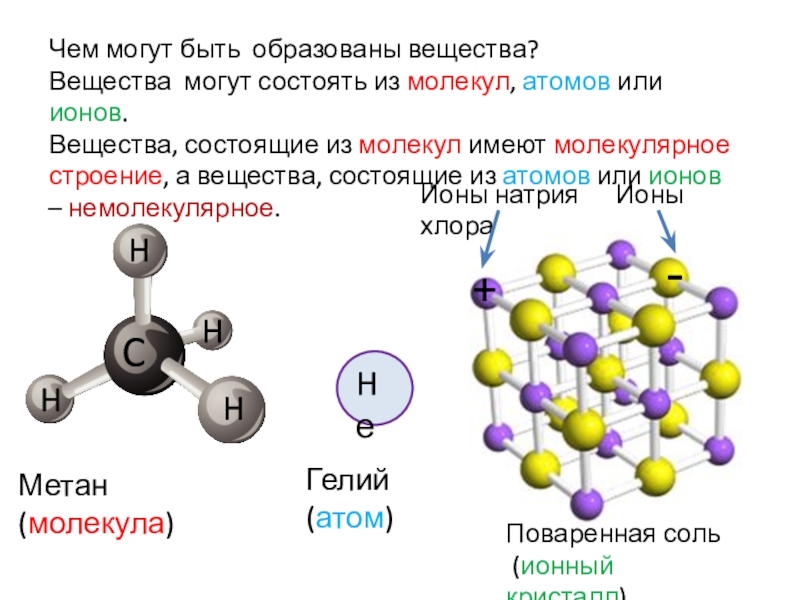
Поваренная соль (ионный кристалл)Чем могут быть образованы вещества?Вещества могут состоять из молекул, атомов или ионов.Вещества, состоящие из молекул имеют молекулярное строение, а вещества, состоящие из атомов или ионов – немолекулярное.-Ионы натрия
Слайды и текст этой презентации
Слайд 1Химические формулы. Относительная атомная и молекулярная масса. Нахождение относительной молекулярной
массы вещества по его химической формуле.
Слайд 3Поваренная соль
(ионный кристалл)
Чем могут быть образованы вещества?
Вещества могут состоять
из молекул, атомов или ионов.
Вещества, состоящие из молекул имеют молекулярное
строение, а вещества, состоящие из атомов или ионов – немолекулярное.-
Ионы натрия Ионы хлора
+
C
H
H
H
H
Метан (молекула)
Hе
Гелий (атом)
Слайд 5Вещества могут иметь постоянный и переменный состав.
Химическая формула — запись
качественного и количественного состава вещества с помощью химических знаков.
Химические формулы
веществ постоянного состава указывают точное количество атомов, а формулы веществ переменного состава отражают только соотношение чисел атомов разных химических элементов в кристалле.Слайд 6Формула означает
качественный (какие) и количественный (сколько) состав одной молекулы вещества.
Н2О
– одна молекула воды
состоит из двух атомов водорода
и
одного атома кислородаСлайд 7C
O
2
Индексы — цифры, которые стоят внизу справа от химического символа
и показывают количество данных атомов в молекуле. Они постоянные.
углерод
кислород
Коэффициенты —
специальные числа, указывающие на количество молекул. Они могут меняться.5
Слайд 9Относительная атомная масса
показывает, во сколько раз масса его атома больше
1/12 массы атома углерода.
Ar
r (relative) — относительный
Относительная атомная масса
Относительная
атомная масса указана в таблице Менделеева рядом с каждым символом
Слайд 11 Mr
Относительная молекулярная масса
Зная относительные атомные массы, можно найти относительную
молекулярную массу молекулы вещества.
Относительная молекулярная масса
рассчитывается на основании химической формулы
молекулы вещества. Относительная молекулярная масса
показывает, во сколько раз масса данной молекулы больше 1/12 массы атома углерода
Слайд 12Относительная молекулярная масса
CH4
C
H
H
H
H
Мr(СН4) = Аr(С) + Аr(Н) · 4 =
12 + 1· 4 = 16
Относительная молекулярная масса веществ рассчитывается
на основании относительных атомных масс атомов, входящих в состав молекулы.H