Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химическое уравнение. Закон сохранения массы веществ
Содержание
- 1. Химическое уравнение. Закон сохранения массы веществ
- 2. Историческая справкаЗакон сохранения массы веществ был открыт
- 3. Закон сохранения массы«Масса веществ, вступивших в реакцию, равна массе образовавшихся веществ»
- 4. Химическим уравнениемназывают условную запись химической реакции с
- 5. Знаки в химических уравнениях:Над стрелкой пишутся условия реакции, под стрелкой иногда указывают продукты реакции.
- 6. Уравнения химических реакций.- реагирующие вещества- продукты реакции- взаимодействие- условие протекания реакцииN2 , H2NH3+
- 7. Уравнения химических реакций.- реагирующие вещества- продукты реакции- взаимодействие- условие протекания реакцииN2 , H2NH3+
- 8. Уравнения химических реакций.- реагирующие вещества- продукты реакции- взаимодействие- условие протекания реакцииN2 , H2NH3+
- 9. Алгоритм составления уравнений:
- 10. 3. Согласно закону сохранения массы веществ число атомов
- 11. 4. Закон сохранения массы вещества не выполнен,
- 12. Упражнения для закрепления 1. Какой коэффициент стоит в
- 13. Ответы к упражнениям. 1. Какой коэффициент стоит в
- 14. Домашнее задание:§ 28, № 1 (б), 2 (в, д - ж), 3 (в, г).
- 15. Скачать презентанцию
Историческая справкаЗакон сохранения массы веществ был открыт М.В.Ломоносовым в 1748 году и подтвержден французским химиком А.Л.Лавуазье в 1789 году.М.ЛомоносовА.Л. Лавуазье
Слайды и текст этой презентации
Слайд 2Историческая справка
Закон сохранения массы веществ был открыт М.В.Ломоносовым в 1748
году и подтвержден французским химиком А.Л.Лавуазье в 1789 году.
Слайд 3Закон сохранения массы
«Масса веществ, вступивших в реакцию, равна массе образовавшихся
веществ»
Слайд 4Химическим уравнением
называют условную запись химической реакции с помощью химических формул
и математических знаков.
Вещества, принимающие участие в реакции, называются реагентами или
исходными веществами.Вещества, образующиеся в результате реакции – продуктами реакции.
Слайд 5Знаки в химических уравнениях:
Над стрелкой пишутся условия реакции, под стрелкой
иногда указывают продукты реакции.
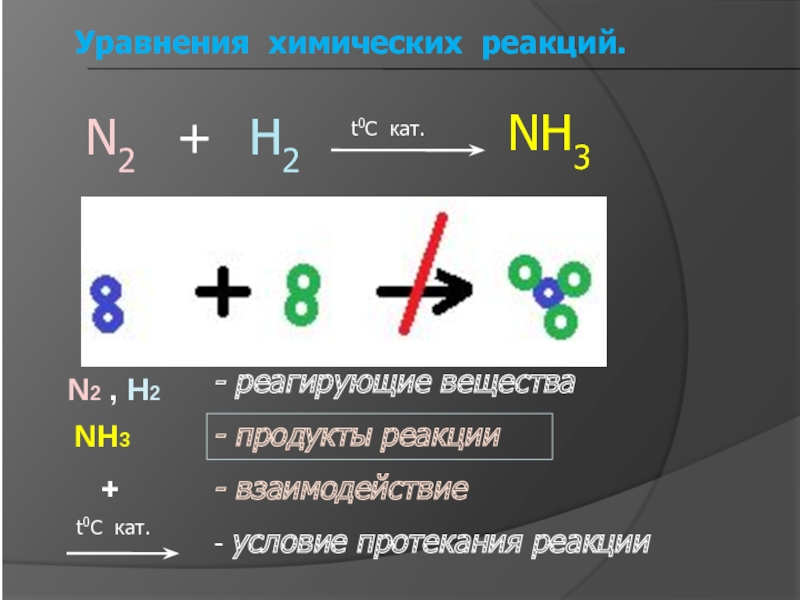
Слайд 6Уравнения химических реакций.
- реагирующие вещества
- продукты реакции
- взаимодействие
- условие протекания
реакции
N2 , H2
NH3
+
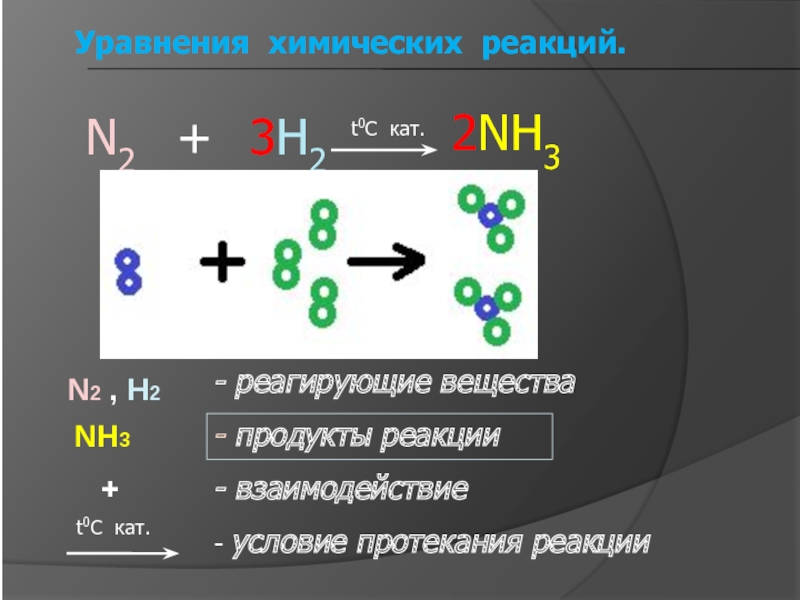
Слайд 7Уравнения химических реакций.
- реагирующие вещества
- продукты реакции
- взаимодействие
- условие протекания
реакции
N2 , H2
NH3
+
Слайд 8Уравнения химических реакций.
- реагирующие вещества
- продукты реакции
- взаимодействие
- условие протекания
реакции
N2 , H2
NH3
+
Слайд 103. Согласно закону сохранения массы веществ число атомов до и после
реакции должно быть одинаковым. Это достигается путём расстановки коэффициентов перед
химическими формулами реагентов и продуктов химической реакции.Вначале уравнивают число атомов, которых в реагирующих веществах (продуктах) содержится больше.
В данном случае это атомы кислорода.
Находим наименьшее общее кратное чисел атомов кислорода в левой и правой частях уравнения. Наименьшее кратное для атомов кислорода –10:
Находим коэффициенты путём
деления наименьшего кратного на
число атомов данного вида,
полученные цифры ставим в
уравнение реакции:
Слайд 114. Закон сохранения массы вещества не выполнен, так как число
атомов фосфора в реагентах и продуктах реакции не равно, поступаем
аналогично ситуации с кислородом:Получаем окончательный вид уравнения химической реакции. Стрелку заменяем на знак равенства. Закон сохранения массы вещества выполнен: 4P + 5O2 = 2P2O5
Слайд 12Упражнения для закрепления
1. Какой коэффициент стоит в уравнении реакции
перед
формулой соляной кислоты?
Na + HCl → NaCl +
H22. Продолжите уравнение реакции, расставьте коэффициенты
Al + O2 →
3. Запишите уравнение реакции и расставьте коэффициенты - Сульфат натрия соединяется с нитратом бария с образованием сульфата бария и нитрата натрия.
4. Найдите ошибки.
Mg + HBr → MgBr2 + H2
BaO +H2So 4 → Ba2SO4 + H2O
ZnO + HNO3 → ZnNO 3 + H2O
5. Закончите уравнение
Li 2 O + SO3 → …………..
Слайд 13Ответы к упражнениям.
1. Какой коэффициент стоит в уравнении реакции перед
формулой соляной кислоты?
2Na + 2HCl
→ 2NaCl + H22. Продолжите уравнение реакции, расставьте коэффициенты
4Al +3 O2 → 2Al2O2
3. Запишите уравнение реакции и расставьте коэффициенты -
Сульфат натрия соединяется с нитратом бария с образованием сульфата бария и нитрата натрия.
Na2 SO4 + Ba(NO3)2 → BaSO4 ↓ + 2Na NO3
4. Найдите ошибки.
Mg + 2 HBr → MgBr2 + H2
BaO +H2So4 → Ba2SO4 + H2O
ZnO + 2 HNO3 → Zn(NO3) 2 + H2O
5. Закончите уравнение
Li 2 O + SO3 =Li 2 SO4