Слайд 1Иммунопатогенез ВИЧ - инфекций
Слайд 2ВИЧ – является исключительным вирусом с точки зрения иммунного ответа.
До сих пор не известно ни одного вирусного заболевания, при
котором у большинства пациентов вирус индуцирует сильнейший иммунный ответ, однако иммунная система не в состоянии справиться с возбудителем.
Причиной поражения является тот факт, что клетки, выполняющие ключевую роль в иммунном ответе, являются основной мишенью для вируса.
Слайд 4
Заболевание, вызываемое ВИЧ, может быть охарактеризовано как иммунодефицитное состояние инфекционной
природы, возникающее вследствие способности вируса паразитировать непосредственно в клетках иммунной
системы. Это сложный процесс взаимодействия возбудителя с организмом хозяина продолжается от момента первичной инфекции до последней смертельной стадии заболевания.
Слайд 5Фазы патогенеза ВИЧ – инфекции:
1-ая фаза. проникновение ВИЧ в организм,
заселение клеток-мишеней, репликация в них вируса;
2-ая фаза – вирусемия;
3 –
я фаза – прогрессирующее повреждение иммунокомпетентных клеток;
4 – ая фаза – углубление иммунодефицита, развитие оппортунистических инфекций или онкозаболеваний;
5 – ая фаза - тотальный иммунодефицит.
Слайд 6
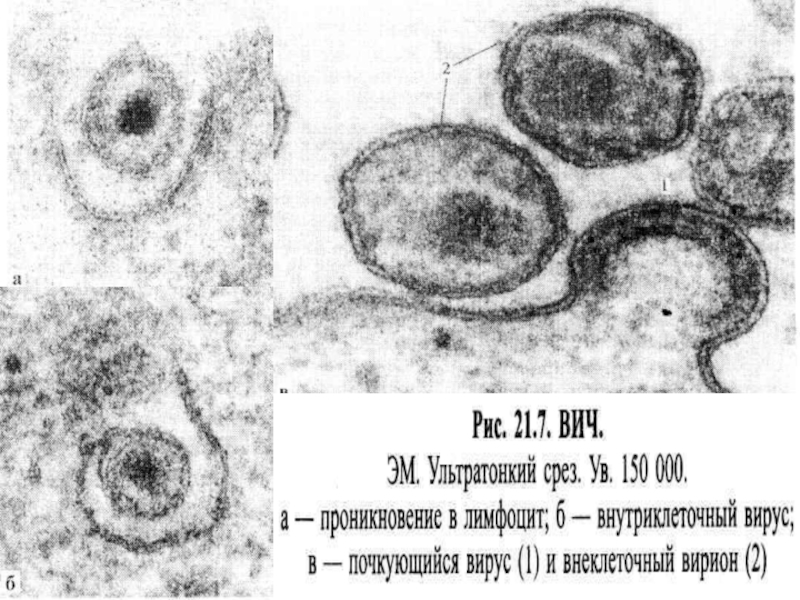
Дендритные клетки (особенно клетки Лангерганса при инфицировании слизистых) и моноциты/макрофаги
инфицируются одними из первых и через циркуляцию доставляют вирус в
кровь и в ближайшие лимфоидные органы, представляя вирус CD4 лимфоцитам. При парентеральном заражении вирус может непосредственно инфицировать CD4 лимфоциты
Слайд 8Дендритные клетки при заражении ВИЧ выполняют подлую роль “Троянского коня”,
перенося вирус с места проникновения к лимфатическим узлам.
Одна дендритная клетка
в течение часа может инфицировать несколько десятков Т-лимфоцитов.
Слайд 9Вирусы, изолируемые в начальных стадиях заболевания, относятся в основном к
макрофаготропным. ВИЧ реплицируются в макрофагах/моноцитах с умеренной интенсивностью и, выходя
из клетки, не оказывает цитотоксического действия. Эти клетки являются хроническим резервуаром вируса и дополнительным фактором распространения ВИЧ в органах и тканях. Инфицированные макрофаги уже на самых ранних стадиях заболевания преодолевают гематоэнцефалический барьер и переносят вирус в ЦНС и др. органы.
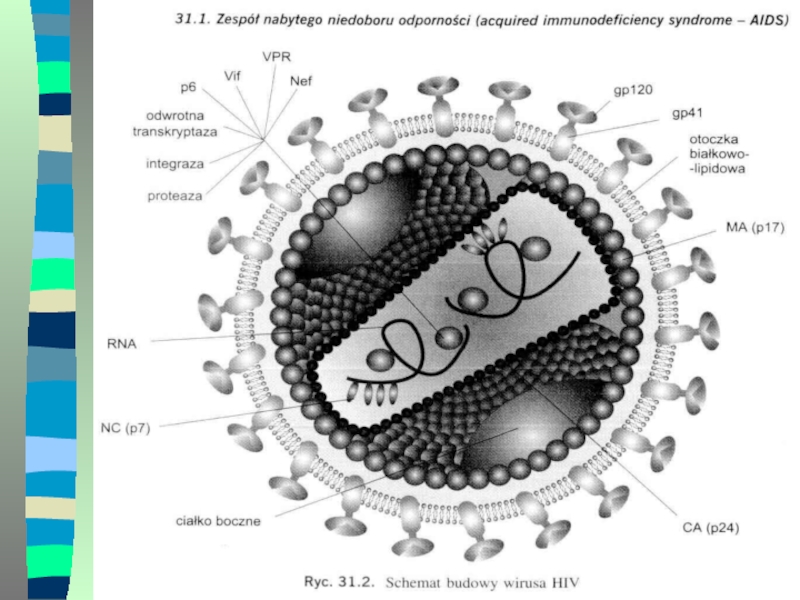
Слайд 10 Основными клетками-“мишенями” для ВИЧ являются клетки, имеющие на своей поверхности
CD4 рецепторы, представленные в основном на мембране Т-лимфоцитов-хелперов.
Слайд 12
CD4 рецепторы имеют моноциты и их тканевые формы – макрофаги,
клетки Лангерганса, фолликулярные клетки лимфоузлов, альвеолярные макрофаги легких, клетки микроглии
и др.
ВИЧ также может инфицировать клетки, не имеющие CD4 рецепторы (фибробласты, керотиноциты, стволовые клетки костного мозга, и даже нейроны). Это связывают с тем, что вирус ВИЧ использует рецепторы не только для CD4, но и для хемокинов.
Слайд 13
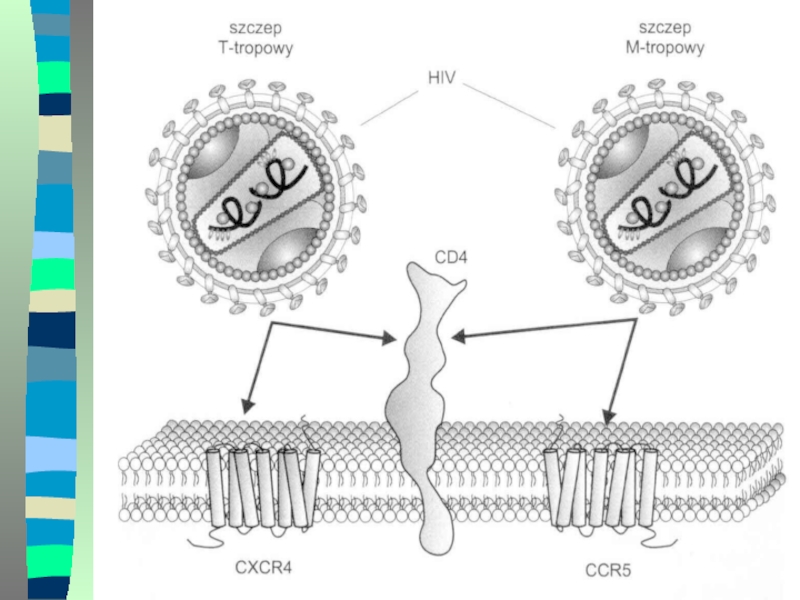
С точки зрения тропизма выделяют два доминирующих рецептора вируса М-тропный
и Т-тропный.
М-тропные рецепторы, обозначаемые R5, проявляют тропизм к макрофагам
и лимфоцитов периферической крови, они используют CCR5 как главный корецептор и отвечают за заражение сексуальным путём. Данный вид превалирует в начале заболевания.
Т-тропные вирусы обозначаемые как Х4 проявляющие тропизм к лимфоцитам в периферической крови, используя корецептор СХСR4 и доминируют в конечной стадии заболевания.
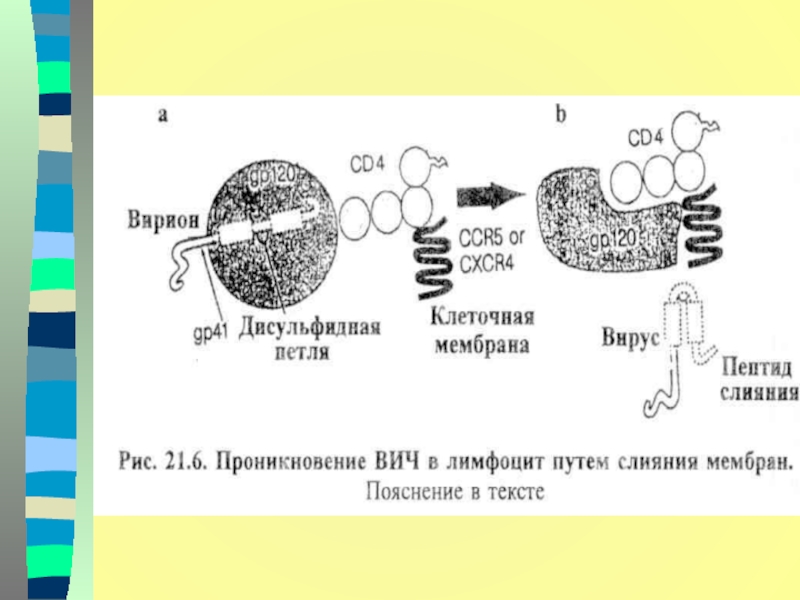
Слайд 15 Вирус становится частью клетки и будет оставаться ею вплоть до
ее гибели.
В дальнейшем происходит проникновение вируса из клетки
в клетку с образованием в терминальной стадии заболевания многоядерного клеточного синцития с последующей гибелью клеток.
Слайд 16 Новые вирусные частицы покидают клетку и лавинообразно инфицируют новые клоны
лимфоцитов. Формируется активный инфекционный процесс.
Слайд 17
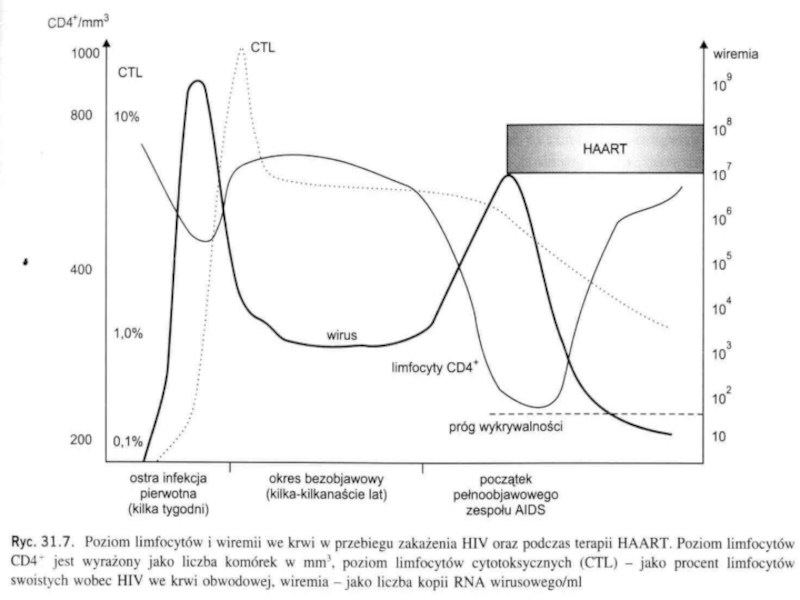
Количество CD4 лимфоцитов в крови уменьшается, а вирусная нагрузка (количество
копий РНК ВИЧ) может достигать 1000 – 10000 инфекционных частиц
в 1 мл плазмы.
У 30-40% больных виремия манифестируется симптомами остролихорадочной стадии первичных проявлений заболевания.
Слайд 18
В стадии первичных проявлений иммунная система сохраняет способность к осуществлению
своих защитных функций, что поддерживает относительное равновесие между репликацией и
элиминацией вируса.
Самокупирование острой ретровирусной инфекции сопровождается нарастанием в крови антител (анти gp. 24, анти gp. 120). При этом вирусемия резко снижается, репликация ВИЧ идет медленно, развивается бессимптомная стадия.
Слайд 19
Частичное купирование острой ретровирусной инфекции корректируется иммунным ответом организма в
основном за счет цитотоксических лимфоцитов и нейтрализующих антител, выявляемых на
3-12 неделе (сероконверсия).
Это сопровождается восстановлением числа CD4 лимфоцитов (но не до исходного уровня) и постепенным снижением уровня репликации вируса (концентрация РНК в периферической крови снижается в 1000-10000 раз).
Слайд 20
Наибольшей активности цитотоксических лимфоцитов соответствует снижение концентрации вируса в крови.
Слайд 22
Тем не менее эти лимфоциты не в состоянии остановить развитие
заболевания, что связывают:
с появлением вариантов вируса которые становятся нераспознаваемыми
с
секвестрацией вируса в клетках, недоступных для иммунной системы (клетки микроглии мозга)
со снижением экспрессии рецепторов МНС класса I
с избытком антигена, приводящего к клональной делеции или анергии
с экспрессией FasL на инфицированных клетках, приводящией к гибели активированных CD8 лимфоцитов.
Слайд 23
Обычно к 6-8 мес. после инфицирования достигается определенное плато (setpoint)
в уровне репликации, которое отражает то равновесие, которое достигается между
организмом и вирусом и заболевание переходит в стадию бессимптомной хронической инфекции.
В латентной стадии часть заражённых лимфоцитов после деления становятся клетками памяти и переходят в состояние покоя.
Слайд 24
Однако, репликация вируса в пределах плато продолжается, погибшие CD4 лимфоциты
еще восполняются адекватным количеством новых.
Лимфатические узлы перегружены внеклеточным и
внутриклеточным вирусом, что приводит к постепенному их разрушению.
Через несколько лет, микросреда лимфатических узлов настолько разрушена, что приводит к невозможности презентации антигенов, без чего невозможен иммунный ответ.
Слайд 25
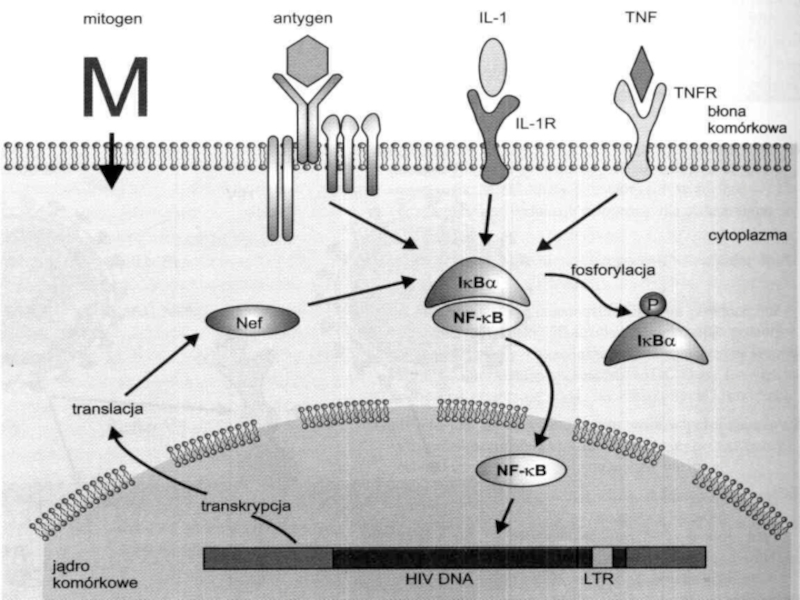
Начало транскрипции генов ВИЧ связано с физиологической активацией клетки. В
зависимости от разновидности клетки различные сигналы могут приводить к транскрипции
вируса.
Слайд 27
Ответом лимфоцита на стимуляцию антигеном или цитокинами, приводит к активации
“дремлющих” вирусов, которые великолепным образом используют физиологические механизмы активации.
Слайд 28
Каждый день в организме инфицированного человека появляется 19 биллионов вирионов,
а число генераций вируса за год – 140!
Любая мутация
в любой позиции генома может происходить много раз в день, а при использовании лекарственных средств может быть генерирован почти любой резистентный мутант.
Этот многократный процесс транскрипции генов вируса и слишком большое разнообразие экспрессированных структурных белков вируса, резко снижает шансы их распознавания системой иммунитета.
Слайд 30
Кроме этого при почковании с поверхности клетки вирусы как наружную
защиту используют клеточную оболочку с находящимися на ней гликопротеинами и
антигенами (это могут быть частицы главного комплекса гистосовместимости, адгезины и т.д.), что затрудняет распознавание вируса.
Слайд 31
Наиважнейшим в патогенезе ВИЧ-инфицирования является
постоянная репликация вируса
в клетках
периферической крови и в лимфатической системе (даже в бессимптомной стадии).
Этому
сопутствует
снижение как количества так и активности Т-хелперов
CD4, играющих ключевую роль в иммунном ответе.
Слайд 32
Причины снижения количества CD4 лимфоцитов:
прямое повреждение лимфоцитов ВИЧ,
аутоиммунное поражение CD4
(разрушение цитотоксическими лимфоцитами),
образование синцития из поражённых лимфоцитов под действием ВИЧ,
токсическое
действие вирусных белков на зрелые лимфоциты и костный мозг,
запускаются механизмы запрограмми-рованной гибели клеток – апоптоз
Слайд 33
Количество лимфоцитов, погибающих ежедневно, может превышать 1 миллиард, что в
100 раз превышает физиологическое их разрушение. Компенсаторное увеличение продукции лимфоцитов,
стимулированное в какой то степени самим вирусом, не может компенсировать эти потери. При образном сравнении эта ситуация напоминает открученный кран, который не в состоянии наполнить ёмкость без пробки.
Слайд 35Терминальная фаза, приводящая к гибели больного.
Развившийся тотальный иммунодефицит затрагивает все
клетки иммунокомпетентной системы, и характеризуется развитием анергии.
Не смотря на активацию
В –звена, нарушается способность к продукции специфических антител с последующим развитием гипоиммуноглобулинемии.
Патологический процесс приобретает необратимый характер, прогрессирует тяжелейшая полиорганная недостаточность.