Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Изменение числа электронов на внешнем энергетическом уровне атомов химических
Содержание
- 1. Изменение числа электронов на внешнем энергетическом уровне атомов химических
- 2. заряды атомных ядер увеличиваются; число электронов на
- 3. металлические свойства увеличиваются, неметаллические свойства уменьшаются.В пределах
- 4. Химическая связь – Это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы.
- 5. Напишите строение атомов натрия, хлора и аргона.Na
- 6. Слайд 6
- 7. Механизм образования ионной связи:1ē
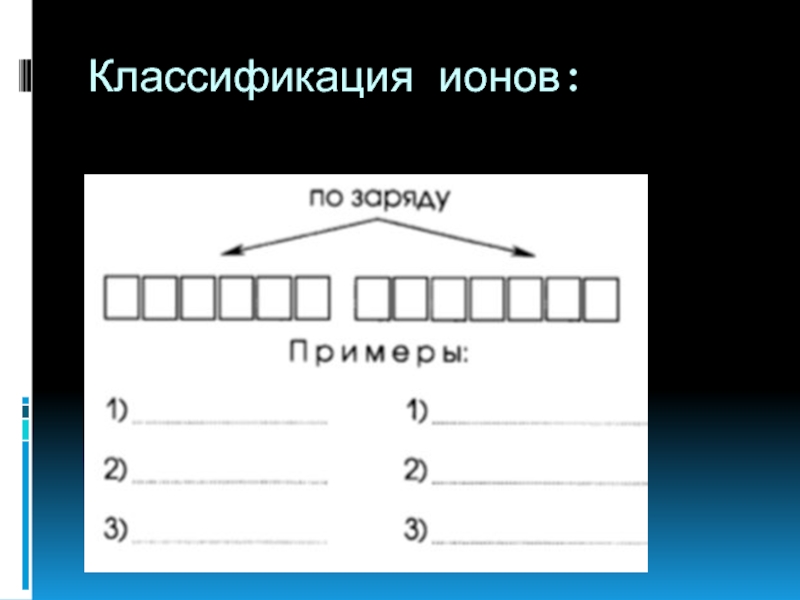
- 8. Классификация ионов:
- 9. Слайд 9
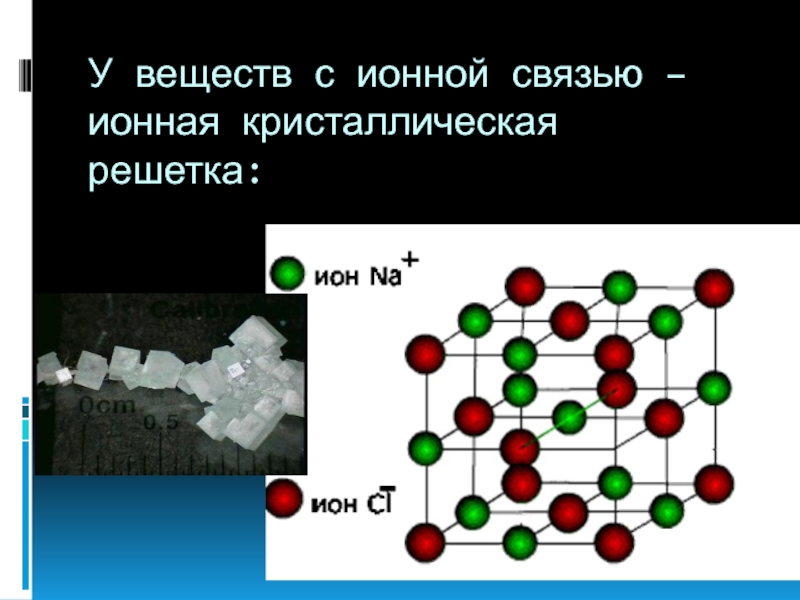
- 10. У веществ с ионной связью – ионная кристаллическая решетка:
- 11. Домашнее задание:§ 10; № 1(б), 2 (б, в), 4.
- 12. Скачать презентанцию
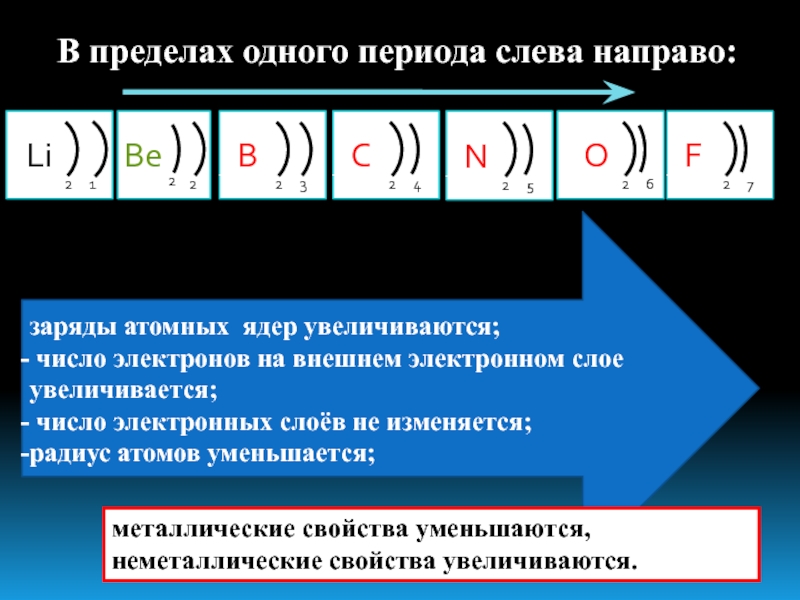
заряды атомных ядер увеличиваются; число электронов на внешнем электронном слое увеличивается; число электронных слоёв не изменяется;радиус атомов уменьшается;В пределах одного периода слева направо:металлические свойства уменьшаются, неметаллические свойства увеличиваются.
Слайды и текст этой презентации
Слайд 1Изменение числа электронов на внешнем энергетическом уровне атомов химических элементов.
Ионная связь.
Слайд 2заряды атомных ядер увеличиваются;
число электронов на внешнем электронном слое
увеличивается;
число электронных слоёв не изменяется;
радиус атомов уменьшается;
В пределах одного
периода слева направо:металлические свойства уменьшаются, неметаллические свойства увеличиваются.
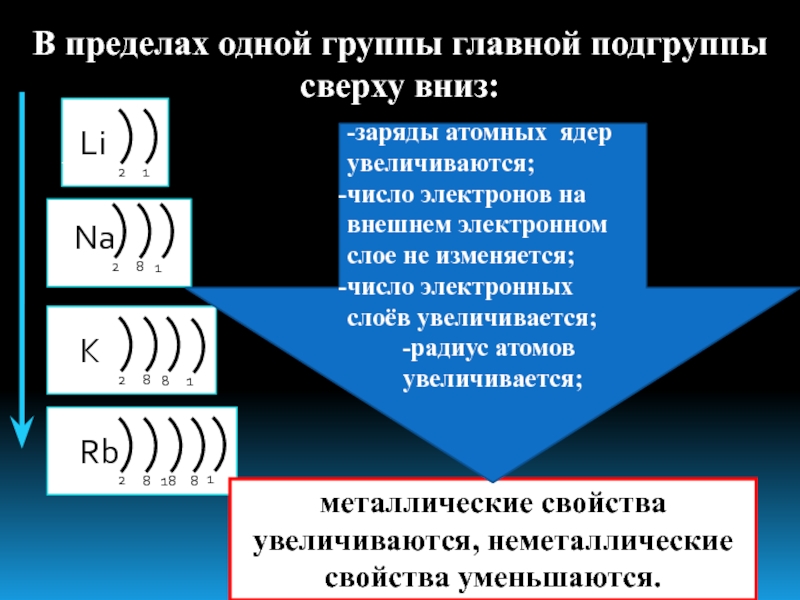
Слайд 3металлические свойства увеличиваются, неметаллические свойства уменьшаются.
В пределах одной группы главной
подгруппы сверху вниз:
-заряды атомных ядер увеличиваются;
число электронов на внешнем электронном
слое не изменяется;число электронных слоёв увеличивается;
радиус атомов увеличивается;