Слайд 1ЛЕКЦИЯ 2
Производные хинолина
19.02.2013
Слайд 2Классификация производных хинолина
1.1. Производные цинхонана (хинина гидрохлорид, хинина дигидрохлорид, хинина
сульфат).
1.2. Производные 8-гидроксихинолина (хинозол, хлорхинальдол, нитроксолин – 5-НОК, энтеросептол).
1.3.
Производные 4-аминохинолина (хлорохин- «Хингамин», гидроксихлорохин – «Плаквенил», трихомонацид).
1.4. Производные 4-хинолона (кислота налидиксовая, кислота оксолиниевая, фторхинолоны - «Офлоксацин», «Ципрофлоксацин», «Ломефлоксацин»).
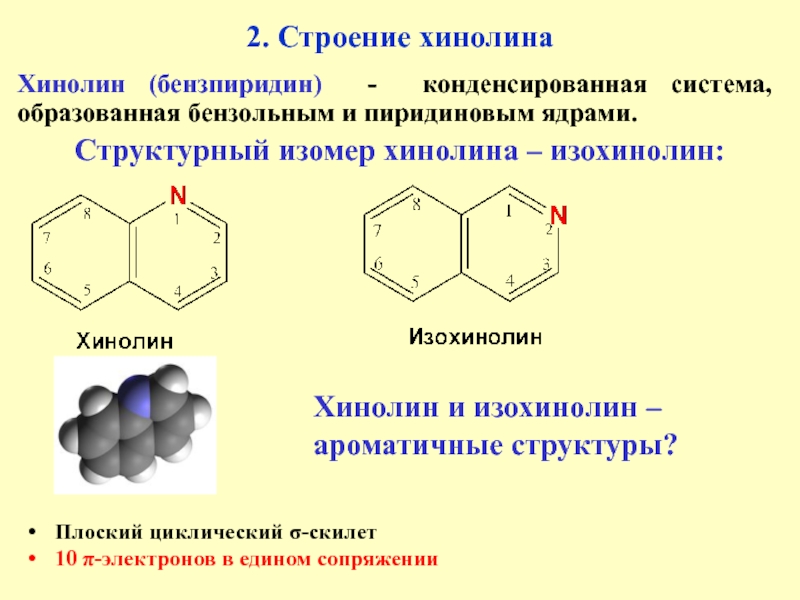
Слайд 32. Строение хинолина
Хинолин (бензпиридин) - конденсированная система, образованная бензольным и
пиридиновым ядрами.
Структурный изомер хинолина – изохинолин:
Плоский циклический σ-скилет
10 π-электронов в
едином сопряжении
Хинолин и изохинолин – ароматичные структуры?
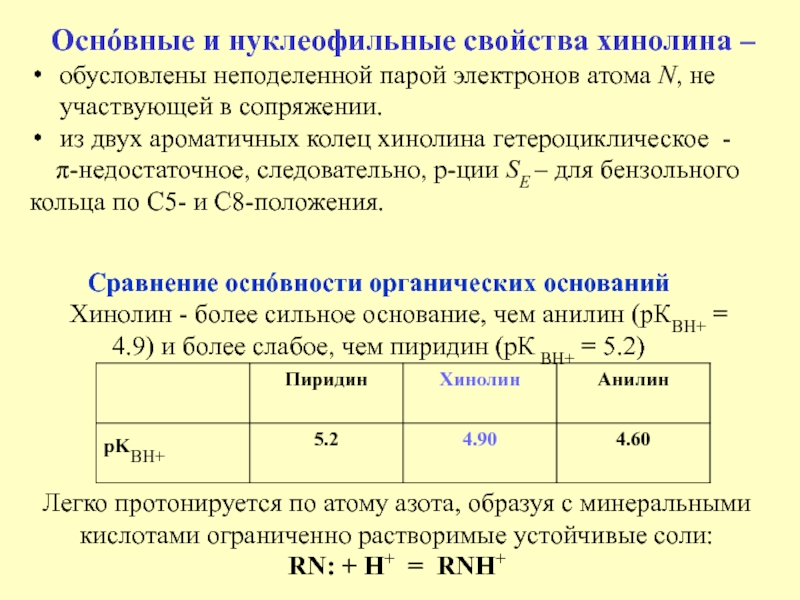
Слайд 4Cравнение оснóвности органических оснований
Хинолин - более сильное основание, чем
анилин (рКBH+ = 4.9) и более слабое, чем пиридин (рК
BH+ = 5.2)
Оснóвные и нуклеофильные свойства хинолина –
обусловлены неподеленной парой электронов атома N, не участвующей в сопряжении.
из двух ароматичных колец хинолина гетероциклическое -
π-недостаточное, следовательно, р-ции SE – для бензольного кольца по С5- и С8-положения.
Легко протонируется по атому азота, образуя с минеральными кислотами ограниченно растворимые устойчивые соли: RN: + H+ = RNH+
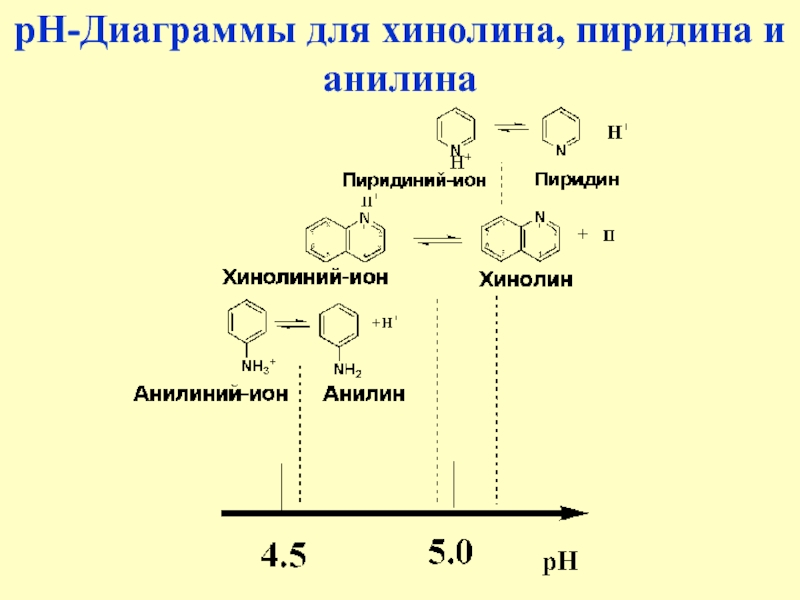
Слайд 5рН-Диаграммы для хинолина, пиридина и анилина
Слайд 63. Из истории алкалоидов группы хинолина
Всего известно около 300 –
выделены из растений 14 семейств –
рутовых, мареновых, астровых
и др.
наибольшее число алкалоидов выделено из хинной корки
– коры южноафриканского растения рода цинхóна
(Cinchona officinalis L , сем. Rubiaceae)
Хинин – важнейший алкалоид группы – б/ц кристаллы очень горького вкуса – старейшее ЛС
История применения ~ с 1636 г.; Изготовив из волшебной коры красного цвета противомалярийный порошок, иезуиты не замедлили провозгласить его "священным". В 1639 г «иезуитский порошок» стали применять в католических странах.
Лидер Английской буржуазии Оливер Кромвель (протестанец!) умер от малярии, т.к. не хотел применять лекарство с названием «иезуитский порошок»!
Хинин и его соли применяются в качестве пищевой горечи в освежающих напитках, их концентратах и пищевых продуктах
Соли хинина дают в водном р-ре синюю флуоресценцию, которая заметна даже в разбавленных р-ах и в прохладительных напитках!
Кора вида Cinchona officinalis
Слайд 7«Хинное дерево» →
«Хинная корка» →
«Хина» (сумма алкалоидов) →
«Хинин»
(основной алкалоид)
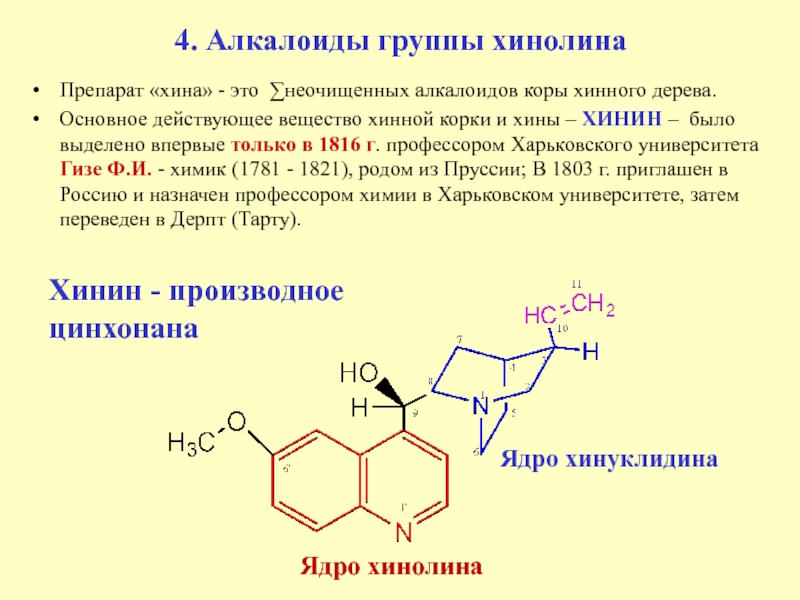
Слайд 84. Алкалоиды группы хинолина
Препарат «хина» - это ∑неочищенных алкалоидов коры
хинного дерева.
Основное действующее вещество хинной корки и хины –
ХИНИН – было выделено впервые только в 1816 г. профессором Харьковского университета Гизе Ф.И. - химик (1781 - 1821), родом из Пруссии; В 1803 г. приглашен в Россию и назначен профессором химии в Харьковском университете, затем переведен в Дерпт (Тарту).
Ядро хинолина
Ядро хинуклидина
Хинин - производное цинхонана
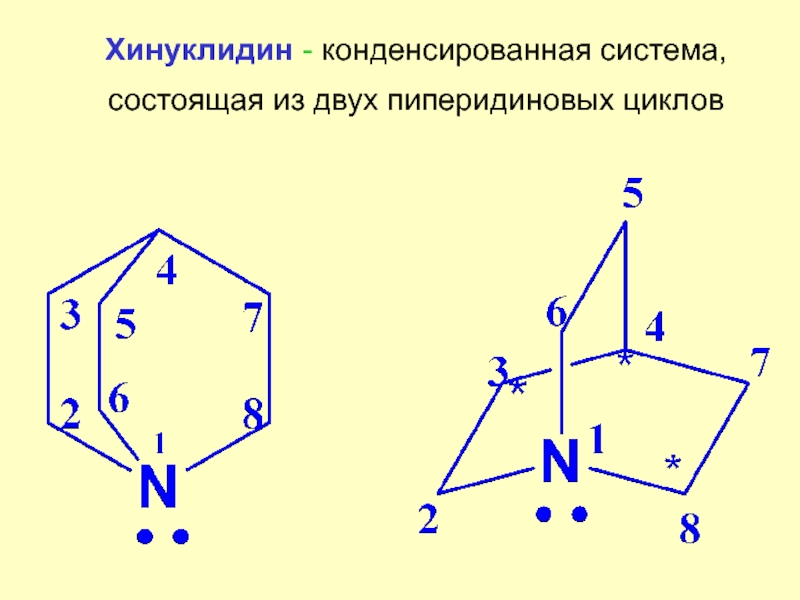
Слайд 9Хинуклидин - конденсированная система, состоящая из двух пиперидиновых циклов
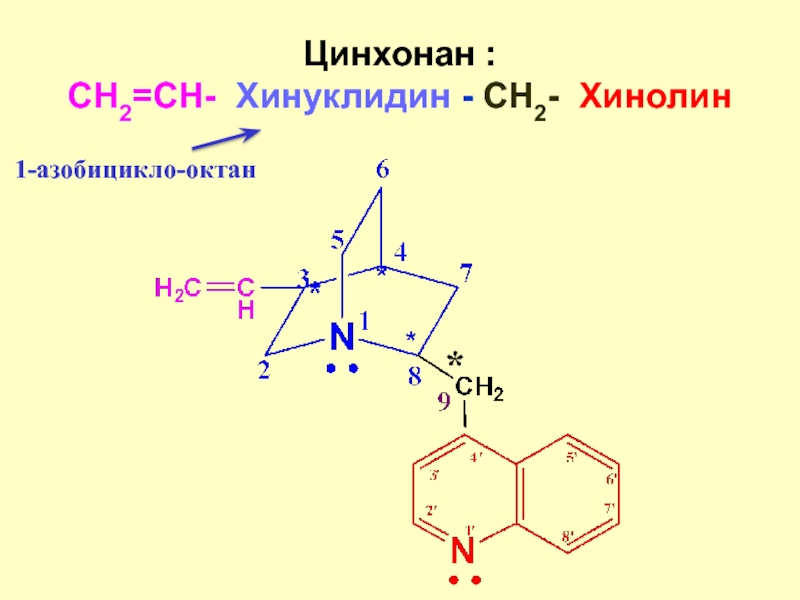
Слайд 10Цинхонан :
CH2=CH- Хинуклидин - СH2- Хинолин
*
1-азобицикло-октан
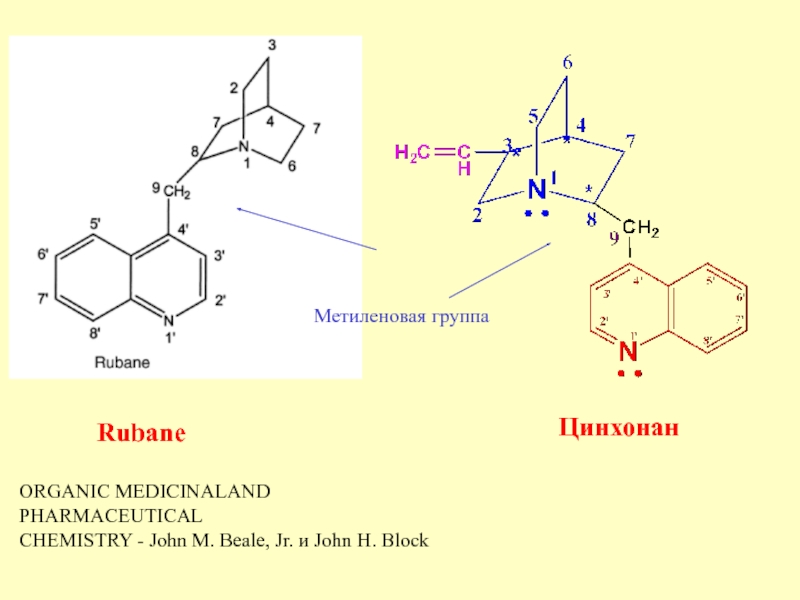
Слайд 11ORGANIC MEDICINALAND PHARMACEUTICAL
CHEMISTRY - John M. Beale, Jr. и John
H. Block
Метиленовая группа
Rubane
Цинхонан
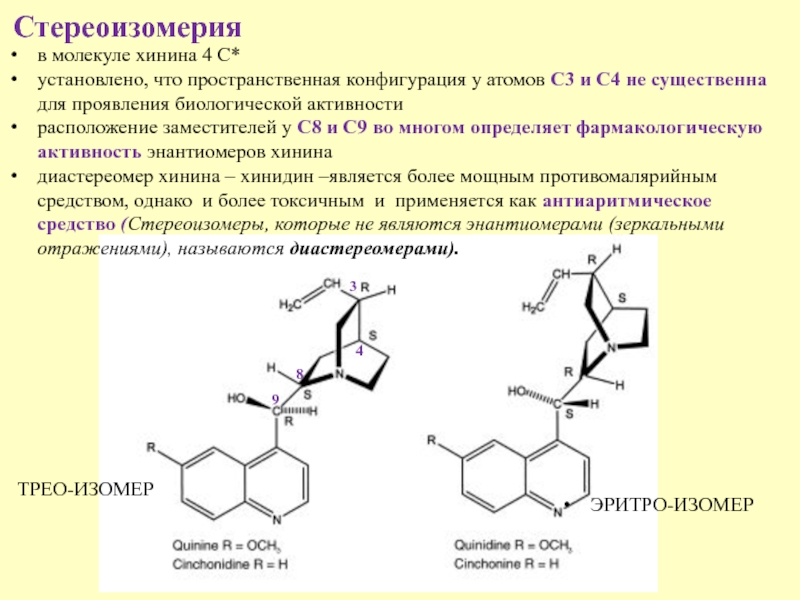
Слайд 12Стереоизомерия
9
8
4
в молекуле хинина 4 С*
установлено, что пространственная конфигурация у
атомов С3 и С4 не существенна для проявления биологической активности
расположение заместителей у С8 и С9 во многом определяет фармакологическую активность энантиомеров хинина
диастереомер хинина – хинидин –является более мощным противомалярийным средством, однако и более токсичным и применяется как антиаритмическое средство (Стереоизомеры, которые не являются энантиомерами (зеркальными отражениями), называются диастереомерами).
3
ТРЕО-ИЗОМЕР
ЭРИТРО-ИЗОМЕР
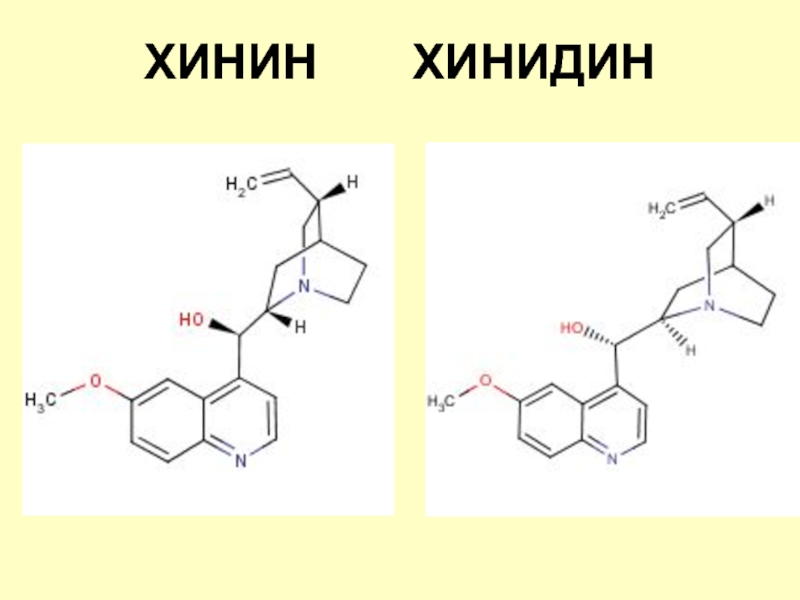
Слайд 14Хинин
Хинин - двукислотное основание,
образует два типа солей.
Центры оснóвности
рКВН+ хинуклидина=11,1
рКВН+ хинолина=4,9
Азот хинуклидинового
ядра –
более мощный основный центр
Слайд 15Хинина гидрохлорид
Chinini hydrochloridum
(R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил] (6-метоксихинолин-4-ил )метанол гидрохлорид
Хинина сульфат
Chinini sulfas
бис[(R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил](6-метоксихинолин-4-ил)метанол] сульфат
Белые или
почти белые, или бесцветные мелкие шелковистые иголочки, растворимы в воде,
растворим в горячей воде, легко растворимы в спирте. Противомалярийное средство.
Белый или почти белый кристаллический порошок, мало растворим в воде, умеренно растворим в кипящей воде и этаноле (96%).
Противомалярийное средство.
Слайд 16Хинина сульфат
Chinini sulfas
Противомалярийное средство
Хинидина сульфат
Chinidini sulfas
бис[(S)-[(2R,4S,5R)-5-этинил-1-азобицикло[
2.2.2]окт-2-ил](6-метоксихинолин-4-ил)
метанол] сульфат
Белый или почти белый
кристаллический порошок, мало растворим в воде, растворим в кипящей воде
и этаноле (96%), практически не растворим в ацетоне.
Антиаритмическое средство.
Слайд 17Европейская фармакопея Ph.Eur
Идентификация:
А: Хроматография в тонком слое (ТСХ)
в качестве неподвижной
фазы используют силикагель;
роль подвижной фазы играет смесь из раствора диэтиламина,
эфира и толуола (10:24:40);
тестируемый раствор и раствор сравнения готовят растворением 0,10 г вещества в метилового спирта;
хроматограмму облучают УФ-светом при длине волны 254 нм: пятно на хроматограмме, соответствующее определяемому веществу должно быть идентично по положению и размеру пятну стандартного вещества (Ph.Eur).
Rf = a/b
а- расстояние, пройденное веществом от точки нанесения пробы до центра пятна;
b- расстояние, пройденное элюентом от точки нанесения пробы до фронта элюента
Слайд 18Идентификация:
В: Таллеохинная проба
С. Синяя флуоресценция сернокислого р-ра соли хинина при
облучении УФ-светом при 366 нм, которая исчезает при добавлении 1
мл р-ра HCl.
D: Реакция на ионы Cl-, SO42-
С: взаимодействие с раствором КI в I2 (общеалкалоидный реактив) – в кислой среде выделяется осадок коричневого цвета. При нейтрализации раствором NaOH осадок растворяется.
D: рН водных р-ов солей: Хинидина сульфат и Хинина хлорид (6,0-6,8); Хинина сульфат рН 5,7-6,6
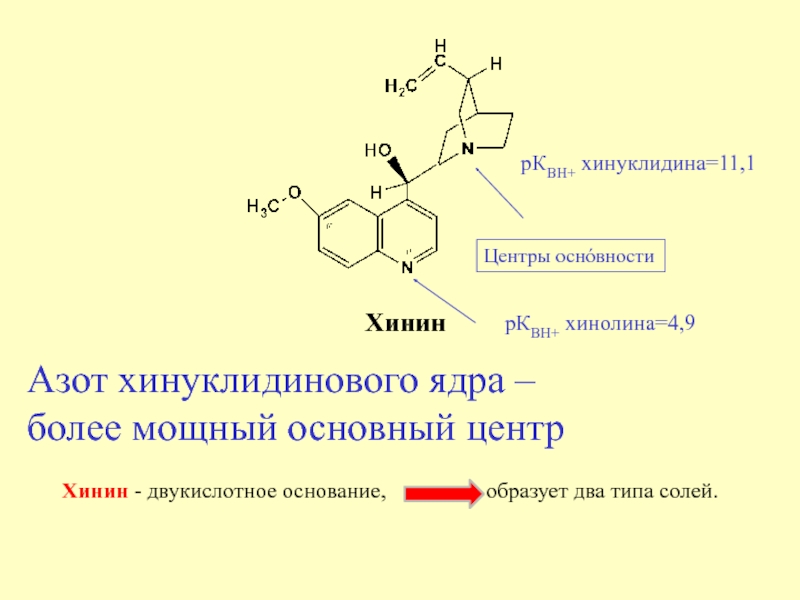
Слайд 19Талейохинная проба
Алкалоиды, не имеющие заместителей в 6'-положении хинолинового цикла,
в эту реакцию не вступают.
Методика: 10 мг субстанции растворяют
в 10 мл воды. К 5мл полученного раствора добавляют 0,2мл бромной воды и 1мл раствора аммиака. Появляется зеленое окрашивание.
В основе талейохинной пробы лежат реакции: окисления, галогенирования, гидратации, изомеризации и конденсации с аммиаком
Стадии 1-4 – Окисление – бромирование – гидратация - изомеризация
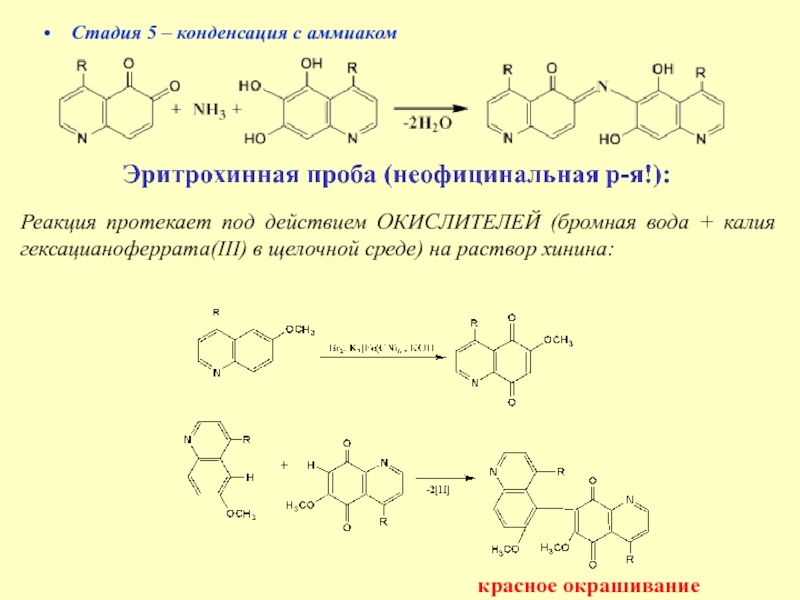
Слайд 20Стадия 5 – конденсация с аммиаком
Реакция протекает
под действием ОКИСЛИТЕЛЕЙ (бромная вода + калия гексацианоферрата(III) в щелочной среде) на раствор хинина:
красное окрашивание
Слайд 21Методы количественного анализа
Гравиметрия. Проводят по основанию, выделяемому из раствора соли
при добавлении раствора натрия гидроксида.
Алкалиметрия в водно-спиртовой среде
Метод неводного титрования:
навеску высушенной до постоянной массы субстанции растворить в хлороформе и добавить уксусный ангидрид. Титровать
0,1 моль/л р-ом HClO4, определяя конец титрования потенциометрически:
Слайд 22
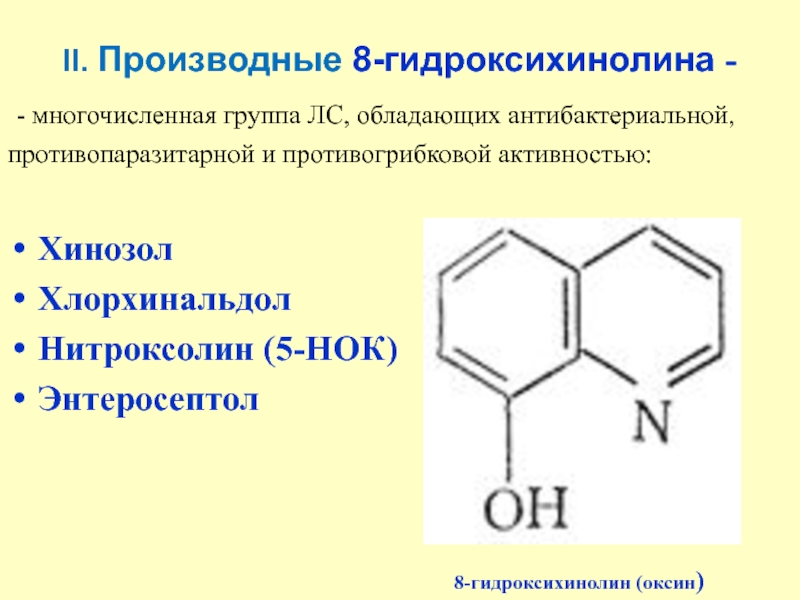
II. Производные 8-гидроксихинолина -
- многочисленная группа ЛС, обладающих
антибактериальной,
противопаразитарной и противогрибковой активностью:
Хинозол
Хлорхинальдол
Нитроксолин (5-НОК)
Энтеросептол
8-гидроксихинолин (оксин)
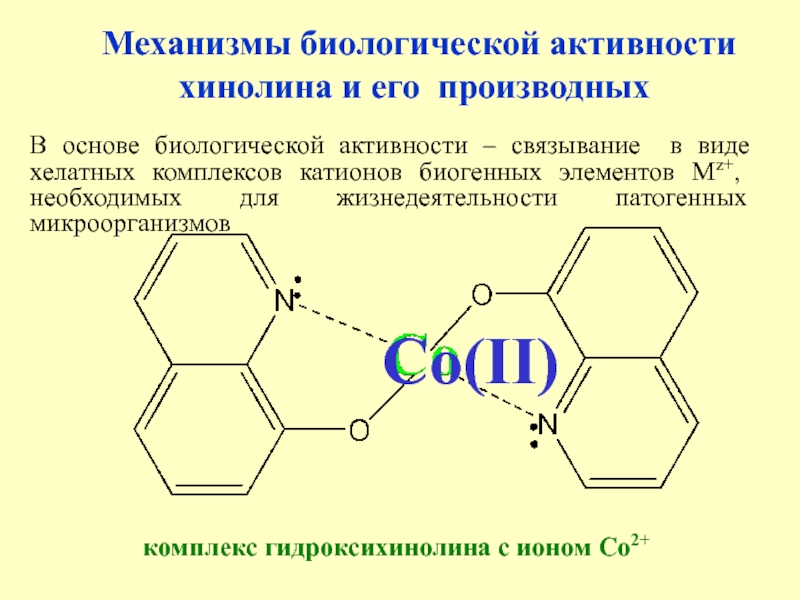
Слайд 23 Механизмы биологической активности хинолина и его производных
В основе
биологической активности – связывание в виде хелатных комплексов катионов биогенных
элементов Мz+, необходимых для жизнедеятельности патогенных микроорганизмов
комплекс гидроксихинолина с ионом Co2+
Сo(II)
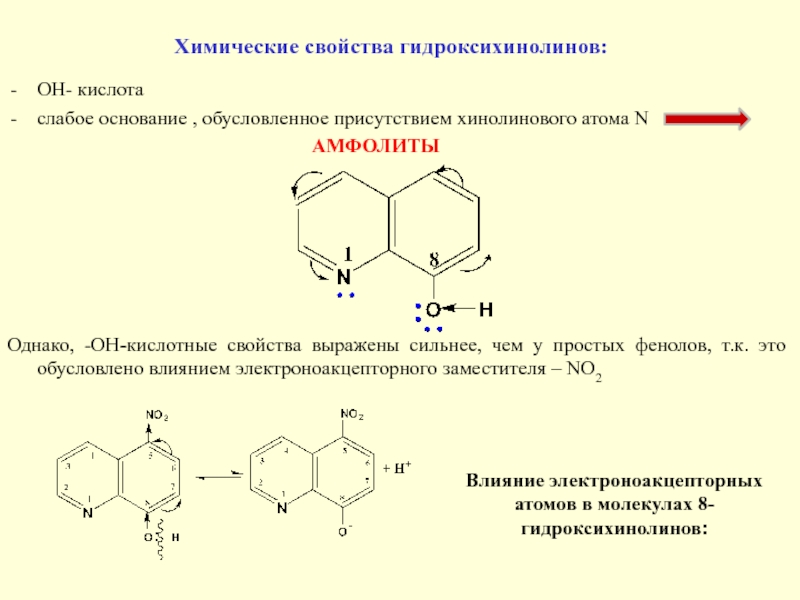
Слайд 24Химические свойства гидроксихинолинов:
OH- кислота
слабое основание , обусловленное присутствием хинолинового атома
N
АМФОЛИТЫ
Однако, -ОН-кислотные свойства выражены сильнее, чем у простых фенолов, т.к. это обусловлено влиянием электроноакцепторного заместителя – NO2
Влияние электроноакцепторных атомов в молекулах 8-гидроксихинолинов:
Слайд 25
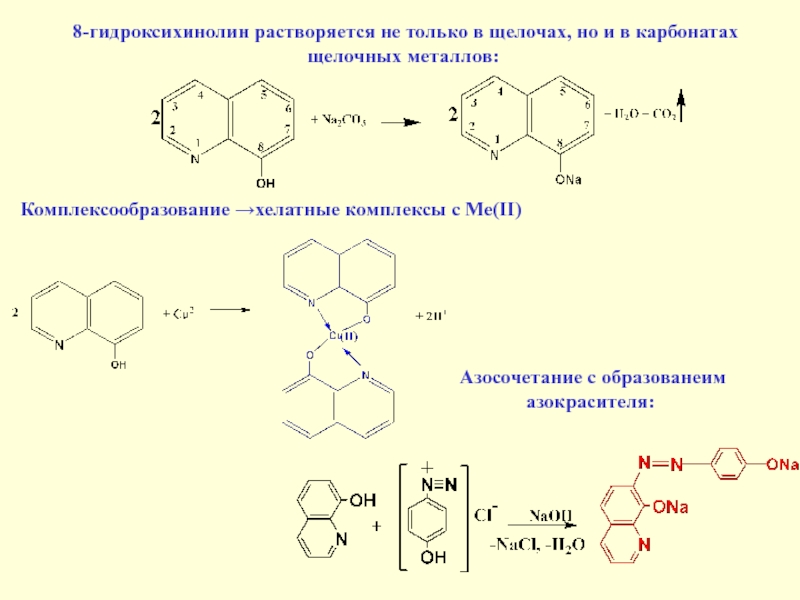
8-гидроксихинолин растворяется не только в щелочах, но и
в карбонатах щелочных металлов:
Комплексообразование →хелатные комплексы с Ме(II)
Азосочетание
с образованеим азокрасителя:
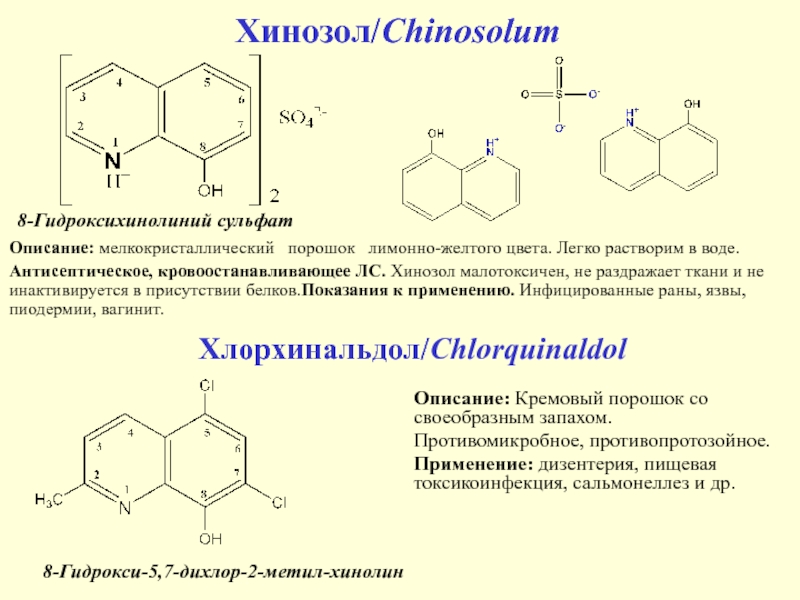
Слайд 26Хинозол/Chinosolum
Описание: мелкокристаллический порошок лимонно-желтого цвета. Легко растворим в
воде.
Антисептическое, кровоостанавливающее ЛС. Хинозол малотоксичен, не раздражает ткани и не
инактивируется в присутствии белков.Показания к применению. Инфицированные раны, язвы, пиодермии, вагинит.
8-Гидроксихинолиний сульфат
Хлорхинальдол/Chlorquinaldol
8-Гидрокси-5,7-дихлор-2-метил-хинолин
Описание: Кремовый порошок со своеобразным запахом.
Противомикробное, противопротозойное.
Применение: дизентерия, пищевая токсикоинфекция, сальмонеллез и др.
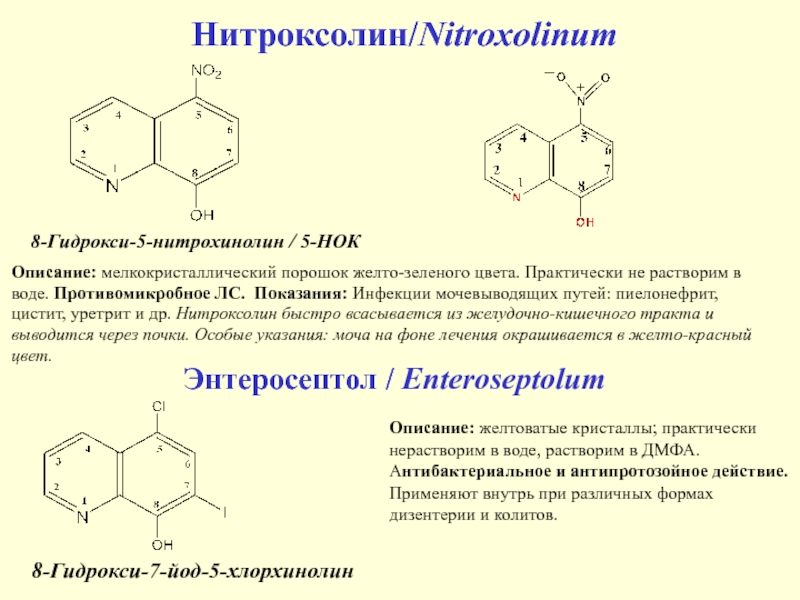
Слайд 27 Нитроксолин/Nitroxolinum
Описание: мелкокристаллический порошок желто-зеленого цвета. Практически не растворим в
воде.
Противомикробное ЛС. Показания: Инфекции мочевыводящих путей: пиелонефрит,
цистит, уретрит и др.
Нитроксолин быстро всасывается из желудочно-кишечного тракта и
выводится через почки. Особые указания: моча на фоне лечения окрашивается в желто-красный
цвет.
8-Гидрокси-5-нитрохинолин / 5-НОК
Энтеросептол / Enteroseptolum
8-Гидрокси-7-йод-5-хлорхинолин
Описание: желтоватые кристаллы; практически нерастворим в воде, растворим в ДМФА. Антибактериальное и антипротозойное действие. Применяют внутрь при различных формах дизентерии и колитов.
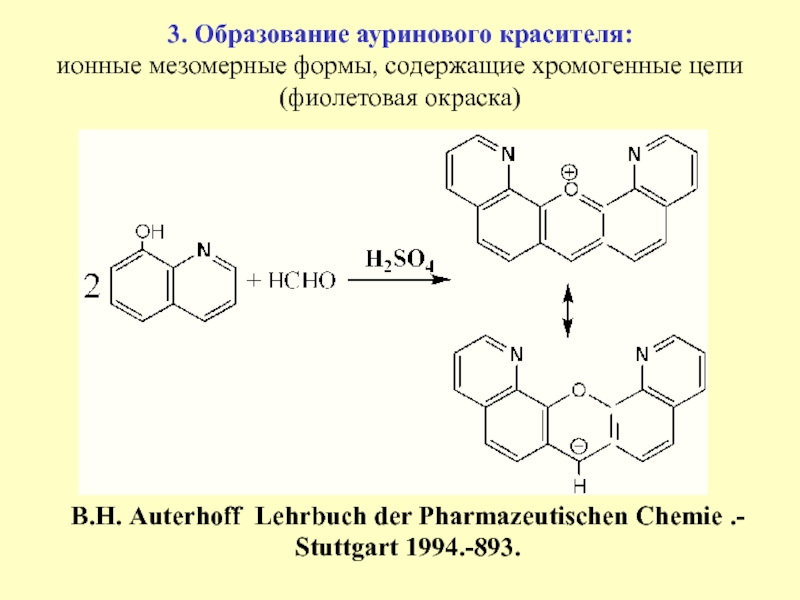
Слайд 283. Образование ауринового красителя:
ионные мезомерные формы, содержащие хромогенные цепи
(фиолетовая окраска)
B.Н. Auterhoff Lehrbuch der Pharmazeutischen Chemie .- Stuttgart 1994.-893.
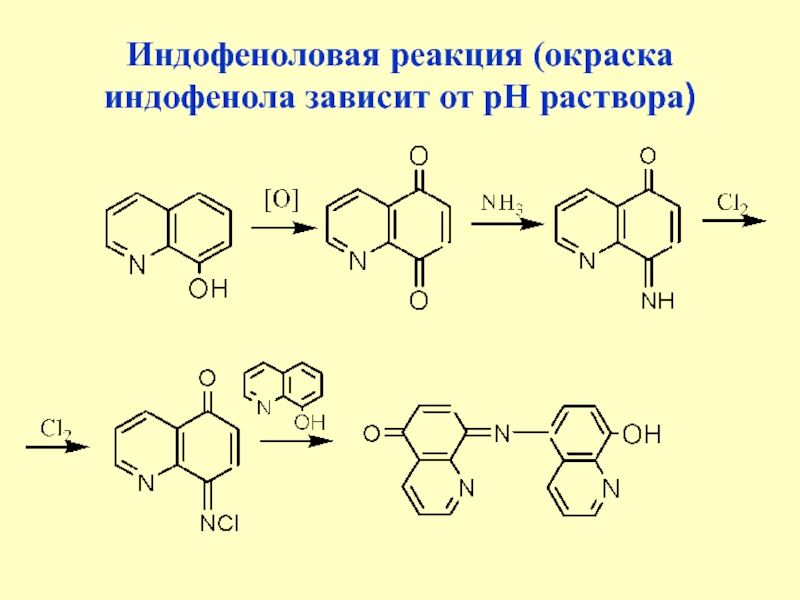
Слайд 29Индофеноловая реакция (окраска индофенола зависит от рН раствора)
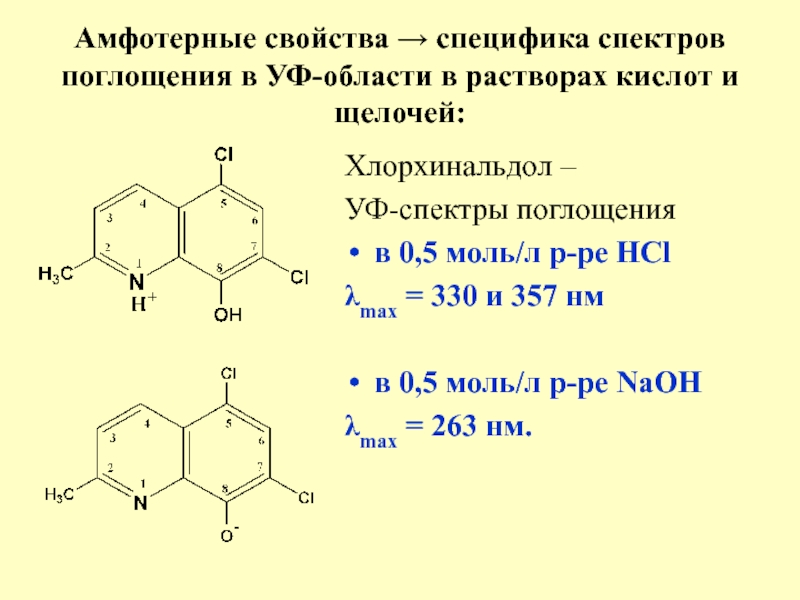
Слайд 30Амфотерные свойства → специфика спектров поглощения в УФ-области в растворах
кислот и щелочей:
Хлорхинальдол –
УФ-спектры поглощения
в 0,5 моль/л
р-ре HCl
λmax = 330 и 357 нм
в 0,5 моль/л р-ре NaOH
λmax = 263 нм.
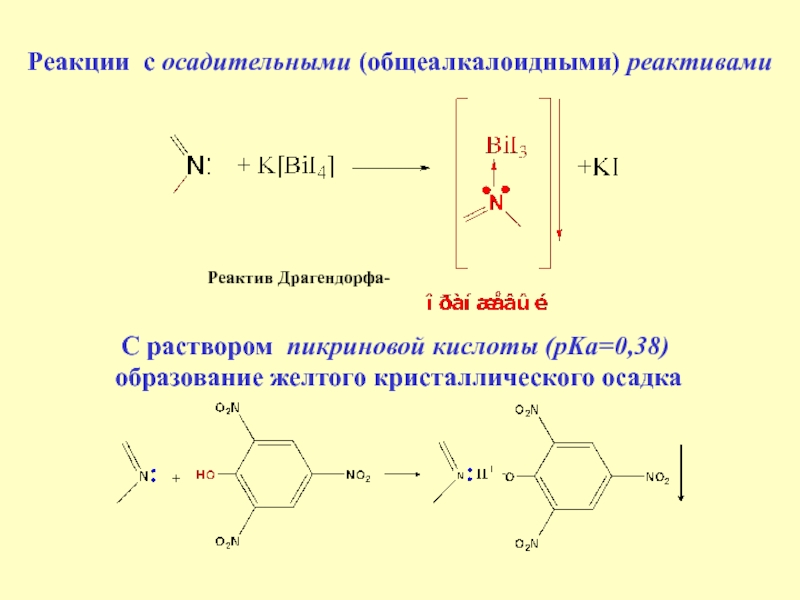
Слайд 31Реакции с осадительными (общеалкалоидными) реактивами
Реактив Драгендорфа-
С раствором пикриновой кислоты
(pKa=0,38)
образование желтого кристаллического осадка
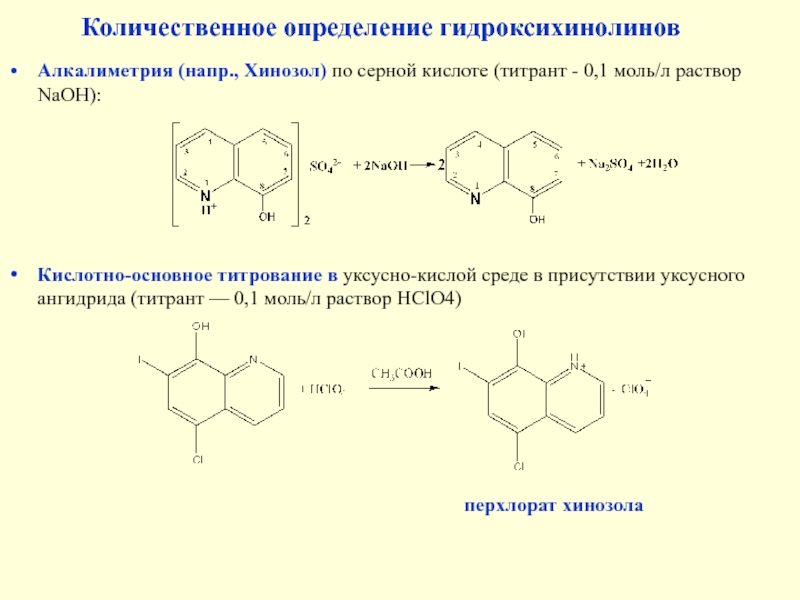
Слайд 32Алкалиметрия (напр., Хинозол) по серной кислоте (титрант - 0,1 моль/л
раствор NaOH):
Количественное определение гидроксихинолинов
Кислотно-основное титрование в уксусно-кислой среде в
присутствии уксусного ангидрида (титрант — 0,1 моль/л раствор HClO4)
перхлорат хинозола
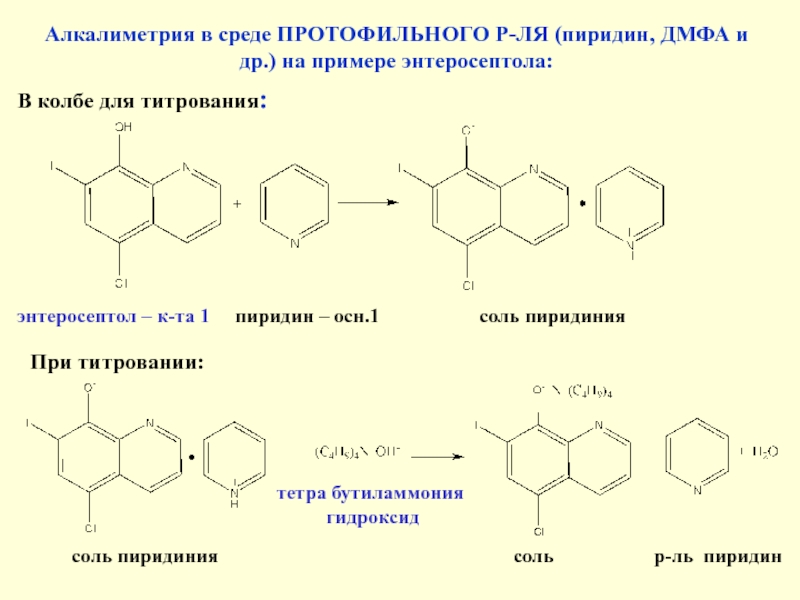
Слайд 33Алкалиметрия в среде ПРОТОФИЛЬНОГО Р-ЛЯ (пиридин, ДМФА и др.) на
примере энтеросептола:
В колбе для титрования:
энтеросептол – к-та 1
пиридин – осн.1 соль пиридиния
При титровании:
соль пиридиния соль р-ль пиридин
тетра бутиламмония
гидроксид
Слайд 34
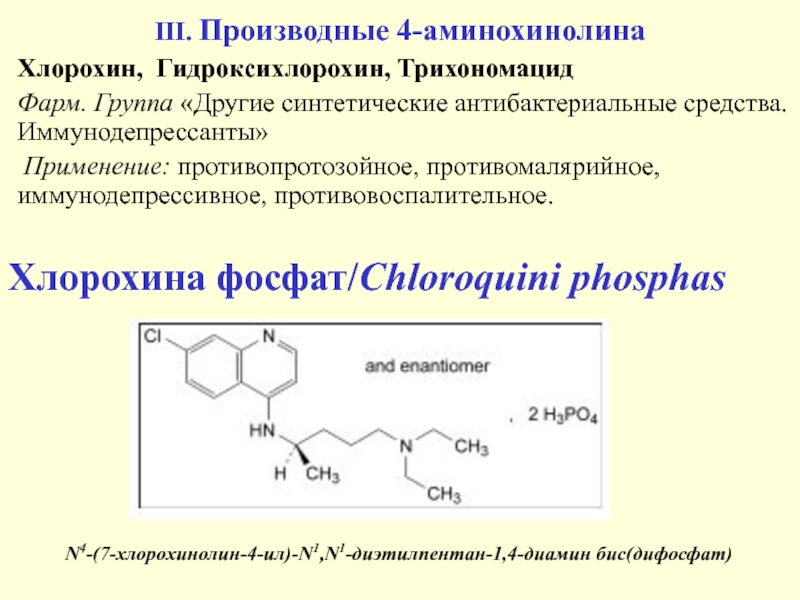
III. Производные 4-аминохинолина
Хлорохин, Гидроксихлорохин, Трихономацид
Фарм. Группа «Другие синтетические антибактериальные средства.
Иммунодепрессанты»
Применение: противопротозойное, противомалярийное, иммунодепрессивное, противовоспалительное.
N4-(7-хлорохинолин-4-ил)-N1,N1-диэтилпентан-1,4-диамин бис(дифосфат)
Хлорохина фосфат/Chloroquini
phosphas
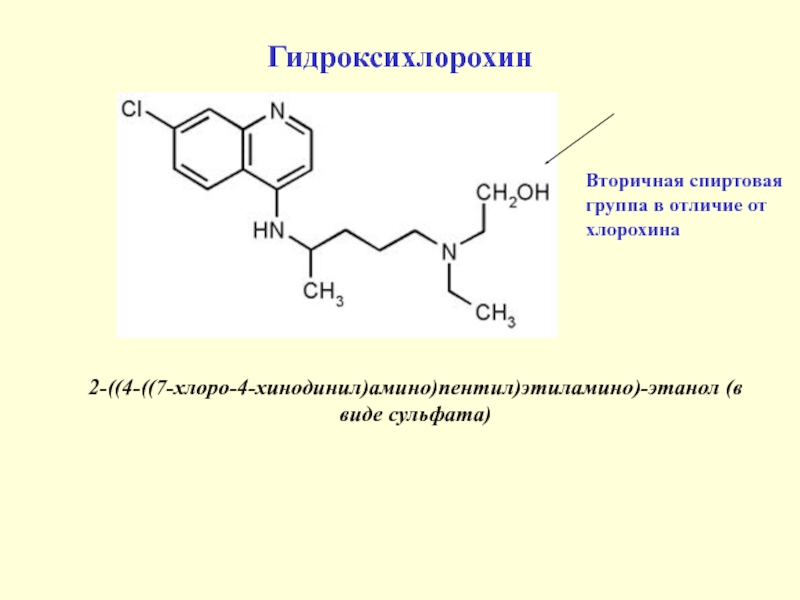
Слайд 35Гидроксихлорохин
2-((4-((7-хлоро-4-хинодинил)амино)пентил)этиламино)-этанол (в виде сульфата)
Вторичная спиртовая
группа в отличие от
хлорохина
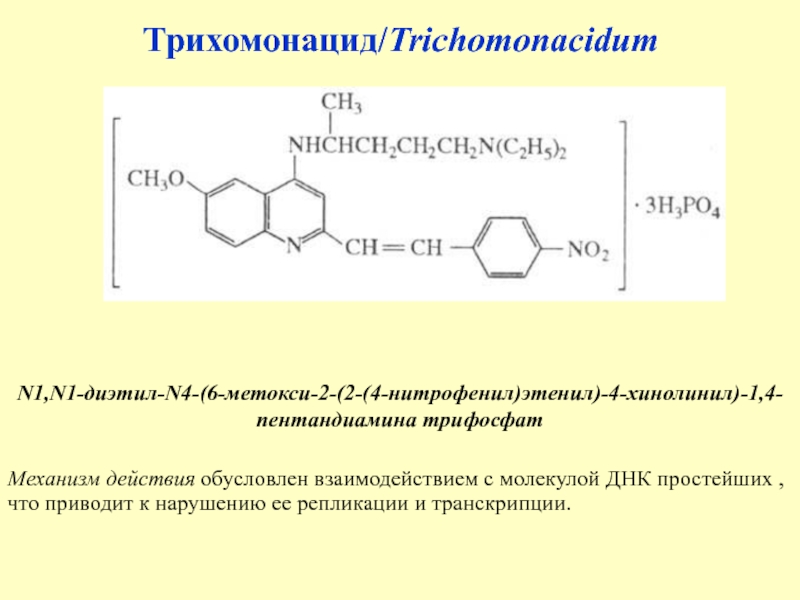
Слайд 36Трихомонацид/Trichomonacidum
N1,N1-диэтил-N4-(6-метокси-2-(2-(4-нитрофенил)этенил)-4-хинолинил)-1,4-пентандиамина трифосфат
Механизм действия обусловлен взаимодействием с молекулой ДНК
простейших , что приводит к нарушению ее репликации и транскрипции.
Слайд 37Особенности анализа качества:
Существует в 2-х кристаллических формах: Тпл = 198
0С и Тпл = 215 0С.
ИК-спектр раствора в хлороформе.
Нейтрализовать фосфорную
кислоту раствором щелочи; экстрагировать основание хлороформом; раствор подкислить азотной кислотой и провести реакцию на фосфаты.
Несколько специфических полос поглощения в УФ- области спектра: λmax = 257, 329 и 343 нм
Осадок с пикриновой кислотой, промытый водой, спиртом и эфиром, имеет Тпл = 206-2090С.
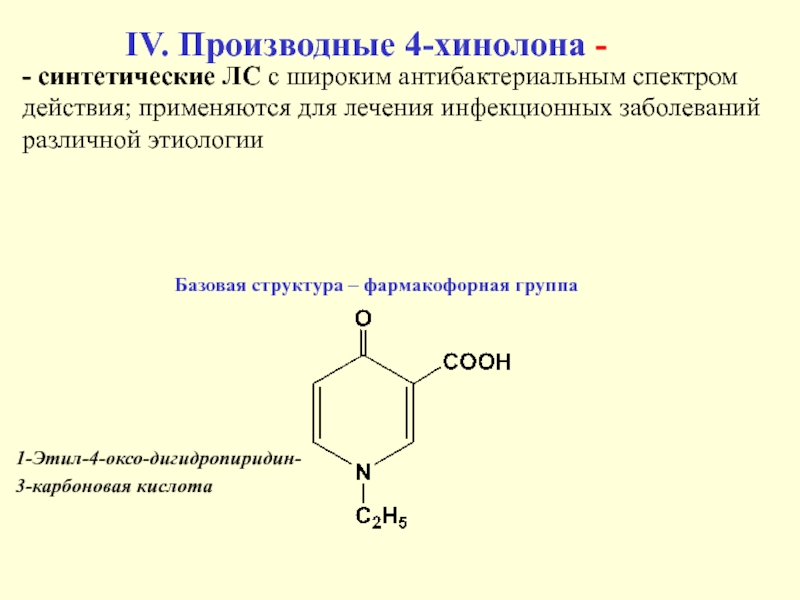
Слайд 38IV. Производные 4-хинолона -
Базовая структура – фармакофорная группа
1-Этил-4-оксо-дигидропиридин-
3-карбоновая
кислота
- синтетические ЛС с широким антибактериальным спектром действия; применяются для
лечения инфекционных заболеваний различной этиологии
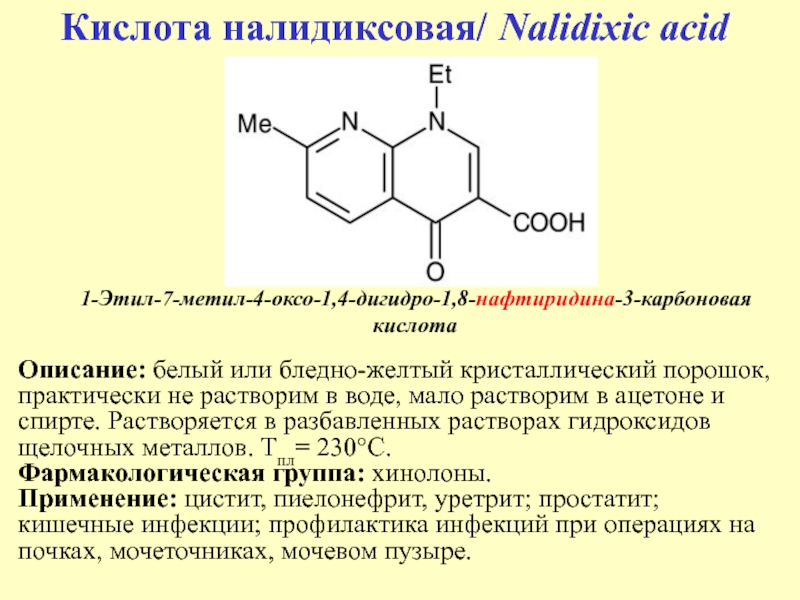
Слайд 401-Этил-7-метил-4-оксо-1,4-дигидро-1,8-нафтиридина-3-карбоновая кислота
Кислота налидиксовая/ Nalidixic acid
Описание: белый или бледно-желтый кристаллический
порошок, практически не растворим в воде, мало растворим в ацетоне
и спирте. Растворяется в разбавленных растворах гидроксидов щелочных металлов. Тпл= 230°C.
Фармакологическая группа: хинолоны.
Применение: цистит, пиелонефрит, уретрит; простатит; кишечные инфекции; профилактика инфекций при операциях на почках, мочеточниках, мочевом пузыре.
Слайд 41Определение подлинности
ИК-спектрометрия (Сравнить спектр с ИК-спектром СRS (Chemicаl Reference Substance)
Налидиксовой кислоты).
Хроматография в тонком слое (ТСХ)
Основное пятно по положению
и размеру должно быть идентично
пятну для раствора сравнения.
Растворить 0,1 г субстанции в 2 мл HCl. Добавить 0,5 мл 10%
раствора β-нафтола в спирте. Появляется оранжево-красная окраска.
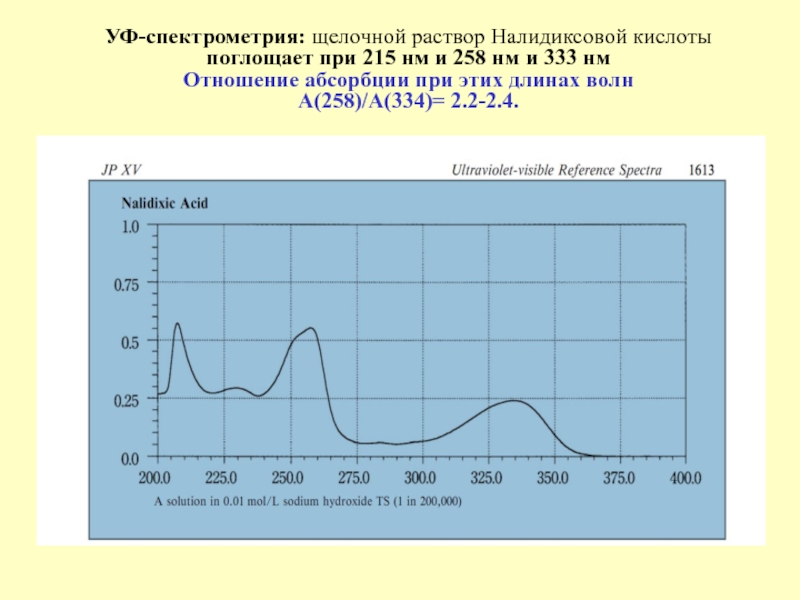
Слайд 42УФ-спектрометрия: щелочной раствор Налидиксовой кислоты
поглощает при 215 нм и
258 нм и 333 нм
Отношение абсорбции при этих длинах
волн
А(258)/А(334)= 2.2-2.4.
Слайд 43Кислота оксолиниевая/Acidum oxolinicum
5-этил-8-оксо-5,8-дигидро-1,3-диоксоло[4,5-g]-хинолин- 7-карбоновая кислота
Описание: белый или желтоватый кристаллический
порошок,
практически нерастворим в воде и спирте. Растворим в разб. растворах
щелочей.
Подлинность: ИК-, УФ-СФ; ТСХ
Количественное определение: алкалиметрия в среде ДМФА
0,1 моль/л раствором N(C4H9)4OH.
Применение: По антибактериальному спектру действия кислота
оксолиниевая существенно не отличается от налидиксовой кислоты.
(НЕ ПУТАТЬ С ОКСОЛИНОВОЙ КИСЛОТОЙ – ПРОИЗВОДНЫМ АМАНТАДИНА!)
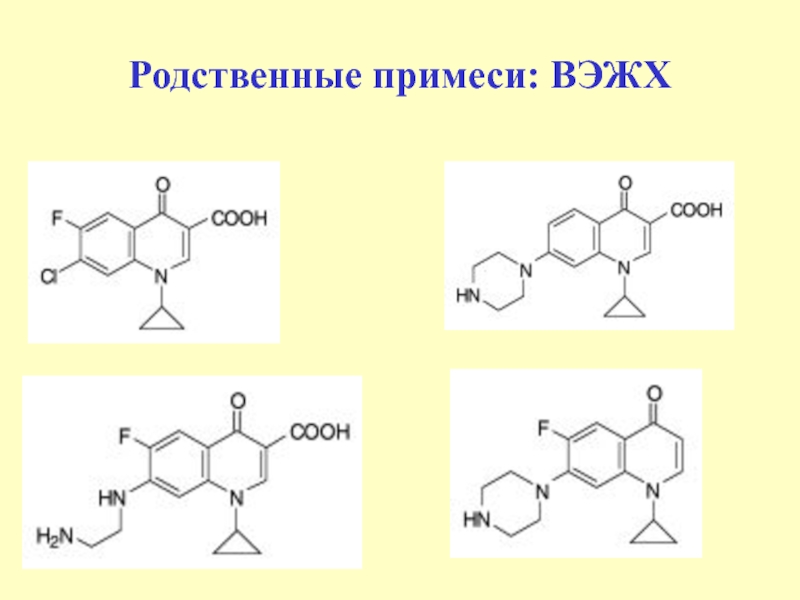
Слайд 44– производные 4-хинолона, содержащие в положении С7 хинолинового ядра незамещенный
или замещенный пиперазиновый цикл, а в положении С6 – атом
F
ЛС этой группы (Офлоксацин, Ципрофлоксацин, Ломефлоксацин, Норфлоксацин и др.) - бактерицидные средства, активные в отношении аэробных грамотрицательных бактерий
Фторхинолоны
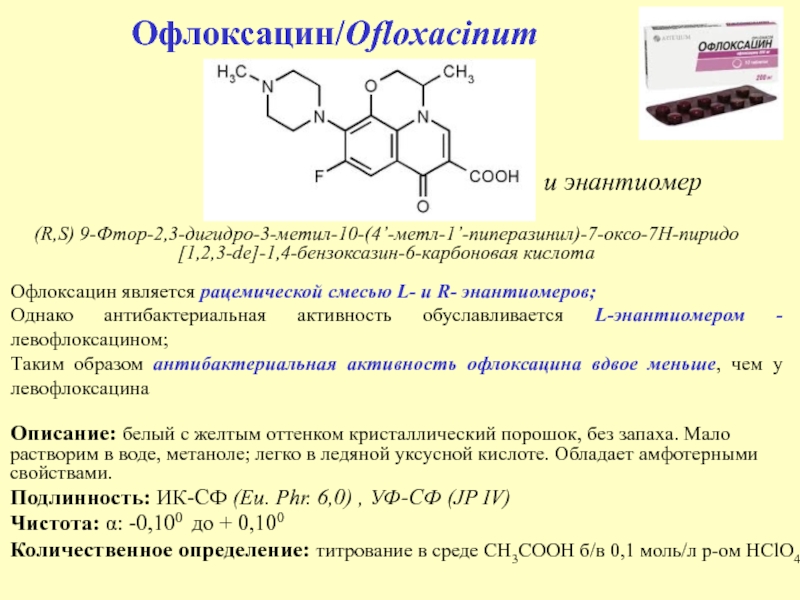
Слайд 46Офлоксацин/Ofloxacinum
Описание: белый с желтым оттенком кристаллический порошок, без запаха. Мало
растворим в воде, метаноле; легко в ледяной уксусной кислоте. Обладает
амфотерными свойствами.
Подлинность: ИК-СФ (Eu. Phr. 6,0) , УФ-СФ (JP IV)
Чистота: α: -0,100 до + 0,100
Количественное определение: титрование в среде CH3COOH б/в 0,1 моль/л р-ом HClO4
(R,S) 9-Фтор-2,3-дигидро-3-метил-10-(4’-метл-1’-пиперазинил)-7-оксо-7Н-пиридо[1,2,3-de]-1,4-бензоксазин-6-карбоновая кислота
и энантиомер
Офлоксацин является рацемической смесью L- и R- энантиомеров;
Однако антибактериальная активность обуславливается L-энантиомером - левофлоксацином;
Таким образом антибактериальная активность офлоксацина вдвое меньше, чем у левофлоксацина
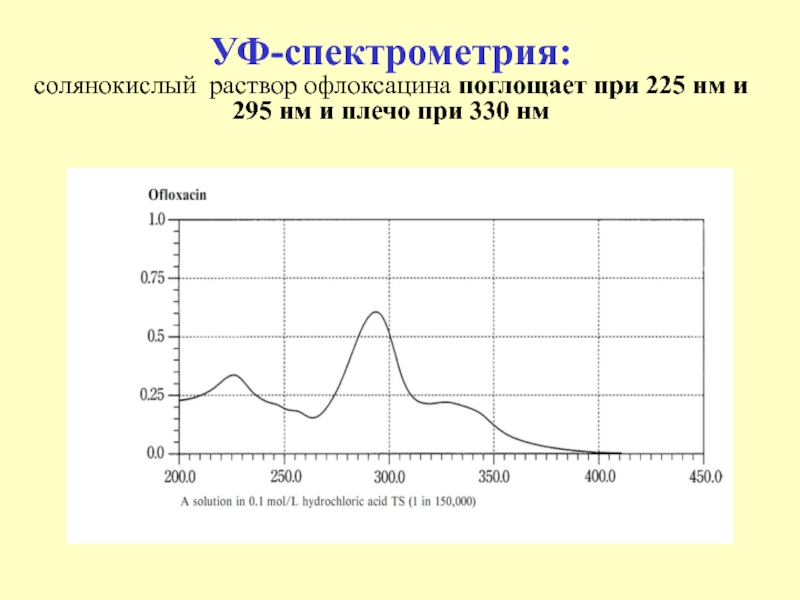
Слайд 47УФ-спектрометрия:
солянокислый раствор офлоксацина поглощает при 225 нм и 295
нм и плечо при 330 нм
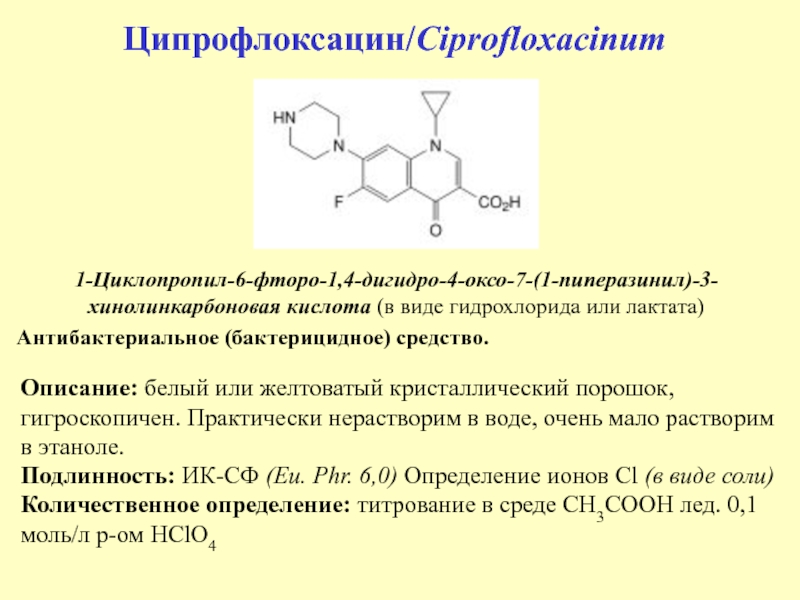
Слайд 48Ципрофлоксацин/Ciprofloxacinum
1-Циклопропил-6-фторо-1,4-дигидро-4-оксо-7-(1-пиперазинил)-3-хинолинкарбоновая кислота (в виде гидрохлорида или лактата)
Антибактериальное (бактерицидное) средство.
Описание:
белый или желтоватый кристаллический порошок, гигроскопичен. Практически нерастворим в воде,
очень мало растворим в этаноле.
Подлинность: ИК-СФ (Eu. Phr. 6,0) Определение ионов Cl (в виде соли)
Количественное определение: титрование в среде CH3COOH лед. 0,1 моль/л р-ом HClO4
Слайд 49Испытания на чистоту
Растворить 0,25 г субстанции в 0,1 моль/л хлороводородной
кислоты, довести объем до 20 мл. раствор должен быть прозрачным
и интенсивность окраски не должна не должна превышать раствор сравнения
Фторхинолоновую кислоту (примесь) обнаруживают методом ТСХ (флуоресцентная индикация при 254 нм).
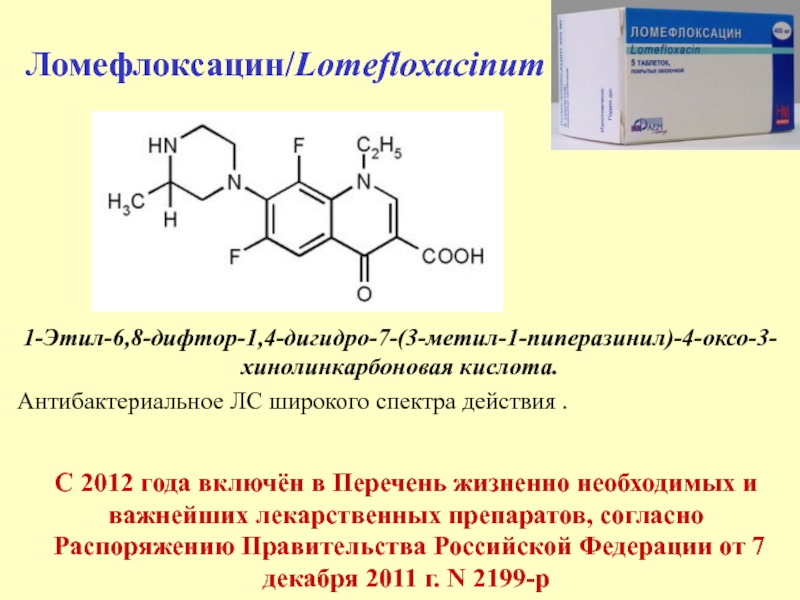
Слайд 51Ломефлоксацин/Lomefloxacinum
1-Этил-6,8-дифтор-1,4-дигидро-7-(3-метил-1-пиперазинил)-4-оксо-3-хинолинкарбоновая кислота.
Антибактериальное ЛС широкого спектра действия .
С 2012 года
включён в Перечень жизненно необходимых и важнейших лекарственных препаратов, согласно
Распоряжению Правительства Российской Федерации от 7 декабря 2011 г. N 2199-р




![ЛЕКЦИЯ 2 Хинина гидрохлорид Chinini hydrochloridum (R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил] (6-метоксихинолин-4-ил )метанол гидрохлоридХинина сульфатChinini sulfasбис[(R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил](6-метоксихинолин-4-ил)метанол] сульфатБелые Хинина гидрохлорид Chinini hydrochloridum (R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил] (6-метоксихинолин-4-ил )метанол гидрохлоридХинина сульфатChinini sulfasбис[(R)-[(2S,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил](6-метоксихинолин-4-ил)метанол] сульфатБелые или почти белые, или бесцветные мелкие](/img/thumbs/8d461584d36e3a4c174dbbcc3ab2c58b-800x.jpg)
![ЛЕКЦИЯ 2 Хинина сульфатChinini sulfasПротивомалярийное средствоХинидина сульфатChinidini sulfasбис[(S)-[(2R,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил](6-метоксихинолин-4-ил)метанол] сульфатБелый или почти белый кристаллический Хинина сульфатChinini sulfasПротивомалярийное средствоХинидина сульфатChinidini sulfasбис[(S)-[(2R,4S,5R)-5-этинил-1-азобицикло[2.2.2]окт-2-ил](6-метоксихинолин-4-ил)метанол] сульфатБелый или почти белый кристаллический порошок, мало растворим в воде, растворим](/img/thumbs/673fcb5ae77db33875c099adaa95c759-800x.jpg)






![ЛЕКЦИЯ 2 Кислота оксолиниевая/Acidum oxolinicum 5-этил-8-оксо-5,8-дигидро-1,3-диоксоло[4,5-g]-хинолин- 7-карбоновая кислотаОписание: белый или желтоватый кристаллический порошок,практически Кислота оксолиниевая/Acidum oxolinicum 5-этил-8-оксо-5,8-дигидро-1,3-диоксоло[4,5-g]-хинолин- 7-карбоновая кислотаОписание: белый или желтоватый кристаллический порошок,практически нерастворим в воде и спирте.](/img/thumbs/b401d4f556291eaba69c4974c306044c-800x.jpg)