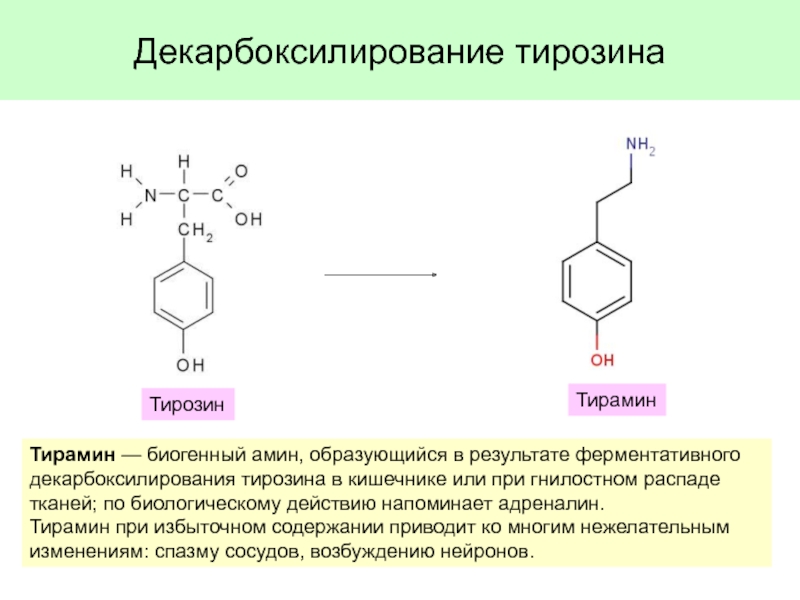
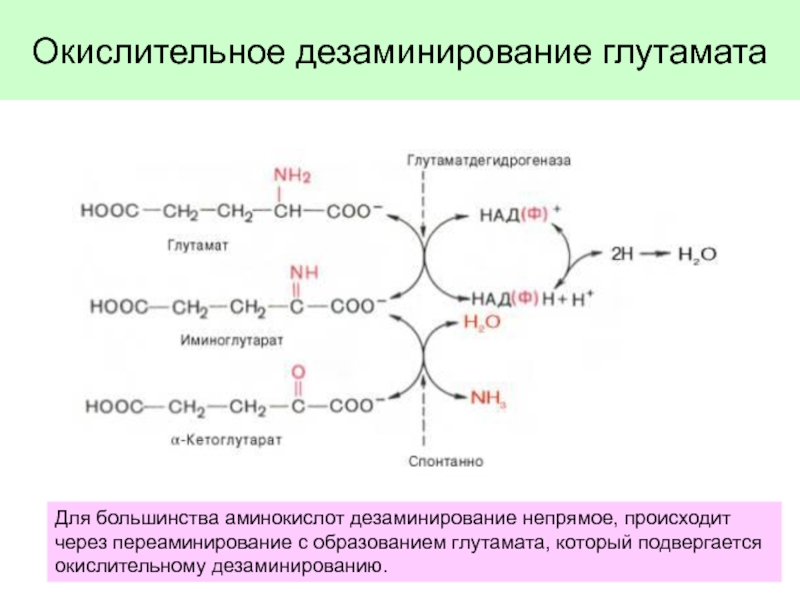
глутамата. Значение.
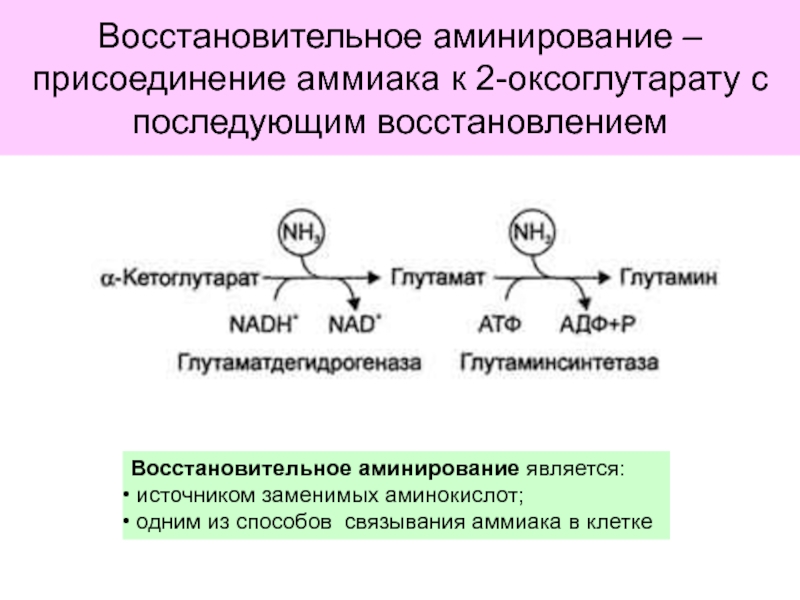
Восстановительное аминирование. Значение.
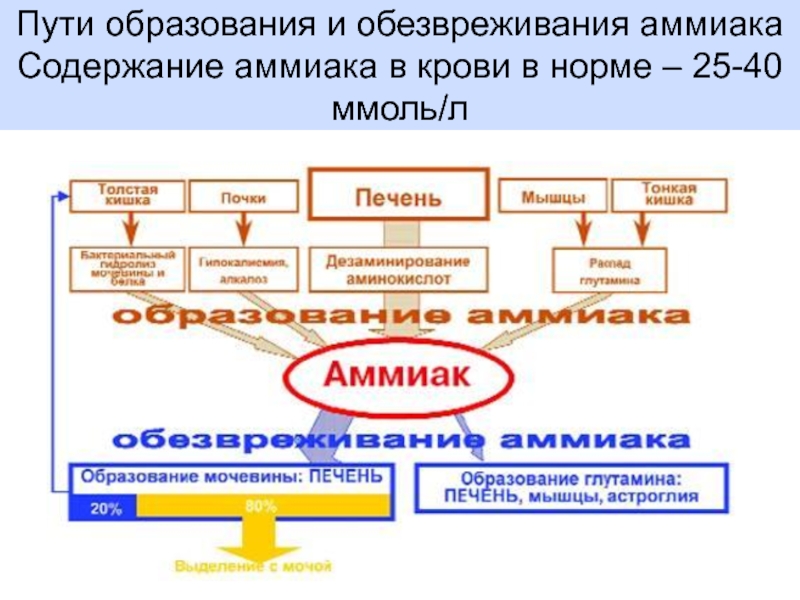
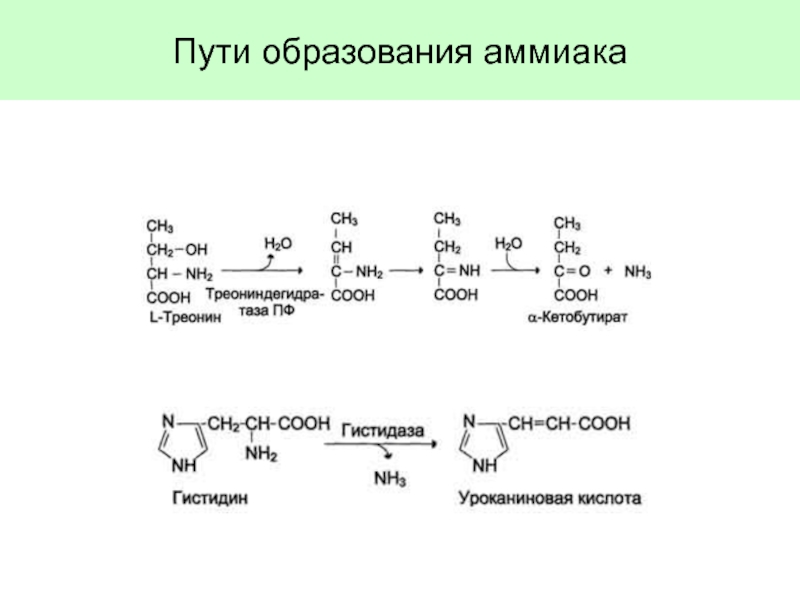
Источники аммиака в организме. Токсичность аммиака.
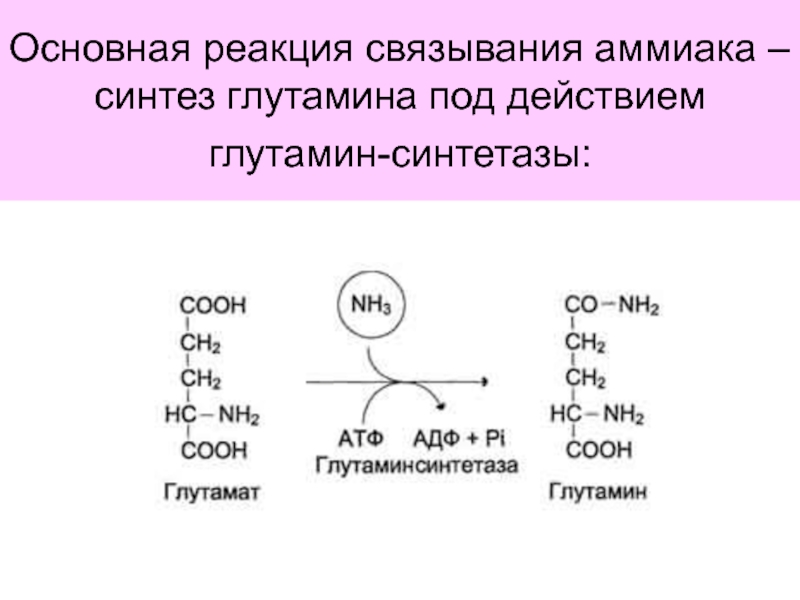
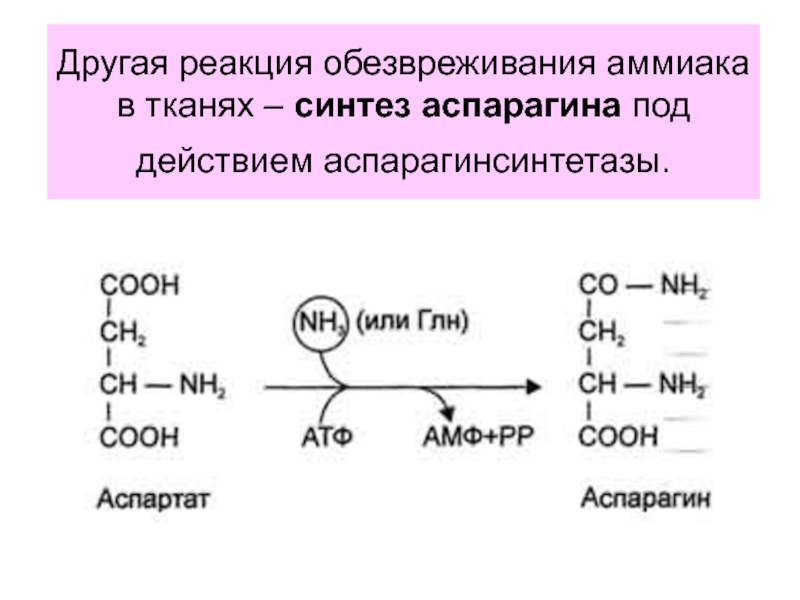
Пути обезвреживания
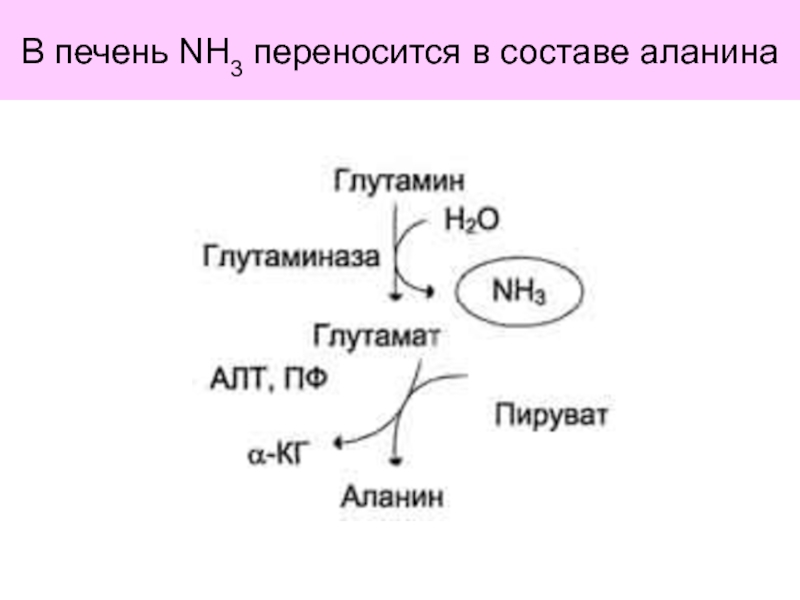
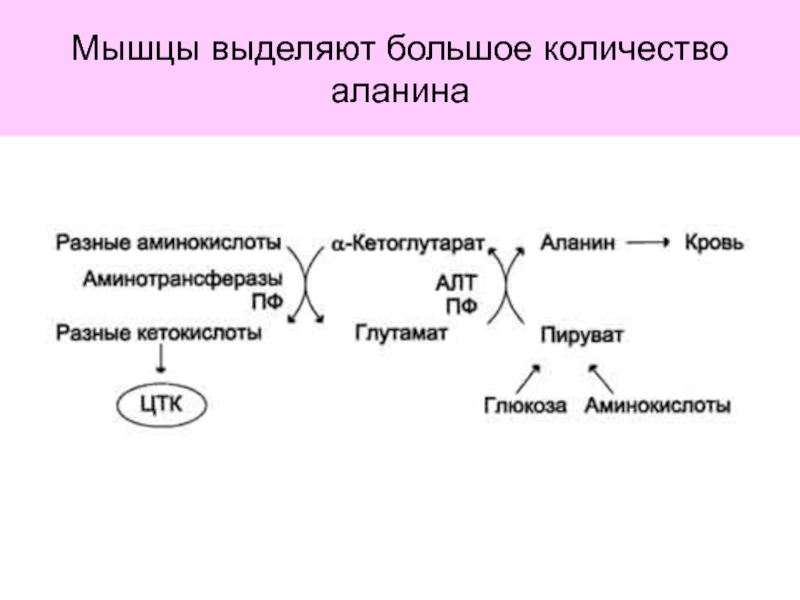
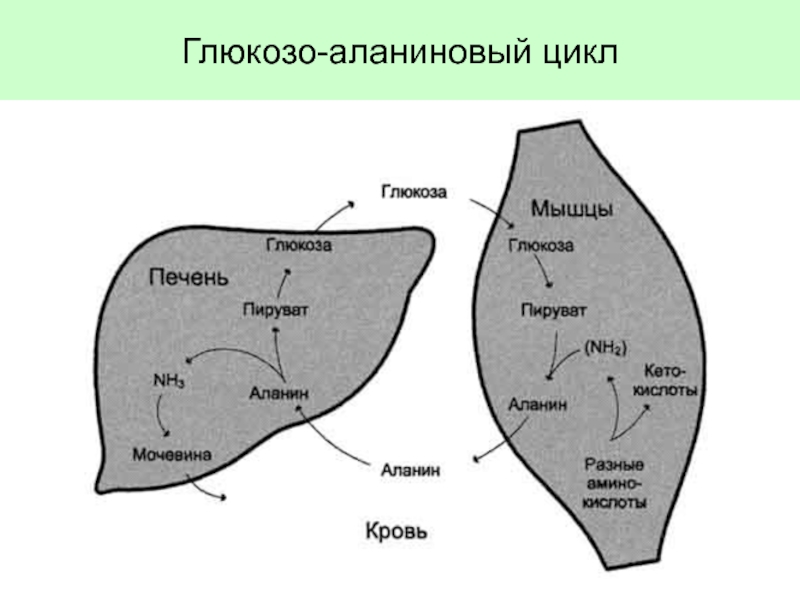
аммиака в клетке: аминирование глутамата и аспартата, восстановительное аминирование.Глюкозо-аланиновый цикл.