Слайд 1Лекция 3
Хромосомные
болезни человека
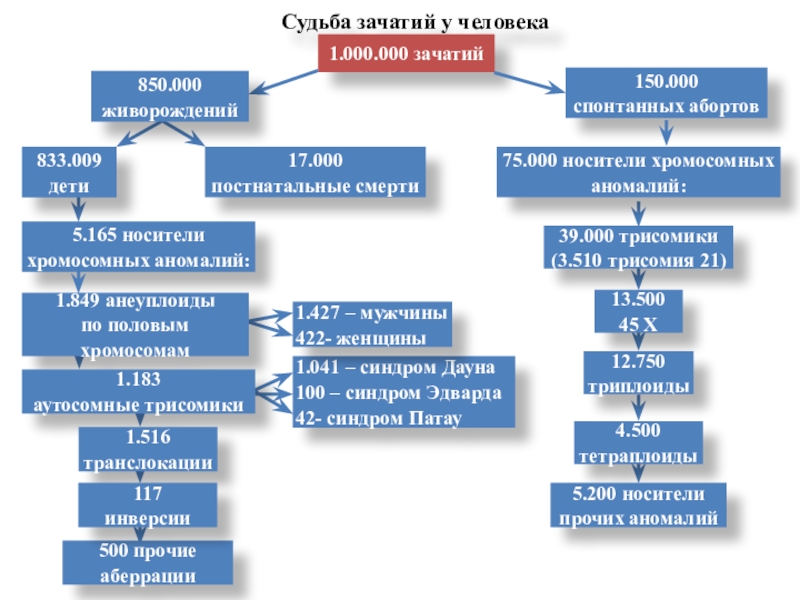
Слайд 2Судьба зачатий у человека
1.000.000 зачатий
150.000
спонтанных абортов
17.000
постнатальные смерти
5.165 носители хромосомных аномалий:
500
прочие аберрации
1.041 – синдром Дауна
100 – синдром Эдварда
42- синдром Патау
1.427
– мужчины
422- женщины
850.000
живорождений
833.009
дети
1.849 анеуплоиды
по половым хромосомам
1.183
аутосомные трисомики
1.516
транслокации
117
инверсии
75.000 носители хромосомных аномалий:
39.000 трисомики
(3.510 трисомия 21)
13.500
45 Х
12.750
триплоиды
4.500
тетраплоиды
5.200 носители
прочих аномалий
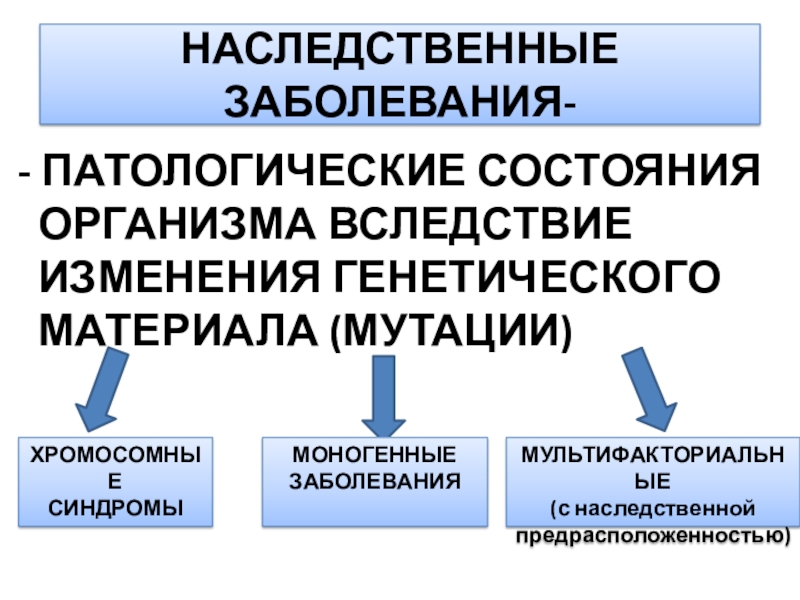
Слайд 3НАСЛЕДСТВЕННЫЕ ЗАБОЛЕВАНИЯ-
- ПАТОЛОГИЧЕСКИЕ СОСТОЯНИЯ ОРГАНИЗМА ВСЛЕДСТВИЕ ИЗМЕНЕНИЯ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА
(МУТАЦИИ)
ХРОМОСОМНЫЕ
СИНДРОМЫ
МОНОГЕННЫЕ
ЗАБОЛЕВАНИЯ
МУЛЬТИФАКТОРИАЛЬНЫЕ
(с наследственной предрасположенностью)
Слайд 4
ХРОМОСОМНЫЕ СИНДРОМЫ
Описано ≈ 1000 аномалий,
≈ 100 - доступно для
клинической диагностики
ПРИЧИНА: изменение количества и /или структуры хромосом (случайные мутации
– de novo).
Не наследуются!
Слайд 5ГЕНОМНЫЕ СИНДРОМЫ
(изменения числа хромосом)
ПРИЧИНА:
Нарушение мейоза у родителей (нерасхождение хромосом),
Дробление зиготы.
СТРУКТУРНЫЕ АБЕРРАЦИИ
(изменения структуры хромосомы)
Изменения числа аутосом
-с. Дауна,
-с. Патау,
-с. Эдвардса
и др.
Изменения числа половых хромосом
-с.Шерешевского- Тернера,
-с.Клайнфельтера,
-с.Трисомии -Х
-с.Кошачьего крика
(46, ХХ,5р-),
-с.Орбели
(46,ХУ,del.13р-)
РАЗЛИЧАЮТ:
Слайд 6Кеннеди, 10 лет (США)
Лучиано, 1 год (Аргентина)
http://www.woman.ru/kids/medley5/article/193151/?startLeaflet=2#8
Саира, 6 лет (Индия)
Джулианна,
13 лет (Германия)
Слайд 7Синдром Дауна
Трисомия 21
1 : 1000
Синдромом Дауна одинаково страдают и девочки
и мальчики, заболевание не имеет этнического распространения и встречается повсеместно.
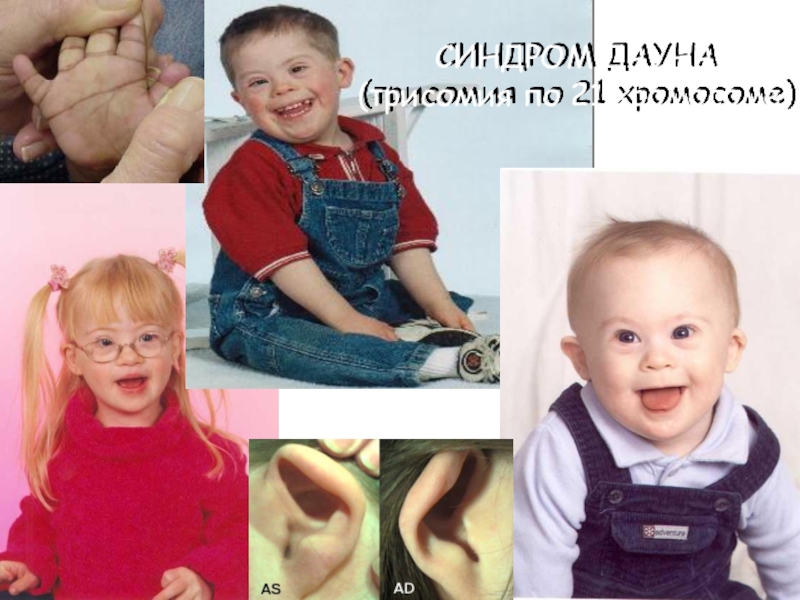
Слайд 8СИНДРОМ ДАУНА
(трисомия по 21 хромосоме)
Слайд 9Объект исследования: пуповинная кровь плода.
Кариотип плода: 47ХХ+21 (синдром Дауна)
Слайд 10Возраст будущей мамы влияет на риск развития синдрома Дауна у
ребенка, вероятность формирования данной патологии составляет :
от 20 до
24 лет – 1 : 1562;
25-35 лет – 1 : 1000;
35-39 лет – 1 : 214;
старше 45 лет риск увеличивается до 1 : 19.
Возраст отца на риск рождения влияет после 42 лет.
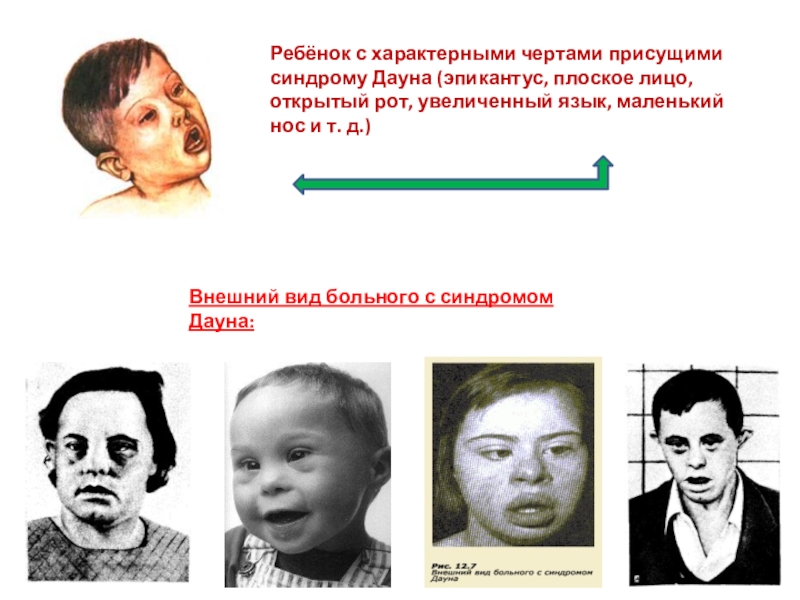
Слайд 11Ребёнок с характерными чертами присущими синдрому Дауна (эпикантус, плоское лицо,
открытый рот, увеличенный язык, маленький нос и т. д.)
Внешний вид
больного с синдромом Дауна:
Слайд 12Диагностика синдрома Дауна в первом триместре –комбинированный скрининг-анализ, определяющий риск
развития этой патологии у плода.
Исследование проводится строго в период
от 11 до 13 недель и 6 дней беременности.
1. Определение уровня β-субъединицы хорионического гонадотропина (гормона беременности ХГЧ) в венозной крови матери. При данной хромосомной патологии плода будет определяться повышенный уровень β-субъединицы ХГ более 2 МоМ;
2. Определение уровня РАРР-А — протеина-А плазмы крови беременной, ассоциированного с беременностью. Высокий риск синдрома сопряжен с показателем РАРР-А менее 0,5 МоМ;
3. Определение толщины воротникового пространства при помощи УЗИ плода. При синдроме Дауна этот показатель превышает 3 мм.
При сочетании трех описанных показателей вероятность синдрома Дауна у плода составляет 86%.
Слайд 13Диагностику синдрома Дауна во втором триместре проводят между 16 и
18 неделями.
Определение уровня ХГЧ в крови беременной – при
синдроме Дауна показатель выше 2 МоМ;
Определение уровня а-фетопротеина в крови беременной (АФП) – при синдроме Дауна показатель менее 0,5 МоМ;
Определение свободного эстриола в крови – показатель менее 0,5 МоМ характерен для синдрома Дауна;
Определение ингибина А в крови женщины – показатель более 2 МоМ характерен для синдрома Дауна;
УЗИ плода:
А) меньшие размеры плода относительно нормы для срока 16-18 недель;
Б) укорочение либо отсутствие носовой кости у плода;
В) уменьшение размеров верхней челюсти;
Г) укорочение плечевых и бедренных костей у плода;
Д) увеличение размера мочевого пузыря;
Е) одна артерия в пуповине вместо двух;
Ж) маловодие либо отсутствие околоплодных вод;
З) учащенное сердцебиение у плода.
При сочетании всех признаков женщине предлагается инвазивная диагностика для проведения генетического исследования: трансабдоминальная аспирация ворсин плаценты; трансабдоминальный кордоцентез с пункцией сосудов пуповины.

Слайд 14Признаки синдрома Дауна у новорожденного: укороченный череп;
маленький размер головы;
неправильная форма ушей;
приплюснутый лицевой череп;
седловидный нос;
плоская переносица;
маленький рот;
маленький подбородок;
толстый, бороздчатый язык;
косой разрез глаз;
открытый рот;
кожные складки, расположенные на внутренних уголках глаз;
короткая шея;
складка кожи на шее;
короткие верхние и нижние конечности;
короткие пальцы;
уплощенные широкие ладони;
горизонтальная складка на ладонях;
вогнутая форма мизинцев;
видимое расстояние между первым и вторым пальцами ног;
слабый тонус мышц.
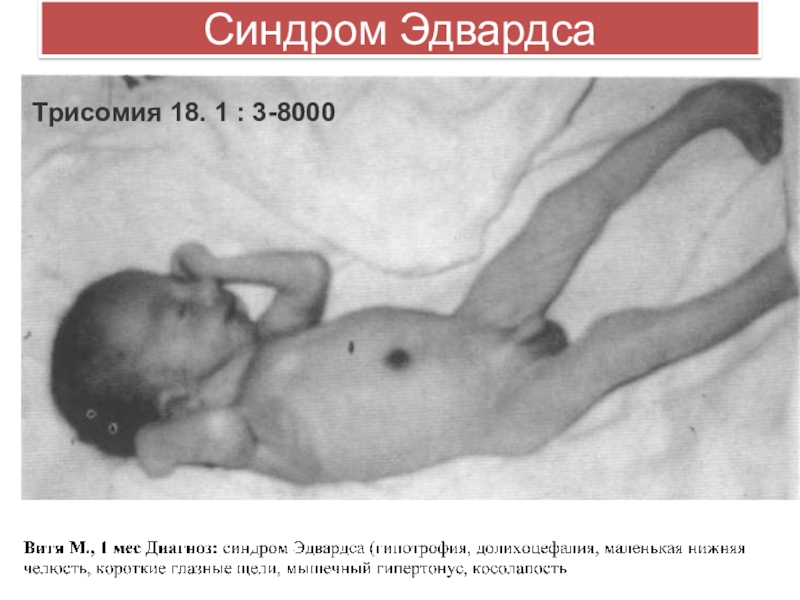
Слайд 15Синдром Эдвардса
Трисомия 18. 1 : 3-8000
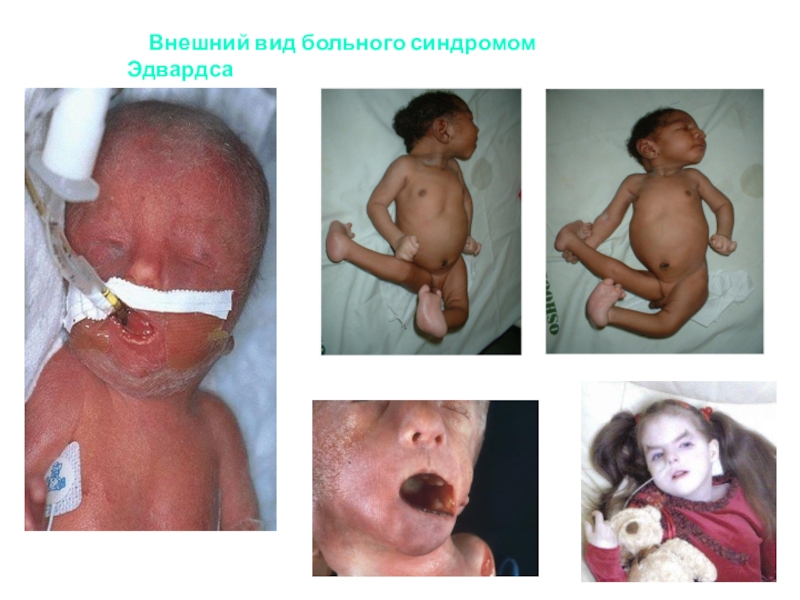
Слайд 16 Внешний вид больного синдромом Эдвардса
Слайд 17У девочек данное заболевание встречается в 3 раза чаще.
Риск синдрома
Эдвардса значительно возрастает, если беременной женщине 30 и более лет.
Пренатальная
диагностика данного синдрома проводится в 2 этапа:
На сроке в А) 8–12 недель биопсия ворсин хориона, Б) 11–13 недель определение кариотипа плода у беременных их группы риска; В) в крови женщины определяется уровень β–хорионического гонадотропина человека и плазменного протеина А. Затем с учетом этих данных, возраста беременной женщины рассчитывается риск рождения ребенка с синдромом Эдвардса, и формируется группа риска беременных.
В 14–18 — амниоцентез (изучение околоплодных вод), спустя 20 недель — кордоцентез (внутриутробное взятие крови из пуповины плода с УЗИ–контролем). После этого в полученном материале определяют наличие или отсутствие дополнительной 18–й хромосомы с помощью КФ–ПЦР (количественной флуоресцентной полимеразной цепной реакции).
Если беременная не прошла генетическое скрининг–обследование, то на более поздних сроках предварительная диагностика синдрома Эдвардса осуществляется с помощью УЗИ.
Прочие косвенные признаки, на основании которых можно заподозрить синдром Эдвардса на более поздних сроках: Наличие аномалий развития костей и мягких тканей головы («волчья пасть», микроцефалия, низкая посадка ушных раковин, «заячья губа» и т.п.). Обнаружение пороков со стороны сердечно–сосудистой, мочеполовой системы, а также опорно–двигательного аппарата.

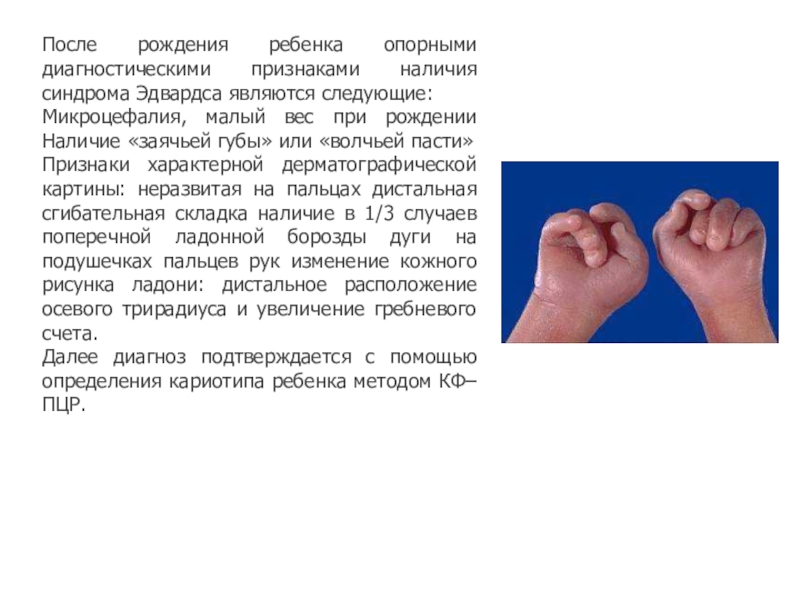
Слайд 18После рождения ребенка опорными диагностическими признаками наличия синдрома Эдвардса являются
следующие:
Микроцефалия, малый вес при рождении Наличие «заячьей губы» или
«волчьей пасти»
Признаки характерной дерматографической картины: неразвитая на пальцах дистальная сгибательная складка наличие в 1/3 случаев поперечной ладонной борозды дуги на подушечках пальцев рук изменение кожного рисунка ладони: дистальное расположение осевого трирадиуса и увеличение гребневого счета.
Далее диагноз подтверждается с помощью определения кариотипа ребенка методом КФ–ПЦР.
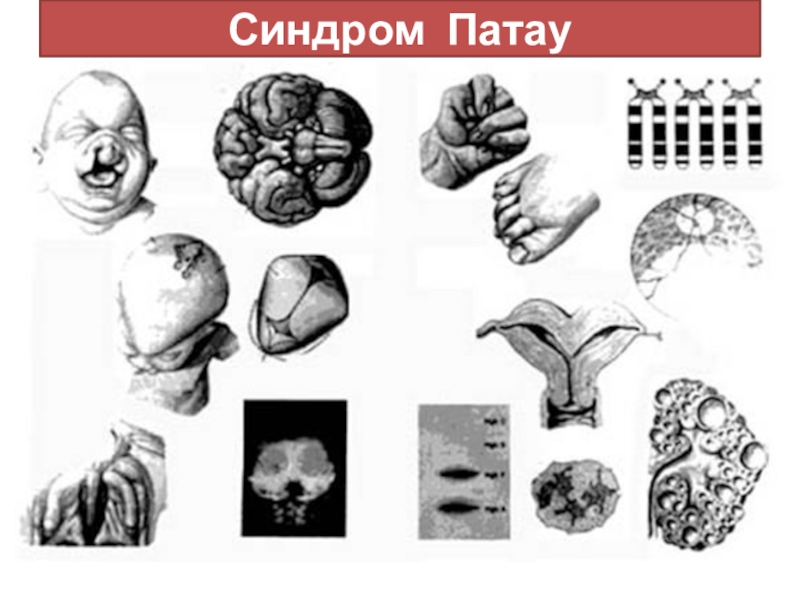
Слайд 20Трисомия 13
1:7000-10000;
соотношение полов примерно одинаковое
Меньшая часть случаев синдрома Патау
представлена несбалансированными транслокациями хромосом 13-й пары, мозаичными формами, изохромосомой.
Слайд 21Врожденные аномалии развития головного мозга, лицевой и мозговой части черепа,
глазных яблок.
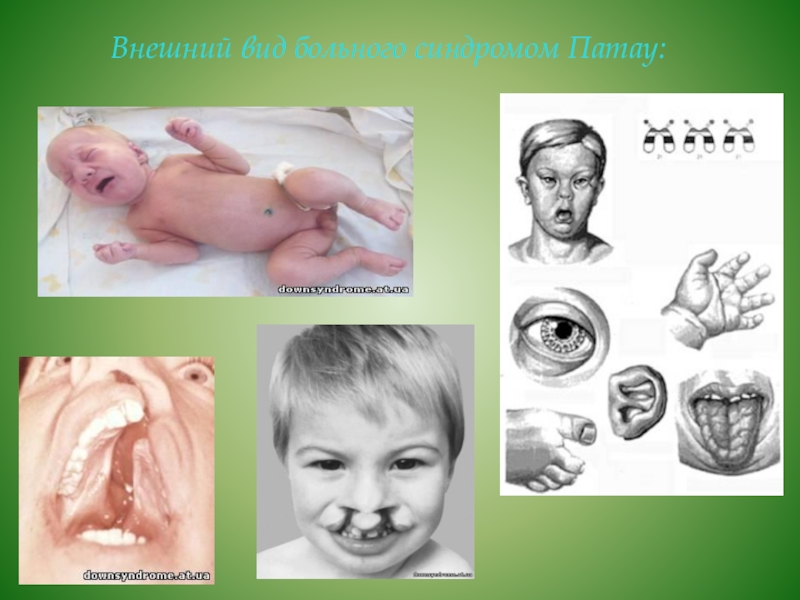
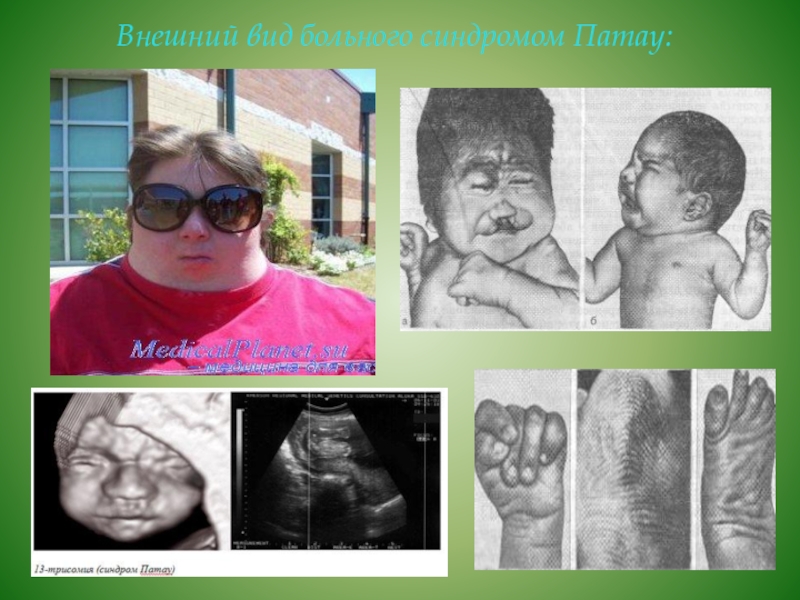
Новорожденные с синдромом Патау имеют характерный внешний вид:
микроцефалия, нередко – тригоноцефалию; низкий, скошенный лоб, узкие глазные щели; плоскую, запавшую переносицу, «волчья пасть» и «заячья губа», низкое расположение и деформация ушных раковин.
Нарушения со стороны ЦНС включают голопрозэнцефалию, гипоплазию мозжечка, гидроцефалию, дисгенезию мозолистого тела, спинномозговые грыжи (менингомиелоцеле). Дети с синдромом Патау всегда имеют глубокую умственную отсталость в степени идиотии, значительно отстают от сверстников в физическом и психическом развитии.
Частыми проявлениями синдрома Патау служат глухота, микрофтальмия, врожденная катаракта, колобомы, дисплазия сетчатки, гипоплазия зрительного нерва.
Аномалии внутренних органов при синдроме Патау могут быть представлены различными комбинациями: врожденными пороками сердца, почек, пищеварительной системы.
Нарушения развития костно-мышечной системы характеризуются полидактилией кистей и стоп, синдактилией, флексорным положением кистей, «стопой-качалкой», наличием эмбриональной пупочной грыжи. У мальчиков с синдромом Патау наблюдается крипторхизм, гипоспадия;
У девочек – гипертрофия клитора и половых губ, удвоение матки и влагалища, двурогая матка.
Прогноз: неблагоприятный 95% больных умирает на первом году жизни.
В развитых странах количество детей, доживающих до 5 лет, не превышает 15%, до 10 лет – 2-3%.

Слайд 22 Внешний вид больного синдромом Патау:
Слайд 23 Внешний вид больного синдромом Патау:
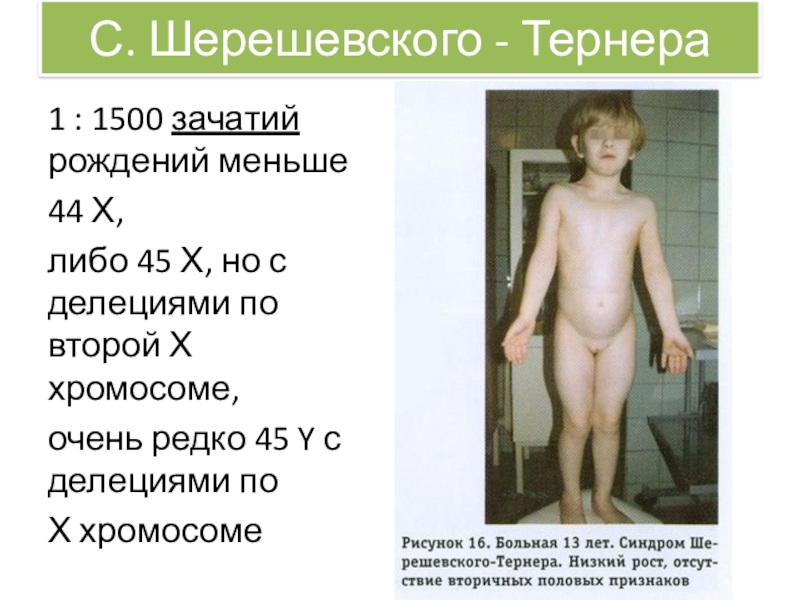
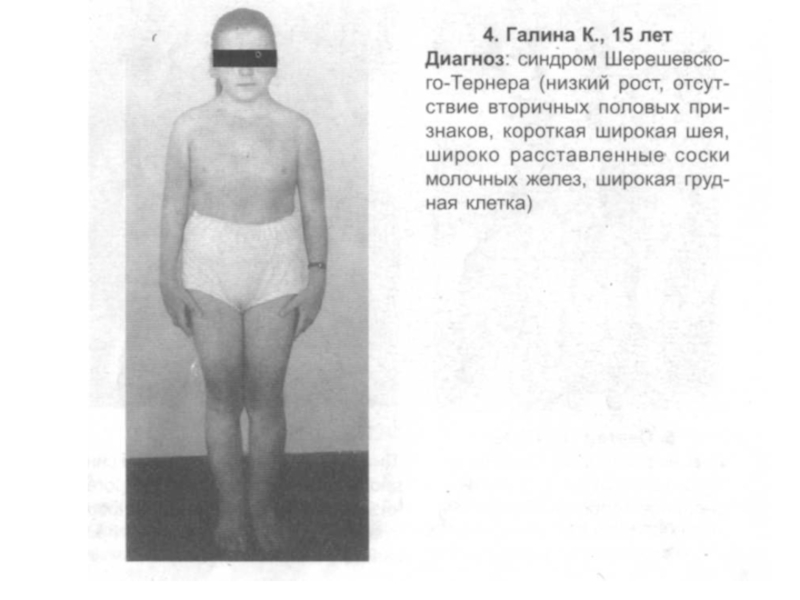
Слайд 24С. Шерешевского - Тернера
1 : 1500 зачатий рождений меньше
44 Х,
либо 45 Х, но с делециями по второй Х хромосоме,
очень
редко 45 Y с делециями по
Х хромосоме
Слайд 25 Складки кожи в области шеи — характерный
признак болезни. На фото: девочка до и после пластической операции
Больная
14 лет. Синдром Шерешевского-Тернера. Крыловидные складки на шее «голова сфинкса».
Слайд 27Основные клинические признаки синдрома Шерешевского-Тернера:
Низкая масса тела и рост
ребенка при доношенной беременности;
Сохранение низкого роста по мере развития
ребенка (как правило, рост не превышает 150-155 см);
«Шея сфинкса» (короткая шея с крыловидными складками);
Широкая грудная клетка;
Маленькие низко расположенные уши;
Искривление локтевых суставов;
Короткие пальцы рук за счет укорочения пястных костей;
Лимфостаз (отечность) стоп и кистей;
Пороки половой системы (уменьшение размеров матки, отсутствие яичников, недоразвитие клитора и малых половых губ, гипертрофированные большие половые губы и др.);
Отсутствие или слабая выраженность вторичных половых признаков (отсутствие менструаций, малое оволосение лобка и подмышечных впадин, недоразвитие молочных желез);
Возможные пороки развития сердечно-сосудистой, мочевыводящей и эндокринной систем;
Склонность к повышенному артериальному давлению и ожирению.
Умственные способности, как правило, не страдают.
Слайд 28Основные диагностические мероприятия:
Анализ крови на гормоны (значительно снижено количество эстрогенов
и повышен уровень ФСГ и ЛГ);
Определение кариотипа, консультация генетика;
Консультация акушера-гинеколога;
УЗИ органов малого таза;
Консультации узких специалистов по необходимости;
Дополнительные методы обследования для выявления пороков развития по показаниям.
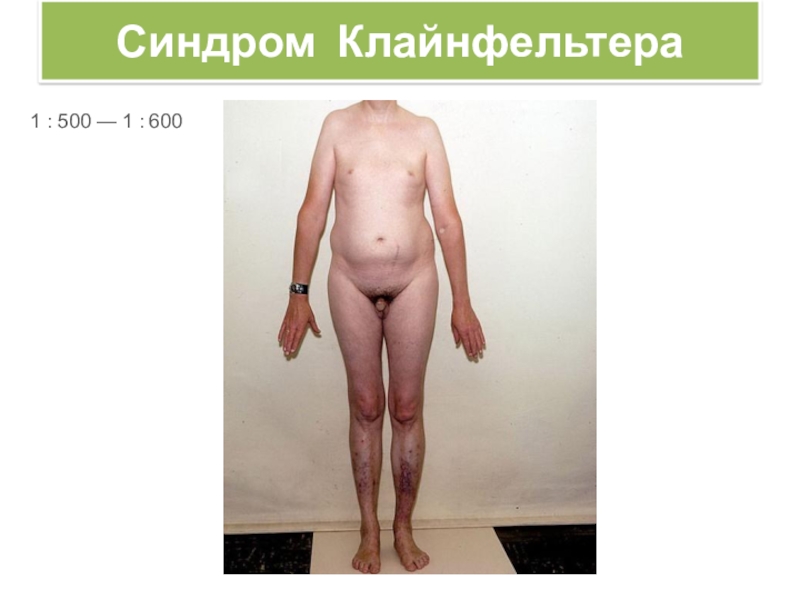
Слайд 29Синдром Клайнфельтера
1 : 500 — 1 : 600
Слайд 30По количеству дополнительных Х-хромосом выделяют несколько видов данного синдрома:
Одна дополнительная хромосома (кариотип
47ХХУ). Данный вид является классическим, встречается чаще всего;
Две дополнительные хромосомы (кариотип
48ХХХУ);
Три дополнительные хромосомы (кариотип 49ХХХХУ);
Одна дополнительная Х-хромосома и одна лишняя У-хромосома (кариотип 48ХХУУ);
Мозаичная форма (дополнительную Х-хромосому имеют только часть клеток организма). Кариотип 46ХУ/47ХХУ.
Слайд 31Ранние проявления синдрома
Благоприятное течение беременности, что отличает данное заболевание от
других хромосомных заболеваний;
Высокий рост (значительная прибавка в возрасте после 5 лет);
Непропорциональное
телосложение (длинные ноги, высокая тонкая талия);
Незначительная задержка речевого развития;
Возможные трудности восприятия материала на слух.
Большинство признаков заболевания появляется в подростковом возрасте:
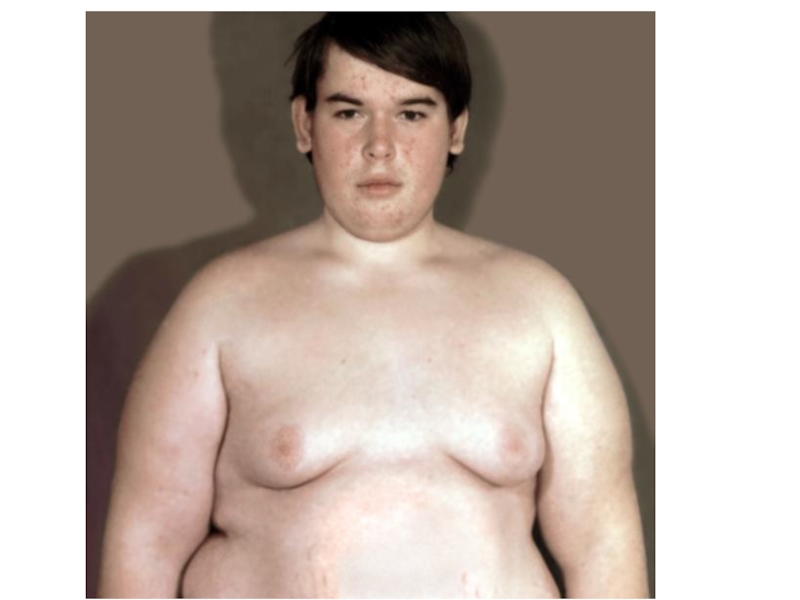
Гинекомастия (увеличение грудных желез, сохраняющееся в течение длительного времени);
Андрогенная недостаточность, вызванная постепенной атрофией яичек (скудная растительность на теле и лице, оволосение лобка по женскому типу, полное отсутствие сперматозоидов, избыточный вес, уменьшение яичек). В более зрелом возрасте (после 25 лет) мужчины нередко предъявляют жалобы на снижение полового влечения и импотенцию;
Высокий рост (выше 180 см), длинные ноги.
Интеллектуальное и психическое развитие:
Коэффициент интеллекта вариабелен: от среднего до высокого уровня;
Возможные трудности с восприятием на слух больших объемов материала;
Сложности с построением длинных грамматических фраз;
Склонность к пониженной самооценке, повышенная чувствительность;
Склонность к алкоголизму и наркомании (точно не доказана).

Слайд 33Одна дополнительная Х-хромосома и У-хромосома (кариотип 48ХХУУ):
Высокий рост (185 см
и выше);
Снижение интеллекта, замедленная речь;
Склонность к депрессивным состояниям и повышенной агрессии;
Трудности в
социальной адаптации.
Варианты течения
Слайд 34Две дополнительные Х-хромосомы (кариотип 48ХХХУ):
Рост колеблется от среднего до высокого;
Частые
пороки развития (сращение локтевой и лучевой костей, плоская переносица, увеличенное
расстояние между глазами и др.);
Вариабельность интеллекта от среднего до легкой умственной отсталости;
Апатичность, инфантильность, агрессия чаще отсутствует.
Варианты течения
Слайд 35Три дополнительные хромосомы (кариотип 49ХХХХУ)
(крайне редкая форма):
Низкий рост;
Частые случаи врожденных
пороков (пороки сердца и крупных сосудов, волчья пасть, заячья губа,
деформации суставов, небольшие размеры яичек и полового члена);
Снижение интеллекта в виде умственной отсталости (от легкой до тяжелой степеней);
Возможные приступы агрессии, в остальное время спокойны и дружелюбны.
Варианты течения
Слайд 36Мозаичная форма (кариотип 46ХУ/47ХХУ):
Слабая выраженность всех симптомов классической формы;
Сохраненная возможность
оплодотворения (олигоспермия).
Варианты течения
Слайд 3744ХХХ
1 : 900-1000
Синдром трисомии Х
Слайд 38Описан Джекобе в 1959 г. 44ХХХ
Есть варианты 44ХХХХ и 44ХХХХХ.
Недоразвитые яичники,
Гипоплазия матки,
Нерегулярный менстр. цикл,
Бесплодие (у 70%),
Незначительное снижение интеллекта,
Психозы
Речевые задержки,
Диспраксия,
Высокий рост,
Низкий мышечный тонус (гипотония) и клинодактилия.
Слайд 39Умеренные лицевые аномалии: вертикальные складки кожи охватывающие внутренние углы глаз,
широко расставленные глаза (гипертелоризм) и маленькая окружность головы.
Диагноз может быть
подтвержден только хромосомным анализом.
Слайд 40Синдром кошачьего крика
Синдром Лежена
Делеция короткого плеча 5-й хромосомы
гены CTNND2, SEMA5A
и TERT
Слайд 41Ген CTNND2 (OMIM : 604275) кодирует дельта-катенин – белок, играющий решающую
роль в нервной системе (изолированный дефект – аутизм)
Ген SEMA5A (OMIM :
609297) кодирует белки семафорины, участвующие в сигнальных процессах аксонального наведения. Оказывают преимущественно отталкивающее действие на конус роста аксона, отклоняя его от прорастания в неподходящие области
Ген TERT (OMIM +187270) кодирует белок – теломеразную обратную транскриптазу (TERT, telomerase reverse transcriptase), входящую в состав фермента теломеразы, которая добавляет повторяющиеся последовательности ДНК (TTAGGG)nк 3'-концу цепи ДНК в области теломер, локализованных на концах всех человеческих хромосом.
Слайд 42Плач похож на крик кошки,
Аномалии развития гортани,
Дети плохо растут,
Отстают в
психическом развитии,
Микроцефалия,
Лицо с гипертелоризмом,
Микрогнатия,
Эпикант,
Уши неправильные, низко посажены
Причиной такого плача являются
следующие дефекты гортанных хрящей:
уменьшение надгортанника;
сужение дыхательных путей в области надгортанника;
размягчение хрящевой ткани;
складки на слизистой оболочке, выстилающей хрящи гортани.
Слайд 43Со стороны глаз существуют 4 основных признака синдрома Лежена:
Антимонголоидный разрез
глаз.
Косоглазие.
Глазной гипертелоризм.
Эпикант.
Слайд 44Проявления синдрома кошачьего крика в детском возрасте :
отставание в умственном
развитии;
пониженный мышечный тонус;
нарушение координации движений;
запоры;
лунообразное лицо;
короткая шея;
лабильность поведения;
проблемы со зрением.
Слайд 45Существует несколько видов мутаций, при которых развивается данное заболевание:
Полное отсутствие
короткого плеча. При полном отсутствии короткого плеча теряется приблизительно четверть
генетической информации, которую кодирует пятая хромосома. Это наиболее частый и наиболее тяжелый вариант заболевания. Помимо генов, которые обуславливают развитие синдрома Лежена, теряется еще несколько важных участков молекулы. Это предрасполагает к более серьезным и многочисленным врожденным аномалиям.
Укорочение короткого плеча. При укорочении плеча теряется лишь часть генетической информации, которая была ближе к концу молекулы (от трети до половины плеча). Если при этом происходит делеция участка 5р12.2 – 5р12.3, на котором расположены ключевые гены, то у ребенка развивается синдром кошачьего крика. В таких случаях наблюдается меньше пороков развития, чем при отсутствии всего плеча (утрачено меньше генетической информации).
Формирование кольцевой хромосомы. Так называемая кольцевая хромосома представляет собой сцепление двух плечей одной и той же хромосомы (длинного и короткого). В результате этого молекула принимает форму кольца. Данная аномалия предусматривает делецию небольшого конечного участка. Если при этом теряются ключевые гены, развивается болезнь.

Слайд 46Мозаичная форма синдрома.
Мозаичная форма синдрома является обычно наиболее легким
вариантом, но встречается крайне редко. Во всех трех предыдущих случаях
дефектную молекулу ДНК ребенок получал от одного из родителей. При мозаичной же форме геном изначально был нормальным. Так называемая зигота (клетка, получившаяся при слиянии сперматозоида и яйцеклетки), имела полноценные пятые хромосомы. Проблема произошла в процессе роста зародыша. При делении хромосом короткое плечо было потеряно (не разделилось между двумя дочерними клетками). Таким образом, часть клеток (обычно большая часть) в будущем будут иметь нормальный геном, а небольшая часть – геном, характерный для синдрома Лежена. Тяжесть патологии при этом будет умеренной, и у детей будет меньше пороков развития (дефекты одних клеток отчасти компенсируются усиленным делением других). Такие дети не бывают нормальными в полном смысле этого слова. Как правило, задержка умственного развития все равно имеет место. Однако отклонений в физическом развитии и тяжелых врожденных пороков внутренних органов обычно не наблюдается.

Слайд 47Диагностики синдрома кошачьего крика:
сбор анамнеза;
кариотипирование родителей;
ультразвуковое исследование;
анализ крови на плазменные
маркеры;
инвазивные исследования;
диагностика на послеродовом этапе.
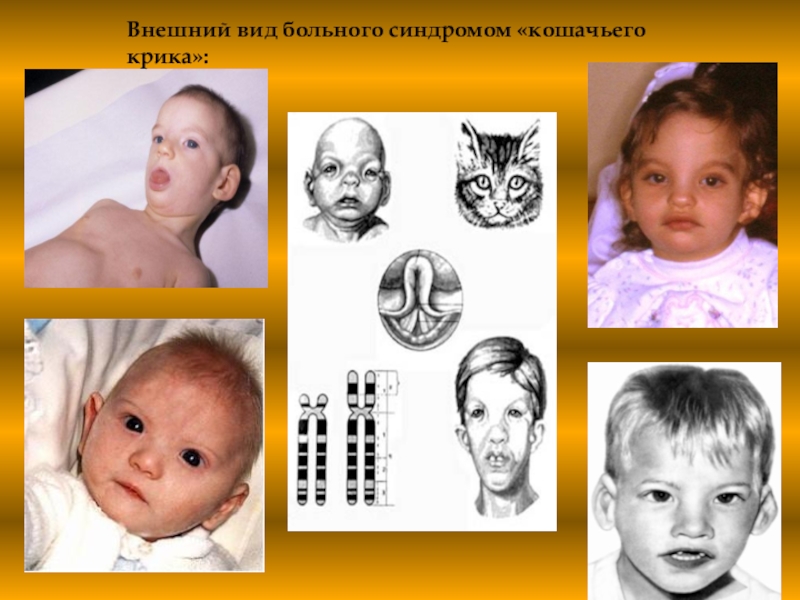
Слайд 48Внешний вид больного синдромом «кошачьего крика»:
Слайд 50МУЛЬТИФАКТОРИАЛЬНЫЕ ЗАБОЛЕВАНИЯ( заболевания с наследственной предрасположенностью)
ПРИЧИНА: неблагоприятное сочетание в генотипе
нескольких, в принципе, нормальных генов + воздействие неблагоприятных факторов окружающей
среды.
Не наследуются по законам Г. Менделя, но всем потомкам предается предрасположенность к заболеванию
Эта группа болезней в настоящее время составляет 92% от общего числа наследственных патологий человека. С возрастом частота заболеваний возрастает. В детском возрасте процент больных составляет не менее 10%, а в пожилом - 25-30%.
Слайд 51Мультифакториальные заболевания
разделяют в зависимости от того, какой орган поражен у
больного человека.
Например, выделяют заболевания:
ЦНС (эпилепсия, шизофрения, и др.) ,
сердечно–сосудистые (ревматизм,
атеросклероз, ИБС, гипертония и др.),
дыхательной (бронхиальная астма,аллергический альвеолит, туберкулез и др.),
Кожные (псориаз, атопический дерматит и др.),
Пищеварительной (язва, цирроз печени, коллит и др),
Выделительной (нефриты, мочекаменная болезнь, энурез и др),
Алкоголизм,
Злокачественные новообразования.