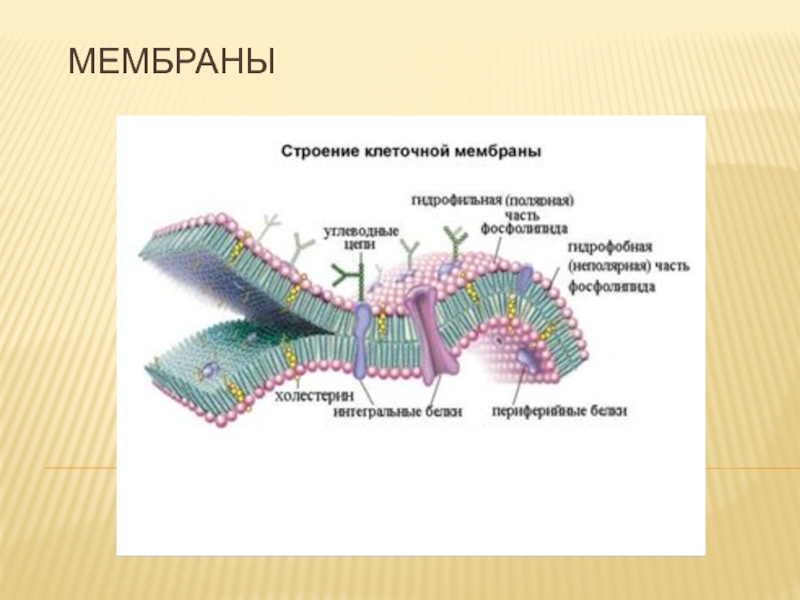
Слайд 2Свойства мембраны
1. Способность к самосборке. После разрушающих воздействий мембрана способна
восстановить свою структуру, т.к. молекулы липидов на основе своих физико-химических
свойств собираются в биполярный слой, в который затем встраиваются молекулы белков.
2. Текучесть. Мембрана не является жесткой структурой, большая часть входящих в её состав белков и липидов может перемещаться в плоскости мембраны, они постоянно флюктуируют за счет вращательных и колебательных движений. Это определяет большую скорость протекания химических реакций на мембране.
3. Полупроницаемость. Мембраны живых клеток пропускают, помимо воды, лишь определённые молекулы и ионы растворённых веществ. Это обеспечивает поддержание ионного и молекулярного состава клетки.
4. Мембрана не имеет свободных концов. Она всегда замыкается в пузырьки.
5. Асимметричность. Состав наружного и внутреннего слоев как белков, так и липидов различен.6. Полярность. Внешняя сторона мембраны несёт положительный заряд, а внутренняя – отрицательный.
Слайд 4ФУНКЦИИ МЕМБРАНЫ
1) Барьерная –плазмалемма отграничивает цитоплазму и ядро от внешней среды.
Кроме того, мембрана делит внутреннее содержимое клетки на отсеки (компартменты),
в которых зачастую протекают противоположные биохимические реакции.
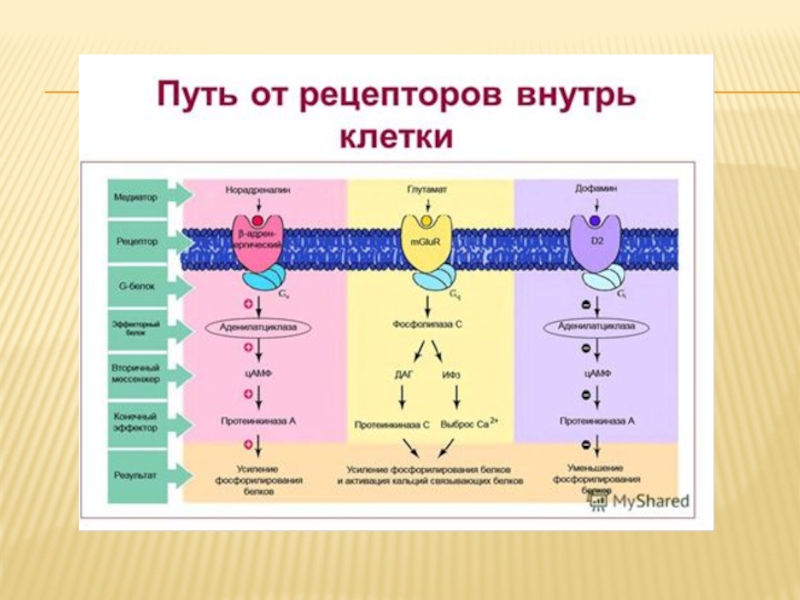
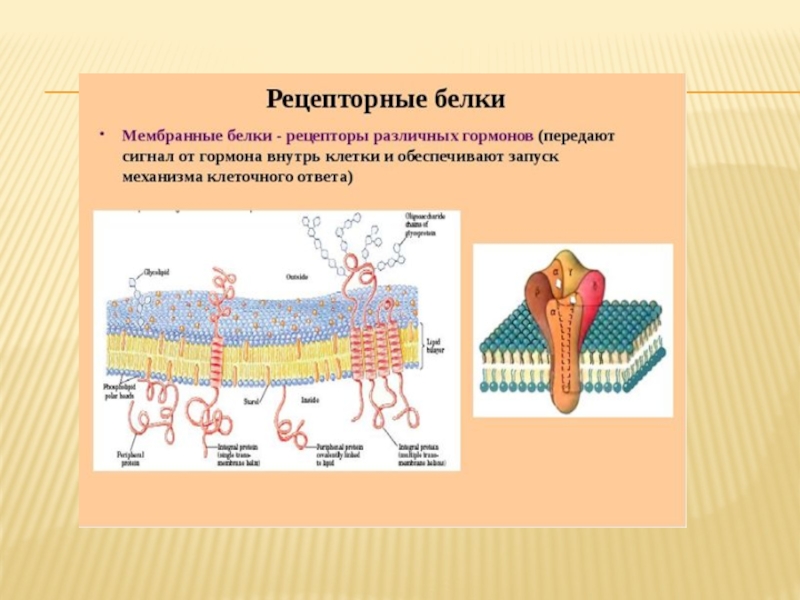
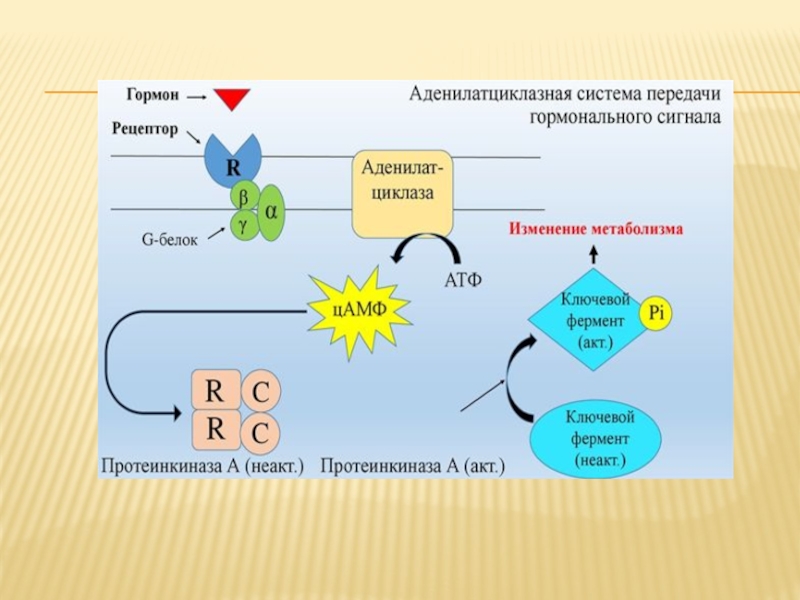
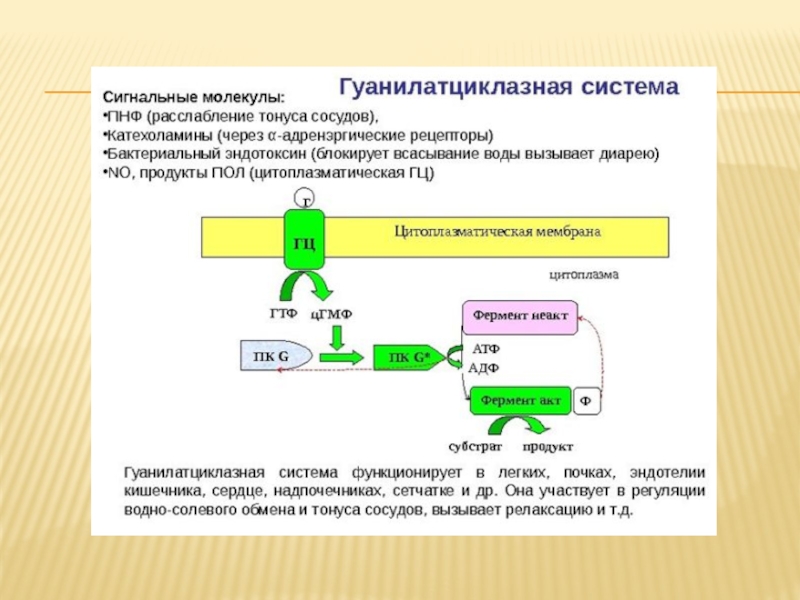
2) Рецепторная(сигнальная) – благодаря важному свойству белковых молекул – денатурации, мембрана способна улавливать различные изменения в окружающей среде. Так, при воздействии на мембрану клетки различных средовых факторов (физических, химических, биологических) белки, входящие в ее состав, меняют свою пространственную конфигурацию, что служит своеобразным сигналом для клетки. Это обеспечивает связь с внешней средой, распознавание клеток и их ориентацию при формировании тканей и т.д. С этой функцией связана деятельность различных регуляторных систем и формирование иммунного ответа.
3) Обменная – в состав мембраны входят не только структурные белки, которые образуют ее, но и ферментативные, являющиеся биологическими катализаторами. Они располагаются на мембране в виде «каталитического конвейера» и определяют интенсивность и направленность реакций метаболизма
.4) Транспортная – молекулы веществ, диаметр которых не превышает 50 нм, могут проникать путем пассивного и активного транспорта через поры в структуре мембраны. Крупные вещества попадают в клетку путем эндоцитоза (транспорт в мембранной упаковке), требующего затраты энергии. Его разновидностями являются фаго- и пиноцитоз. Пассивный транспорт – вид транспорта, в котором перенос веществ осуществляется по градиенту химической или электрохимической концентрации без затраты энергии АТФ. Выделяют два вида пассивного транспорта: простая и облегченная диффузия. Диффузия – это перенос ионов или молекул из зоны более высокой их концентрации в зону более низкой концентрации, т.е. по градиенту.Простая диффузия – ионы солей и вода проникают через трансмембранные белки или жирорастворимые вещества по градиенту концентрации.Облегченная диффузия – специфические белки-переносчики связывают вещество и переносят его через мембрану по принципу «пинг-понга». Таким способом через мембрану проходят сахара и аминокислоты. Скорость такого транспорта значительно выше, чем простой диффузии. Кроме белков- переносчиков, в облегченной диффузии принимают участие некоторые антибиотики – например, грамитидин и ваномицин. Поскольку они обеспечивают транспорт ионов, их называют ионофорами. Активный транспорт – это вид транспорта, при котором расходуется энергия АТФ, он идёт против градиента концентрации. В нем принимают участие ферменты АТФ-азы. В наружной клеточной мембране находятся АТФ-азы, которые осуществляют перенос ионов против градиента концентрации, это явление называется ионным насосом. Примером является натрий-калиевый насос. В норме в клетке больше ионов калия, во внешней среде – ионов натрия. Поэтому по законам простой диффузии калий стремится из клетки, а натрий – в клетку. В противовес этому натрий-калиевый насос накачивает против градиента концентрации в клетку ионы калия, а ионы натрия выносит во внешнюю среду. Это позволяет поддерживать постоянство ионного состава в клетке и её жизнеспособность. В животной клетке одна треть АТФ расходуется на работу натрий-калиевого насоса.Разновидностью активного транспорта является транспорт в мембранной упаковке – эндоцитоз. Крупные молекулы биополимеров не могут проникать через мембрану, они поступают в клетку в мембранной упаковке. Различают фагоцитоз и пиноцитоз. Фагоцитоз – захват клеткой твердых частиц, пиноцитоз – жидких частиц. В этих процессах выделяют стадии:1) узнавание рецепторами мембраны вещества; 2) впячивание (инвагинация) мембраны с образованием везикулы (пузырька); 3) отрыв пузырька от мембраны, слияние его с первичной лизосомой и восстановление целостности мембраны; 4) выделение непереваренного материала из клетки (экзоцитоз).
Эндоцитоз является способом питания для простейших. У млекопитающих и человека имеется ретикуло-гистио-эндотелиальная система клеток, способная к эндоцитозу – это лейкоциты, макрофаги, клетки Купфера в печени.

Слайд 5ОСМОТИЧЕСКИЕ СВОЙСТВА КЛЕТКИ
Осмос – односторонний процесс проникновения воды через полупроницаемую
мембрану из области с меньшей концентрацией раствора в область с
более высокой концентрацией. Осмос обусловливает осмотическое давление.
Диализ – односторонняя диффузия растворенных веществ.
Раствор, в котором осмотическое давление такое же, как и в клетках, называют изотоническим. При погружении клетки в изотонический раствор её объем не изменяется. Изотонический раствор называют физиологическим – это 0,9% раствор хлорида натрия, который широко применяется в медицине при сильном обезвоживании и потери плазмы крови.
Раствор, осмотическое давление которого выше, чем в клетках, называют гипертоническим. Клетки в гипертоническом растворе теряют воду и сморщиваются. Гипертонические растворы широко применяются в медицине. Марлевая повязка, смоченная в гипертоническом растворе, хорошо впитывает гной.
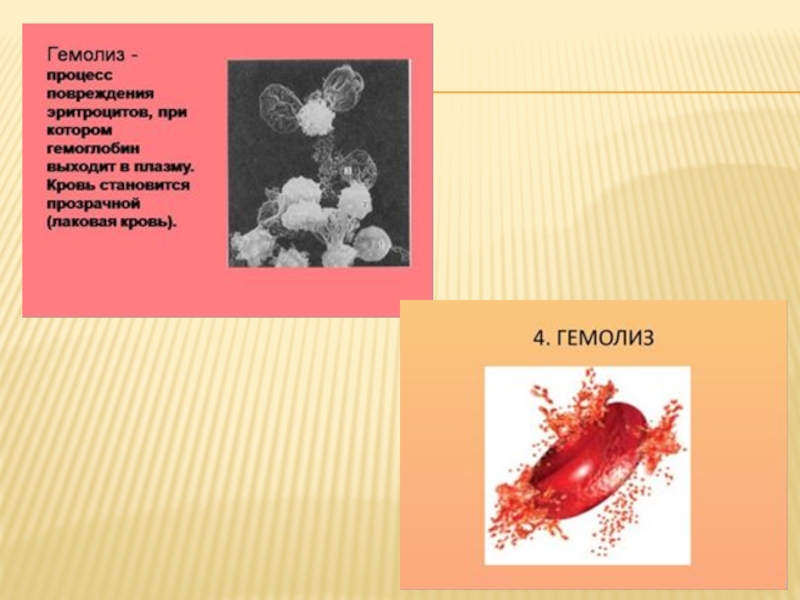
Раствор, где концентрация солей ниже, чем в клетке, называют гипотоническим. При погружении клетки в такой раствор вода устремляется в нее. Клетка набухает, ее тургор увеличивается, и она может разрушиться. Гемолиз – разрушение клеток крови в гипотоническом растворе.
Осмотическое давление в организме животного в целом регулируется системой органов выделения.

Слайд 10Свободные радикалы
Свободные радикалы - это активные молекулы, имеющие возможность
для присоединения еще одного электрона. Молекула имеет один непарный электрон,
и с легкостью вступает в химические реакции, обеспечивающие ей заполнение этой пустоты. Обеспечив это присоединение, она становится неопасной. Однако, химические реакции, вызванные свободными радикалами, не проходят бесследно для организма.
Слайд 13Антиоксиданты
Антиоксиданты - вещества, которые ингибируют окисление; любое из многочисленных химических
веществ, в том числе естественные продукты деятельности организма и питательные
вещества, поступающие с пищей, которые могут нейтрализовать окислительное действие свободных радикалов и других веществ
Слайд 14Ферментативная антиоксидантная система
К ферментам, защищающим клетки от действия активных форм
кислорода, относят супе-роксиддисмутазу, каталазу и глутатионпероксидазу. Наиболее активны эти ферменты
в печени, надпочечниках и почках, где содержание митохондрий, цитохрома Р450и пероксисом особенно велико.
Супероксиддисмутаза(СОД) превращает супероксидные анионы в перекись водорода:
2О∙2 + 2H+ → H2O2+ O2
Каталаза- геминовый фермент, катализирует реакцию разрушения перекиси водорода. При этом образуется вода и молекулярный кислород:
2Н2О2 → H2O+ O2.
Глутатионпероксидаза— обеспечивает разрушение перекиси водорода и гидропероксидов липидов при окислении глутатиона (у-глутамилцистеинилглицин): Н2О2+ 2 GSH → 2 Н2О + G-S-S-G. Глутатионпероксидаза в качестве кофермента содержит селен.
Глутатионредуктазавосстанавливает окисленный глутатион с участием НАДФН2:
GS-SG + НАДФН2 → 2 GSH + НАДФ+.
Недостаток глутатиона в клетках, например эритроцитах, который может быть обусловлен действием токсических веществ, например ионами тяжелых металлов или наследственным недостатком глутатионредуктазы приводит к активации перекисного окисления; это, в частности, наблюдается при некоторых видах гемолитических анемий.

Слайд 15
2. Неферментативная антиоксидантная система
Неферментативная антиоксидантная система - Витамины А.
Е, убихинон (коэнзим Q), тироксин. Аскорбаты- витамин С. некоторые аминокислоты
и метаболиты( мочевая кислота).Глютатион.
Слайд 16Реакции переписного окисления липидов (ПОЛ)
Реакции переписного окисления липидов (ПОЛ) являются
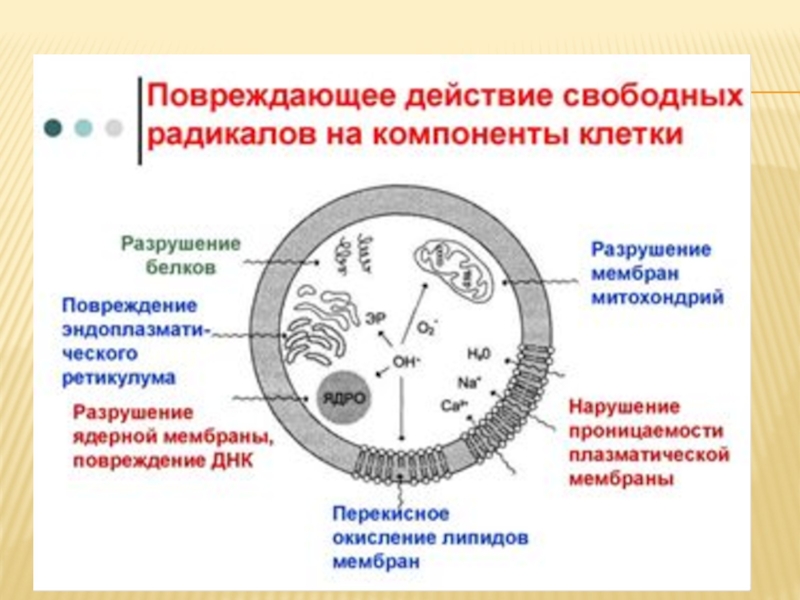
свободнорадикальными и по¬стоянно происходят в организме. Свободно-радикальное окисление нарушает структуру
мно¬гих молекул. В белках окисляются некоторые аминокислоты. В результате разрушается струк¬тура белков, между ними образуются ковалент-ные «сшивки», всё это активирует протеолити-ческие ферменты в клетке, гидролизующие повреждённые белки. Активные формы кисло¬рода легко нарушают и структуру ДНК. Неспе¬цифическое связывание Fe2+ молекулой ДНК облегчает образование гидроксильных радика¬лов, которые разрушают структуру азотистых оснований. Но наиболее подвержены действию активных форм кислорода жирные кислоты, содержащие двойные связи, расположенные через СН2-группу. Именно от этой СН2-группы свободный радикал (инициатор окисления) лег¬ко отнимает электрон, превращая липид, содер¬жащий эту кислоту, в свободный радикал. ПОЛ — цепные реакции, обеспечивающие расширенное воспроизводство свободных ра¬дикалов, частиц, имеющих неспаренный элек¬трон, которые инициируют дальнейшее распро¬странение перекисного окисления.

Слайд 19Метаболизм Железа и нуклеотидов.
Железо является необходимым биохимическим компонентом в ключевых
процессах метаболизма, роста и пролиферации клеток. Исключительная роль железа определяется
важными биологическими функциями белков, в состав которых входит этот биометалл. К наиболее известным железосодержащим белкам относятся гемоглобин и миоглобин.
Слайд 20Всасывание железа. Основным местом всасывания железа является тонкий кишечник. Железо
в пище содержится в основном в форме Fе+3, но лучше
всасывается в двухвалентной форме Fе+2. Под воздействием соляной кислоты желудочного сока железо высвобождается из пищи и превращается из Fе+3 в Fе+2. Этот процесс ускоряется аскорбиновой кислотой, ионами меди, которые способствуют всасыванию железа в организме. Присутствие высоких концентраций кальция, являющегося конкурентным ингибитором DСТ1, снижает всасывание железа.В энтероцитах содержатся трансферрин и ферритин, которые регулируют в них абсорбцию железа. Таким образом, транспортная система энтероцитов кишечника способна поддерживать оптимальный уровень абсорбции железа, поступающего с пищей.
Транспорт железа в крови. Железо в сосудистом русле соединяется с трансферрином - гликопротеид с Мм 88 кДа, синтезируется в печени. Биологическая функция трансферрина заключается в его способности легко образовывать диссоциирующие комплексы с железом, что обеспечивает создание нетоксического пула железа в кровотоке, который доступен и позволяет распределять и депонировать железо в организме.

Слайд 21Внутриклеточный метаболизм железа.Большинство клеток, в том числе эритрокариоциты и гепатоциты,
содержат на мембране рецепторы к трансферрину, необходимые для поступления железа
в клетку Комплекс Fе3+ - трансферрин попадает в клетки с помощью эндоцитоза В клетке ионы железа освобождаются, а комплекс трансферрин-рецептор расщепляется, в результате чего рецепторы и трансферрин независимо возвращаются на поверхность клетки. Экспрессия трансферриновых рецепторов (СD71) зависит от потребности клетки в железе. При перегрузке железом число клеточных и растворимых рецепторов к трансферрину снижается. При сидеропении лишенная железа клетка реагирует повышенной экспрессией трансферриновых рецепторов на своей мембране Таким образом, экспрессия рецепторов трансферрина зависит от двух факторов - количества депонированного железа в составе ферритина и пролиферативной активности клетки.
Депонирование железа. Основными формами депонированного железа являются ферритин и гемосидерин, которые связывают "избыточное" железо и откладываются, практически, во всех тканях организма, но особенно интенсивно в печени, селезенке, мышцах, костном мозге. Гемосидерин - Это ферритин в макрофаге в аморфном состоянии. После того как макрофаг поглощает молекулы железа, например, после фагоцитоза старых эритроцитов, немедленно начинается синтез апоферритина, который накапливается в цитоплазме, связывает железо, образуя ферритин. Макрофаг насыщается железом в течение 4 ч, после чего в условиях перегрузки железом в цитоплазме молекулы ферритина агрегируют в мембранно-связанные частицы, известные как сидеросомы. В сидеросомах молекулы ферритина кристаллизуются , формируется гемосидерин. Гемосидерин "упакован" в лизосомах и включает комплекс, состоящий из ферритина, окисленных остатков ли-пидов и других компонентов. Гранулы гемосидерина представляют собой внутриклеточные отложения железа, которые выявляются при окраске цитологических и гистологических препаратов по Перлсу.

Слайд 22Выведение железа. Железо выделяется с мочой, со слущивающимся эпителием
кожи. Кал содержит как невсосавшееся железо, так и железо, выделяющееся
с желчью и в составе слущивающегося эпителия кишечника.Согласно современным представлениям, наиболее адекватными тестами для оценки метаболизма железа в организме являются определение уровня железа, трансферрина, насыщения трансферрина железом, ферритина, содержания растворимых трансферриновых рецепторов в сыворотке.
Основными причинами дефицита железа могут быть:
1. Разнообразные кровопотери;
2. Недостаточное поступление и усвоение железа из пищи;
3. Повышенные его затраты при интенсивном росте, беременности и занятиями физической культурой.
4. нарушения пищеварения в связи с заболеваниями желудка и кишечника.
5. Некоторые инфекционно-воспалительные заболевания могут привести к перераспределению железа в организме и тем самым вызвать сидеропению.
Слайд 24Метаболизм гема.
Гем является простетической группой многих белков: гемоглобина, миоглобина,
цитохромов митохондриальной ЦПЭ, цитохрома Р450, участвующего в микросомальном окислении. Ферменты
каталаза, пероксидаза, цитохромоксидаза содержат гем в качестве кофермента.Все клетки организма имеют гемсодержащие белки, поэтому синтез гема идёт во всех клетках, за исключением эритроцитов, не имеющих, как известно, белоксинтезирующей системы.При распаде гема в клетках РЭС образуется жёлчный пигмент билирубин. Дальнейший катаболизм билирубина в печени, кишечнике и почках приводит к образованию конечных продуктов распада гема стеркобилина и уробилина, содержащихся, соответственно, в кале и моче. Железо, освобождающееся при распаде гема, снова используется для синтеза железосодержащих белков.
Слайд 25Синтез гема и гемоглобина.
Гем синтезируется во всех тканях, но с
наибольшей скоростью в костном мозге и печени . В костном
мозге гем необходим для синтеза гемоглобина в ретикулоцитах, в гепатоцитах - для образования цитохрома. Дефицит пиридоксальфосфата (В6) и лекарственные препараты, которые являются его структурными аналогами, снижают активность 5-амино-левулинатсинтазы.
Слайд 26Нарушения биосинтеза гема. Порфирии.
содержания порфириногенов - называют порфириями («порфирин» в
переводе с греч. означает пурпурный). Моча больных имеет красный цвет.
( болезнь вампиров). Hаследственные порфирии обусловлены генетическими дефектами ферментов, участвующих в синтезе гема, это приводит к накоплению промежуточных продуктов синтеза гема - 5-аминолевулиновой кислоты и порфириногенов.При тяжёлых формах порфирий наблюдают нейропсихические расстройства. В коже на солнце в результате взаимодействия с порфиринами кислород переходит в синглетное состояние. Синглетный кислород вызывает ускорение ПОЛ клеточных мембран и разрушение клеток, поэтому порфирии часто сопровождаются фотосенсибилизацией и изъязвлением открытых участков кожи. Нейропсихические расстройства при порфириях связаны с тем, что 5-аминолевулинат и порфириногены являются нейротоксинами. Иногда при лёгких формах наследственных порфирий заболевание может протекать бессимптомно, но приём лекарств, являющихся индукторами синтеза 5-аминолевулинатсинтазы, может вызвать обострение болезни. Индукторами синтеза 5-аминолевулинатсинтазы являются такие известные лекарства, как сульфанил-ами-ды, барбитураты, диклофенак, вольтарен, стероиды, гестагены. Некоторые галогенсодержащие гербициды и инсектициды являются индукторами синтеза 5-аминолевулинатсинтазы, поэтому попадание их в организм сопровождается симптомами порфирии.

Слайд 27Метаболиз нуклеиотидов.
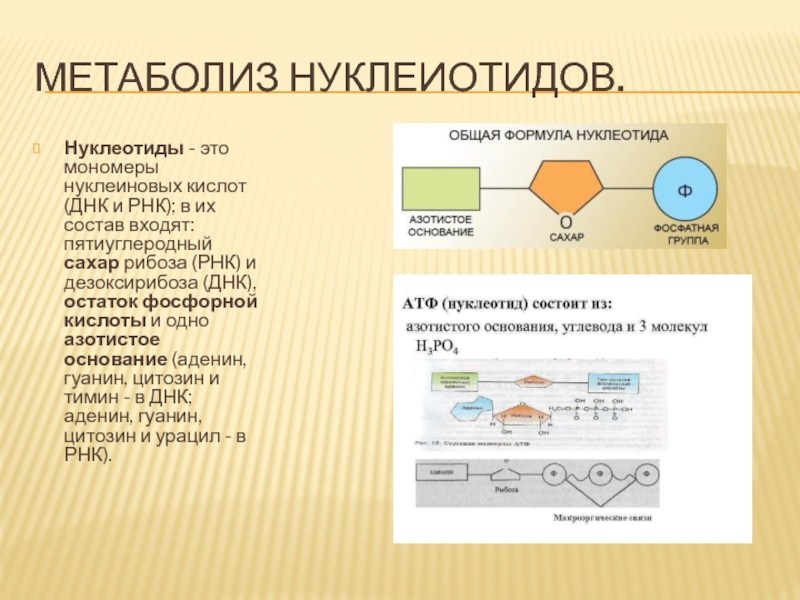
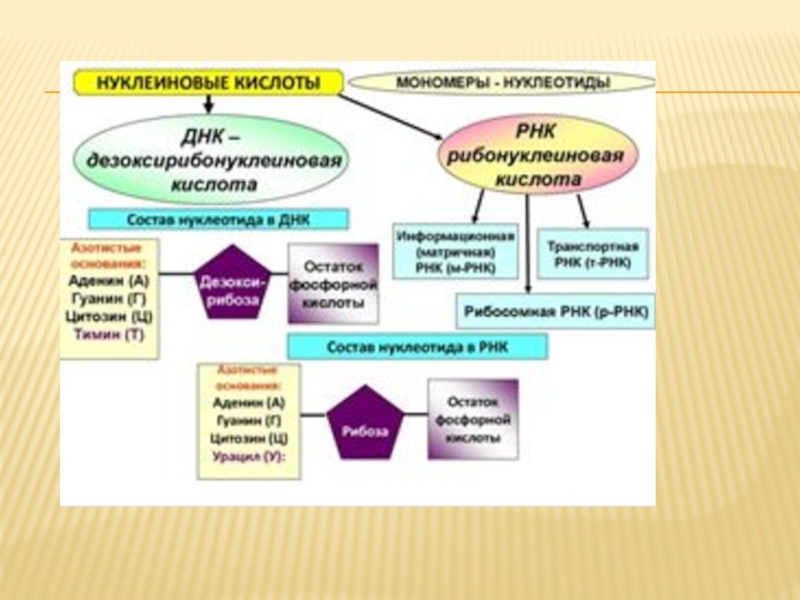
Нуклеотиды - это мономеры нуклеиновых кислот (ДНК и РНК);
в их состав входят: пятиуглеродный сахар рибоза (РНК) и дезоксирибоза
(ДНК), остаток фосфорной кислоты и одно азотистое основание (аденин, гуанин, цитозин и тимин - в ДНК; аденин, гуанин, цитозин и урацил - в РНК).
Слайд 29Переваривание нуклеотидов.
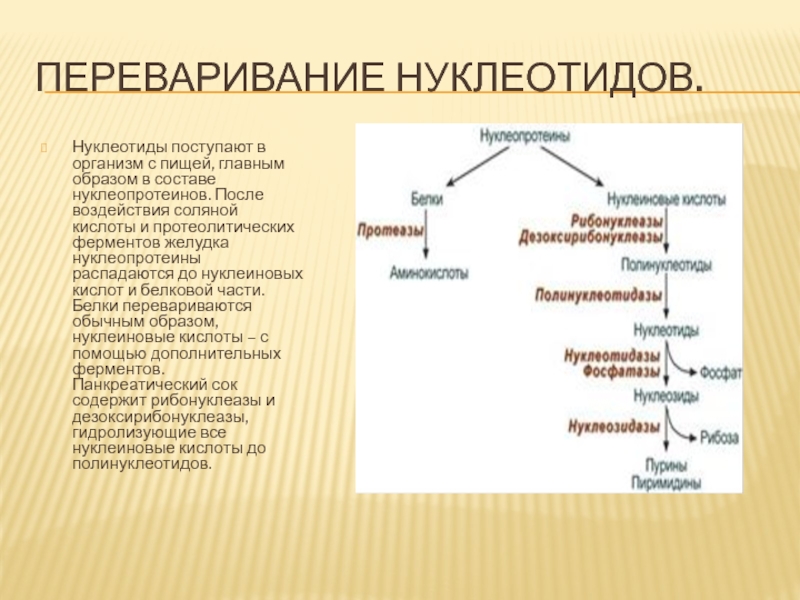
Нуклеотиды поступают в организм с пищей, главным образом в
составе нуклеопротеинов. После воздействия соляной кислоты и протеолитических ферментов желудка
нуклеопротеины распадаются до нуклеиновых кислот и белковой части. Белки перевариваются обычным образом, нуклеиновые кислоты – с помощью дополнительных ферментов. Панкреатический сок содержит рибонуклеазы и дезоксирибонуклеазы, гидролизующие все нуклеиновые кислоты до полинуклеотидов.
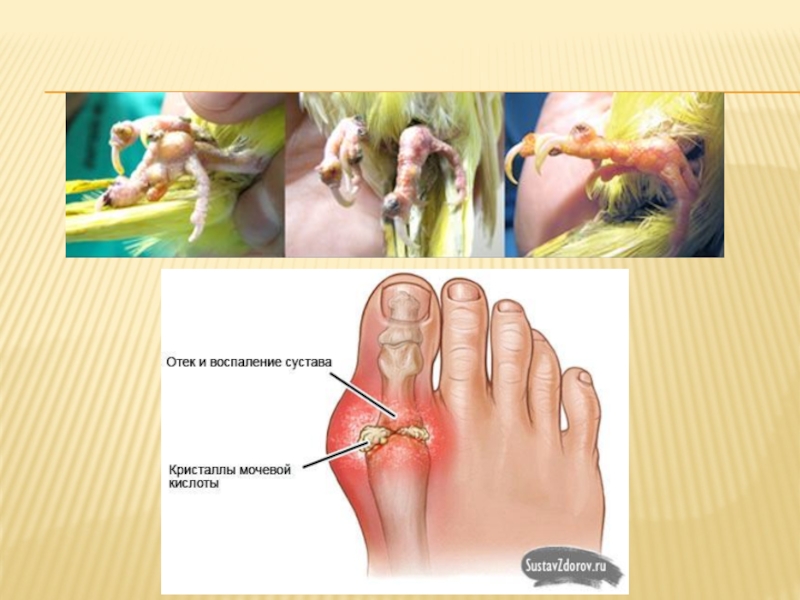
Слайд 31Падагра
Падагра - Когда в плазме крови концентрация мочевой кислоты превышает
норму, то возникает гиперурикемия. Вследствие гиперурикемии может развиться подагра -
заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. К характерным признакам подагры относят повторяющиеся приступы острого воспаления суставов - так называемого острого подагрического артрита. Заболевание может прогрессировать в хронический подагрический артрит. Поскольку лейкоциты фагоцитируют кристаллы уратов, то причиной воспаления является разрушение лизосомальных мембран лейкоцитов кристаллами мочевой кислоты. Освободившиеся лизосомальные ферменты выходят в цитозоль и разрушают клетки, а продукты клеточного катаболизма вызывают воспаление. У Собак и кошек встречается крайне редко. У птиц и рептилий часто.