Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
№7.Нуклеофильное замещение у насыщенного атома углерода, S N у C sp 3
Содержание
- 1. №7.Нуклеофильное замещение у насыщенного атома углерода, S N у C sp 3
- 2. ОСОБЕННОСТИ СТРОЕНИЯ и РЕАКЦИОННОЙ СПОСОБНОСТИ ГАЛОГЕНоПРОИЗВОДНЫХ
- 3. Моногалогенопроизводные углеводородов
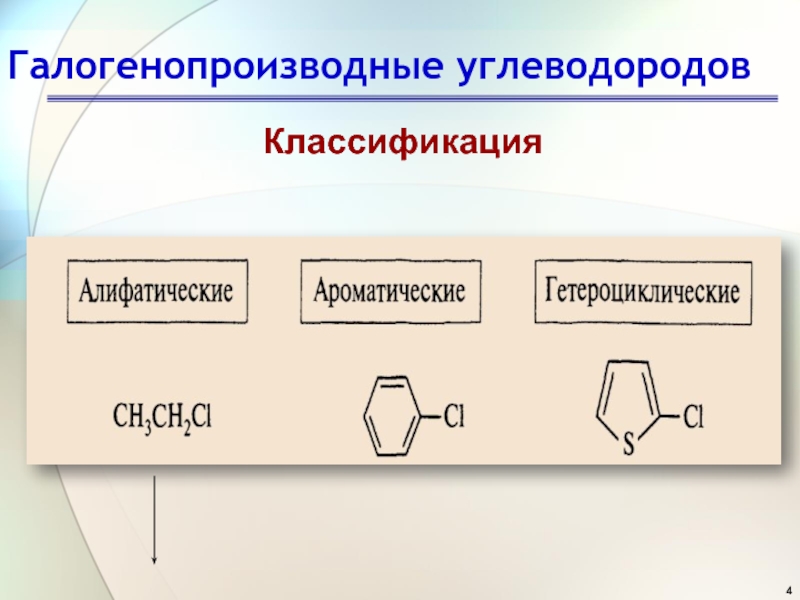
- 4. Галогенопроизводные углеводородовКлассификация
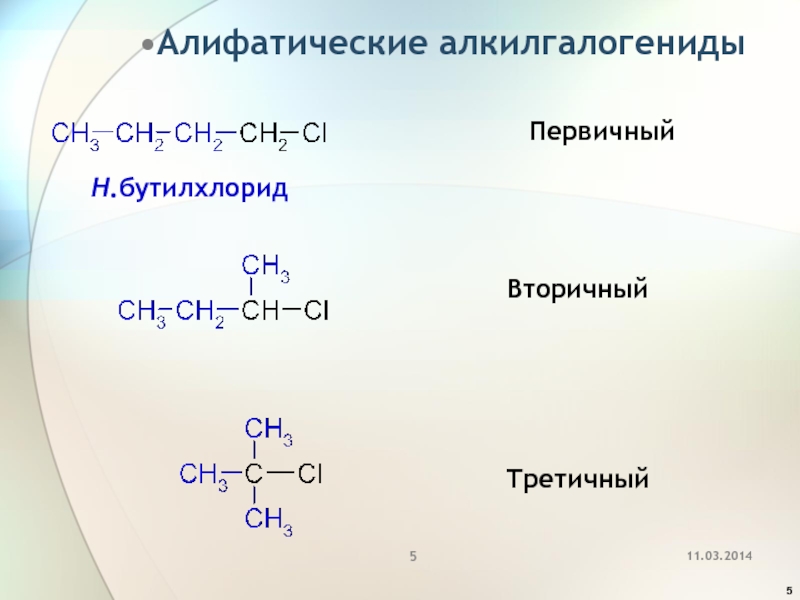
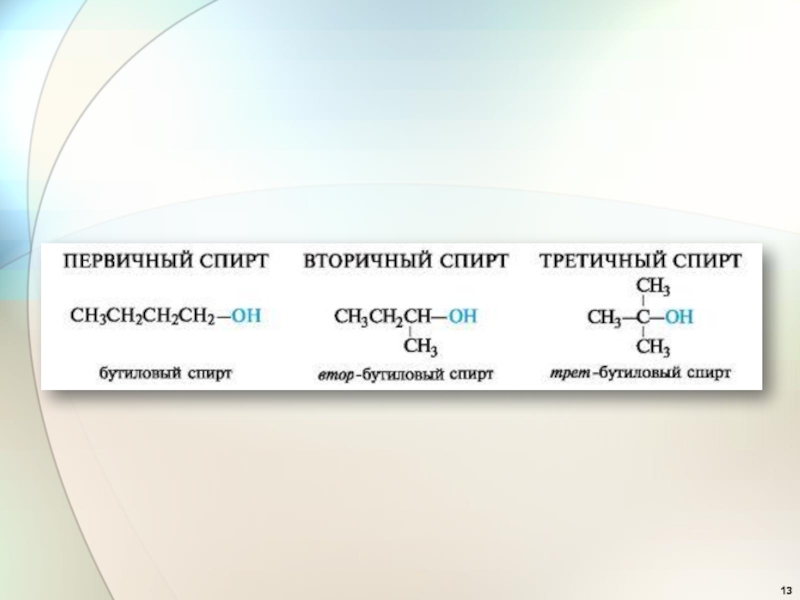
- 5. Алифатические алкилгалогениды ПервичныйВторичныйТретичныйН.бутилхлорид
- 6. Csp3 – Hal: полярность связиHal не проявляют
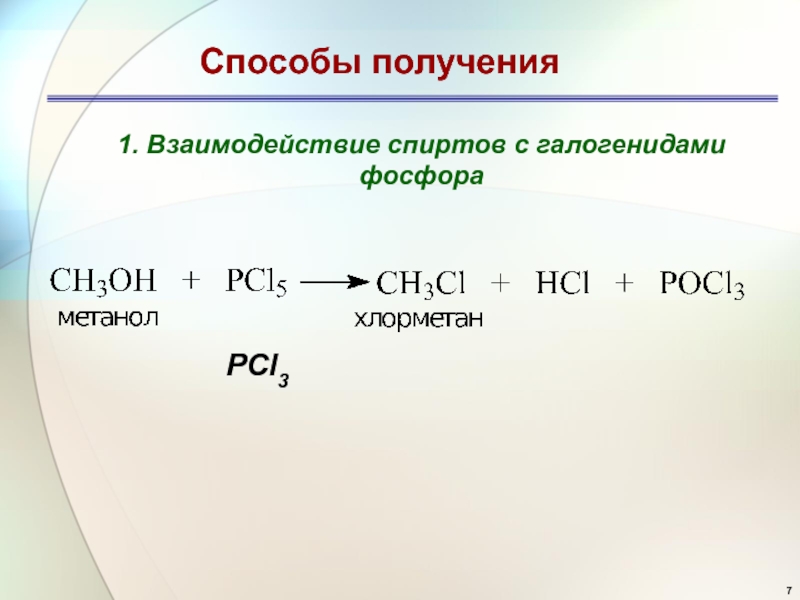
- 7. Способы получения1. Взаимодействие спиртов с галогенидами фосфораPCl3
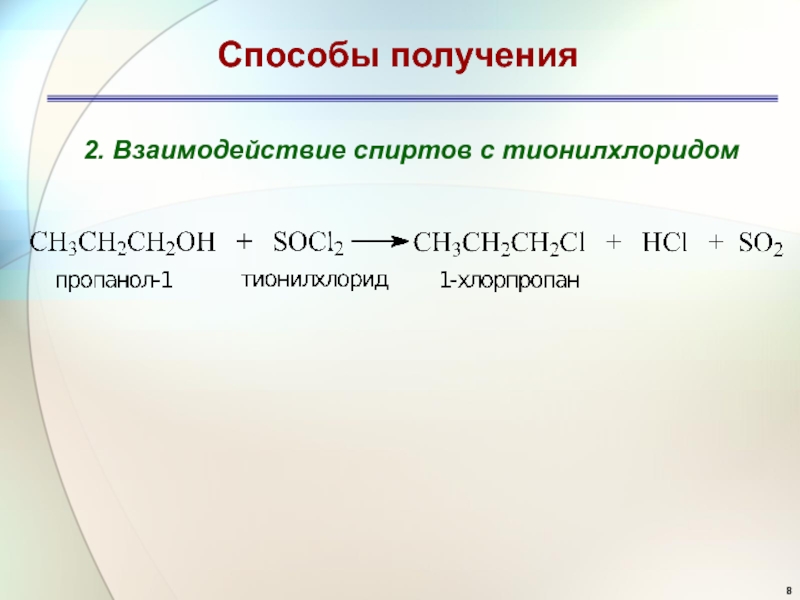
- 8. Способы получения2. Взаимодействие спиртов с тионилхлоридом
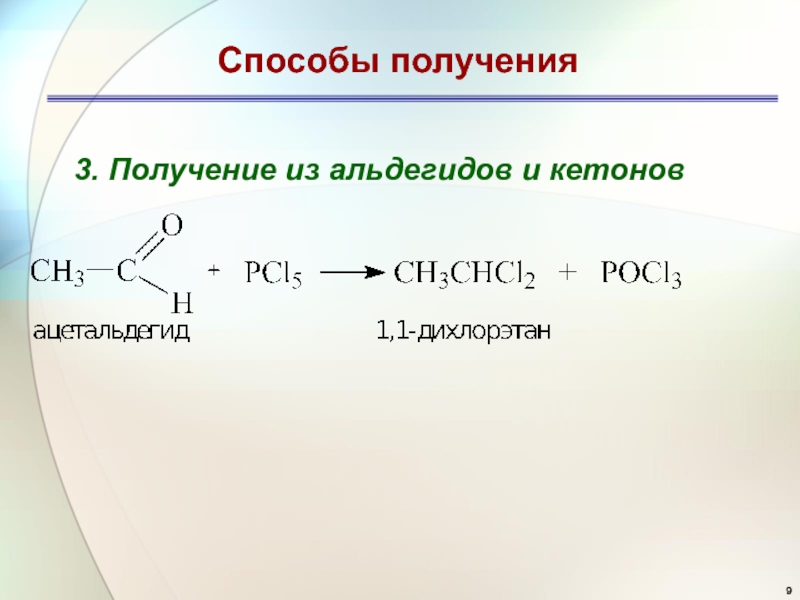
- 9. Способы получения3. Получение из альдегидов и кетонов
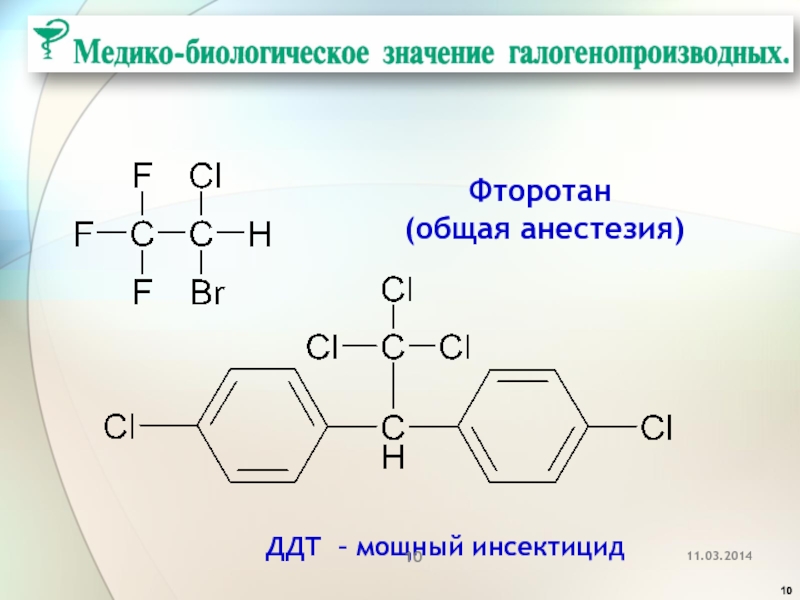
- 10. Фторотан (общая анестезия) ДДТ – мощный инсектицид
- 11. Соединения с гидроксильной группой и их производные.
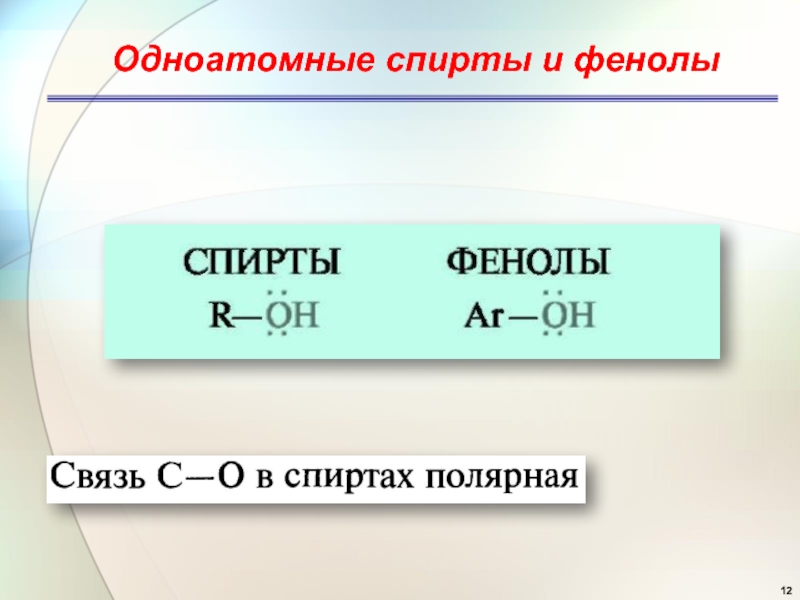
- 12. Одноатомные спирты и фенолы
- 13. Слайд 13
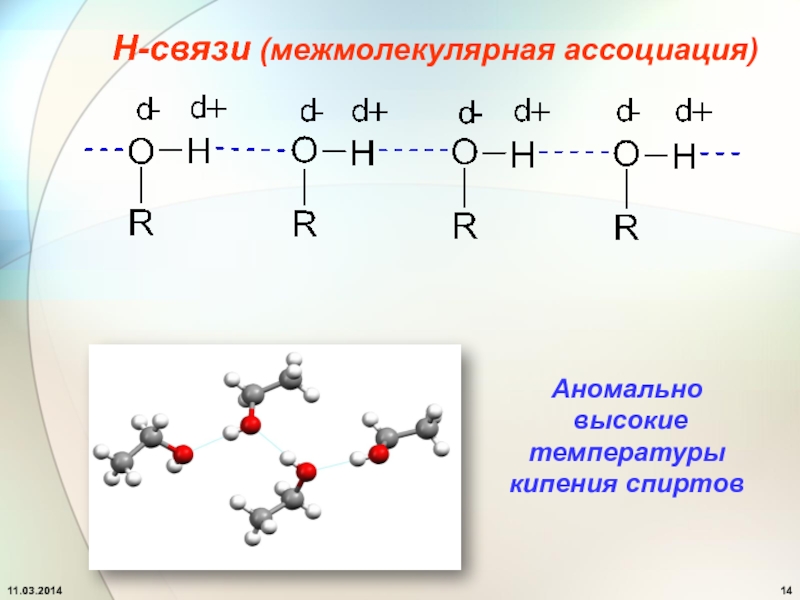
- 14. Аномально высокие температуры кипения спиртовН-связи (межмолекулярная ассоциация)
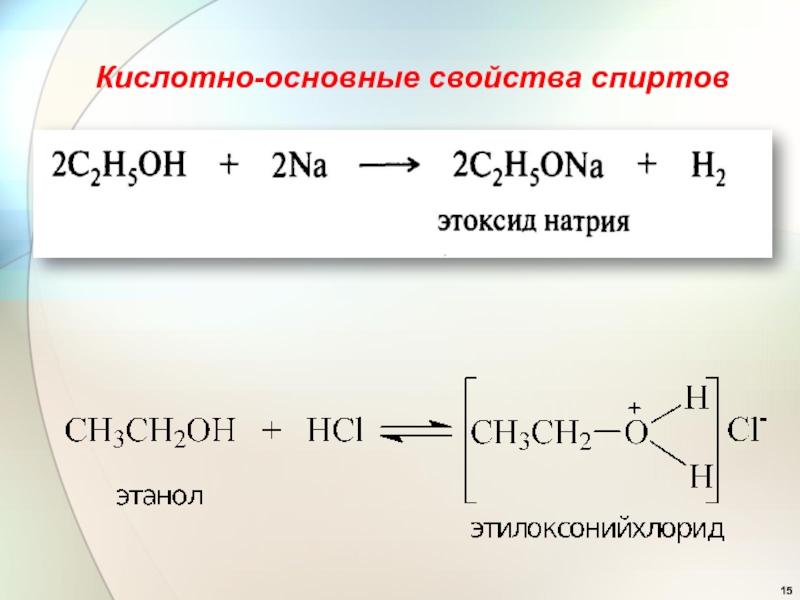
- 15. Кислотно-основные свойства спиртов
- 16. Метиловый спирт считается самым ядовитым спиртом. Вызывает слепоту или смерть.
- 17. Токсическое действие метанола связано с угнетением центральной
- 18. СпиртыФизические свойстваCH3CH2OHЭтанол
- 19. Этиловый спирт оказывает опьяняющее действие. Злоупотребление этанолом
- 20. - В высоких концентрациях этанол оказывает
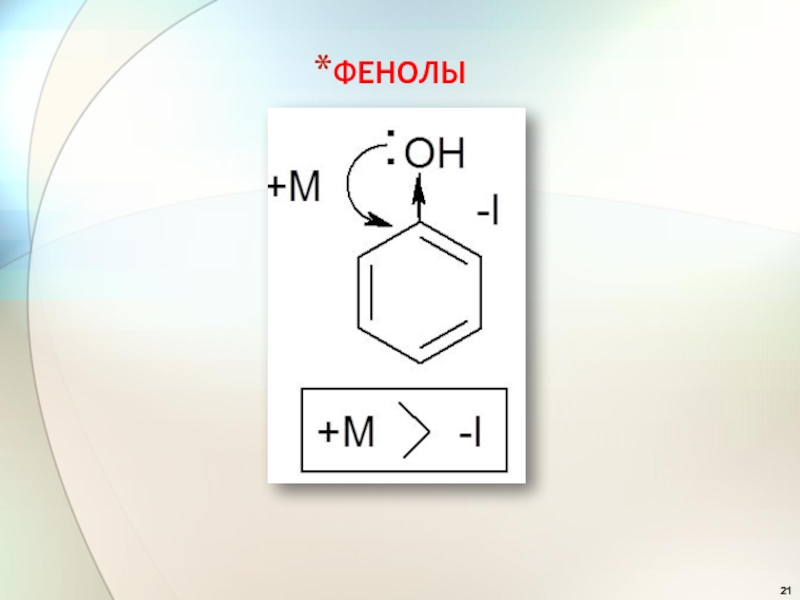
- 21. ФЕНОЛЫ
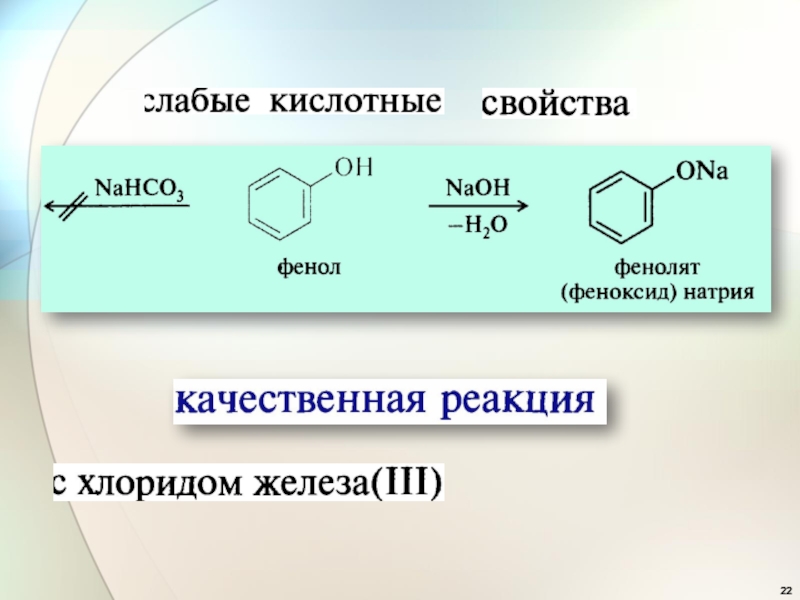
- 22. Слайд 22
- 23. Фенол очень токсичен, при попадании на кожу
- 24. Слайд 24
- 25. смешанный эфирнесмешанный эфир Тетрагидрофуран –циклический эфир. диметиловый
- 26. Основные свойства простых эфиров.слабые нейтральные n - основания ̈конц.
- 27. 22
- 28. Простые эфиры являются довольно инертными соединениями, и
- 29. ВИНИЛИН - «бальзам Щостаковского»поливинилбутиловый эфир Обладает
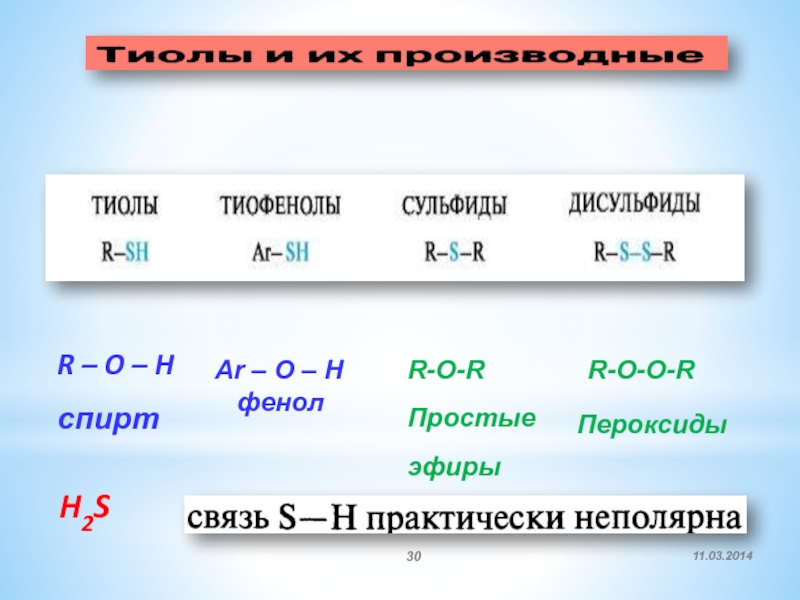
- 30. H2SR – O – HспиртAr – O
- 31. Достаточно высокая кислотность: ̈практически не обладают основными свойствами
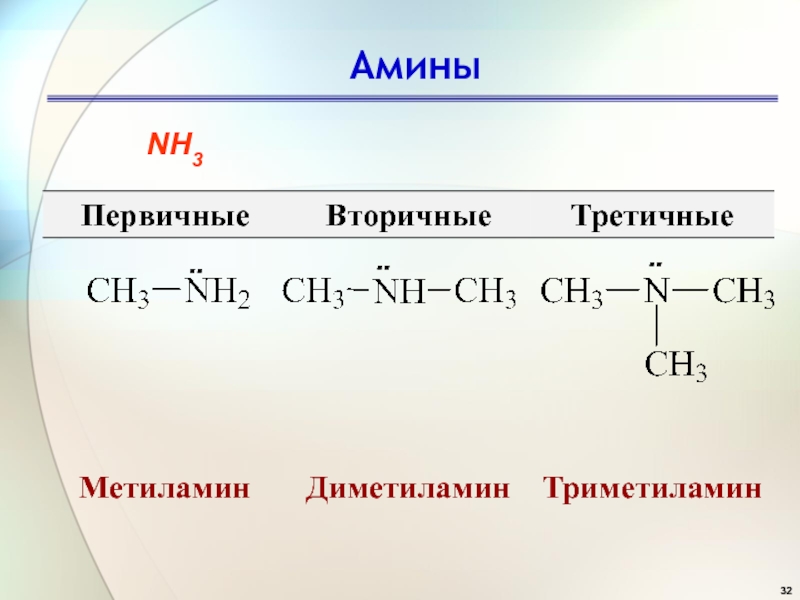
- 32. Амины NH3 ̈ ̈ ̈
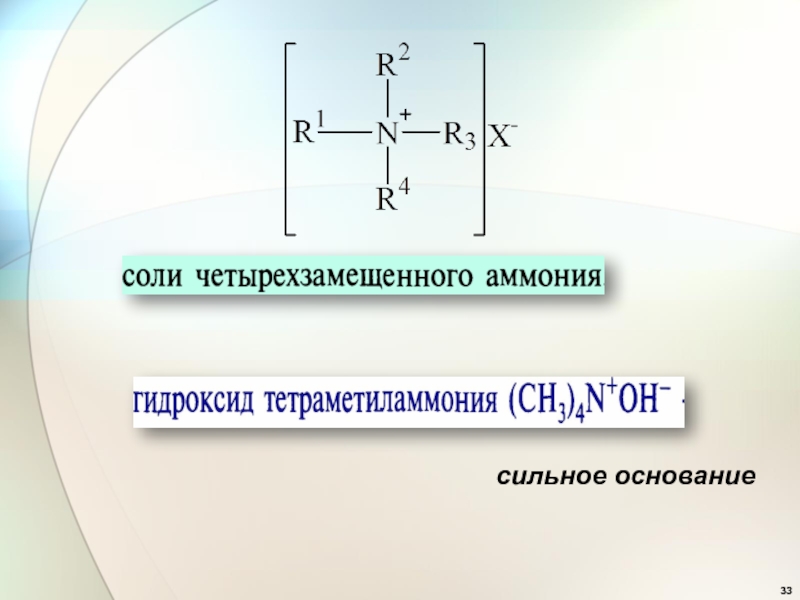
- 33. сильное основание
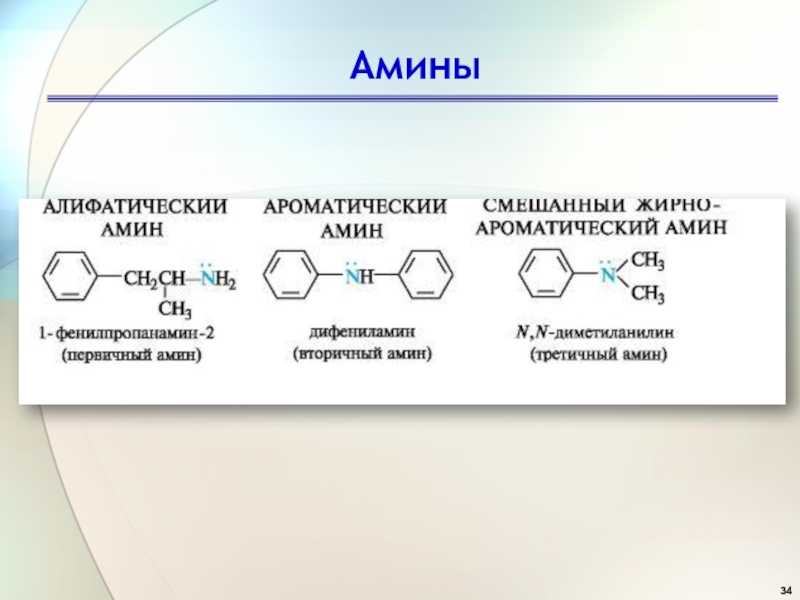
- 34. Амины
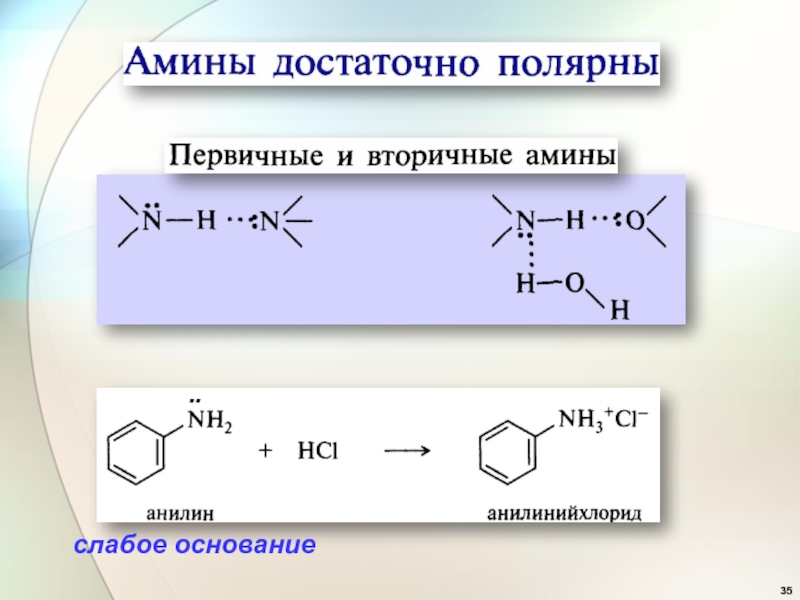
- 35. ̈слабое основание
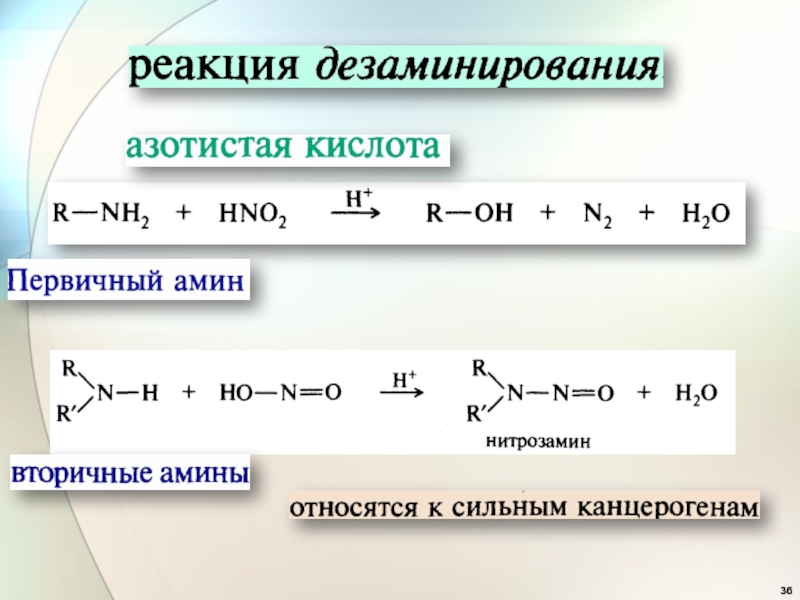
- 36. Слайд 36
- 37. Общие закономерности реакций нуклеофильного замещения, SN
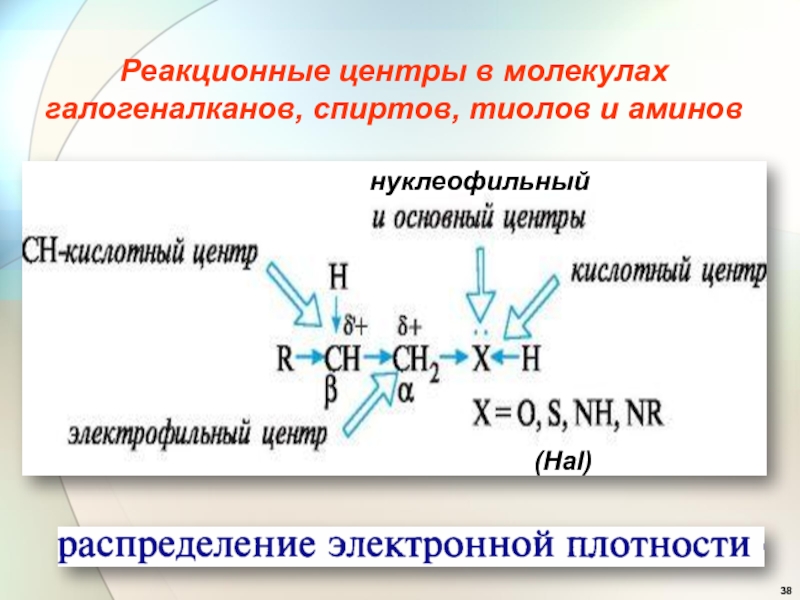
- 38. Реакционные центры в молекулах галогеналканов, спиртов, тиолов и аминов(Hal)нуклеофильный
- 39. Реакции нуклеофильного замещенияSN .
- 40. Бимолекулярное нуклеофильное
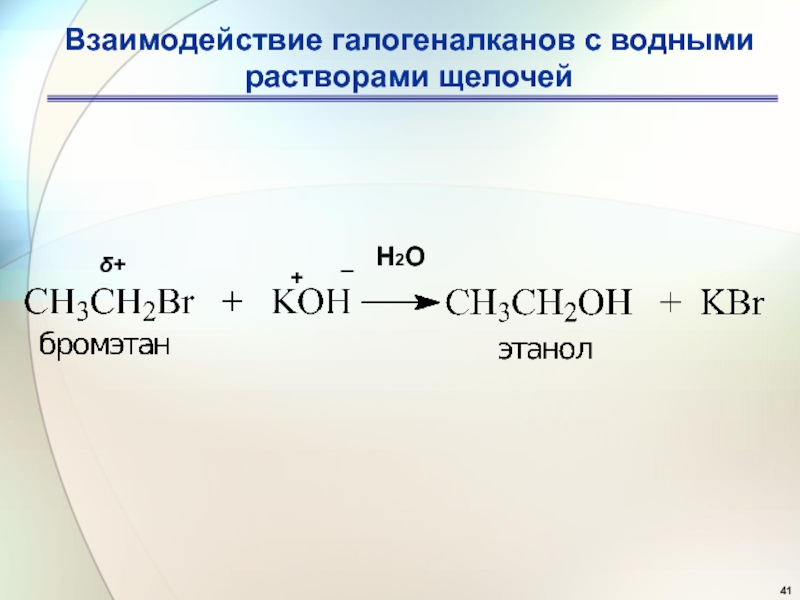
- 41. Взаимодействие галогеналканов с водными растворами щелочей Н2О+_ δ+
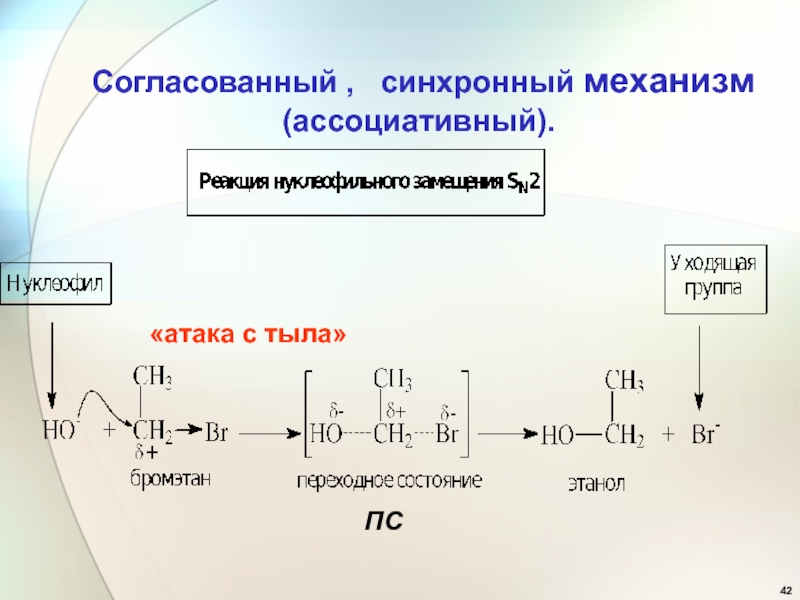
- 42. Согласованный , синхронный механизм(ассоциативный).«атака с тыла» ПС
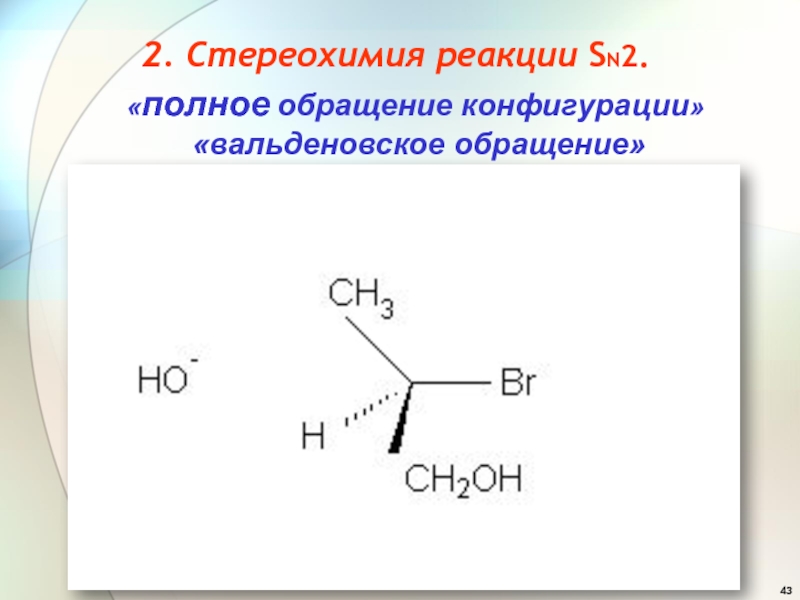
- 43. «полное обращение конфигурации» «вальденовское обращение» 2. Стереохимия реакции SN2.
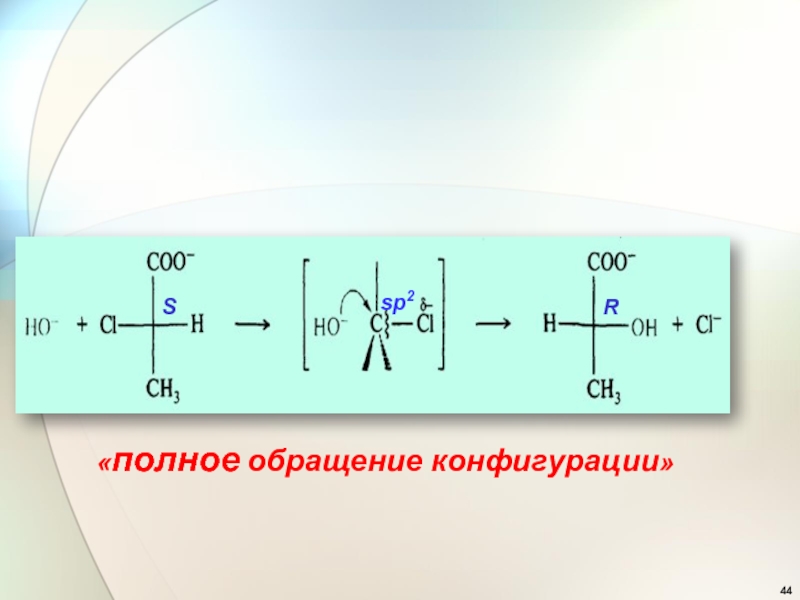
- 44. «полное обращение конфигурации» R Ssp2
- 45. 3. Влияние степени замещения реакционного
- 46. трет. галогеналкан
- 47. 4. Влияние растворителя. Нужен неполярный растворитель!Сольватация анионов
- 48. 5. Нуклеофильная реакционная способность реагента NH3 >
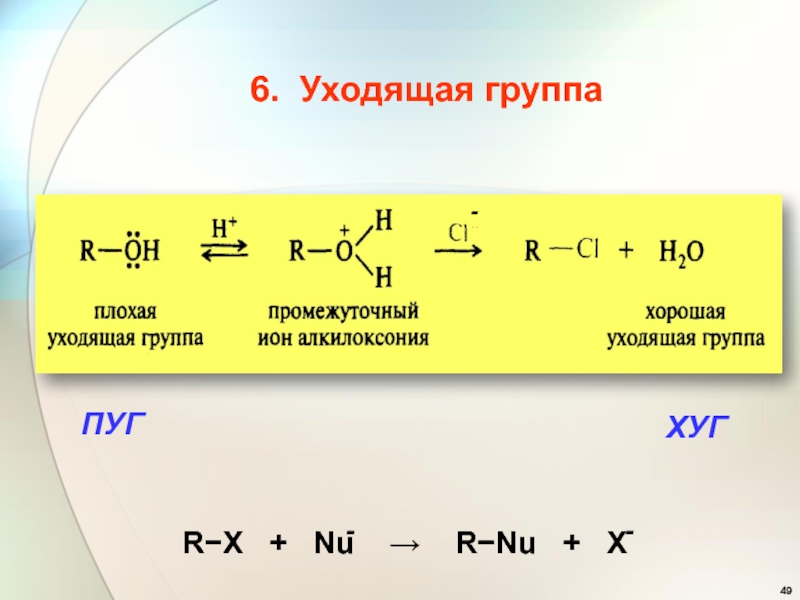
- 49. 6. Уходящая группаХУГПУГ-RX + Nu
- 50. Слайд 50
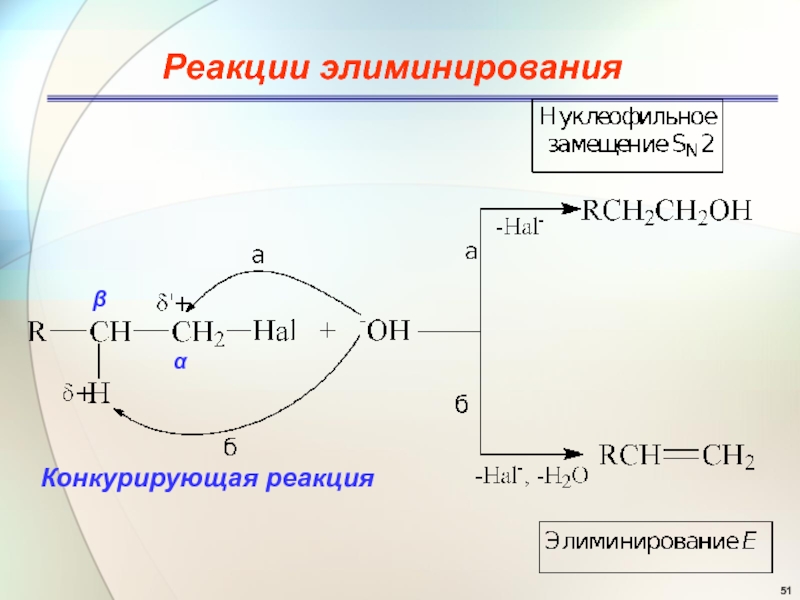
- 51. Реакции элиминированияαβКонкурирующая реакция
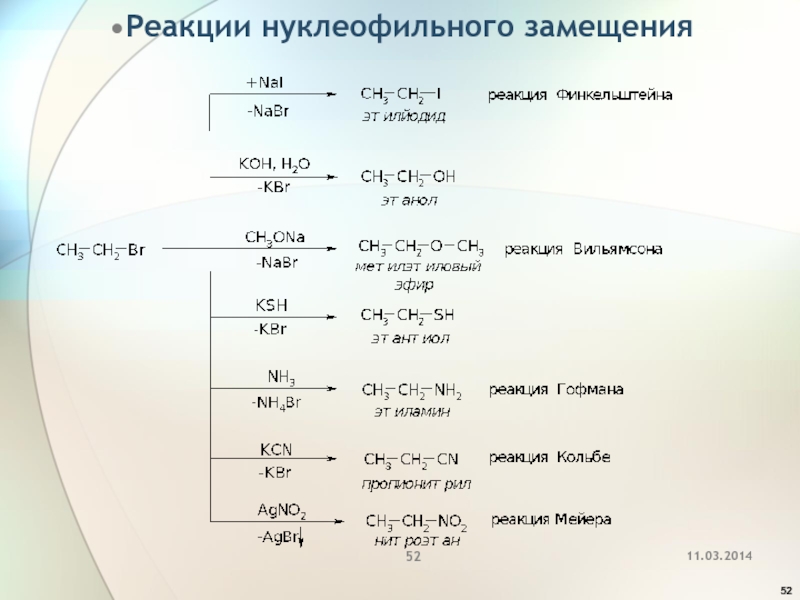
- 52. Реакции нуклеофильного замещения
- 53. Мономолекулярное нуклеофильное замещение, SN1. (асинхронный
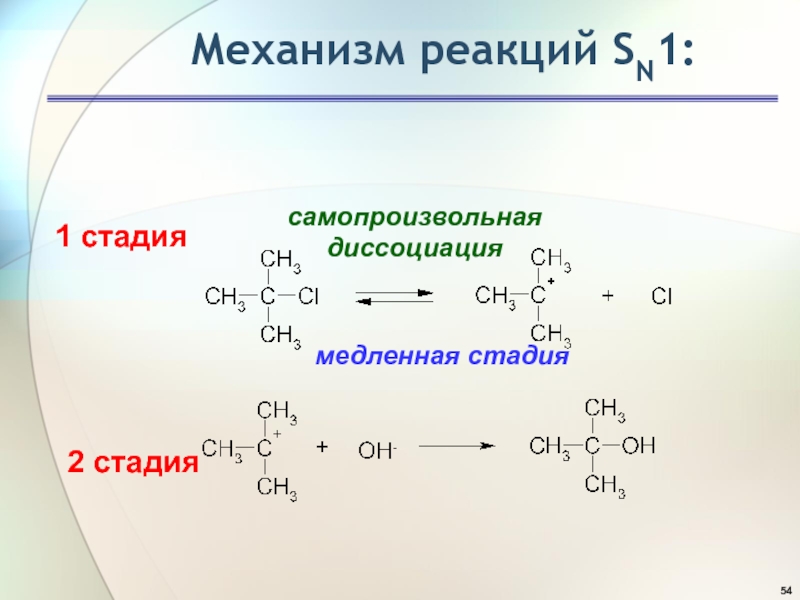
- 54. 1 стадия2 стадияМеханизм реакций SN1:самопроизвольная диссоциациямедленная стадия
- 55. Кинетический признак v = k RX Субстрат Скорость реакции
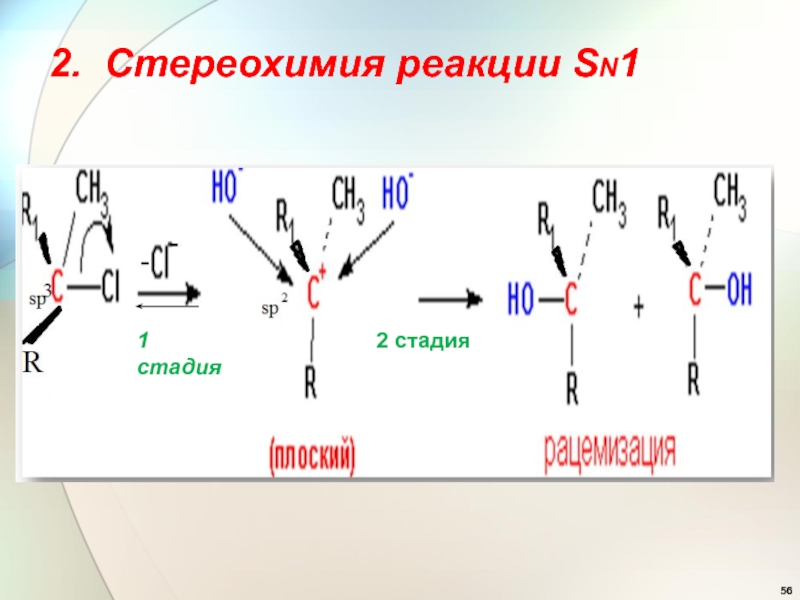
- 56. 2. Cтереохимия реакции SN1 1 стадия2 стадия
- 57. 3. Влияние R- в субстратестабильность
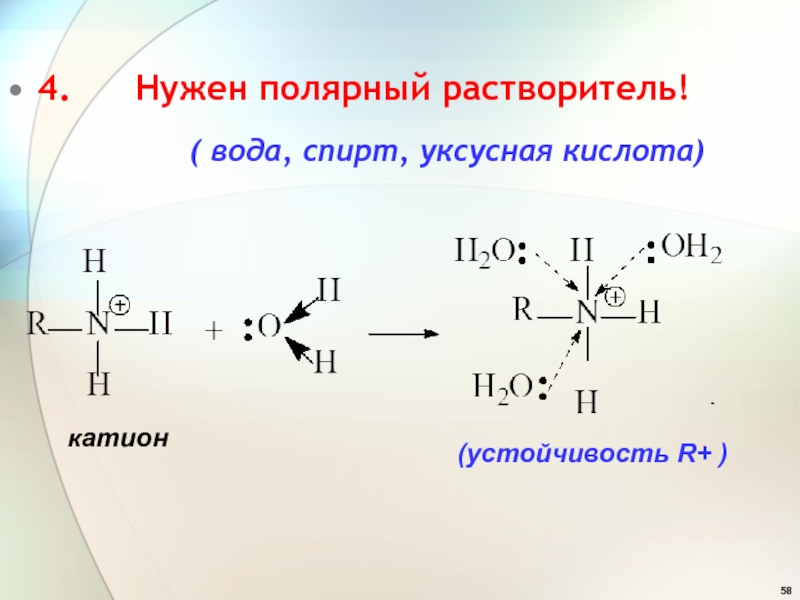
- 58. 4. Нужен полярный растворитель!
- 59. 5. Сила нуклеофила – не влияет
- 60. 1. Получение простых эфиров[ + El ]
- 61. Алкилирование аминов(реакция Гофмана, 1850) 19.02.1660 - 12.11.1742, ГаллеГофман Фридрих2. Аминолиз галогенопроизводных
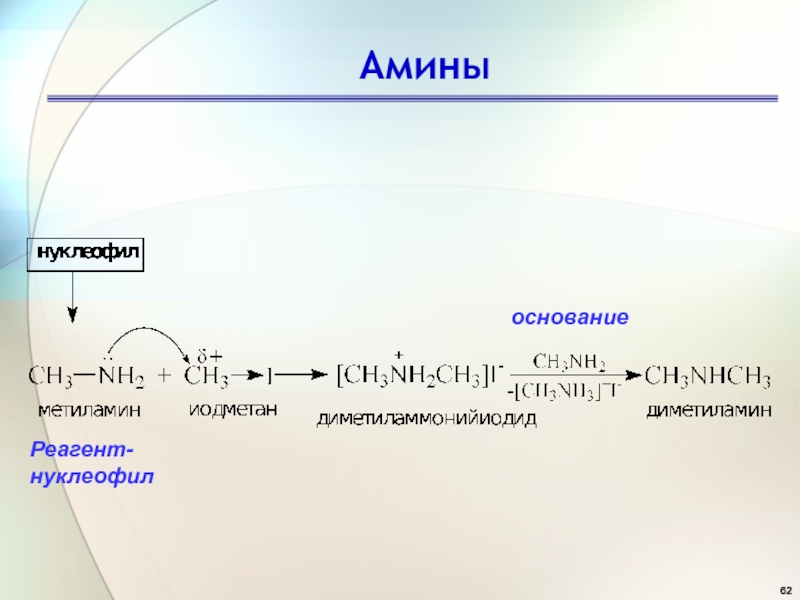
- 62. АминыРеагент-нуклеофил основание
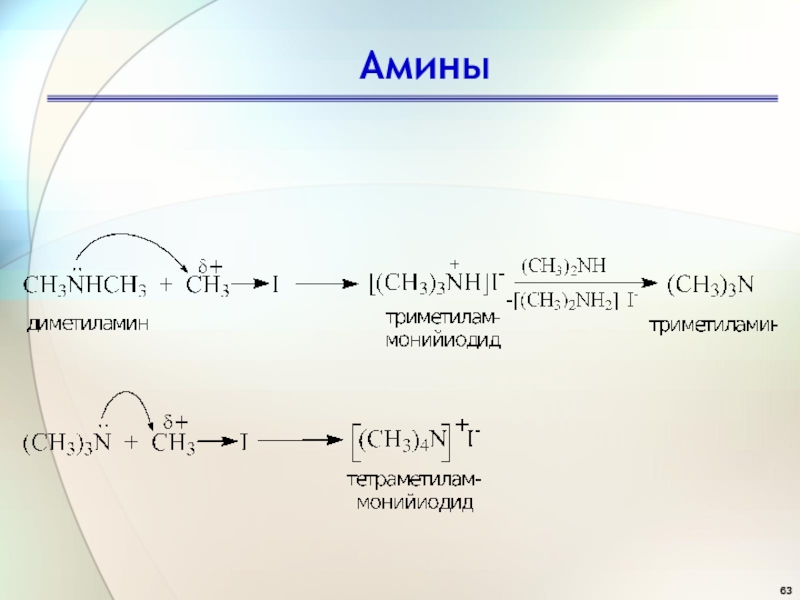
- 63. Амины
- 64. 3.Взаимодействие галогеналканов с цианидами δ+ -+
- 65. 4. Гидролиз моногалогенопроизводных (получение спиртов): RCl +H2O + KOH ROH + KCl + H2O.Моногалогено-производноеспирт δ+
- 66. Гидролиз геминального дигалогенопроизводного:Гидролиз гем.тригалогенопроизводного: карбонильное производное карбоновая кислота δ+ δ+
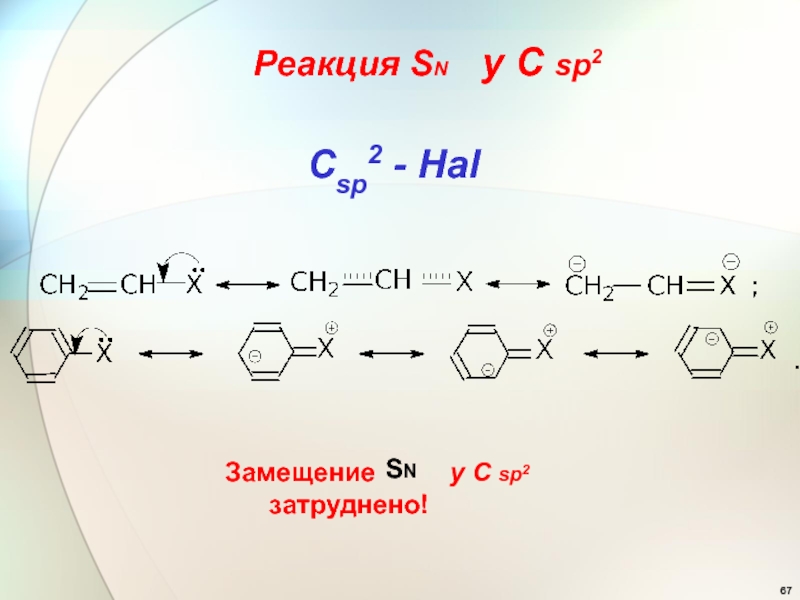
- 67. Замещение у С
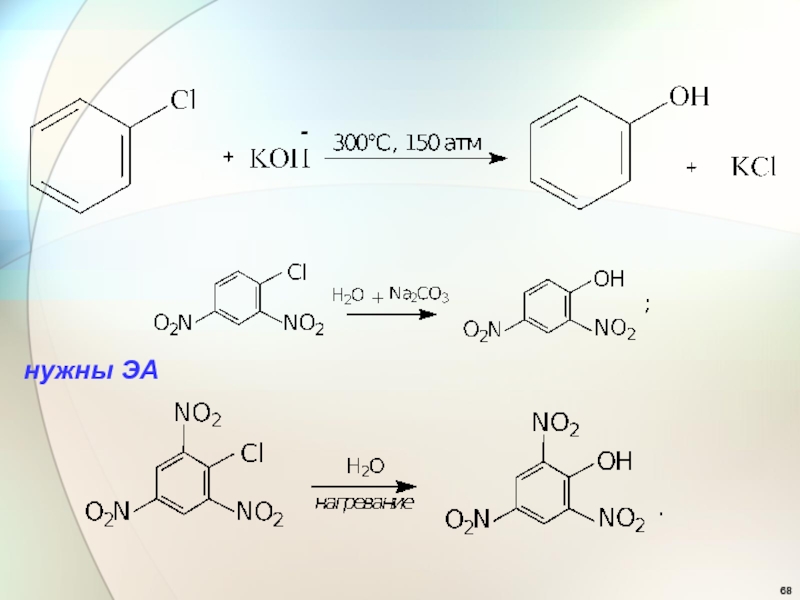
- 68. нужны ЭА -
- 69. 6. Замещение на
- 70. 8. Замещение одного галогена на другой, более
- 71. Реакции спиртов 1.Замещение
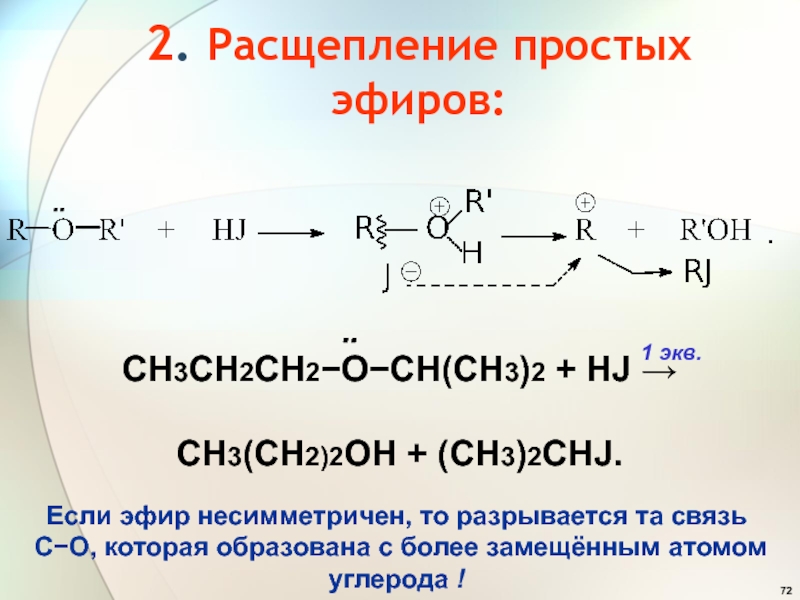
- 72. 2. Расщепление простых эфиров:СН3СН2СН2ОСН(СН3)2 + HJ
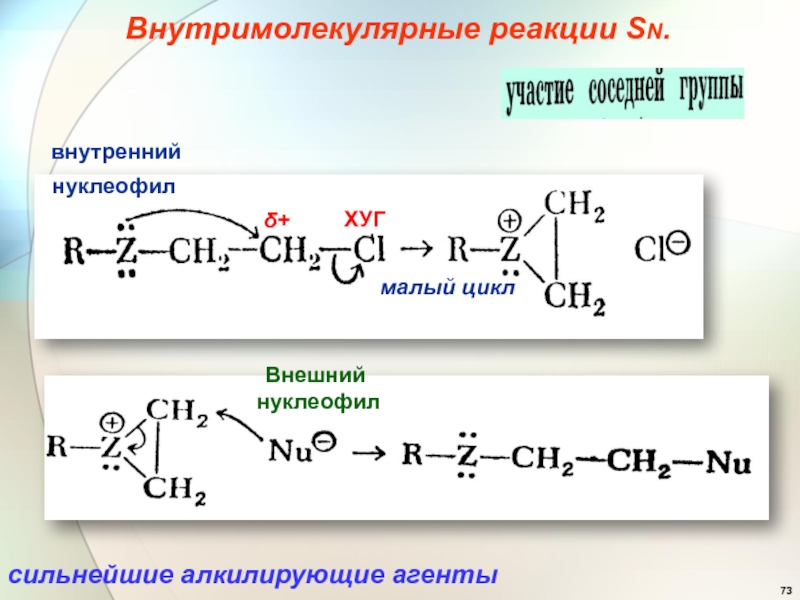
- 73. Внутримолекулярные реакции SN.малый цикл нуклеофил внутреннийХУГ Внешний нуклеофил сильнейшие алкилирующие агенты δ+
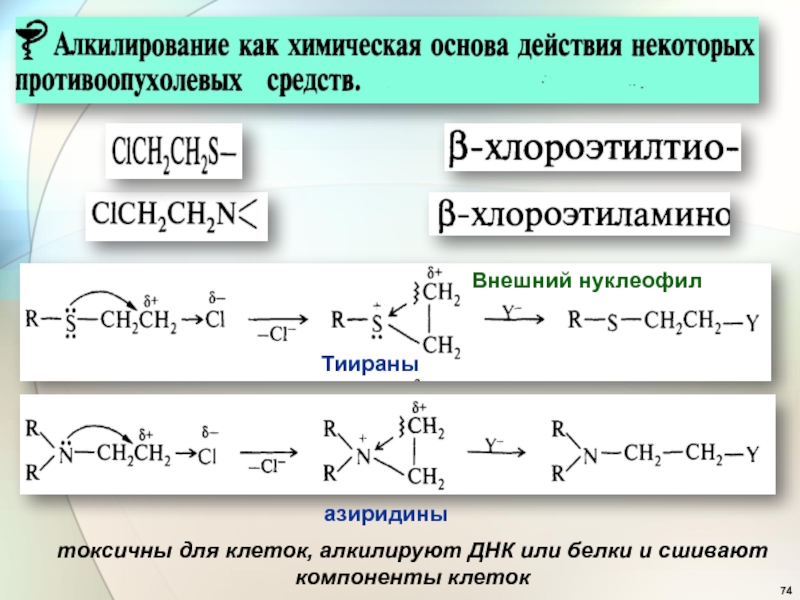
- 74. Тиираны азиридины токсичны для клеток, алкилируют ДНК или белки и сшивают компоненты клетокВнешний нуклеофил
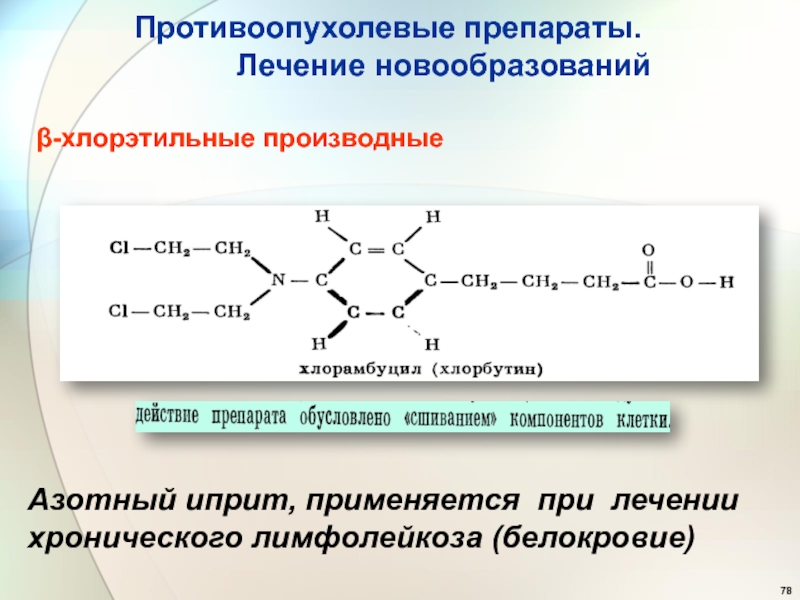
- 75. Цитотокси́ческие препараты или цитоста́тики,— это лекарственные
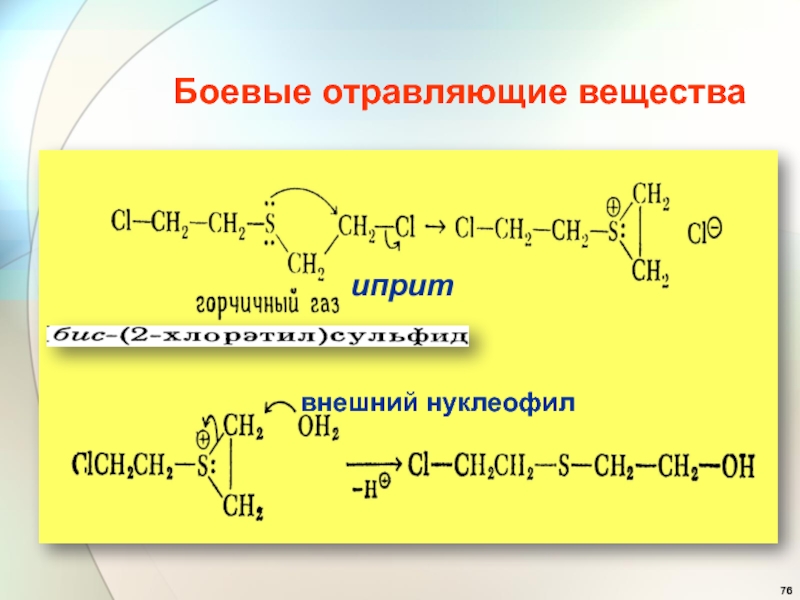
- 76. Боевые отравляющие вещества иприт внешний нуклеофил
- 77. Последствия применения иприта ( кожно-нарывное действие )
- 78. -хлорэтильные производныеАзотный иприт, применяется при лечении хронического
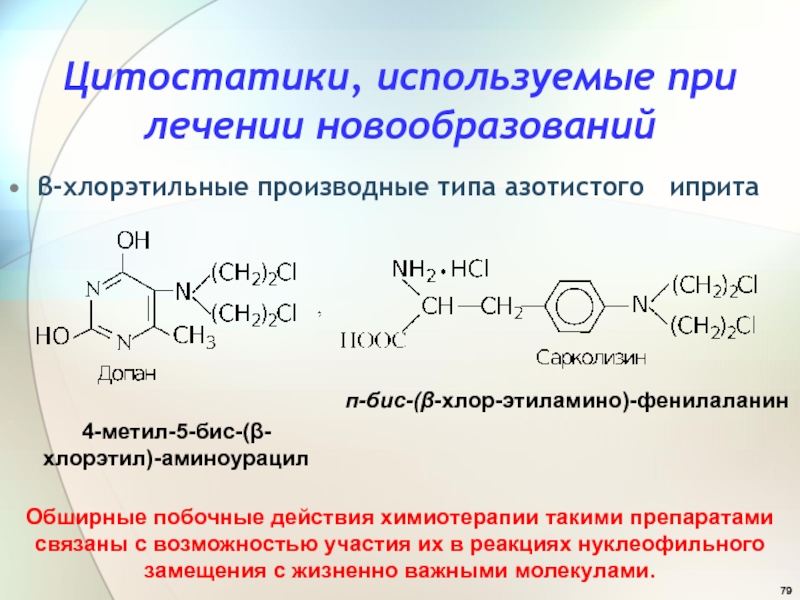
- 79. Цитостатики, используемые при лечении новообразований-хлорэтильные производные типа
- 80. Биологическое значение реакций SN
- 81. Слайд 81
- 82. Скачать презентанцию
Слайды и текст этой презентации
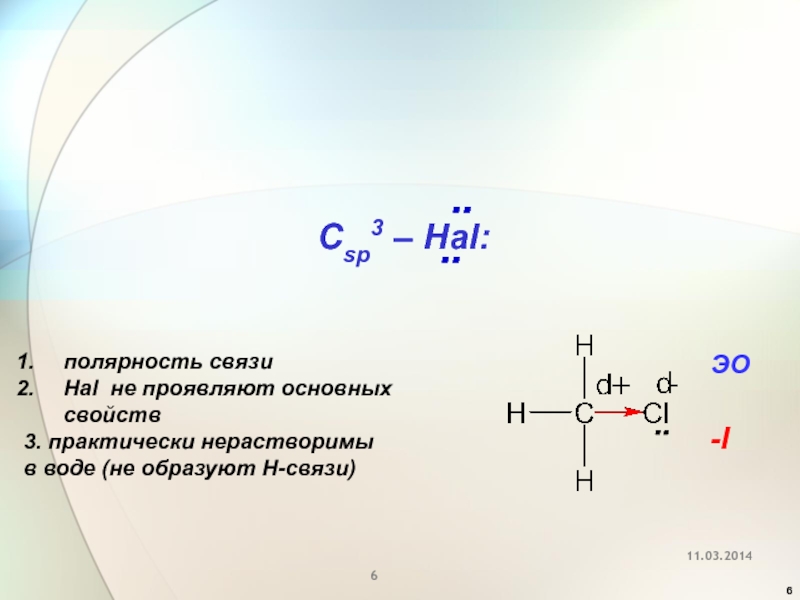
Слайд 6Csp3 – Hal:
полярность связи
Hal не проявляют основных свойств
3. практически нерастворимы
в воде (не образуют Н-связи)
̈ ̈
-I
̈
ЭО
Слайд 17Токсическое действие метанола связано с угнетением центральной нервной системы, развитием
тяжелого метаболического ацидоза, поражением сетчатки глаза и дистрофией зрительного нерва.
Летальная
доза при приёме внутрь — 100 мл (без предварительного приёма этанола).Клиника интоксикации
Опьянение выражено слабо. Метиловый спирт обычно вызывает алкогольное оглушение без типичного опьянения. Далее наступает латентный период, который длится в среднем 12-24 часа (от 1 часа до 40 часов).
С окончанием латентного периода усиливаются симптомы интоксикации — тошнота, рвота, боли в животе, головная боль, головокружение, боль в икроножных мышцах. Нарушается зрение (снижение остроты зрения, неясность видения, мелькание «мушек» перед глазами, диплопия, слепота); отмечаются мидриаз и ослабленная реакция зрачков на свет.
Сознание спутано, возможно психомоторное возбуждение или кома, судороги или гипертонус мышц конечностей. Развивается быстропрогрессирующая острая сердечно-сосудистая недостаточность в сочетании с центральными нарушениями дыхания. Смерть наступает от остановки дыхания, отёка мозга.
Слайд 19
Этиловый спирт
оказывает
опьяняющее
действие.
Злоупотребление этанолом ведёт к развитию
алкоголизма, деградации личности психическим расстройствам и соматическим заболеваниям!
Слайд 20- В высоких концентрациях этанол оказывает анестезирующее действие.
-
Используется для приготовления настоек и в качестве антисептического средства.
Слайд 23Фенол очень токсичен, при попадании на кожу вызывает ожоги. Фенол
обладает хорошими дезинфицирующими свойствами; это было первое вещество, которое использовалось
для дезинфекции (Дж. Листер, 1867)Фенолы входят в состав креозота – жидкости, получаемой из каменноугольной смолы и используемой для пропитки шпал для предотвращения их гниения. Очищенный креозот используется как антисептик в медицине.
Пентахлорфенол применяется для пропитки древесины как антисептик, инсектицид и фунгицид. Пентахлорфенолятом натрия обработаны брёвна Кижских церквей.
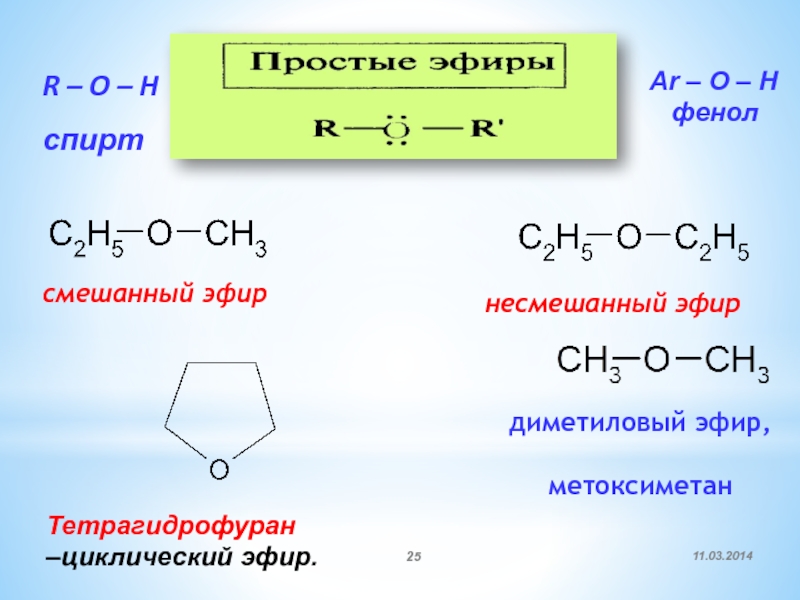
Слайд 25смешанный эфир
несмешанный эфир
Тетрагидрофуран
–циклический эфир.
диметиловый эфир,
метоксиметан
R – O
– H
спирт
Ar – O – H
фенол
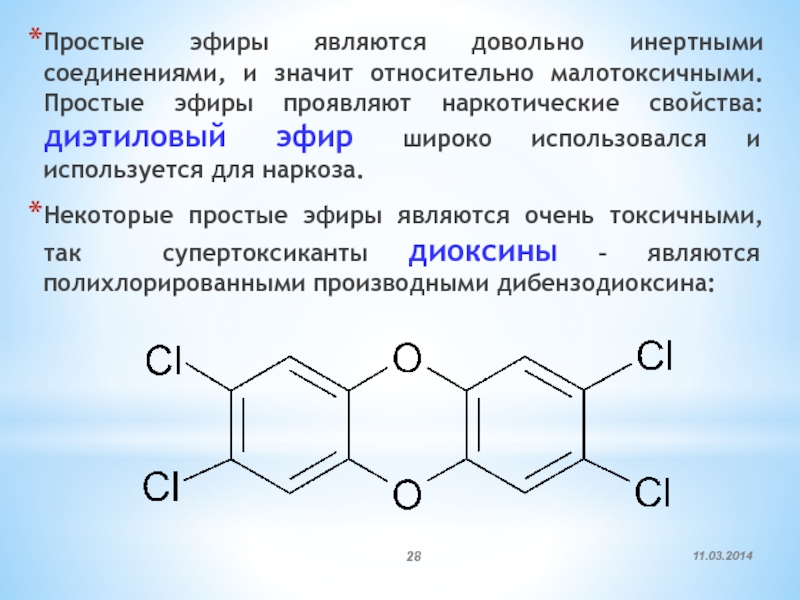
Слайд 28Простые эфиры являются довольно инертными соединениями, и значит относительно малотоксичными.
Простые эфиры проявляют наркотические свойства: диэтиловый эфир широко использовался и
используется для наркоза.Некоторые простые эфиры являются очень токсичными, так супертоксиканты диоксины – являются полихлорированными производными дибензодиоксина:
Слайд 29ВИНИЛИН - «бальзам Щостаковского»
поливинилбутиловый эфир
Обладает противомикробным действием, способствует
очищению ран, регенерации тканей и эпителизации. При приеме внутрь действует
как обволакивающее, противовоспалительное и бактериостатическое средство.CH3CH2CH2CH2 – 0 – CH = CH2
Ранозаживляющее средство
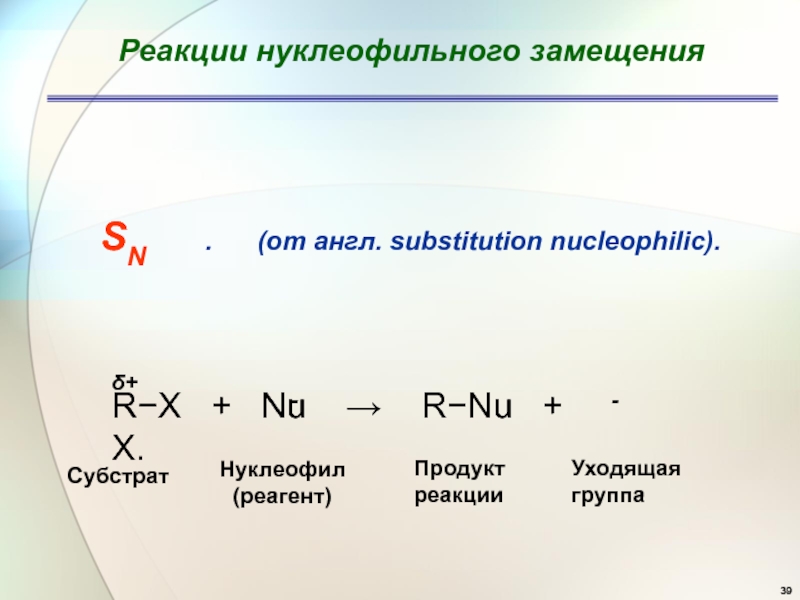
Слайд 39Реакции нуклеофильного замещения
SN . (от
англ. substitution nucleophilic).
RX + Nu
RNu + X.Субстрат
Нуклеофил
(реагент)
Продукт
реакции
Уходящая
группа
δ+
-
-
Слайд 40 Бимолекулярное нуклеофильное замещение,
SN2
v = k
RX ] [ Nu ]RX + Nu RNu + X
Кинетический признак
δ+
_
_
Субстрат
Нуклеофил
(реагент)
Продукт
реакции
Уходящая
группа
_
скорость реакции
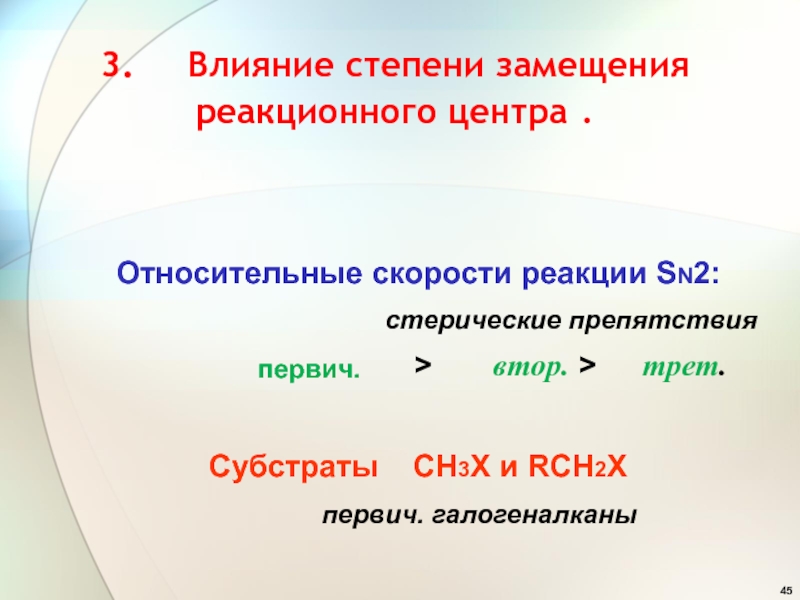
Слайд 453. Влияние степени замещения реакционного центра .
Относительные скорости
реакции SN2:
> втор. > трет.
Субстраты СН3Х и RСН2Х
первич. галогеналканы
первич.
стерические препятствия
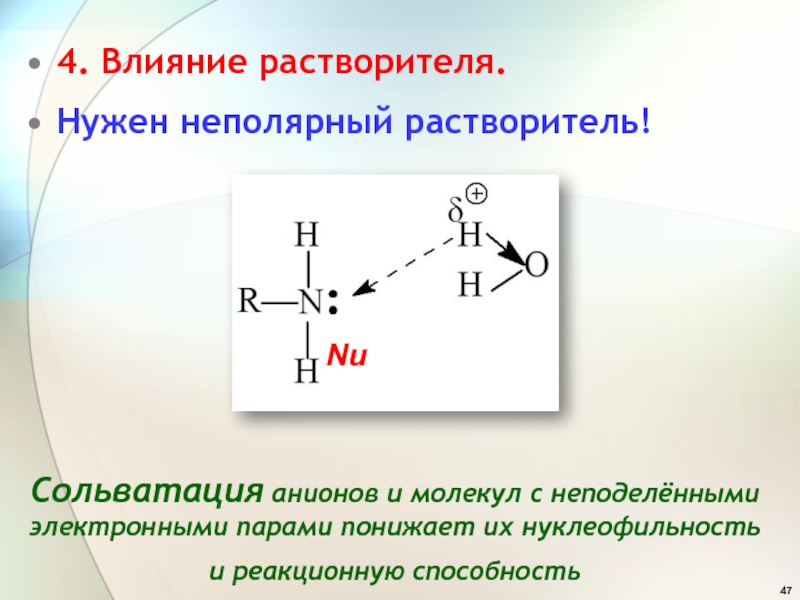
Слайд 474. Влияние растворителя.
Нужен неполярный растворитель!
Сольватация анионов и молекул с
неподелёнными электронными парами понижает их нуклеофильность и реакционную способность
Nu
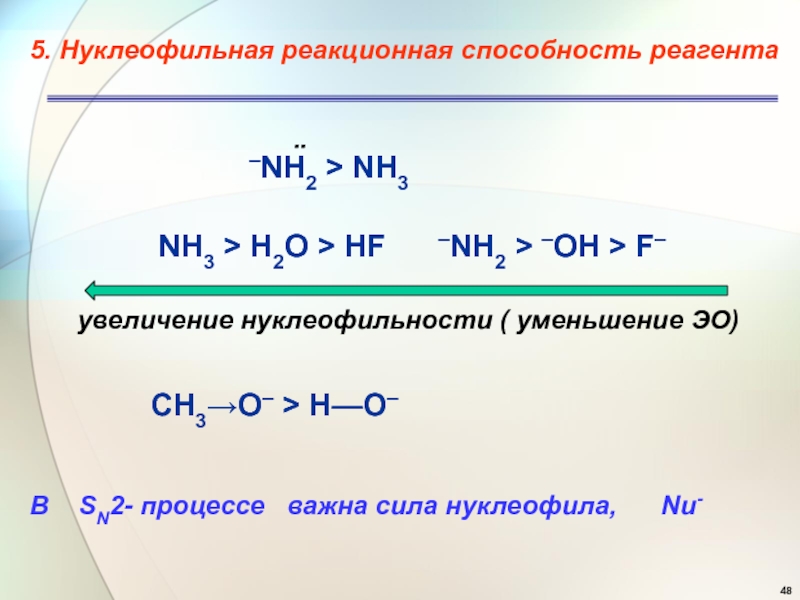
Слайд 485. Нуклеофильная реакционная способность реагента
NH3 > H2O > HF –NH2
> –OH > F–
–NH2 > NH3
CH3O– > H—O–
̈
увеличение нуклеофильности
( уменьшение ЭО)В SN2- процессе важна сила нуклеофила, Nu-
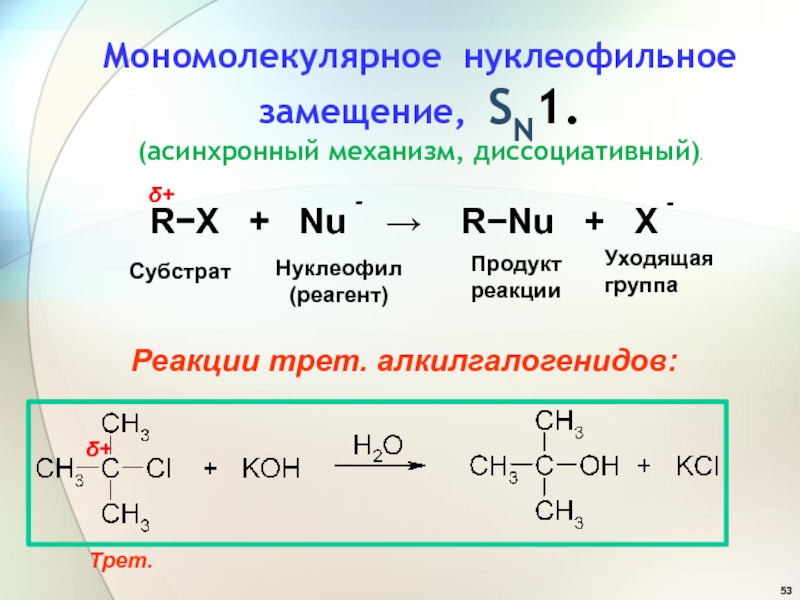
Слайд 53Мономолекулярное нуклеофильное замещение, SN1.
(асинхронный механизм, диссоциативный)а
RX +
Nu RNu + X
-
-
Трет.
Субстрат
Нуклеофил
(реагент)
δ+
Уходящая
группа
Продукт
реакции
Реакции трет. алкилгалогенидов:
δ+
Слайд 573. Влияние R- в субстрате
стабильность возникающего карбкатиона
(
возможность перегруппировок R+ )
Слайд 595. Сила нуклеофила – не влияет
( можно использовать нейтральные реагенты C2H5OH,
а не C2H5ONa )
Сравнение
реакций SN1 и SN2 ( табл.) ̈
Слайд 601. Получение простых эфиров
[ + El ]
Алкоголиз галогенопроизводных
(получение простых эфиров по
Вильямсону):Побочный
процесс
перв.
алкоголят Na
фенолят Na
простой эфир
алкоголят Na
δ+
Слайд 61Алкилирование аминов
(реакция Гофмана, 1850)
19.02.1660 - 12.11.1742,
Галле
Гофман Фридрих
2. Аминолиз
галогенопроизводных
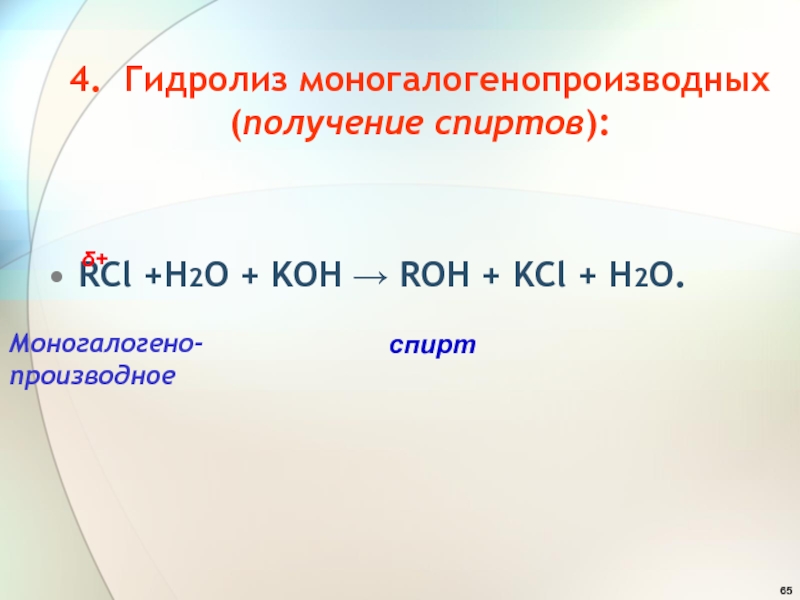
Слайд 654. Гидролиз моногалогенопроизводных (получение спиртов):
RCl +H2O + KOH
ROH + KCl + H2O.
Моногалогено-
производное
спирт
δ+
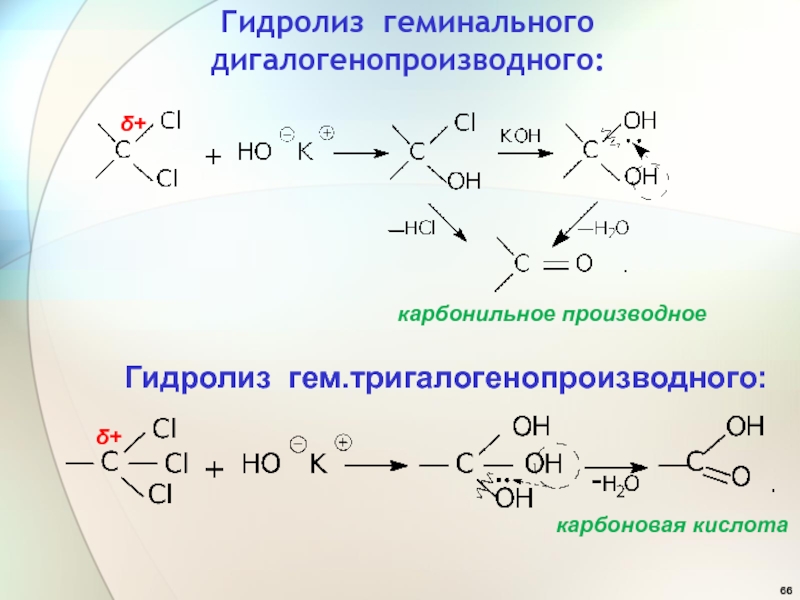
Слайд 66Гидролиз геминального дигалогенопроизводного:
Гидролиз гем.тригалогенопроизводного:
карбонильное производное
карбоновая кислота
δ+
δ+
Слайд 69 6. Замещение на карбоксилат-анион (получение сложных
эфиров):
RHal + R'COONa+ ROCOR' + NaHal.
7. Замещение на нуклеофильную серу:а) получение тиолов:
ОН -
RHal + H2S RSH + HHal;
б) получение сульфидов:
RHal + NaSR1 RSR1 + NaHal.
алкилтиолят натрия
сульфид
δ+
δ+
δ+
-
̈
Слайд 708. Замещение одного галогена на другой, более нуклеофильный
ацетон
RBr (RCl) + NaJ RJ + NaBr (NaCl).
нуклеофильность реагента
качество уходящей группы
J Br Cl F
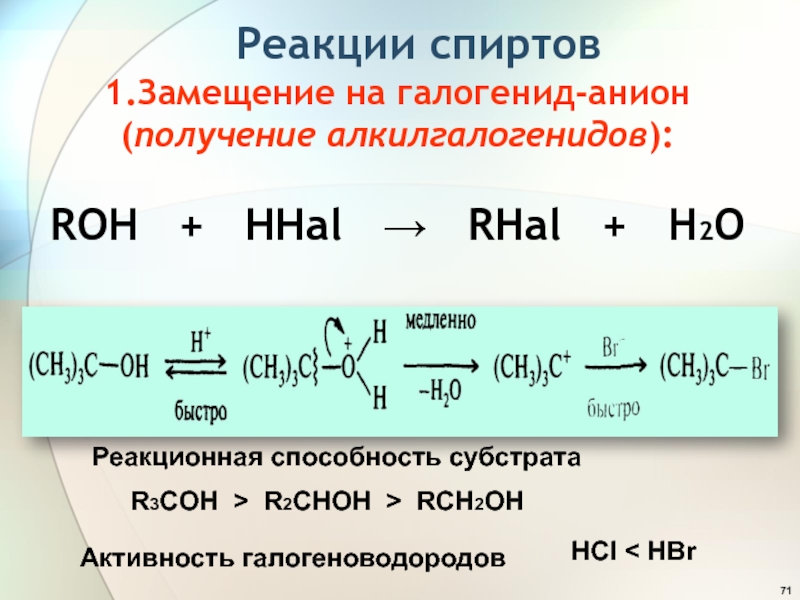
Слайд 71 Реакции спиртов 1.Замещение на галогенид-анион (получение алкилгалогенидов):
ROH + HHal RHal
+ H2O Реакционная способность субстрата
R3COH R2CHOH RCH2OH
Активность галогеноводородов
HCl HBr




















![№7.Нуклеофильное замещение у насыщенного атома углерода, S N у C sp 3 1. Получение простых эфиров[ + El ] Алкоголиз 1. Получение простых эфиров[ + El ] Алкоголиз галогенопроизводных (получение](/img/thumbs/44fb7149e6fa7c1482768511733f0637-800x.jpg)