Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Общие свойства металлов
Содержание
- 1. Общие свойства металлов
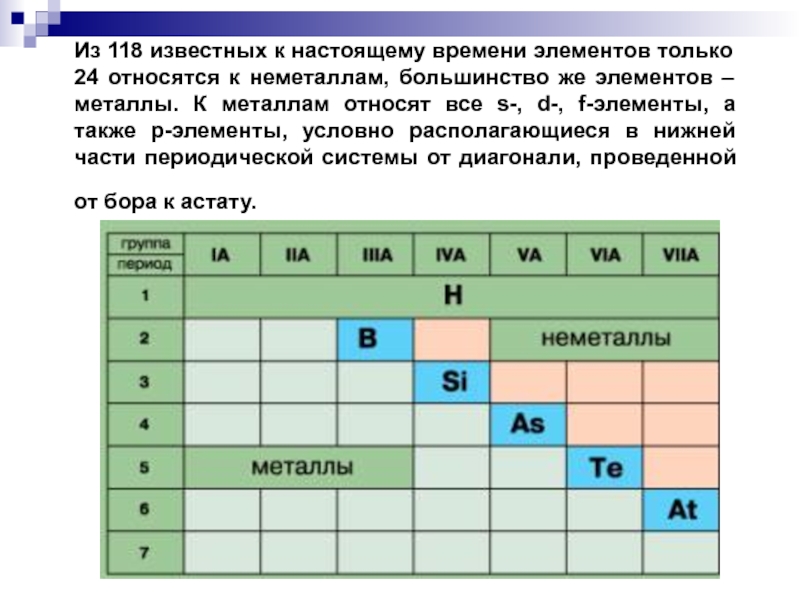
- 2. Из 118 известных к настоящему времени элементов
- 3. Металлыэто элементы, между атомами которых осуществляется металлическая
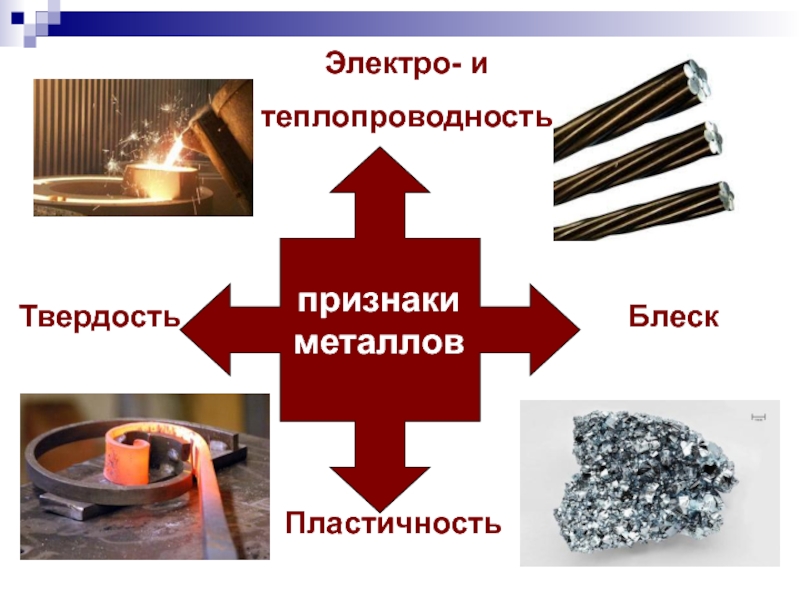
- 4. признаки металловТвердостьПластичностьБлескЭлектро- и теплопроводность
- 5. Классификация металловВ технике основана на различии физических
- 6. По температурам плавления, периодически изменяющимся с ростом
- 7. Классификация металловМеталлы отличаются также своим отношением к
- 8. В практике имеет место исторически сложившееся деление
- 9. под металлами принято понимать элементы, атомы которых
- 10. Слайд 10
- 11. В больших периодах между s- и p-элементами
- 12. Характер оксидов d-элементов зависит от степени окисления
- 13. К f-металлам относятся лантаноиды и актиноиды. У
- 14. Атомы металлов кристаллизуются лишь в трех структурах
- 15. Металлы в природеСамый распространенный металл на Земле – алюминий (более 8% земной коры)
- 16. Состав руд чрезвычайно разнообразен, часто металлы представлены
- 17. пиролюзит MnO2касситерит SnO2
- 18. Сульфидные минералы гaленит PbSарсенопирит FeAsS
- 19. халькопирит СuFeS2пирит FeS2молибденит MoS2
- 20. Силикаты и алюмосиликаты:ZrSiO4 – циркон;3BeO· Al2O3· 6SiO2
- 21. Получением металлов занимается металлургия – одна из наиболее древних отраслей химической технологии.
- 22. Слайд 22
- 23. ПирометаллургияПирометаллургическими считаются методы высокотемпературного извлечения металлов из
- 24. Сульфидные руды подвергают окислительному обжигу, а карбонатные
- 25. Восстановление водородом проводится, как правило, тогда, когда
- 26. Металлотермия используется обычно при восстановлении наиболееустойчивых соединений. Cr2O3 + 2Al = 2Cr + Al2O3
- 27. Гидрометаллургия связана с низкотемпературными процессами получения металлов,
- 28. Выщелачивание металлов из руд с помощью серной кислоты - один из основных процессов гидрометаллургии
- 29. Электрометаллургия включает процессы получения металлов с применением
- 30. Электролиз в настоящее время успешно применяется в
- 31. Химические свойстваХимическую активность металлов в компактном состоянии
- 32. Ряд напряжений по существу представляет собой ряд
- 33. Активные металлы вытесняют из солей менее активные
- 34. Взаимодействие металлов с неметалламиВ результате возможно образование
- 35. Взаимодействие с кислотамиВ химической практике наиболее часто
- 36. РАЗБАВЛЕННАЯ СЕРНАЯ КИСЛОТА реагирует с металлами различной
- 37. Концентрированная серная кислота служит окислителем особенно при
- 38. Например:8Na + 5H2SO4 (к)
- 39. Взаимодействие разбавленной азотной кислоты с металлами различной
- 40. Например,4Ca + 10HNO3 =
- 41. HNO3 концентрированная является одним из самых сильных
- 42. Стандартный электродный потенциал системы2H2O + 2ē =
- 43. Взаимодействие металлов со щелочамиСо щелочами взаимодействуют только
- 44. Скачать презентанцию
Слайды и текст этой презентации
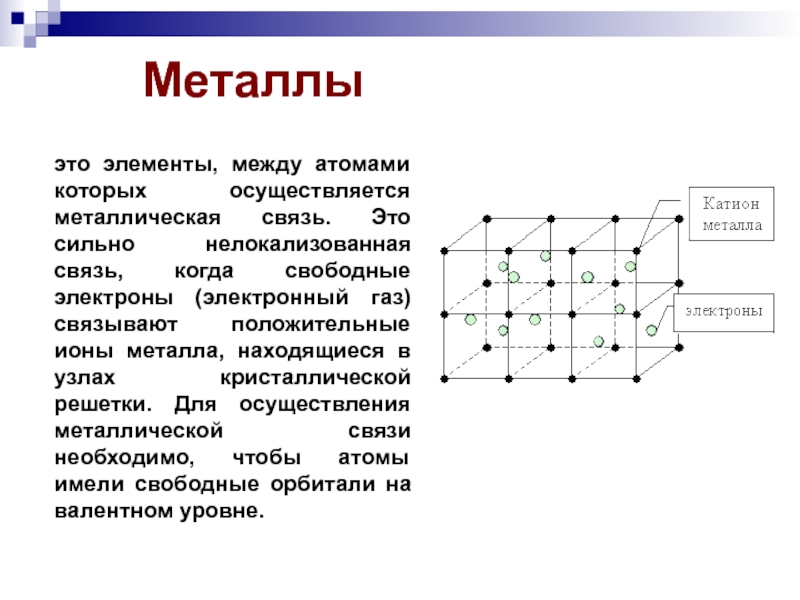
Слайд 3Металлы
это элементы, между атомами которых осуществляется металлическая связь. Это сильно
нелокализованная связь, когда свободные электроны (электронный газ) связывают положительные ионы
металла, находящиеся в узлах кристаллической решетки. Для осуществления металлической связи необходимо, чтобы атомы имели свободные орбитали на валентном уровне.Слайд 5Классификация металлов
В технике основана на различии физических свойств
По величине плотности
их делят на
легкие (ρ < 5 г/см3) и
тяжелые
(ρ > 5 г/см3). Самым легким считается
Литий (ρ = 0,53 г/см3),
максимальную
плотность имеет осмий
(ρ = 22,5 г/см 3).
Слайд 6По температурам плавления, периодически изменяющимся с ростом порядкового номера элемента,
различают
легкоплавкие металлы, с температурой плавления ниже 1000 °С, и
тугоплавкие – выше 1500 °С.Классификация металлов
Минимальную температуру
плавления имеет ртуть (-38,89 °С),
максимальную –
вольфрам (3410 °С).
Слайд 7Классификация металлов
Металлы отличаются также своим отношением к магнитным полям. По
этому свойству они делятся на три группы:
ферромагнитные металлы – способные
намагничиваться при действии слабых магнитных полей (железо, кобальт, никель, гадолиний);парамагнитные металлы – проявляющие слабую способность к намагничиванию (алюминий, хром, титан и большая часть лантаноидов);
диамагнитные металлы – не притягивающиеся к магниту и даже слегка отталкивающиеся от него (висмут, олово, медь).
Слайд 8В практике имеет место исторически сложившееся деление металлов на черные
и цветные.
Классификация металлов
Все остальные металлы
объединяют в группу цветных.
К
черным принято относить железо, сплавы на его основе и металлы,
которые применяются
в этих сплавах (Mn, Cr).
Слайд 9под металлами принято понимать элементы, атомы которых благодаря низким ионизационным
потенциалам склонны к отдаче электронов и образованию положительных ионов:
Na –
ē = Na+Ba – 2 ē = Ba2+
С электрохимической точки зрения
На основании структуры электронной оболочки атомов
к металлам относят
s-элементы (кроме водорода и гелия);
p-элементы ( Al, Ga, In, Tl, Sn, Pb, Bi ) ;
d- и f-элементы.
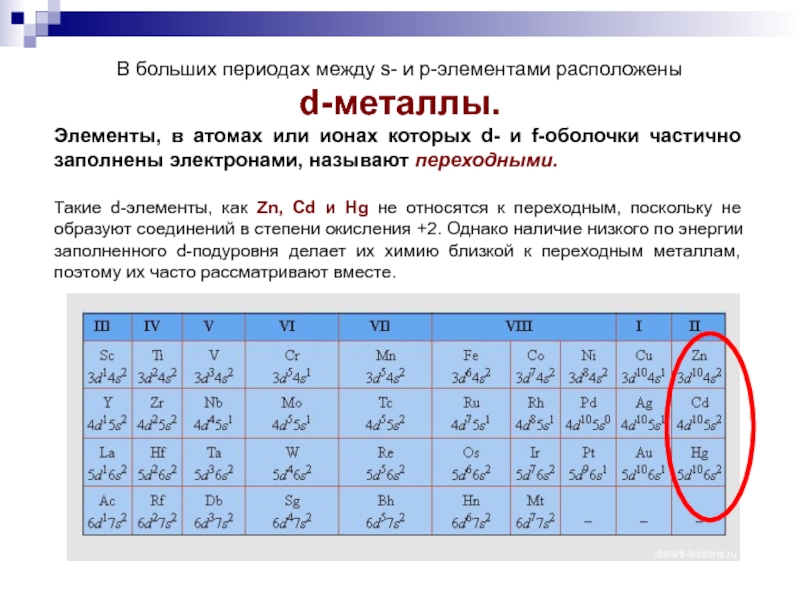
Слайд 11В больших периодах между s- и p-элементами расположены
d-металлы.
Элементы, в
атомах или ионах которых d- и f-оболочки частично заполнены электронами,
называют переходными.Такие d-элементы, как Zn, Cd и Hg не относятся к переходным, поскольку не образуют соединений в степени окисления +2. Однако наличие низкого по энергии заполненного d-подуровня делает их химию близкой к переходным металлам, поэтому их часто рассматривают вместе.
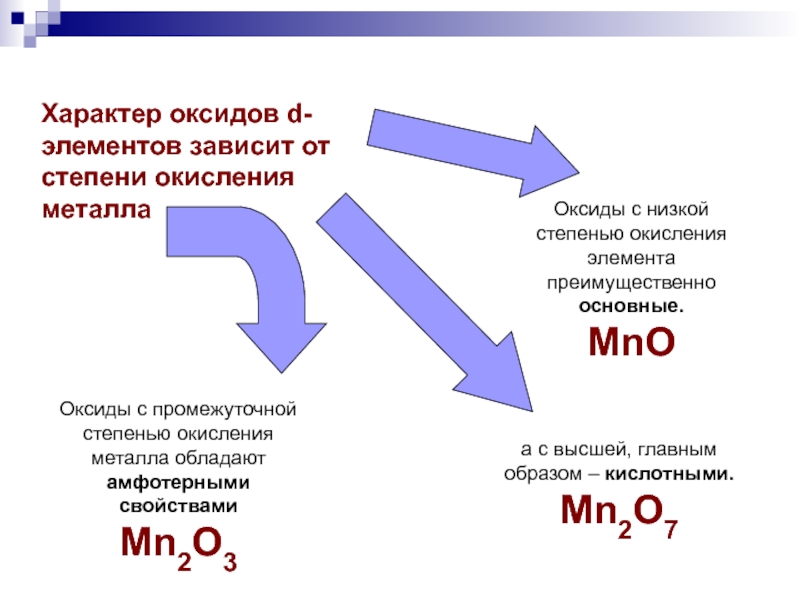
Слайд 12Характер оксидов d-элементов зависит от степени окисления металла
Оксиды с
низкой степенью окисления элемента преимущественно основные.
MnO
Оксиды с промежуточной степенью окисления
металла обладают амфотерными свойствамиMn2O3
а с высшей, главным образом – кислотными.
Mn2O7
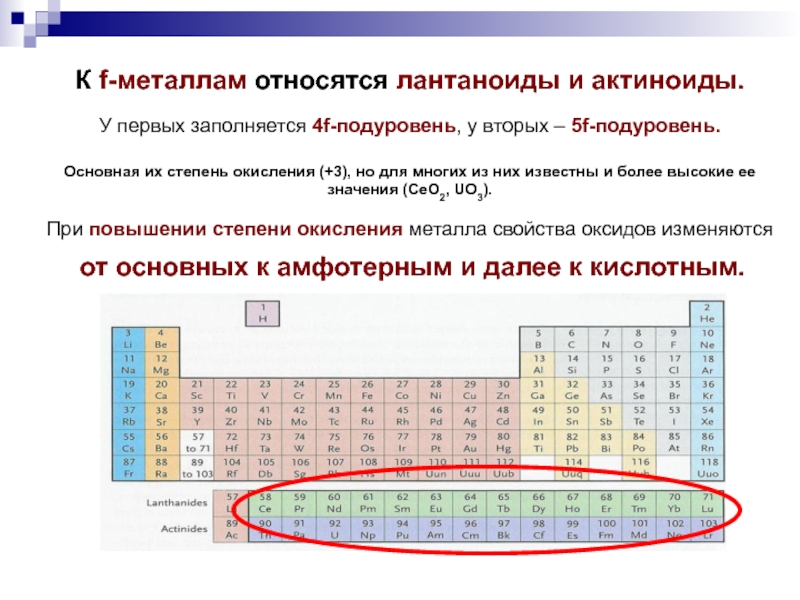
Слайд 13К f-металлам относятся лантаноиды и актиноиды.
У первых заполняется 4f-подуровень,
у вторых – 5f-подуровень.
Основная их степень окисления (+3), но
для многих из них известны и более высокие ее значения (CeO2, UO3). При повышении степени окисления металла свойства оксидов изменяются
от основных к амфотерным и далее к кислотным.
Слайд 14Атомы металлов кристаллизуются лишь в трех структурах с плотней-
шей упаковкой
частиц:
1) объемноцентрированной кубической (кч = 8) – Li, Na, K,
Rb, Cs, Ba;2) гранецентрированной кубической (кч =12) – Ca, Sr, Cu, Ag. Au и др.;
3) гексоганальной (кч = 12) – Be, Mg, Ca, Os и др.
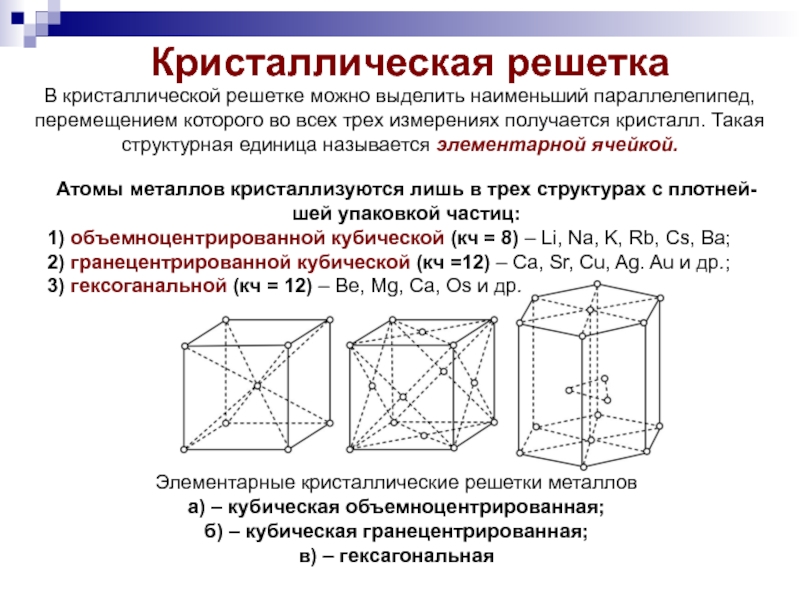
Кристаллическая решетка
В кристаллической решетке можно выделить наименьший параллелепипед, перемещением которого во всех трех измерениях получается кристалл. Такая структурная единица называется элементарной ячейкой.
Элементарные кристаллические решетки металлов
а) – кубическая объемноцентрированная;
б) – кубическая гранецентрированная;
в) – гексагональная
Слайд 16Состав руд чрезвычайно разнообразен, часто металлы представлены в них в
виде оксидных или сульфидных минералов.
Оксидные минералы
гематит Fe2O3
боксит Al2O3 ·
n H2Oкуприт Cu2O
Слайд 20Силикаты и алюмосиликаты:
ZrSiO4 – циркон;
3BeO· Al2O3· 6SiO2 –берилл;
Na2O (K2O) ·Al2O3
·2SiO2 – нефелин.
Минералы-соли
Карбонаты:
CaCO3 – кальцит (мел, мрамор, известняк);
SrCO3 –
стронцианит;CaCO3 · MgCO3- доломит.
Сульфаты:
BaSO4 – барит;
CaSO4 2H2O – гипс;
Na2SO4·10H2O – мирабилит;
Галиды:
KCl – сильвин;
NaCl · KCl – сильвинит;
KCl ·MgCl2 ·H2O – карналлит;
3NaF· AlF3 – криолит;
Полиметаллические руды:
FeTiO3 – ильменит (титанат);
CaWO4 – шеелит (вольфрамат);
PbCrO4 – кроксит (хромат) и др.
Некоторые металлы не образуют рудных залежей. Их принято называть
рассеянными – Ga, In, Tl и др.
Слайд 21Получением металлов занимается металлургия – одна из наиболее древних отраслей
химической технологии.
Слайд 23Пирометаллургия
Пирометаллургическими считаются методы высокотемпературного извлечения металлов из различных соединений.
Чаще
всего это процессы восстановления:
более активными металлами
Al, Mg,
Ca, Na и др. (металлотермия),
кремнием (силикатотермия),
водородом,
гидридами металлов и т. д.
Слайд 24Сульфидные руды подвергают окислительному обжигу, а карбонатные – прокаливанию. Полученные
оксиды затем восстанавливают:
2PbS + 3O2 = 2PbO + 2SO2;
PbO +CO
= Pb + CO2;ZnCO3 = ZnO + CO2;
2ZnO + C = 2Zn + CO2
Например,
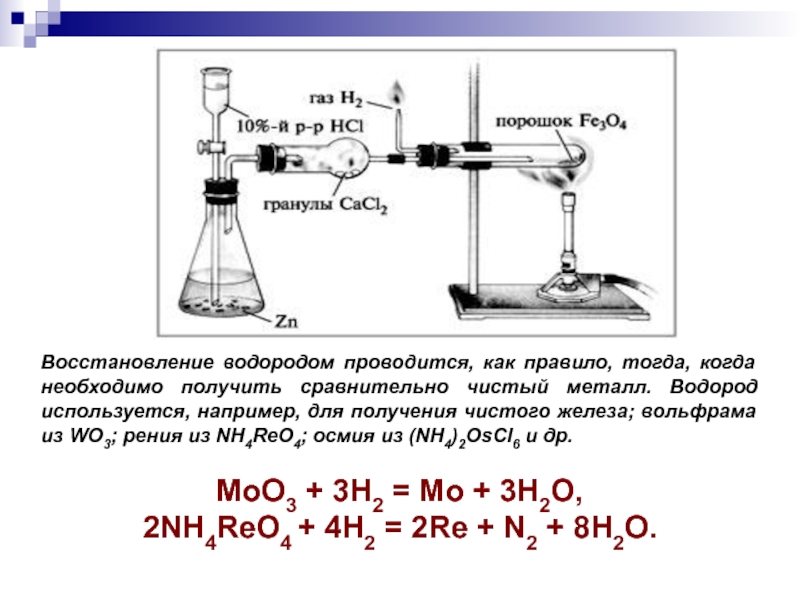
Слайд 25Восстановление водородом проводится, как правило, тогда, когда необходимо получить сравнительно
чистый металл. Водород используется, например, для получения чистого железа; вольфрама
из WO3; рения из NH4ReO4; осмия из (NH4)2OsCl6 и др.MoO3 + 3H2 = Mo + 3H2O,
2NH4ReO4 + 4H2 = 2Re + N2 + 8H2O.
Слайд 26Металлотермия
используется обычно при восстановлении наиболее
устойчивых соединений.
Cr2O3 + 2Al
= 2Cr + Al2O3
Слайд 27Гидрометаллургия
связана с низкотемпературными процессами получения металлов, протекающими в растворах
(преимущественно в водных).
В гидрометаллургических процессах обычно подбирается растворитель, который
переводит в раствор металл и оставляет нерастворенной пустую породу: CuS + Fe2(SO4)3 = CuSO4 + 2FeSO4 + S.
Медь из раствора может быть выделена восстановлением более активным металлом или электролизом.
Гидрометаллургическим методом отделяют Ag, Au, Pb и другие металлы от пустой породы.
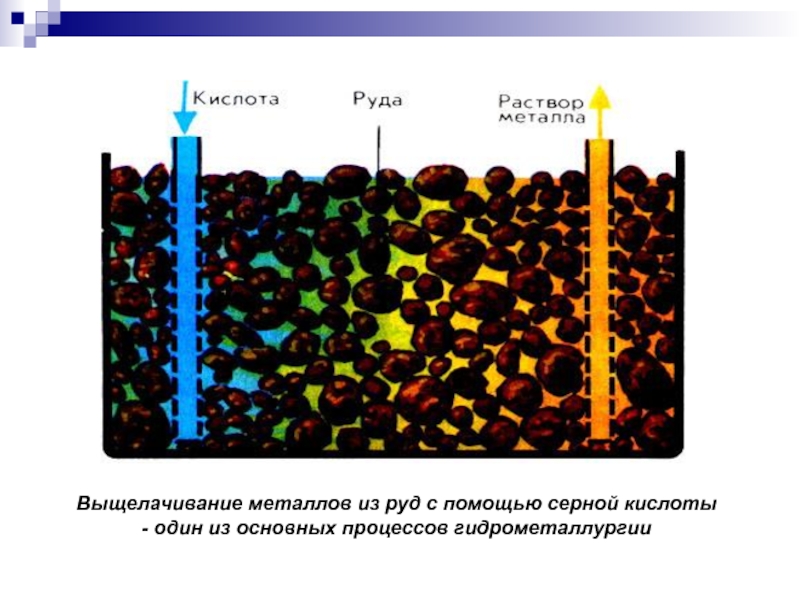
Слайд 28Выщелачивание металлов из руд с помощью серной кислоты - один
из основных процессов гидрометаллургии
Слайд 29Электрометаллургия
включает процессы получения металлов с применением электрического тока –
это электротермия и электролиз.
При электротермии электрический ток служит источником создания
высоких температур (например, выплавка стали в электропечах);при электролизе – используется для непосредственного выделения металлов из соединений.
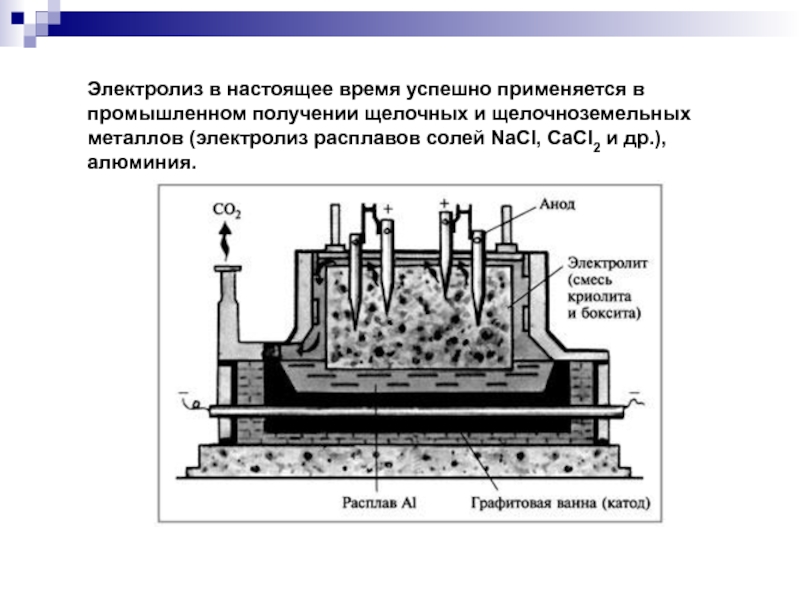
Слайд 30Электролиз в настоящее время успешно применяется в промышленном получении щелочных
и щелочноземельных металлов (электролиз расплавов солей NaCl, CaCl2 и др.),
алюминия.Слайд 31Химические свойства
Химическую активность металлов в компактном состоянии оценивают обычно по
энергии ионизации: чем меньше энергия или потенциал ионизации, тем легче
атомы отдают электроны и тем активнее металл.В подгруппах s- и р-элементов (сверху вниз) наблюдается значительное увеличение радиуса атома и снижение энергии ионизации. Самые низкие значения энергии ионизации (4–5 эВ/моль) имеют щелочные металлы.
В подгруппах d-элементов энергия ионизации изменяется немонотонно. При переходе от 5 к 6 периоду возрастание числа электронных слоев компенсируется вследствие лантаноидного сжатия (f-сжатия), вызванного заполнением электронами 4f-подуровня.
Поскольку отличие в структуре 4f-элементов (лантаноиды) и 5f-элементов (актиноиды) проявляются в третьем снаружи слое, то это мало влияет на химические свойства элементов и приводит к близким свойствам элементов для каждого из f-семейств.
Слайд 32Ряд напряжений по существу представляет собой ряд активности, в начале
которого располагаются наиболее активные металлы – щелочные и щелочноземельные, за
ними следуют металлы средней активности (после Al до Н2), а непосредственно перед водородом и после него находятся малоактивные металлы (Cu, Ag, Au).Слайд 33Активные металлы вытесняют из солей менее активные (металлы расположены в
порядке убывания активности в ряду напряжений),
например,
Zn + CuSO4
= ZnSO4 + CuСлайд 34Взаимодействие металлов с неметаллами
В результате возможно образование следующих типов соединений:
МехОу
– оксиды. Все металлы, за исключением благородных, непосредственно соединяются с
кислородом при различных температурах.МехСу – карбиды. Их получают нагреванием порошкообразных металлов с углеродом или с парами углеводородов. Карбиды имеют очень высокую температуру плавления и твердость.
МехNу – нитриды. Образуются при нагревании металлов с азотом или аммиаком, обладаю высокой твердостью, высокими температурами плавления, проявляют огнеупорные свойства.
МехНу – гидриды. Получают при нагревании металлов с водородом.
Слайд 35Взаимодействие с кислотами
В химической практике наиболее часто используются соляная, серная
и азотная кислоты. Состав продуктов взаимодействия с ними в значительной
степени зависит от концентрации кислоты, активности металла, температуры и других факторов.В СОЛЯНОЙ КИСЛОТЕ и в других бескислородных кислотах роль окислителя играют ионы водорода (Н+), поэтому с ними взаимодействуют металлы, стоящие в ряду напряжений до водорода, вытесняя его:
Al + 6HCl = 2AlCl3 + 3H2,
Ео (Al/Al3+) = –1,66 B,
Ео (H2/2H +) = 0,00 B,
ЭДС = 0 + 1,66 = 1,66 В.
Металлы, стоящие в ряду напряжений после водорода, с указанными кислотами не взаимодействуют.
Слайд 36РАЗБАВЛЕННАЯ СЕРНАЯ КИСЛОТА
реагирует с металлами различной активности аналогично соляной:
2Al
+ 3H2SO4 = Al2 (SO4)3 + 3H2
Слайд 37Концентрированная серная кислота служит окислителем особенно при нагревании. Окислителем в
этом случае является сульфат-ион SO42-, поэтому с ней взаимодействуют и
некоторые металлы, стоящие в ряду напряжений после водорода (Cu, Ag и др.).Приближенно взаимодействие концентрированной серной кислоты с металлами различной активности можно представить схемой:
H2SO4 (к) +
актив. Ме → сульфат + H2S + H2O
ср. акт. Ме → сульфат + S + H2O
мал. акт. Ме → сульфат + SO2 + H2O
Слайд 38 Например:
8Na + 5H2SO4 (к) = 4Na2SO4 +
H2S + 4H2O,
3Cd + 4H2SO4 (к) = 3CdSO4 + S
+ 4H2O,2Bi + 6H2SO4 (к) = Bi2(SO4)3 + 3SO2 + 6H2O
Некоторые металлы средней активности (Fe, Co, Ni, Cr и др.) пассивируются концентрированной серной кислотой, вероятно, образуя нерастворимые оксиды, и без нагревания с ней не взаимодействуют.
Слайд 39Взаимодействие
разбавленной азотной кислоты
с металлами различной активности можно приближенно
выразить схемой:
HNO3 (разб.) +
акт. Ме → нитрат + NH3 (NH4NO3)
+ H2Oср. акт. Ме→ нитрат + N2 (N2O, N2O3, HNO2)
+Н2O
малоакт. Ме → нитрат + NO + H2O
Слайд 40 Например,
4Ca + 10HNO3 = 4Ca(NO3)2 + NH4NO3
+3H2O,
4Mg + 10HNO3 = 4Mg(NO3)2 + N2O + 5H2O,
5Co +
12HNO3 = 5Co(NO3)2 + N2 + 6H2O,3Ag + 4HNO3 = 3AgNO3 + NO + 2H2O.
Следует помнить, что HNO3 взаимодействует с металлами практически без выделения водорода, так как роль окислителя в ней играют нитрат-ионы NO3-. Чем более разбавлена кислота и активнее металл, тем глубже идет процесс восстановления иона NO3-.
Слайд 41HNO3 концентрированная
является одним из самых сильных окислителей.
Основным продуктом
восстановления будет NO2 и только при взаимодействии с наиболее активными
металлами (щелочными и щелочноземельными) образуется N2O.Концентрированная азотная кислота аналогично серной пассивирует на холоде некоторые довольно активные металлы (Al, Cr, Fe)
Слайд 42Стандартный электродный потенциал системы
2H2O + 2ē = H2 +2OH-
составляет –
0,628B, поэтому с водой взаимодействуют только довольно активные металлы (потенциал
которых меньше указанной величины). Причем, взаимодействие протекает с высокой скоростью, если образующийся гидроксид растворим в воде:2Na + 2H2O = 2NaOH + H2
Взаимодействие металлов с водой
Слайд 43Взаимодействие металлов со щелочами
Со щелочами взаимодействуют только те металлы, оксиды
и гидроксиды которых обладают амфотерными свойствами. При этом образуется комплексная
соль металла и выделяется газообразный водород из щелочи:2NaOH + Zn + 2H2O = Na2[Zn(OH)4] + H2
или
2NaOH + Zn = Na2ZnO2 + H2