– 5 минут
Уровень сложности задания – повышенный
Максимальный балл за выполнение
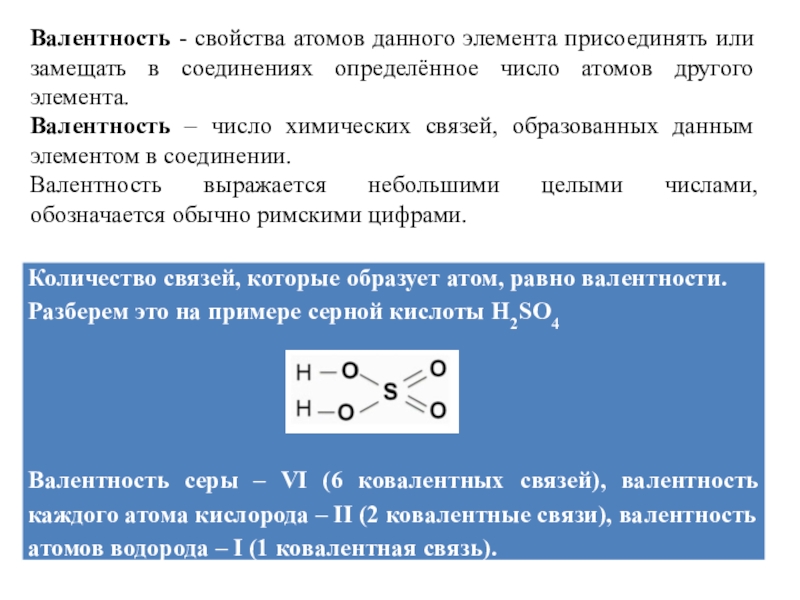
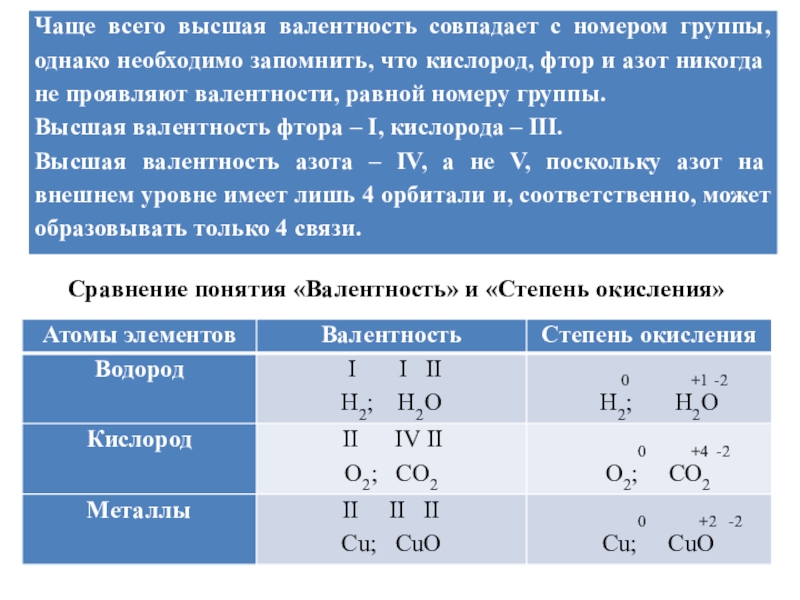
задания - 2Задание № 4 направлено на проверку знания важнейших химических понятий «электроотрицательность», «валентность» и «степень окисления», а также умения определять степень окисления и валентность элементов в соединениях.
Задание содержит в одном столбце формулы (названия) веществ, во втором – степени окисления или валентность химических элементов. К каждой позиции, обозначенной буквой, необходимо подобрать соответствующую позицию, обозначенную цифрой. В ответе нужно записать получившуюся последовательность цифр. Цифры могут повторяться.