Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕФТЕЙ И НЕФТЕПРОДУКТОВ Доц. Каф
Содержание
- 1. ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕФТЕЙ И НЕФТЕПРОДУКТОВ Доц. Каф
- 2. Товарные качества нефтей и нефтяных фракций характеризуются
- 3. СВОЙСТВА нефтей и нефтепродуктов ФИЗИКО-ХИМИЧЕСКИЕ ВЯЗКОСТНО - ТЕМПЕРАТУРНЫЕТЕПЛОВЫЕ НИЗКО-ТЕМПЕРАТУРНЫЕОПТИЧЕСКИЕ
- 4. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА нефтей и нефтепродуктов 1. Плотность2.
- 5. 1. ПлотностьОдна из важнейших и широко употребляемых
- 6. Определение плотности нефтяного сырья можно проводить при
- 7. 2. Средняя температура кипения нефтяной фракцииЛюбая нефтяная
- 8. 3. Характеризующий факторЭто условный параметр (называемый также
- 9. 4. Молярная массаПредставляет собой массу усредненного моля
- 10. Зависимость между молярной массой и относительной плотностью
- 11. 5. Давление насыщенных паров (ДНП)ДНП - давление,
- 12. 6. Температура кипения при нестандартных давлениях В
- 13. 7. Критические свойстваКритическая температура (Ткр), названная по
- 14. 8. Фугитивность (сжимаемость)Характеризует степень отклонения свойств реальных
- 15. ВЯЗКОСТНО - ТЕМПЕРАТУРНЫЕ СВОЙСТВАВязкость является одной из
- 16. В технических требованиях на нефтепродукты обычно нормируется
- 17. ТЕПЛОВЫЕ СВОЙСТВАПри технологических расчетах аппаратов НПЗ используют
- 18. ТЕПЛОЕМКОСТЬТеплоемкость системы – отношение количества тепла, сообщаемой
- 19. Различают изобарную теплоемкость (при постоянном давлении -
- 20. ЭНТАЛЬПИЯУдельная энтальпия жидких нефтепродуктов при температуре T
- 21. Количество тепла, выделяющегося при полном сгорании единицы
- 22. Теплота испарения (парообразования) показывает сколько необходимо тепла
- 23. НИЗКОТЕМПЕРАТУРНЫЕ СВОЙСТВАХарактеристики низкотемпературных свойств нефти и нефтепродуктов
- 24. ОПТИЧЕСКИЕ СВОЙСТВАДля определения химического состава нефтепродуктов в
- 25. ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПРИРОДНЫХ ГАЗОВДоц. Каф. ТОНСЛеденев С.М.Волгоградский государственный технический университетХимия нефти и газа
- 26. СВОЙСТВА ПРИРОДНЫХ ГАЗОВЗнание свойств и поведения
- 27. СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА СМЕСЕЙ И СВЯЗЬ
- 28. Слайд 28
- 29. Слайд 29
- 30. Слайд 30
- 31. Слайд 31
- 32. ПЛОТНОСТЬ ГАЗОВПлотность газовой смеси, как аддитивное свойство,
- 33. Слайд 33
- 34. Слайд 34
- 35. ВЯЗКОСТЬ ГАЗОВВязкостью или внутренним трением жидкости или
- 36. Относя силу к единице площади, из уравнения
- 37. В системе СГС за единицу динамической вязкости
- 38. 1– гелий, 2– воздух, 3– азот, 4–
- 39. В аналитическом виде зависимость вязкости индивидуальных газов
- 40. Вязкость газовой смеси (природный газ, нефтяной газ)
- 41. Отношение вязкости при высоком давлении к вязкости
- 42. КРИТИЧЕСКИЕ И ПРИВЕДЕННЫЕ ДАВЛЕНИЯ И ТЕМПЕРАТУРЫ Критической
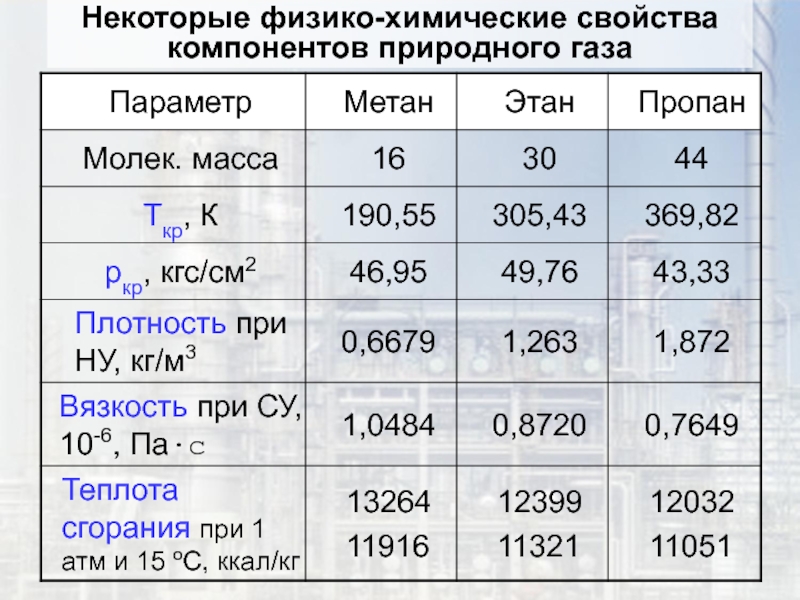
- 43. Некоторые физико-химические свойства компонентов природного газа
- 44. ОСНОВНЫЕ НАПРАВЛЕНИЯ ПЕРЕРАБОТКИ НЕФТЕЙ И ГАЗОКОНДЕНСАТОВДоц. Каф. ТОНСЛеденев С.М.Волгоградский государственный технический университетХимия нефти и газа
- 45. Основные направления переработки нефти: топливное;топливно - масляное;нефтехимическое
- 46. При топливном направлении нефть и газовый конденсат
- 47. По топливно-масляному варианту переработки нефти наряду с
- 48. Методы выделения компонентов и исследования состава нефти
- 49. Физические методы разделения компонентов нефти, газа и продуктов их переработки
- 50. Классификация процессов переработки нефти, газовых конденсатов и
- 51. Физические процессы По типу массообмена можно подразделить
- 52. Химические процессыХимические процессы, применяемые на современных НПЗ, по способу активации химических реакций подразделяются на:термические;каталитические.
- 53. Термические процессы по типу протекающих химических реакций
- 54. Каталитические процессыпо типу катализа можно классифицировать на
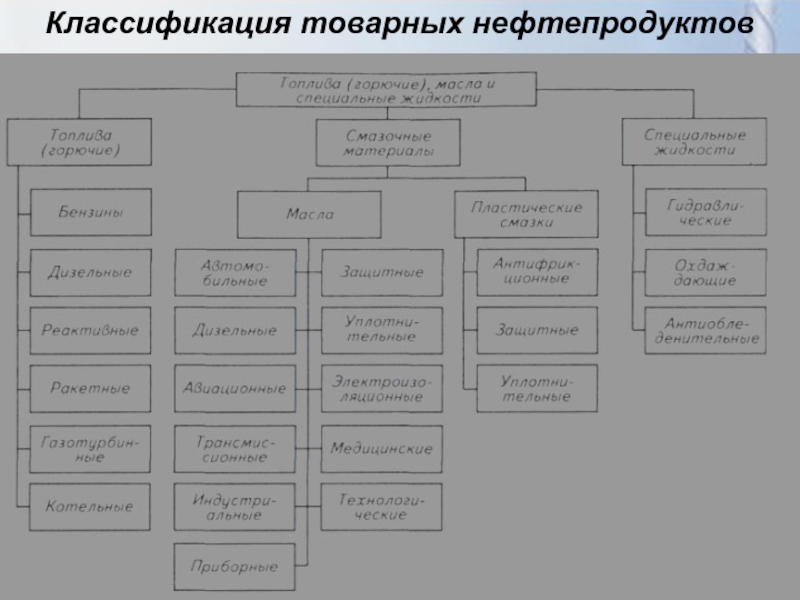
- 55. Классификация товарных нефтепродуктов
- 56. Слайд 56
- 57. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕФТЕЙ И НЕФТЕПРОДУКТОВ
Доц. Каф. ТОНС
Леденев С.М.
Волгоградский государственный
технический университет
Слайд 2Товарные качества нефтей и нефтяных фракций характеризуются помимо фракционного и
химического составов также многими показателями их физико-химических свойств.
Некоторые из
них входят в ГОСТы на товарные нефтепродукты, косвенно или непосредственно характеризуя их эксплуатационные свойства.Другие показатели используются для лабораторного контроля и автоматического регулирования технологических процессов нефтепереработки.
Значения показателей физико-химических свойств нефтей и их фракций необходимы для расчета нефтезаводской аппаратуры.
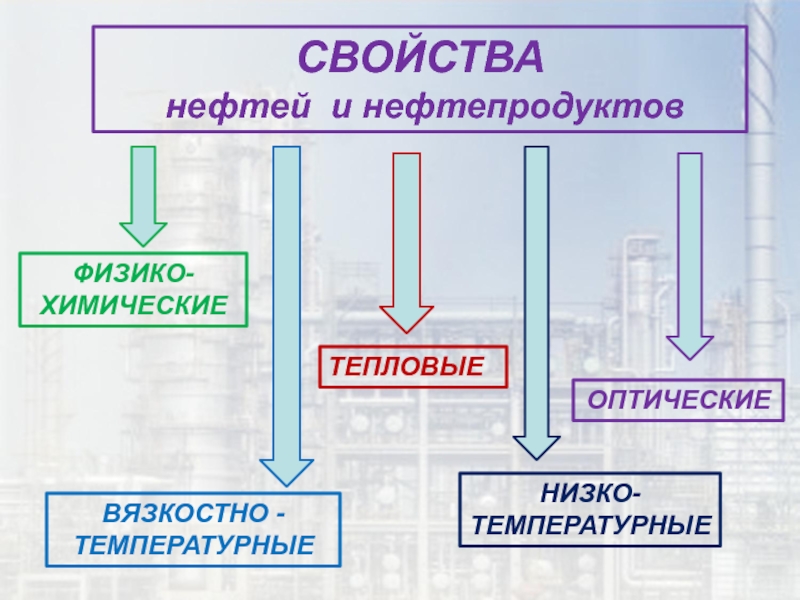
Слайд 3СВОЙСТВА
нефтей и нефтепродуктов
ФИЗИКО-ХИМИЧЕСКИЕ
ВЯЗКОСТНО - ТЕМПЕРАТУРНЫЕ
ТЕПЛОВЫЕ
НИЗКО-
ТЕМПЕРАТУРНЫЕ
ОПТИЧЕСКИЕ
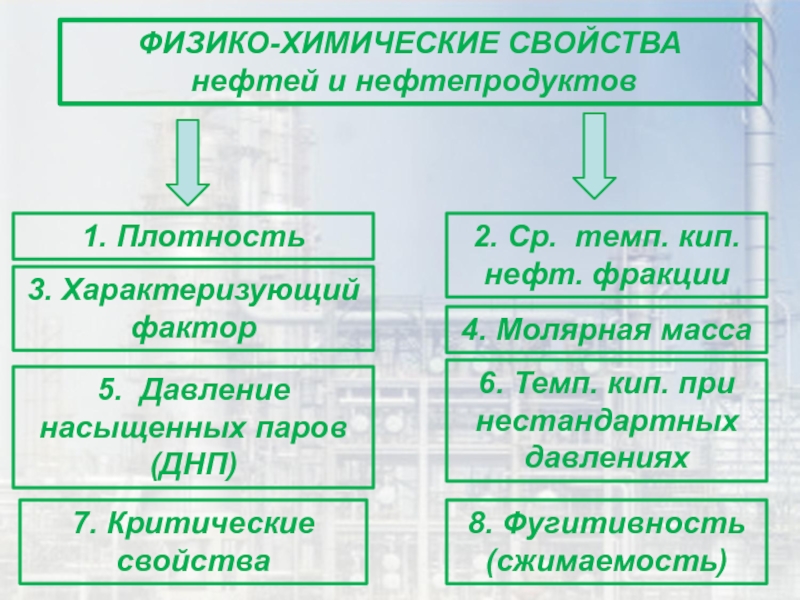
Слайд 4ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
нефтей и нефтепродуктов
1. Плотность
2. Ср. темп. кип.
нефт. фракции
3. Характеризующий фактор
4. Молярная масса
5. Давление насыщенных паров (ДНП)
6.
Темп. кип. при нестандартных давлениях 7. Критические свойства
8. Фугитивность (сжимаемость)
Слайд 51. Плотность
Одна из важнейших и широко употребляемых показателей качества нефтей
и нефтепродуктов.
Плотность определяется как масса единицы объема жидкости при
определенной температуре (кг/м3, г/см3 или г/мл). На практике чаще используют относительную плотность - безразмерную величину, численно равную отношению истинных плотностей нефтепродукта и дистиллированной воды, взятых при определенных температурах. В качестве стандартных температур для воды и нефтепродукта приняты в США и Англии -15,6°С (60°F*), в других странах, в т.ч. и России - 4°С и 20°С (ρ420).
t °С = 5/9(t °F - 32).
*°F - градусы по шкале Фаренгейта, в которой температуры таяния льда и кипения воды приняты соответственно за 32 и 212 единиц;
Слайд 6Определение плотности нефтяного сырья можно проводить при любой температуре (ρ4t),
а затем вычислить значение ρ420 по формуле Д.И. Менделеева (применима
от 0 до 50°С):ρ420 = ρ4t + a(t- 20), а = 0,000903 - 0,00132(ρ420 - 0,7),
где а - средний температурный коэффициент расширения на один градус (справочная литература).
Формула пересчета плотности ρ1515 в ρ420:
ρ1515 = 0,994 ρ420 + 0,0093
Плотность большинства нефтей в среднем колеблется от 0,81 до 0,90, хотя встречаются нефти легче или тяжелее указанных пределов. Плотности последовательных фракций нефти плавно увеличиваются.
Плотность узких нефтяных фракций зависит от химического их состава и возрастает в зависимости от преобладания классов углеводородов в следующем порядке:
алканы → цикланы → арены.
Слайд 72. Средняя температура кипения нефтяной фракции
Любая нефтяная фракция, как и
нефть, представляет собой сложную смесь углеводородов, выкипающих в некотором температурном
интервале. В инженерных расчетах используется понятие средней температуры кипения нефтяной фракции. Существует несколько ее модификаций, но наиболее употребительной является средняя молярная температура Тcp.м , которая рассчитывается по формулеТср.м. =
где i - число компонентов (узких фракций) от 1 до n;
xi - мольная доля i-гo компонента;
ti - среднеарифметическая температура кипения узкой фракции, в °С.
Слайд 83. Характеризующий фактор
Это условный параметр (называемый также фактор парафинистости Ватсона),
представляющий собой функцию плотности и средней молярной температуры кипения нефтепродукта
(Тср.м., °К), отражающий его химическую природу:К = 1,216
Средние значения К :
парафинистые нефтепродукты 12,5-13,0
нафтеноароматические 10-11
ароматизированные 10
продукты крекинга 10-11
Формула расчета характеризующего фактора применяется обычно для последующего расчета молекулярной массы узких нефтяных фракций.
Слайд 94. Молярная масса
Представляет собой массу усредненного моля нефтепродукта (кг/кмоль), определяемую
экспериментально или расчетом по эмпирическим формулам.
С повышением температуры кипения нефтяных
фракций молярная масса (М) растет. Эта закономерность лежит в основе формулы Б.П. Воинова (применима только для нормальных алканов с числом углеродных атомов от 4 до15) :М = 60 + 0,3Тср.м + 0,001(Тср.м )2.
Более точные результаты дает формула Б.П. Воинова - А.С. Эйгенсона, выведенная с учетом характеризующего фактора:
М = 7K-21,5 + (0,76 - 0,04K)Тcp.м+ (0,0003K-0,00245)Т2cp.м .
Слайд 10Зависимость между молярной массой и относительной плотностью выражает формула Крэга:
М
= 44,29 / (1-
).Молярная масса смеси нефтяных фракций рассчитывается по правилу аддитивности исходя из известного их состава и молярных масс:
М=∑Мiхi׳ или М = 1 / ∑(хi/Мi),
где хi׳ и хi, - соответственно мольная и массовая доля нефтяных фракций.
Для расчетов М любых углеводородов и нефтяных фракций (с погрешностью менее 1,5% отн.) С.А. Ахметовым предложена следующая формула:
М=3,9802
где τs= Ткип /100;
α0 =3,1612; α1 =1,3014; α2 = -0,0287; α3 = -2,3986; α4 = 1,0844.
Слайд 115. Давление насыщенных паров (ДНП)
ДНП - давление, развиваемое парами, находящимися
над жидкостью в условиях равновесия при определенной температуре.
Для нефти.и
нефтяных фракций оно зависит не только от температуры, но и от температуры их кипения и плотности. Для узких фракций нефти можно с известной степенью приближения считать pT = f(T,Ткип). На этом базируются различные формулы, из которых чаще других используется формула Ашворта:lg(ρT - 3158) = 7,6715 - 2,68f(T)/f(T0) , (Па),
где f(T) =[1250/( + 108000 - 307,6)] - 1, f(T0) - аналогичная функция, только при Т0 - средней температуре кипения фракции при атмосферном давлении, °С.
ДНП - является одним из фундаментальных физических свойств химических веществ и более информативно характеризует физико-химическую сущность фазовых переходов и энергетику межмолекулярного взаимодействия в них. ДНП широко используется в химической технологии для инженерных расчетов массо-теплообменных процессов, определяет также эксплуатационные свойства нефтепродуктов.
Слайд 126. Температура кипения при нестандартных давлениях
В химической технологии информацией
о температуре кипения химических веществ при нестандартных давлениях П (Тпкип)
пользуются при расчетах технологических процессов, осуществляемых при вакууме или давлениях выше атмосферного, и обычно довольствуются табулированными экспериментальными данными или же номограммами.Поскольку Тпкип определяется из условия равенства ДНП жидкости Рт внешнему давлению П, то барическую зависимость температуры кипения химических веществ следует рассматривать как обратную функцию термической зависимости ДНП при условии РТ=П.
Слайд 137. Критические свойства
Критическая температура (Ткр), названная по предложению Д.И. Менделеева
абсолютной температурой кипения - температура, при которой исчезает различие между
жидким и газообразным состоянием вещества. Критическое давление (Ркр) - давление насыщенных паров химических веществ при критической температуре. Критический объем (VKp) - удельный объем, занимаемый веществом при критических температуре и давлении.При температурах свыше Ткр вещество переходит в сверхкритическое состояние без кипения и парообразования (фазовый переход 2-го рода), при котором теплота испарения, поверхностное натяжение и энергии межмолекулярного взаимодействия равны нулю. Вещество в сверхкритическом состоянии можно представить как совокупность изолированных друг от друга молекул (как молекулярный «песок»).
Для веществ, находящихся в сверхкритическом состоянии, не применимы закономерности абсорбции, адсорбции, экстракции и ректификации. Их в смесях с «докритическими» жидкостями можно разделить лишь гравитационным отстоем.
Слайд 148. Фугитивность (сжимаемость)
Характеризует степень отклонения свойств реальных газов и паров
от рассчитываемых по уравнениям состояния идеального газа. Фугитивность (f) измеряется
в тех же единицах, что и ДНП и заменяет его в уравнениях идеального состояния применительно к реальным газам, парам и жидкостям:F = ZP,
где Z - коэффициент фугитивности (сжимаемости). Для идеального газа z = 1.
Установлено, что Z является функцией приведенных температуры и давления. При инженерных расчетах значения коэффициента фугитивности Z определяют по эмпирическим уравнениям или по специальным номограммам.
Слайд 15ВЯЗКОСТНО - ТЕМПЕРАТУРНЫЕ СВОЙСТВА
Вязкость является одной из важнейших характеристик нефтей
и нефтепродуктов. Она определяет подвижность нефтепродуктов в условиях эксплуатации двигателей,
машин и механизмов, существенно влияет на расход энергии при транспортировании, фильтрации, перемешивании.Различают динамическую (η), кинематическую (ν) и условную (ВУ) вязкости.
В нефтепереработке наиболее широко пользуются кинематической вязкостью, численно равной отношению динамической вязкости нефтепродукта к его плотности
ν = η / ρ
Единицей измерения ν является см2/с (стокс) или мм2/с (сантистокс).
Вязкость сильно зависит от температуры, поэтому всегда указывается температура.
Слайд 16В технических требованиях на нефтепродукты обычно нормируется вязкость при 50
и 100, реже 20°С.
Для оценки вязкостно-температурных свойств нефтяных масел
предложены различные показатели, такие, как индекс вязкости (ИВ), отношение вязкостей v50 / v100 и др. Индекс вязкости - условный показатель, представляющий собой сравнительную характеристику испытуемого масла и эталонных масел. Значение ИВ рассчитывается по специальным таблицам на основании значений v50 и v100 масел.
Чем меньше меняется вязкость масла с изменением температуры, тем выше его ИВ.
Установлено, что ИВ зависит от химического состава масла и структуры углеводородов.
Наибольшим значением ИВ обладают парафиновые углеводороды, наименьшим - полициклические ароматические с короткими боковыми цепями.
Слайд 17ТЕПЛОВЫЕ СВОЙСТВА
При технологических расчетах аппаратов НПЗ используют такие значения тепловых
свойств нефтей и нефтепродуктов, как:
ТЕПЛОЕМКОСТЬ - количество тепла, необходимое для
нагревания единицы массы вещества на один градус;ЭНТАЛЬПИЯ (теплосодержание);
ТЕПЛОТА СГОРАНИЯ (теплотворная способность) - количество тепла (в Дж), выделяющееся при полном сгорании единицы массы (кг) топлива (нефти, нефтепродуктов) при нормальных условиях;
ТЕПЛОТА ИСПАРЕНИЯ - количество теплоты, поглощаемое жидкостью при переходе ее в насыщенный пар и др..
Слайд 18ТЕПЛОЕМКОСТЬ
Теплоемкость системы – отношение количества тепла, сообщаемой системе в каком-либо
процессе, к соответствующему изменению ее температуры.
Различают истинную (Сист) и
среднюю (Сср.) теплоемкости, соответствующие либо бесконечно малому изменению или разности температур.Сист = dQ/dT, Сср.= Q / ∆T = Q / T2 – T1
В зависимости от способа выражения состава вещества различают следующие теплоемкости:
массовую,
мольную,
объемную.
Слайд 19Различают изобарную теплоемкость (при постоянном давлении - Ср) и изохорную
теплоемкость (при постоянном объеме - Cν). При этом Ср >
Cν.Для жидкостей разность невелика Ср- Cν, а для идеальных газов Ср - Cν = R = 8,315 кДж/(моль•К).
Для расчета средней теплоемкости жидких нефтепродуктов предложены:
уравнение Фортча и Уитмена:
Ср = 1, 444+0,000371(Тср - 273) (2,1 – )
уравнение Крэга:
Ср = (0,762-0,0034Тср) / и др.
Для определения средней теплоемкости паров и нефтяных фракций в интервале до 350°С можно пользоваться уравнением Бальке и Кей:
Ср = (4 - )(1,8Т + 211) / 1541 .
Слайд 20ЭНТАЛЬПИЯ
Удельная энтальпия жидких нефтепродуктов при температуре T численно равна количеству
тепла (в кДж), необходимому для нагрева единицы количества продукта от
температуры 0°С до заданной температуры. Энтальпия паров ( ) больше энтальпии жидкости ( ) на величину теплоты испарения и перегрева паров. Наиболее часто используемые уравнения для расчета энтальпии жидких и парообразных нефтепродуктов (в кДж/кг) при атмосферном давлении:уравнение Фортча и Уитмена:
= (0,001855T2 + 0,4317T - 256,11)(2,1 - ),
уравнение Уэйра и Итона:
= (129,58 + 0,134T + 0,00059T2)(4- ) - 308,99.
Слайд 21Количество тепла, выделяющегося при полном сгорании единицы массы или объема
вещества или топлива, называют теплотой сгорания. Различают высшую (Qв) и
низшую (Qн) теплоты сгорания. Qв отличается от Qн на величину теплоты полной конденсации водяных паров, образующихся из влаги топлива и при сгорании углеводородов:Qн = Qв - 2500(9Н + W)
Для расчета Qв используются формула Д.И. Менделеева :
Qв = 339,1C + 1030H - 108,9(O-S) - 16,75W (в кДж/кг),
где С, Н, О, S, W - содержание (в % масс.) в топливе углерода, водорода, кислорода, серы и влаги соответственно.
Существуют также эмпирические формулы расчета теплоты сгорания топлива, если известна его плотность:
Qв =12400 – 2100 ( )2, Qн = Qв -5045Н , где
Н = (26 – 15 ) / 100
ТЕПЛОТА СГОРАНИЯ
Слайд 22
Теплота испарения (парообразования) показывает сколько необходимо тепла для того, чтобы
превратить единицу массы жидкости при данной температуре в парообразное.
Единицы измерения
теплоты испарения – Дж / мольДля определения теплоты испарения парафинистых низкокипящих нефтепродуктов можно использовать уравнение Крэга:
L = (354Д - 0,3768Тср.м.) / .
Теплота испарения может быть найдена по разности известных энтальпий нефтепродукта в паровой и жидкой фазе при одинаковых температуре и давлении.
ТЕПЛОТА ИСПАРЕНИЯ
Слайд 23НИЗКОТЕМПЕРАТУРНЫЕ СВОЙСТВА
Характеристики низкотемпературных свойств нефти и нефтепродуктов :
температура помутнения
– температура появления мути (для нефти, дизельных и котельных топлив);
температура
застывания - температура, при которой нефть или нефтеподукт теряет подвижность;температура начала кристаллизации - максимальная температура, при которой в топливе невооруженным глазом обнаруживаются кристаллы ароматических углеводородов, прежде всего бензола, который затвердевает при 5,5°С (для карбюраторных и реактивных топлив).
Метод их определения заключается в охлаждении образца нефтепродукта в стандартных условиях в стандартной аппаратуре.
Слайд 24ОПТИЧЕСКИЕ СВОЙСТВА
Для определения химического состава нефтепродуктов в дополнение к химическим
методам анализа используют такие оптические свойства, как:
цвет;
коэффициент
(показатель) преломления;оптическая активность;
молекулярная рефракция;
дисперсия.
Данные показатели внесены в ГОСТы на некоторые нефтепродукты. Кроме того, по оптическим показателям можно судить о глубине очистки нефтепродуктов, о возрасте и происхождении нефти.
Слайд 25ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПРИРОДНЫХ ГАЗОВ
Доц. Каф. ТОНС
Леденев С.М.
Волгоградский государственный технический
университет
Химия нефти и газа
Слайд 26 СВОЙСТВА ПРИРОДНЫХ ГАЗОВ
Знание свойств и поведения природного газа позволяет
рационально решать вопросы его добычи, переработки и транспорта.
Наиболее важным
является вопрос о фазовом состоянии, в котором находятся компоненты природного газа.Рассмотрим следующие свойства природных газов и их компонентов:
молекулярная масса;
плотность;
вязкость;
теплотворная способность;
влажность.
Слайд 27 СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА СМЕСЕЙ И СВЯЗЬ МЕЖДУ НИМИ
Массовая доля
– масса i-го компонента, отнесенная к общей массе системы:
Число молей
равно массе вещества mi, деленной на молекулярную массу Mi:
Молярная (мольная) доля – число молей i-го компонента, отнесенное к общему числу молей в системе:
Слайд 32ПЛОТНОСТЬ ГАЗОВ
Плотность газовой смеси, как аддитивное свойство, можно рассчитать по
составу газа и плотности каждого компонента:
где yi = Ni
или vi в долях единицы;ρi - плотность компонента газа.
Слайд 35ВЯЗКОСТЬ ГАЗОВ
Вязкостью или внутренним трением жидкости или газа называется свойство,
проявляющееся в сопротивлении, которое жидкость или газ оказывает его сдвигу
под влиянием действующей силыСопротивление сдвига пропорционально скорости сдвига, а не силе сдвига, как у твердых тел.
Закон течения Ньютона связывает тангенциальную силу, приложенную к жидкости (газу) и сопротивление стационарному течению:
S - площадь, к которой приложена
сила F.
Слайд 36Относя силу к единице площади,
из уравнения Ньютона получаем тангенциальное
напряжение:
откуда
Эта величина называется коэффициентом вязкости, коэффициентом внутреннего трения, динамической вязкостью
или просто вязкостью.Слайд 37В системе СГС за единицу динамической вязкости принят один пуаз
(П).
Пуаз — это динамическая вязкость жидкости, оказывающей взаимному перемещению двух
ее слоев площадью в 1 см2, находящихся друг от друга на расстоянии 1 см и перемещающихся друг относительно друга со скоростью 1 см/сек, силу сопротивления, равную 1 дине: В системе СИ единица динамической вязкости имеет размерность (н∙с)/м2 или Па∙с, мПа∙с. Эта единица в 10 раз больше пуаза.
1 П = 0,1 (н∙сек)/м2.
Слайд 381– гелий, 2– воздух,
3– азот,
4– углекислый газ,
5-
сероводород, 6- метан,
7- этилен, 8- этан,
9- пропан, 10-
изобутан, 11- н-бутан, 12- н-пентан,
13- н-гексан, 14- н-гептан,
15- н-октан, 16- н-нонан, 17- н-декан
Температура, оС
Вязкость, спз
Вязкость газов при атмосферном давлении
Слайд 39В аналитическом виде зависимость вязкости индивидуальных газов и паров от
температуры (при атмосферном давлении) установлена Сатерлендом:
- вязкость газа при
заданной температуре Т;о - вязкость того же газа при 0 К;
Т - абсолютная температура газа;
С - константа, зависящая от свойств газа:
ССН4 = 170;
СС2Н6 = 280;
СС3Н8 = 318;
ССО2 = 240; СN2 = 110; СВозд = 124.
Расчет вязкости при атмосферном давлении
Слайд 40Вязкость газовой смеси (природный газ, нефтяной газ) при атмосферном давлении
можно рассчитать, если известен ее компонентный состав:
см - вязкость смеси
газов;i - вязкость i – го компонента;
Ni - молярная доля i – го компонента;
Mi - молярная масса i – го компонента.
Вязкость смеси газов не обладает свойством аддитивности.
Слайд 41Отношение вязкости при высоком давлении к вязкости при атмосферном давлении,
является функцией приведенного давления и приведенной температуры:
где Tr, pr –
псевдоприведенные температура и давление смеси газов, Т, р и Тс, рс – рабочие и псевдокритические значения температур и давлений, соответственно.Расчет вязкости при высоком давлении
Слайд 42КРИТИЧЕСКИЕ И ПРИВЕДЕННЫЕ ДАВЛЕНИЯ И ТЕМПЕРАТУРЫ
Критической принято называть такую
температуру, выше которой газ под действием давления любого значения не
может быть обращен в жидкость.Давление, необходимое для сжижения газа при критической температуре, называется критическим.
Критические давление и температуру для смеси газов можно определить по формулам:
Слайд 44ОСНОВНЫЕ НАПРАВЛЕНИЯ ПЕРЕРАБОТКИ НЕФТЕЙ И ГАЗОКОНДЕНСАТОВ
Доц. Каф. ТОНС
Леденев С.М.
Волгоградский государственный
технический университет
Химия нефти и газа
Слайд 45Основные направления переработки нефти:
топливное;
топливно - масляное;
нефтехимическое или комплексное (топливно-нефтехимическое
или топливно-масляно-нефтехимическое).
Выбор конкретного направления, соответственно схем переработки нефтяного сырья
и ассортимента выпускаемых нефтепродуктов обусловливается прежде всего качеством нефти, ее отдельных топливных и масляных фракций, требованиями на качество товарных нефтепродуктов, а также потребностями в них данного экономического района.Слайд 46При топливном направлении нефть и газовый конденсат в основном перерабатываются
на моторные и котельные топлива.
Переработка нефти на НПЗ топливного
профиля может быть глубокой и неглубокой. Технологическая схема НПЗ с неглубокой переработкой отличается небольшим числом технологических процессов и небольшим ассортиментом нефтепродуктов. Выход моторных топлив по этой схеме не превышает 55 - 60 % масс, и зависит в основном от фракционного состава перерабатываемого нефтяного сырья. Выход котельного топлива составляет 30-35 % масс.При глубокой переработке стремятся получить максимально высокий выход высококачественных моторных топлив путем вовлечения в их производство остатков атмосферной и вакуумной перегонок, а также нефтезаводских газов. Выход котельного топлива в этом варианте сводится к минимуму. Глубина переработки нефти при этом достигает до 70 - 90 % масс.
Слайд 47По топливно-масляному варианту переработки нефти наряду с моторными топливами получают
различные сорта смазочных масел. Для производства последних подбирают обычно нефти
с высоким потенциальным содержанием масляных фракций с учетом их качества.Нефтехимический (комплексный) вариант
переработки нефти предусматривает наряду с топливами и маслами производство сырья для нефтехимии (ароматические углеводороды, парафины, сырье для пиролиза и др.), а в ряде случаев - выпуск товарной продукции нефтехимического синтеза.
Слайд 48Методы выделения компонентов и исследования состава нефти и газа
Различают химические
и физические методы разделения компонентов нефти и газа.
Химические методы основаны
на неодинаковой реакционной способности разделяемых компонентов.Физические методы — на различии концентраций в сосуществующих равновесных фазах . К физическим методам разделения относятся также разнообразные варианты хроматографии.
Методы разделения, в которых изменение концентрации веществ в сосуществующих фазах достигается лишь за счет сообщения системе энергии, условно названы простыми, а методы с применением дополнительных веществ, увеличивающих различие составов фаз,— сложными.
Слайд 50Классификация процессов переработки нефти, газовых конденсатов и газов
Технологические процессы НПЗ
принято классифицировать на две группы:
физические - достигается разделение нефти
на составляющие компоненты (топливные и масляные фракции) без химических превращений и удаление (извлечение) из фракций нефти, нефтяных остатков, масляных фракций, газоконденсатов и газов нежелательных компонентов (полициклических ароматических углеводородов, асфальтенов, тугоплавких парафинов), неуглеводородных соединений.; химические - переработка нефтяного сырья осуществляется путем химических превращений с получением новых продуктов, не содержащихся в исходном сырье.
Слайд 51Физические процессы
По типу массообмена можно подразделить на следующие типы:
гравитационные
(ЭЛОУ);
ректификационные (AT, ABT, ГФУ и др.);
экстракционные (деасфальтизация, селективная очистка, депарафинизация
кристаллизацией);адсорбционные (депарафинизация цеолитная, контактная очистка);
абсорбционные (АГФУ, очистка от H2S, C02).
Слайд 52Химические процессы
Химические процессы, применяемые на современных НПЗ, по способу активации
химических реакций подразделяются на:
термические;
каталитические.
Слайд 53Термические процессы
по типу протекающих химических реакций можно подразделить на
следующие типы:
термодеструктивные
(термический крекинг, висбрекинг, коксование, пиролиз, пекование, производство
технического углерода и др.);термоокислительные
(производство битума, газификация кокса, углей).
В термодеструктивных процессах протекают преимущественно реакции распада (крекинга) молекул сырья на низкомолекулярные, а также реакции конденсации с образованием высокомолекулярных продуктов, например кокса, пека и др.
Слайд 54Каталитические процессы
по типу катализа можно классифицировать на следующие типы:
гетеролитические, протекающие
по механизму кислотного катализа (каталитический крекинг, алкилирование, полимеризация, производство эфиров
и др.);гомолитические, протекающие по механизму окислительно - восстановительного катализа (производства водорода и синтез газа, метанола, элементной серы);
гидрокаталитические, протекающие по механизму бифункционального (сложного) катализа (гидроочистка, гидрообессеривание гидрокрекинг, каталитический риформинг, изомеризация, гидродеароматизация, селективная гидродепарафинизация и др.).