Слайд 1Подходы к анализу производных барбитуровой кислоты
Слайд 2 Приказ по МЗ СССР г.Москва
№
1021 от 25 декабря 1973г
«О введении нового
перечня токсикологических веществ, подлежащих судебно – химическому исследованию в лабораториях бюро судебно – медицинской экспертизы»
1. Группы веществ, на которые должны производиться исследования при общем анализе
1.3. Органические вещества, изолируемые подкисленной водой или подкисленным
спиртом, другими органическими растворителями:
Барбитал, фенобарбитал, барбамил, этаминал, циклобарбитал, гексобарбитал, бензонал.
2. Вещества, на которые расширяют общий анализ в зависимости от клинической и секционной картины, результатов гистологического, гистохимического исследования, особенностей течения химических реакций и т. д.
производные барбитуровой и тиобарбитуровой кислот, не указанные в п. 1.3;
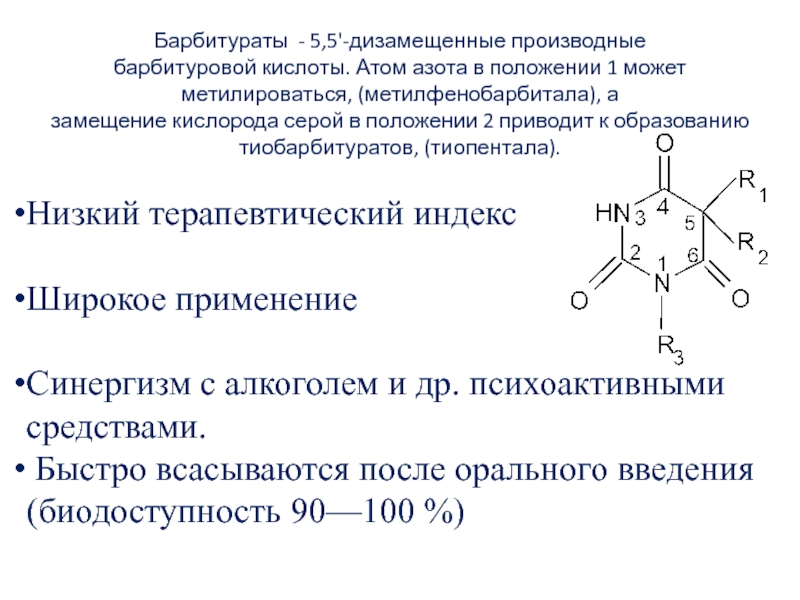
Слайд 3Барбитураты - 5,5'-дизамещенные производные
барбитуровой кислоты. Атом азота в положении 1
может
метилироваться, (метилфенобарбитала), а
замещение кислорода серой в положении 2 приводит к
образованию
тиобарбитуратов, (тиопентала).
Низкий терапевтический индекс
Широкое применение
Синергизм с алкоголем и др. психоактивными средствами.
Быстро всасываются после орального введения
(биодоступность 90—100 %)
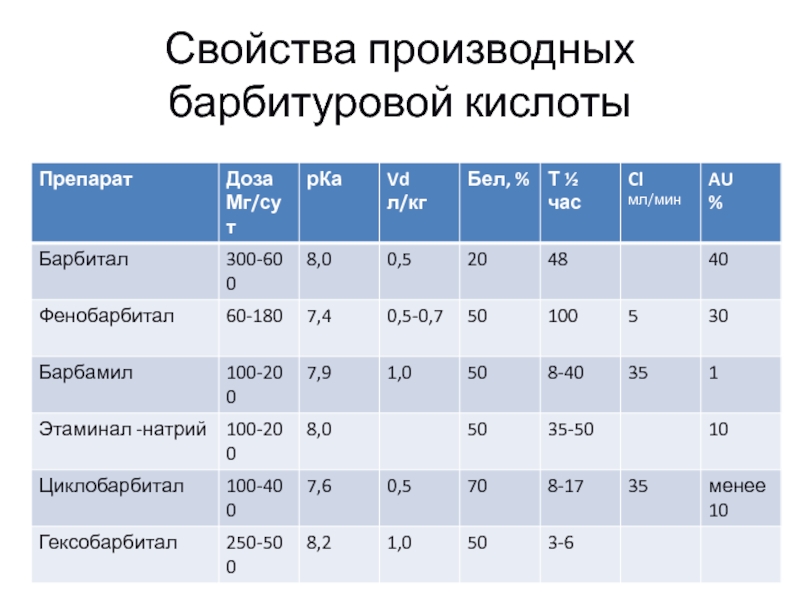
Слайд 4Свойства производных барбитуровой кислоты
Слайд 5Свойства.
Барбитураты плохо растворяются в воде, хорошо растворимы в этаноле, хлороформе,
эфире, в водных растворах щелочей.
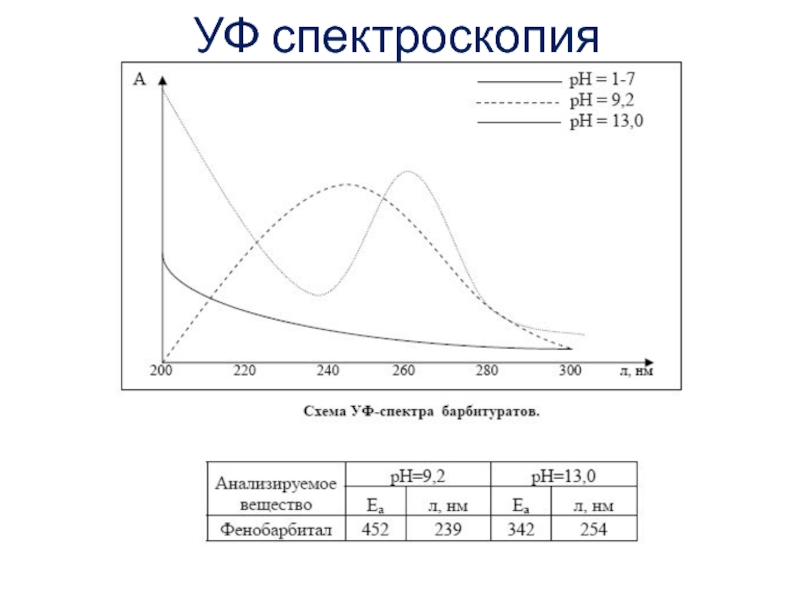
УФ-спектры большинства производных барбитуровой кислоты схожи,
они не имеют заметного поглощения в области 200 — 330 нм при кислых инейтральных значениях рН, но имеют два максимума поглощения при щелочных значениях рН, которые характеризуют поглощение ионизированных форм первой (238 — 240 нм) и второй (254 — 256 нм) ступени диссоциации.
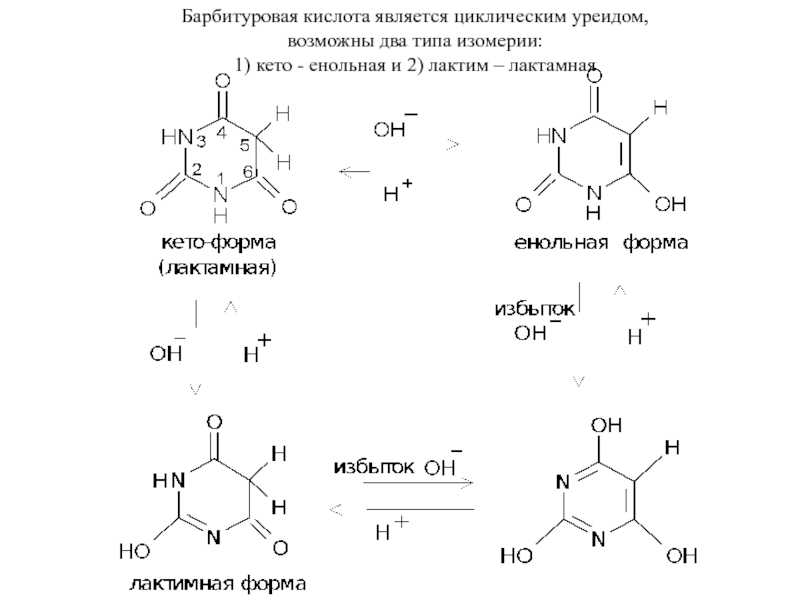
Слайд 6Барбитуровая кислота является циклическим уреидом,
возможны два типа изомерии:
1)
кето - енольная и 2) лактим – лактамная
Слайд 7Основные характеристические частоты ИК-спектров барбитуратов (см-1):
–NH– (деформационные) 1680–1693;
С=O
(валентные) 1712–1725;
–CONH–(валентные) 1744–1770;
=C–N– (валентные) 1300–1320;
C=O(деформационные) 1210–1245;
=C–H
(деформационные) 830–875.
Слайд 8Биотрансформация
Фенобарбитал –
1. N-глюкозилирование по азоту в 1.
2. окисление
фенольного фрагмента в пара-положении и его конъюгация с глюкуроновой кислотой.
Этаминал
натрия –
1. гидроксилирование: азота в положении 1;
2.в радикале в положении 3 и его окисление через кетон до карбоновой кислоты
Слайд 9Биотрансформация
Барбамил –
1. конъюг. с глюкуроновой кислотой по азоту в
1.
2. Окисление в радикале по 3 положению до карбоновой кислоты.
Циклобарбитал
– окисление до кетоциклобарбитала в мета- положении радикала.
Слайд 10Выделение
Общие методы (Васильевой, Стасса-Отто) – кислое хлороформенное извлечение.
Частные методы:
Метод Валова
(подщелоченой водой)
Метод Швайковой (подкисленной водой, с очисткой переэкстраккцией)
Метод Попова (водой
подкисленной серной кислотой)
Слайд 11Обнаружение барбитуратов
Цветные и микрокристаллические реакции
ТСХ в частных системах
ИК и УФ
спектроскопия
Иммунно-ферментный анализ
ВЭЖХ и ГЖХ
Масс-спектрометрия
Слайд 12Цветные реакции
Реакция Парри (фиолетовое окрашивание)
Реакция Цвиккера (розовая или красная окраска)
Реакция
с пиридином и солями меди. (аморфный осадок)
Мурексидная проба (розовая окраска)
Реакция
с родамином (комплексы светло-оранжевые или оранжево-красные в четыреххлористом углероде)
Микрокристаллические реакции
Выделение кислотной формы барбитуратов.
Реакция с хлорцинкиодом
Реакция со смесью растворов хлорида железа и иодида калия.
Реакция с дииодокупратом калия в растворе иода.
Реакция с подкисленным спиртовым раствором иодида калия.
Слайд 14ТСХ
Сорбент – силикагель КСК, забуференный 0,1н раствором борной кислоты.
Растворители –
хлороформ:н-бутанол:25% раствор аммиака (70:40:5)
Обнаружение – дифенилкарбазоном (ДФК) – 0,1% раствор
в хлороформе и раствором сульфата ртути – 5% раствор в концентрированной серной кислоте.
Rf фенобарбитала = 0,4
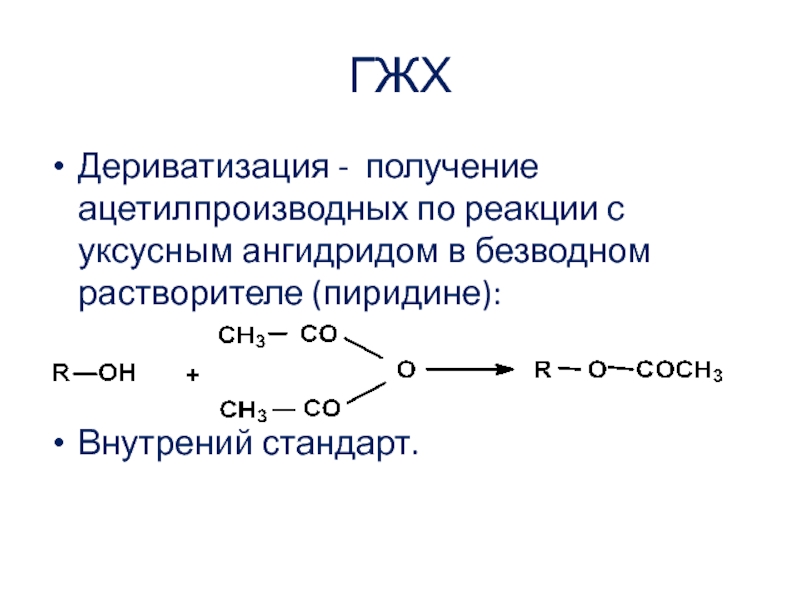
Слайд 15ГЖХ
Дериватизация - получение ацетилпроизводных по реакции с уксусным ангидридом в
безводном растворителе (пиридине):
Внутрений стандарт.
Слайд 16ГЖХ
Хромагрофическая система: Shimadzu GC-14A газовый хроматограф (Shimadzu Corp., Kyoto,
Japan).
Колонка: метилсилоксановая капиллярная колонка DB-1, 15 м , 0.53 мм
Температура
колонки: 60 °C → 8 °C/мин → 250 °C; температура инжектора: 250 °C ;
Газ носитель: He (15 мл/мин); осушающий газ: He (30 мл/мин);
детектор: ПИД и азотно-фосфорный детектор
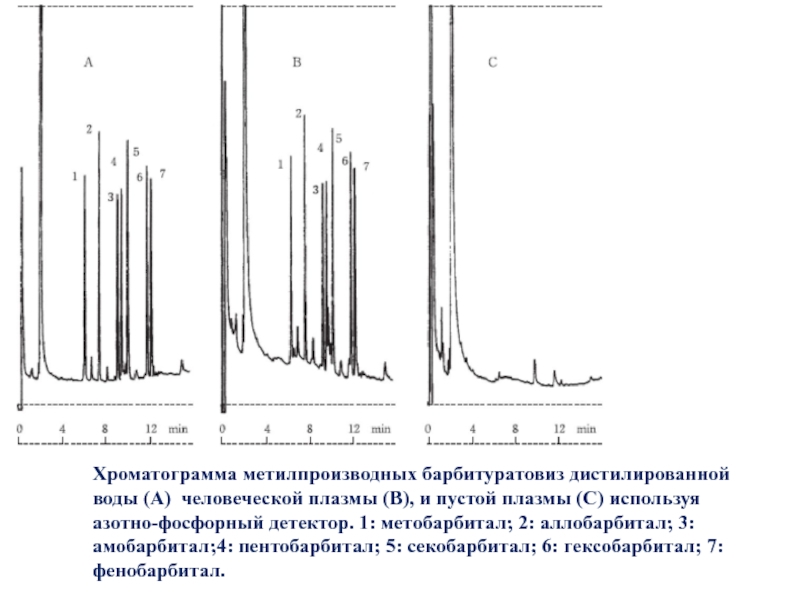
Слайд 17Хроматограмма метилпроизводных барбитуратовиз дистилированной воды (A) человеческой плазмы (B), и
пустой плазмы (C) используя азотно-фосфорный детектор. 1: метобарбитал; 2: аллобарбитал;
3: амобарбитал;4: пентобарбитал; 5: секобарбитал; 6: гексобарбитал; 7: фенобарбитал.
Слайд 18ВЭЖХ
Колонка: обращенная фаза ( ODS-80 Ts, 10 cm 4.6 мм,
размер частиц 2мкм, Toso, Tokyo, Japan).
Подвижная фаза: 8 мM фосфорной
кислоты раствор/ацетонитрил (3:7, v/v).
Детектирование: 215 нм;
Скорость потока: 0.4 мл/мин;
Температура: 20 С.
Слайд 19ВЭЖХ
Детекция - 240нм
Сорбент – ODS
Элюэнт – смесь метанол – р-р
фосфата аммония
Количественное определение – метод добавок
Слайд 20Подходы к анализу производных
1,4 бенздиазепина
Слайд 21 Приказ по МЗ СССР г.Москва
№
1021 от 25 декабря 1973г
«О введении нового
перечня токсикологических веществ, подлежащих судебно – химическому исследованию в лабораториях бюро судебно – медицинской экспертизы»
2. Вещества, на которые расширяют общий анализ в зависимости от клинической и секционной картины, результатов гистологического, гистохимического исследования, особенностей течения химических реакций и т. д.
элениум, нитразепам, седуксен;
Слайд 221,4 Бенздиазепины
Доступность
Высокий терапевтический индекс
Широкий спектр действия
Меньшее количество побочных эфектов
Высока частота
случаев отравления феназепамом.
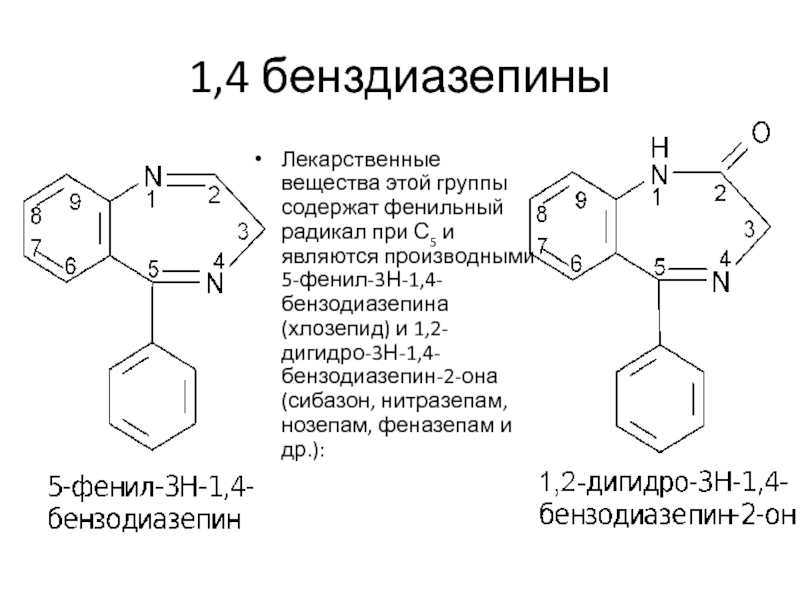
Слайд 231,4 бенздиазепины
Лекарственные вещества этой группы содержат фенильный радикал при С5
и являются производными 5-фенил-3Н-1,4-бензодиазепина (хлозепид) и 1,2-дигидро-3Н-1,4-бензодиазепин-2-она (сибазон, нитразепам, нозепам,
феназепам и др.):
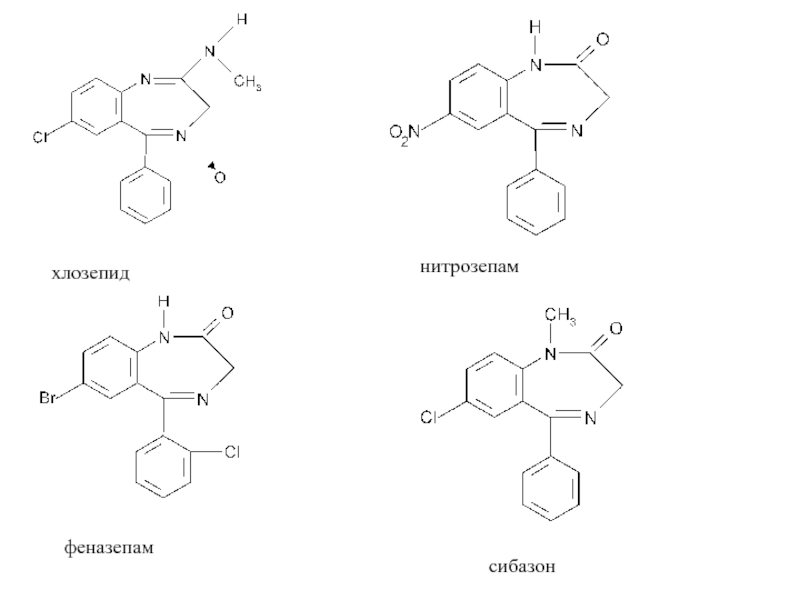
Слайд 24хлозепид
нитрозепам
феназепам
сибазон
Слайд 25Свойства
Большинство 1,4-бенздиазепинов представляют собой бесцветные, хорошо кристаллизующиеся вещества. Практически нерастворимы
в воде, растворимы в воде соли 1,4-бенздиазепинов, содержащих амино- (как
у хлордиазепоксида) или карбоксильную группу в качестве заместителей. В органических растворителях растворимость зависит от структуры. Наиболее высокая растворимость наблюдается в апротонных растворителях (диметилформамиде, диметилсульфоксиде).
Слайд 26Свойства
Кислотно-основные свойства 1,4-бенздиазепины являются слабыми основаниями. Основность увеличивается при
наличии основных заместителей. Так, хлордиазепоксид дает устойчивые соли с сильными
кислотами, выступая в качестве днокислотного
основания.
При введении в ядро 1,4-бенздиазепинов нитро-, окси- и других групп основность соединений снижается.
1,2-дигидропроизводные 1,4-бенздиазепина (оксазепам, нитразепам) проявляют также слабокислые свойства за счет наличия в молекуле амидной группы.
Слайд 27УФ - спектры
В электронных спектрах производных 1,4-бенздиазепина имеется 3 полосы
поглощения
с λmax в областях:
1. 200-215 нм
2. 220-240 нм
3. 290-330 нм
Две
первые полосы соответствуют возбуждению ароматических хромофоров.
Третью длинноволновую полосу относят к азометиновой связи, сопряженной с
бензогруппой.
По характеру поглощения в УФ-области 1,4-бенздиазепины относятся к
соединениям, абсорбция которых изменяется от величины значений рН:
- в кислой среде – за счет протонирования атома азота;
- в щелочной среде в молекуле 1,2-дигидропроизводных 1,4-бенздиазепина
наблюдается изменение хромофорной системы (увеличение сопряжения за счет лактим-лактамной таутомерии азометиновой связи в положения 1,2 - нитразепам, оксазепам).
Это свойство положено в основу идентификации соединений данной группы по
электронным спектрам поглощения.
Слайд 28Тосикокинетика
Механизм всасывания - простая диффузия. Попадая в кровь, на 80-95%
связываются с белками плазмы, поэтому скорость абсорбции достаточно высокая (градиент
концентрации направлен в кровь).
Максимальная концентрация в крови при введении через рот достигается через 2-5 часов после введения терапевтических доз и через 4-8 часов – токсических доз препаратов. Далее концентрация их в крови сохраняется в течение 2-х часов на одном уровне, после чего начинает медленно снижаться.
Наибольшее содержание 1,4-бенздиазепинов в ЖКТ, тканях печени, почек.
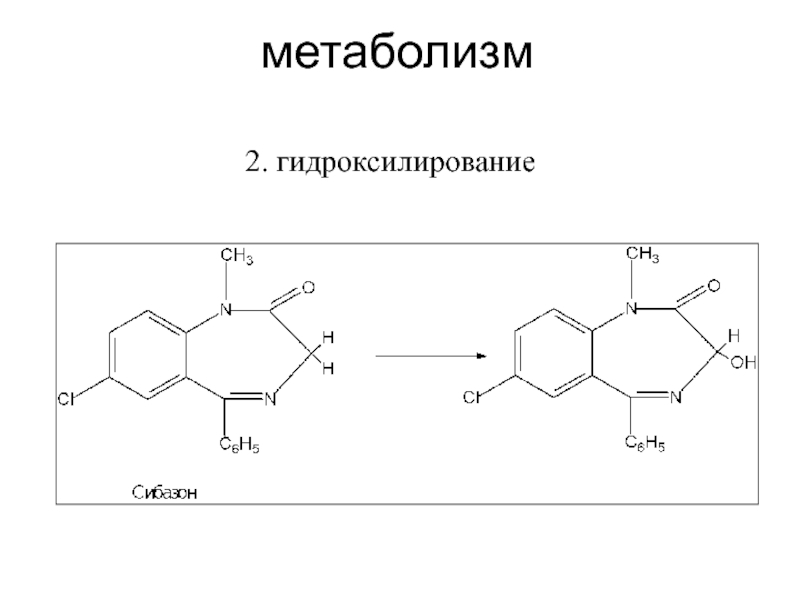
Слайд 29Метаболиты, образованные в результате процессов окисления и восстановления, фармакологически активны.
Наибольшей активностью обладают метаболиты, полученные в процессе деалкилирования.
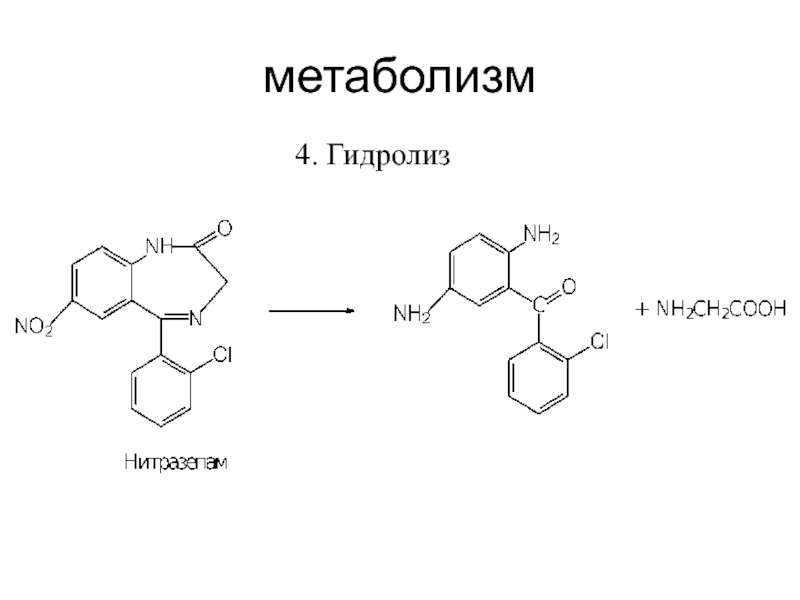
Разрыв азепинового
кольца при гидролизе 1,4- бенздиазепинов и образование глюкуронидов приводит к потере фармакологической активности.
Наряду с основными соединениями продукты метаболизма обнаруживаются во всех тканях организма.
Выводятся, в основном, почками в виде основных соединений и метаболитов.
Время полувыведения (Т ½) при введении соединений через рот
хлордиазепоксид - 8-28 часов
диазепам - 20-42 часа
оксазепам - 10-14 часов
нитразепам - 7-10 часов
Интервал Т 1/2 зависит от принятой дозы
LD > 500 мг
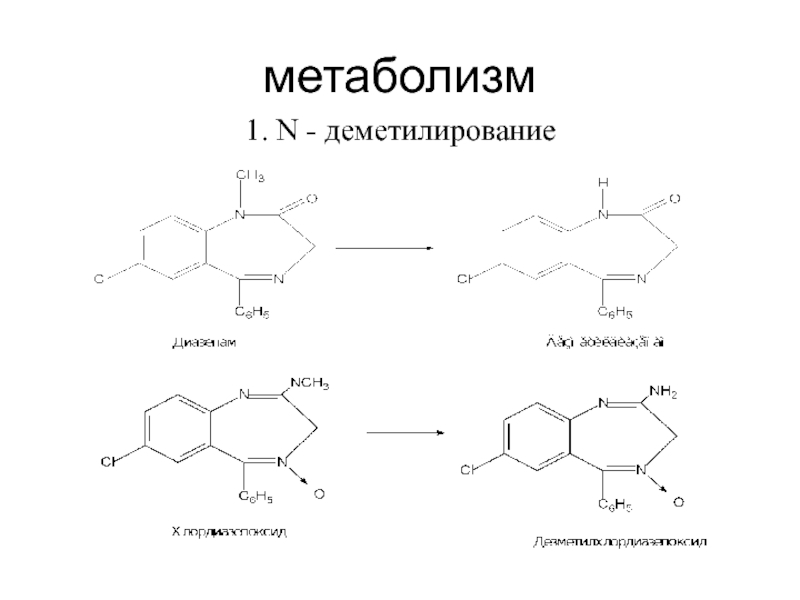
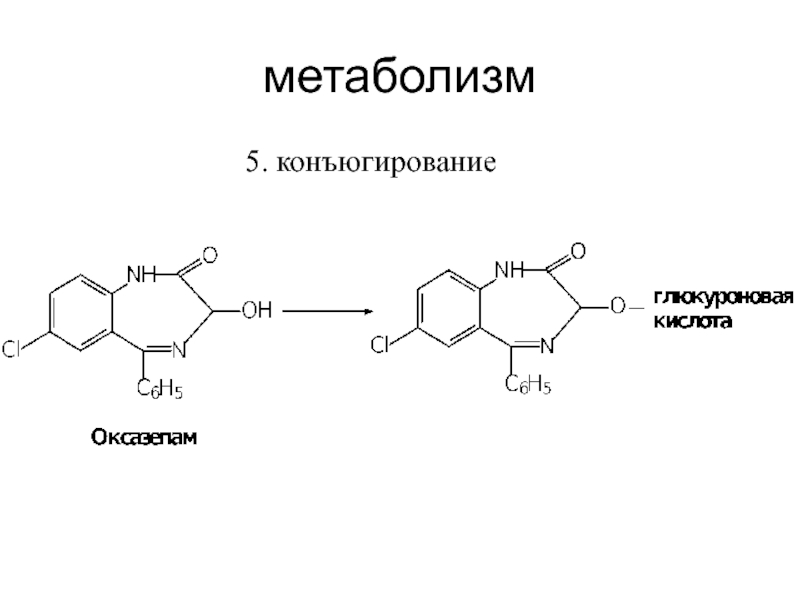
Слайд 30метаболизм
1. N - деметилирование
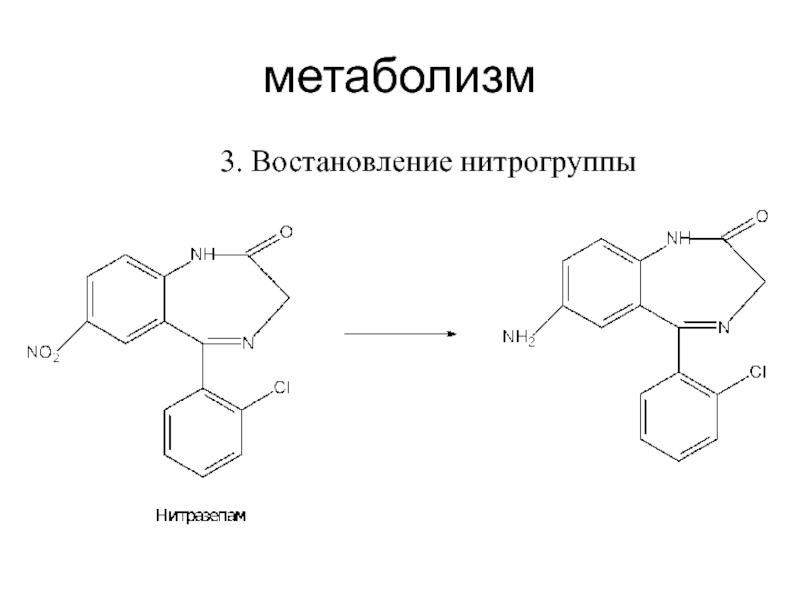
Слайд 32метаболизм
3. Востановление нитрогруппы
Слайд 35Направления анализа 1,4 бенздиазепинов
По продуктам гидролиза (2-аминобензофенонам)
Суммарное определение бенздиазепинов и
их метаболитов
Отрицательное судебно-химическое значение
По нативным соединениям
Установление структуры токсиканта и его
метаболитов
Слайд 36Основные этапы анализа по продуктам гидролиза
1. Гидролиз образца (6н НСL,
120 С, 20мин)
2. Экстракция 2-аминобензофенонов хлороформом (1:1 Х3)
3. ТСХ (элюент
– бензол, декция – собственная окраска, УФ, азокраситель)
4. Элюирование пятна с пластины
5 УФ- спектрофотометрия при 2-х рН менее 5 и более 7
6. Количественное определение ФЭК по реакции образования азокрасителя.
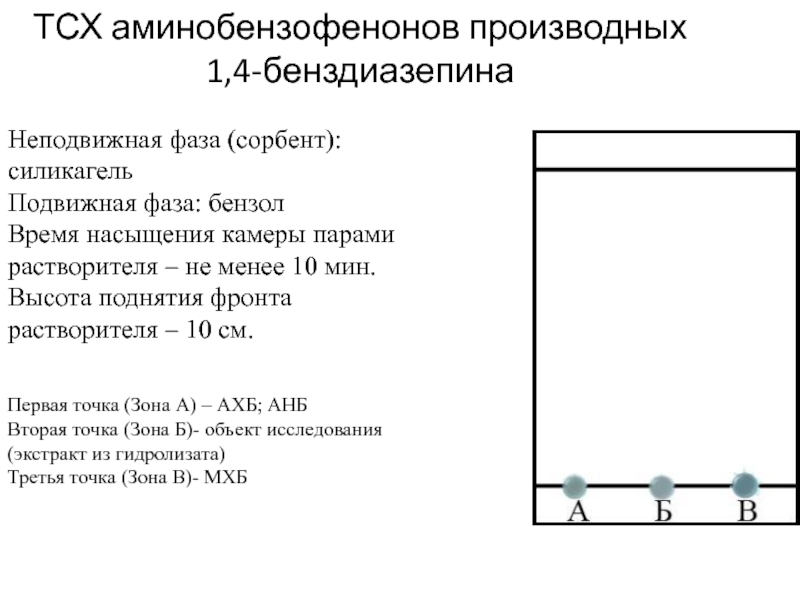
Слайд 37ТСХ аминобензофенонов производных 1,4-бенздиазепина
Неподвижная фаза (сорбент): силикагель
Подвижная фаза: бензол
Время насыщения
камеры парами растворителя – не менее 10 мин.
Высота поднятия фронта
растворителя – 10 см.
Первая точка (Зона А) – АХБ; АНБ
Вторая точка (Зона Б)- объект исследования (экстракт из гидролизата)
Третья точка (Зона В)- МХБ
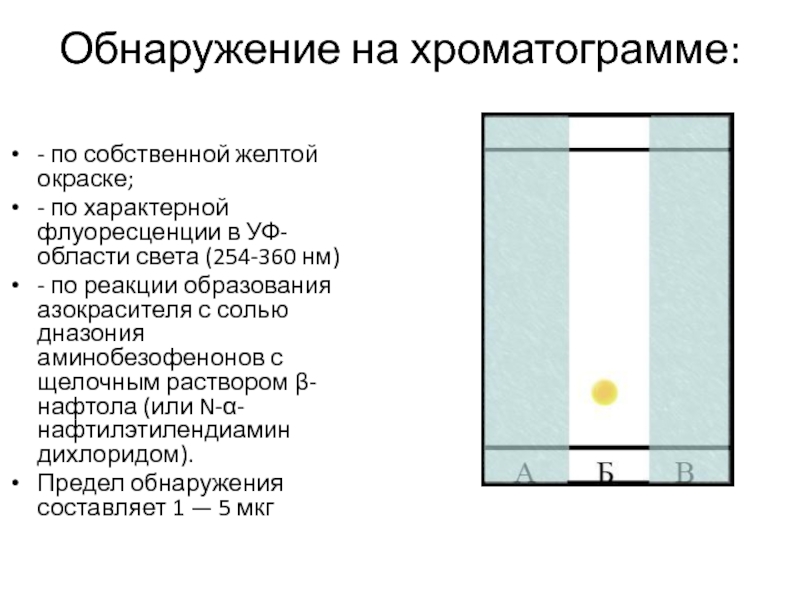
Слайд 38Обнаружение на хроматограмме:
- по собственной желтой окраске;
- по характерной флуоресценции
в УФ-области света (254-360 нм)
- по реакции образования азокрасителя с
солью дназония аминобезофенонов с щелочным раствором β-нафтола (или N-α-нафтилэтилендиамин дихлоридом).
Предел обнаружения составляет 1 — 5 мкг
Слайд 39Основные этапы анализа по нативным соединениям бенздиазепинов
1 Этап : 1а
– извлечение из биологического объекта
2а – экстракция в органический растворитель
2.
Этап – разделение и очистка с помощью ТСХ (элюирование пятна) или ТФЭ
3. Этап – Идентификация по спектрам или хроматографическим параметрам.
Слайд 40При проведении исследования на 1,4-бензодиазепины по нативным соединениям объектами являются
кровь, плазма, сыворотка, моча (не менее 10мл), ткани печени, почек
(не менее 200 г), желудок и тонкий кишечник с содержимым (не менее 200 г).
Изъятые объекты должны быть быстро направлены на исследование в замороженном состоянии.
Консервирование этанолом не рекомендуется.
Слайд 41ГЖХ/МС
Колонка: DB-5 модифицированная капиллярная колонка (30м 0.25 мм, J
& W Scientifi c, Folsom, CA, USA).
Хроматографическая система: GC-17A газоввый
хроматограф (Shimadzu Corp., Kyoto, Japan);
Температура колонки: 150 °C (1 мин) → 20 °C/мин → 300 °C (6.5 мин);
Температура инжектора: 250 °C; газ носитель: He; скорость потока: 0.9 мл/мин;
Ввод пробы: сброс пробы 1 мин.
MS условия: QP-5050A масс-спектрометр (Shimadzu Corp.); ионизация: Электронный удар; энерги электрона 70 eV; температура интерфейса: 250 °C.
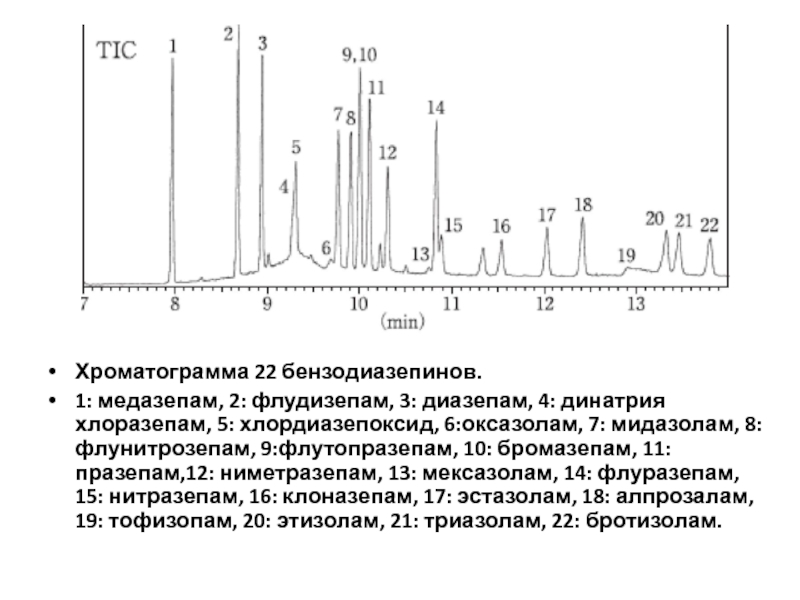
Слайд 42Хроматограмма 22 бензодиазепинов.
1: медазепам, 2: флудизепам, 3: диазепам, 4: динатрия
хлоразепам, 5: хлордиазепоксид, 6:оксазолам, 7: мидазолам, 8: флунитрозепам, 9:флутопразепам, 10:
бромазепам, 11: празепам,12: ниметразепам, 13: мексазолам, 14: флуразепам, 15: нитразепам, 16: клоназепам, 17: эстазолам, 18: алпрозалам, 19: тофизопам, 20: этизолам, 21: триазолам, 22: бротизолам.
Слайд 43ВЭЖХ/МС
Колонка: Wakopak WS GP-N6 (150мм 4.6 мм, Wako Pure Chemical
Industries, Ltd.,Osaka, Japan)
Хроматографическая система: LC 1100 Series ВЭЖХ (Agilent
Technologies,Palo Alto, PA, USA);
Подвижная фаза: ацетатный буфер/ацетонитрил (75:25, v/v)
Скорость ПФ: 0.3 мл/мин.
МС условия: Масс-спектрометр с йонной ловушкой (Th ermoFinnigan Corp., San Jose, CA,USA);
ионизация: электроспрей (ESI); температура капилляра: 230 °C; осушающий газ: N2