Слайд 1РАЗМЕН ЭНЕРГИИ ВОЗБУЖДЕННОГО СОСТОЯНИЯ
Слайд 2ХАРАКТЕРИСТИКИ ЭЛЕКТРОННО-ВОЗБУЖДЕННЫХ СОСТОЯНИЙ
ОПРЕДЕЛЕННАЯ ЭНЕРГИЯ
ВРЕМЯ ЖИЗНИ
СТРУКТУРНЫЕ СВОЙСТВА
Слайд 3ПОЛНАЯ ЭНЕРГИЯ МОЛЕКУЛЫ
ПРИ ПОГЛОЩЕНИИ КВАНТА СВЕТА МОЛЕКУЛОЙ ПРОИСХОДИТ ПЕРЕХОД ЭЛЕКТРОНОВ
С ОСНОВНОГО СИНГЛЕТНОГО SO УРОВНЯ НА ВОЗБУЖДЕННЫЕ УРОВНИ S *
ВОЗБУЖДЕННОЕ
СОСТОЯНИЕ С ТОЧКИ ЗРЕНИЯ ТЕРМОДИНАМИКИ – НЕРАВНОВЕСНОЕ СОСТОЯНИЕ.
ИЗБЫТОЧНАЯ ЭНЕРГИЯ ДОЛЖНА РАСТРАТИТЬСЯ НА РАЗЛИЧНЫЕ ПРОЦЕССЫ.
Слайд 4РАЗМЕН ЭНЕРГИИ ВОЗБУЖДЕННОГО СОСТОЯНИЯ
S*
ТЕПЛО
ЛЮМИНЕСЦЕНЦИЯ (флуоресценция, фосфоресценция)
МИГРАЦИЯ ЭНЕРГИИ
ФОТОХИМИЧЕСКАЯ РЕАКЦИЯ
Слайд 5ЛЮМИНЕСЦЕНЦИЯ: ХАРАКТЕРИСТИКИ И ЗАКОНЫ
Слайд 6ХАРАКТЕРИСТИКИ ФЛУОРЕСЦЕНЦИИ
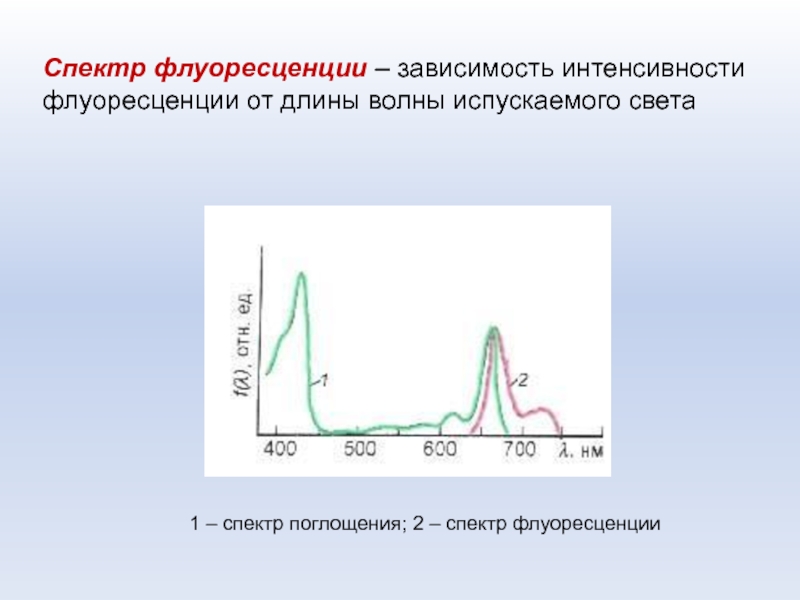
Слайд 7Спектр флуоресценции – зависимость интенсивности флуоресценции от длины волны испускаемого
света
1 – спектр поглощения; 2 – спектр флуоресценции
Слайд 8Спектр возбуждения флуоресценции – зависимость интенсивности флуоресценции от длины волны
возбуждающего света
Квантовый выход флуоресценции – отношение количества испускаемых квантов к
количеству поглощенных.
При возбуждении молекул линейно поляризованным светом наблюдается частичная поляризация флуоресценции. В этом случае измеряют степень поляризации флуоресценции
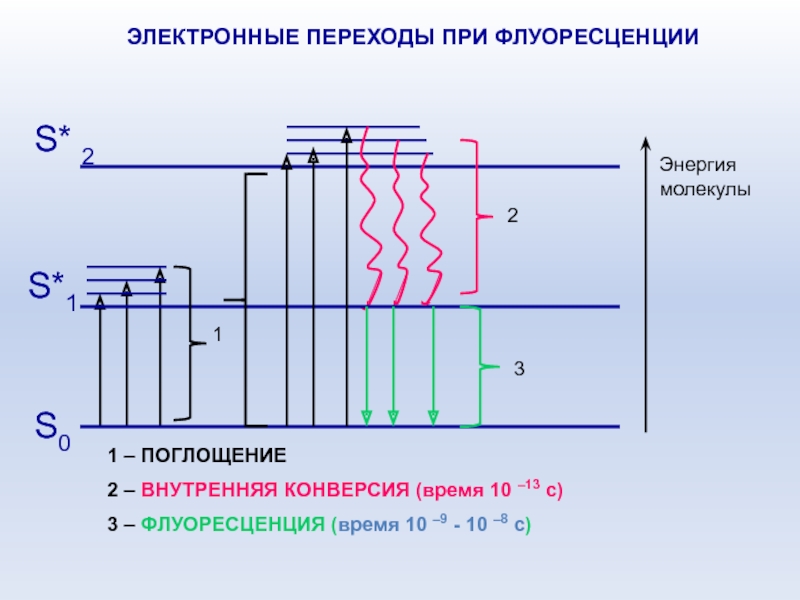
Слайд 91 – ПОГЛОЩЕНИЕ
2 – ВНУТРЕННЯЯ КОНВЕРСИЯ (время 10 –13 с)
3
– ФЛУОРЕСЦЕНЦИЯ (время 10 –9 - 10 –8 с)
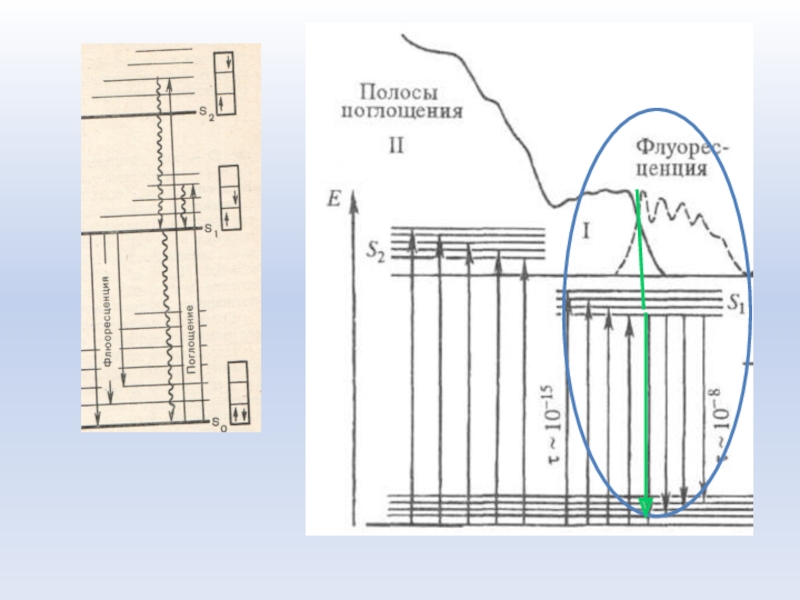
ЭЛЕКТРОННЫЕ ПЕРЕХОДЫ
ПРИ ФЛУОРЕСЦЕНЦИИ
Энергия молекулы
Слайд 11ЗАКОНЫ ФЛУОРЕСЦЕНЦИИ
ЗАКОН СТОКСА
ПРАВИЛО ЛЕВШИНА
ПРАВИЛО КАША
ЗАКОН ВАВИЛОВА
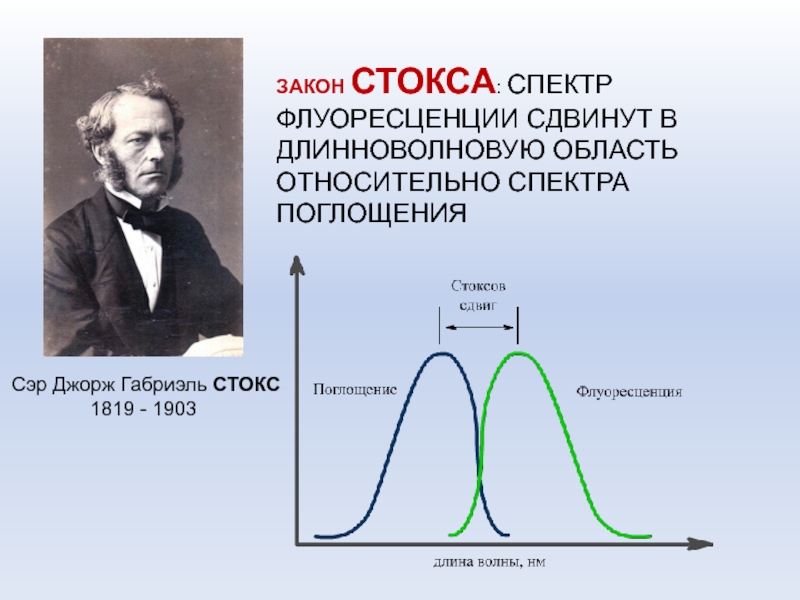
Слайд 12ЗАКОН СТОКСА: СПЕКТР ФЛУОРЕСЦЕНЦИИ СДВИНУТ В ДЛИННОВОЛНОВУЮ ОБЛАСТЬ ОТНОСИТЕЛЬНО СПЕКТРА
ПОГЛОЩЕНИЯ
Сэр Джорж Габриэль СТОКС
1819 - 1903
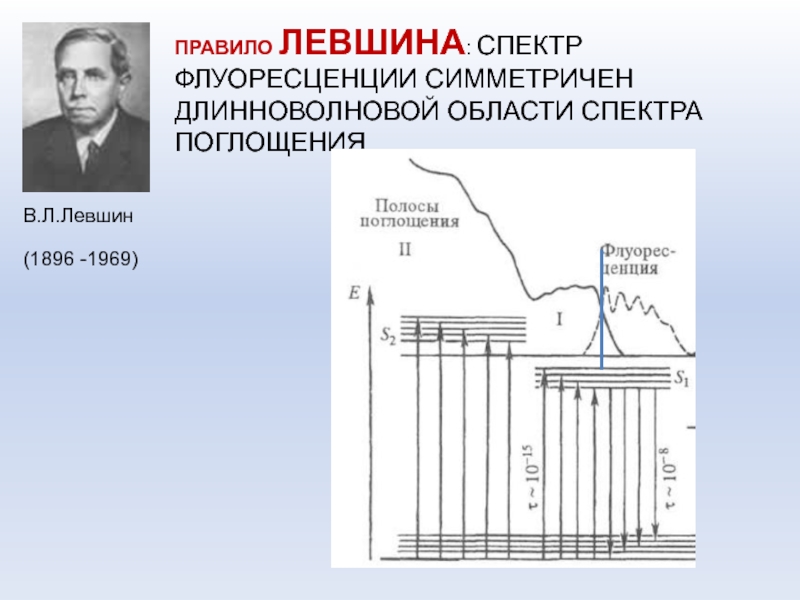
Слайд 14ПРАВИЛО ЛЕВШИНА: СПЕКТР ФЛУОРЕСЦЕНЦИИ СИММЕТРИЧЕН ДЛИННОВОЛНОВОЙ ОБЛАСТИ СПЕКТРА ПОГЛОЩЕНИЯ
(1896 -1969)
В.Л.Левшин
Слайд 15ПРАВИЛО КАША
Майкл КАША
р.1920
Предложено химиком Майклом Каша (Michael Kasha) в 1950.
Правило Каша: при облучении молекула будет излучать только за счет
низшего по энергии возбужденного состояния.
Слайд 16ПРАВИЛО ВАВИЛОВА: НЕЗАВИСИМОСТЬ КВАНТОВОГО ВЫХОДА ϕ ФЛУОРЕСЦЕНЦИИ ОТ ДЛИНЫ ВОЛНЫ
ВОЗБУЖДАЮЩЕГО СВЕТА
С.И.Вавилов
Слайд 18Фосфоресцентный порошок при облучении видимым светом (1), ультрафиолетовым светом (2)
и в полной темноте (3).
1 2 3
Слайд 19S0
S*1
S* 2
1
2
3
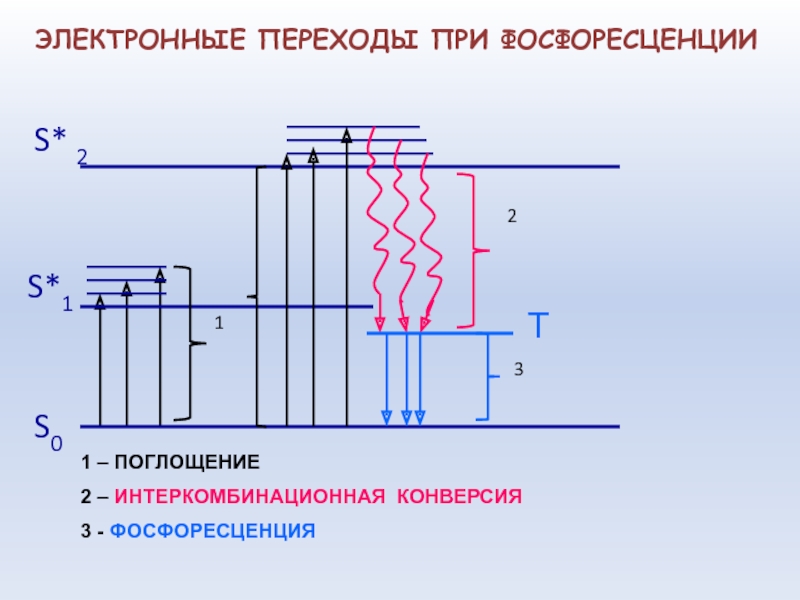
ЭЛЕКТРОННЫЕ ПЕРЕХОДЫ ПРИ ФОСФОРЕСЦЕНЦИИ
Т
1 – ПОГЛОЩЕНИЕ
2 – ИНТЕРКОМБИНАЦИОННАЯ КОНВЕРСИЯ
3
- ФОСФОРЕСЦЕНЦИЯ
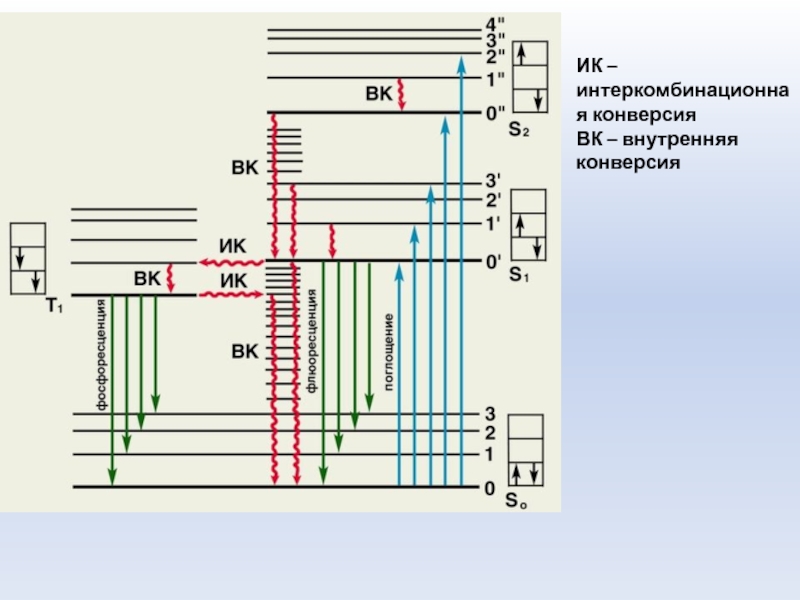
Слайд 20ИК – интеркомбинационная конверсия
ВК – внутренняя конверсия
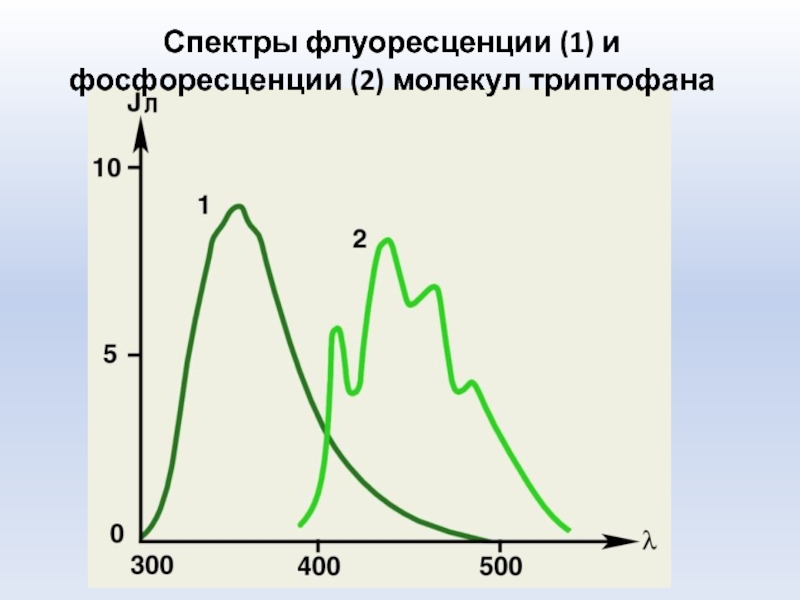
Слайд 22Спектры флуоресценции (1) и фосфоресценции (2) молекул триптофана
Слайд 23МЕТОДЫ ОБНАРУЖЕНИЯ ТРИПЛЕТНЫХ УРОВНЕЙ
ЭПР
ИМПУЛЬСНЫЙ ФОТОЛИЗ
ТЕРМОЛЮМИНЕСЦЕНЦИЯ
ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
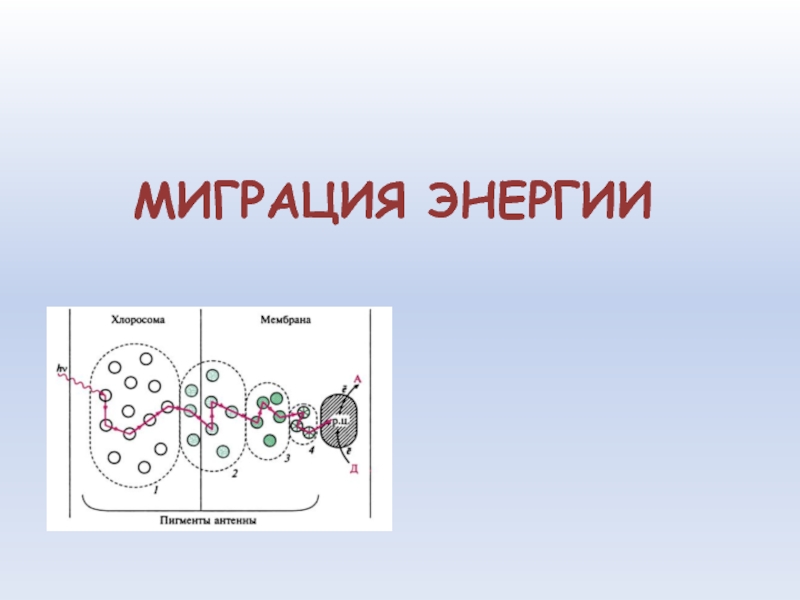
Слайд 25МИГРАЦИЯ ЭНЕРГИИ - это
D+hν → D* + A →
D + A*
БЕЗИЗЛУЧАТЕЛЬНЫЙ ПЕРЕНОС ЭНЕРГИИ
НА РАССТОЯНИЯ, ПРЕВЫШАЮЩИЕ МЕЖАТОМНЫЕ,
БЕЗ
СОУДАРЕНИЯ ДОНОРА И АКЦЕПТОРА
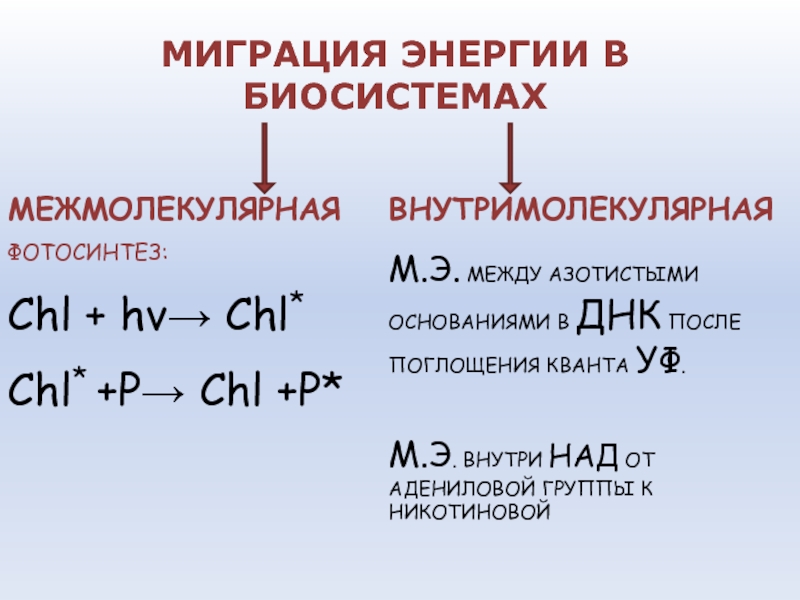
Слайд 26МИГРАЦИЯ ЭНЕРГИИ В БИОСИСТЕМАХ
МЕЖМОЛЕКУЛЯРНАЯ
ФОТОСИНТЕЗ:
Chl + hν→ Chl*
Chl*
+P→ Chl +P*
ВНУТРИМОЛЕКУЛЯРНАЯ
М.Э. МЕЖДУ АЗОТИСТЫМИ ОСНОВАНИЯМИ В ДНК ПОСЛЕ ПОГЛОЩЕНИЯ КВАНТА УФ.
М.Э. ВНУТРИ НАД ОТ АДЕНИЛОВОЙ ГРУППЫ К НИКОТИНОВОЙ
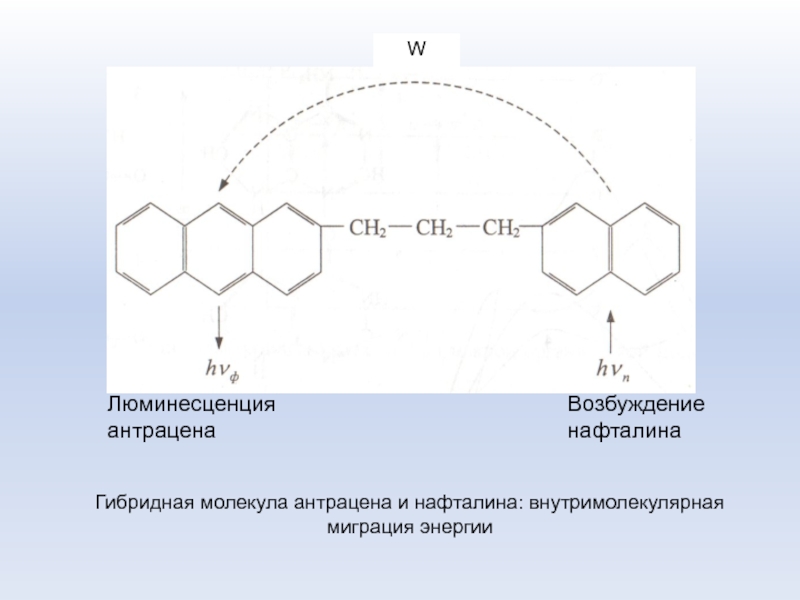
Слайд 27W
Гибридная молекула антрацена и нафталина: внутримолекулярная миграция энергии
Возбуждение нафталина
Люминесценция антрацена
Слайд 29ИНДУКТИВНО-РЕЗОНАНСНАЯ МИГРАЦИЯ ЭНЕРГИИ
Слайд 30УСЛОВИЯ ИНДУКТИВНО-РЕЗОНАНСНОЙ МИГРАЦИИ
(Правила Ферстера)
Слайд 311. ДОНОР СПОСОБЕН К ФЛУОРЕСЦЕНЦИИ
Слайд 322. СПЕКТР ФЛУОРЕСЦЕНЦИИ ДОНОРА ДОЛЖЕН ПЕРЕКРЫВАТЬСЯ СО СПЕКТРОМ ПОГЛОЩЕНИЯ АКЦЕПТОРА
Слайд 333. ДОНОР И АКЦЕПТОР РАСПОЛОЖЕНЫ НА ОПРЕДЕЛЕННОМ РАССТОЯНИИ (2 –
10 нм)
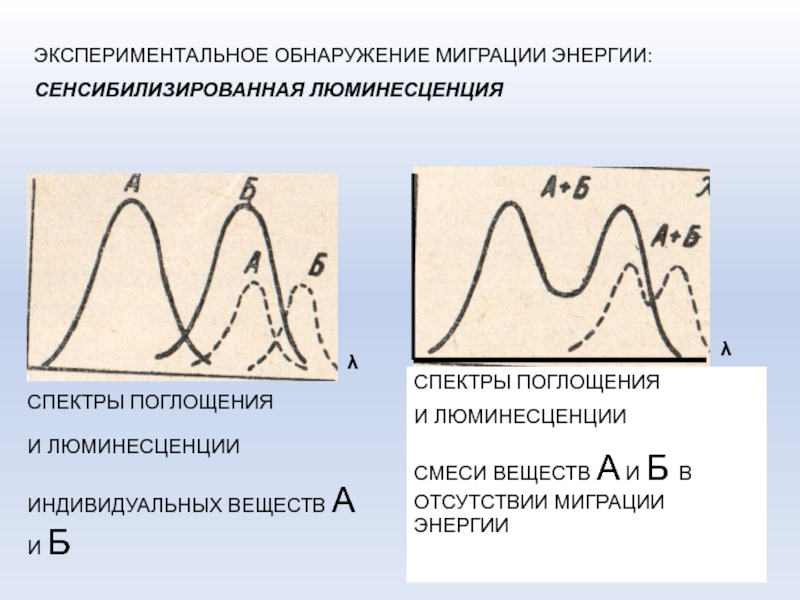
Слайд 34ЭКСПЕРИМЕНТАЛЬНОЕ ОБНАРУЖЕНИЕ МИГРАЦИИ ЭНЕРГИИ:
СЕНСИБИЛИЗИРОВАННАЯ ЛЮМИНЕСЦЕНЦИЯ
СПЕКТРЫ ПОГЛОЩЕНИЯ
И ЛЮМИНЕСЦЕНЦИИ
ИНДИВИДУАЛЬНЫХ ВЕЩЕСТВ А И
Б
СПЕКТРЫ ПОГЛОЩЕНИЯ
И ЛЮМИНЕСЦЕНЦИИ
СМЕСИ ВЕЩЕСТВ А И Б В ОТСУТСТВИИ МИГРАЦИИ
ЭНЕРГИИ
λ
λ
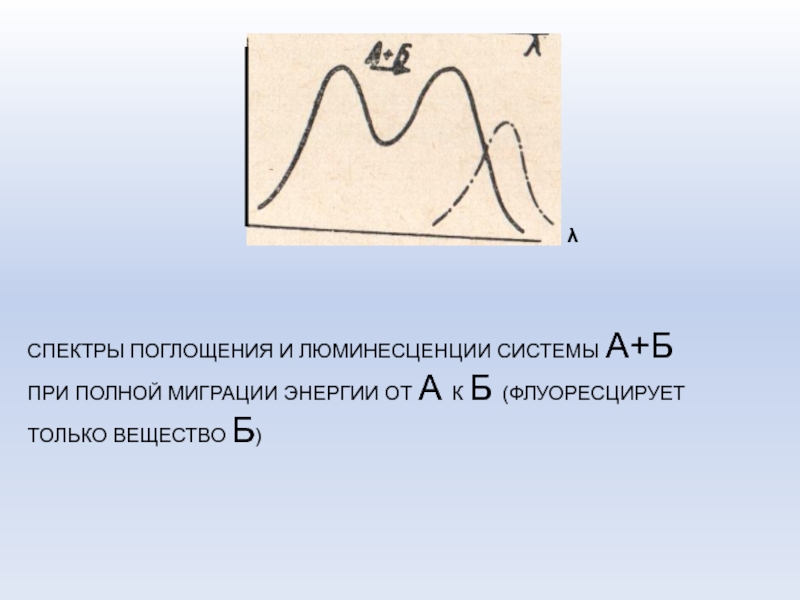
Слайд 35СПЕКТРЫ ПОГЛОЩЕНИЯ И ЛЮМИНЕСЦЕНЦИИ СИСТЕМЫ А+Б ПРИ ПОЛНОЙ МИГРАЦИИ ЭНЕРГИИ
ОТ А К Б (ФЛУОРЕСЦИРУЕТ ТОЛЬКО ВЕЩЕСТВО Б)
λ
Слайд 36ДРУГИМ ДОКАЗАТЕЛЬСТВОМ МИГРАЦИИ ЭНЕРГИИ СЛУЖИТ
СЕНСИБИЛИЗИРОВАННАЯ ФОТОХИМИЧЕСКАЯ РЕАКЦИЯ
А + hν
→ A*
A* + B → A + B* (МИГРАЦИЯ)
B* →
С (ФОТОХИМИЧЕСКАЯ РЕАКЦИЯ)
Слайд 37ОБМЕННО-РЕЗОНАНСНАЯ МИГРАЦИЯ ЭНЕРГИИ
ПЕРЕНОС ЭНЕРГИИ ОСУЩЕСТВЛЯЕТСЯ С Т-УРОВНЯ ДОНОРА НА Т-УРОВЕНЬ
АКЦЕПТОРА ПРИ ПРЯМОМ ПЕРЕКРЫВАНИИ ТРИПЛЕТНЫХ УРОВНЕЙ ЗА СЧЕТ ЭЛЕКТРОСТАТИЧЕСКИХ ВЗАИМОДЕЙСТВИЙ
ЭЛЕКТРОНОВ ДОНОРА И АКЦЕПТОРА.
ОБНАРУЖЕНИЕ: СЕНСИБИЛИЗИРОВАННАЯ ФОСФОРЕСЦЕНЦИЯ
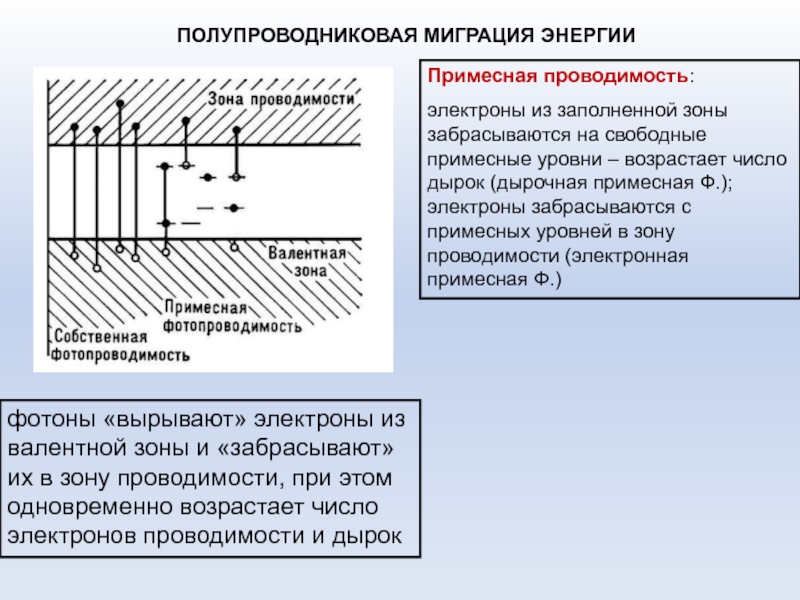
Слайд 38ПОЛУПРОВОДНИКОВАЯ МИГРАЦИЯ ЭНЕРГИИ
Примесная проводимость:
электроны из заполненной зоны забрасываются на свободные
примесные уровни – возрастает число дырок (дырочная примесная Ф.); электроны
забрасываются с примесных уровней в зону проводимости (электронная примесная Ф.)
фотоны «вырывают» электроны из валентной зоны и «забрасывают» их в зону проводимости, при этом одновременно возрастает число электронов проводимости и дырок
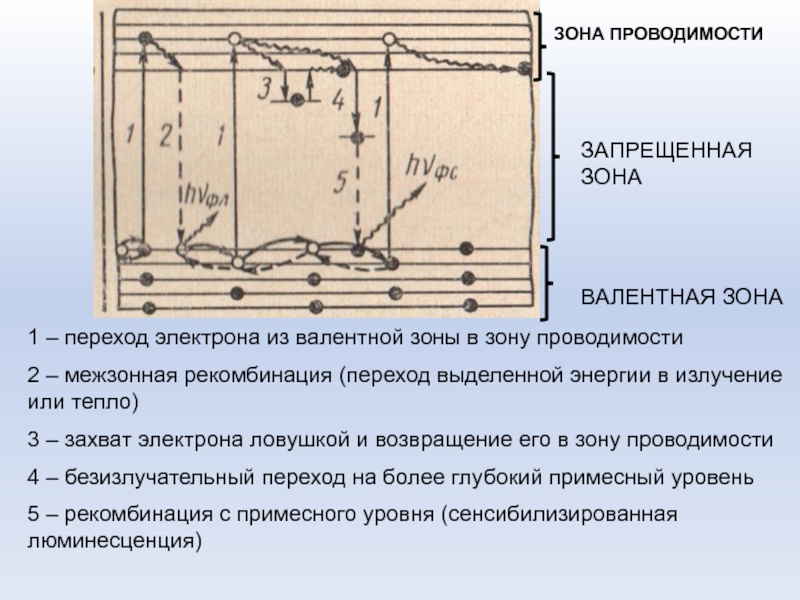
Слайд 391 – переход электрона из валентной зоны в зону проводимости
2
– межзонная рекомбинация (переход выделенной энергии в излучение или тепло)
3
– захват электрона ловушкой и возвращение его в зону проводимости
4 – безизлучательный переход на более глубокий примесный уровень
5 – рекомбинация с примесного уровня (сенсибилизированная люминесценция)
ЗАПРЕЩЕННАЯ ЗОНА
ВАЛЕНТНАЯ ЗОНА
ЗОНА ПРОВОДИМОСТИ
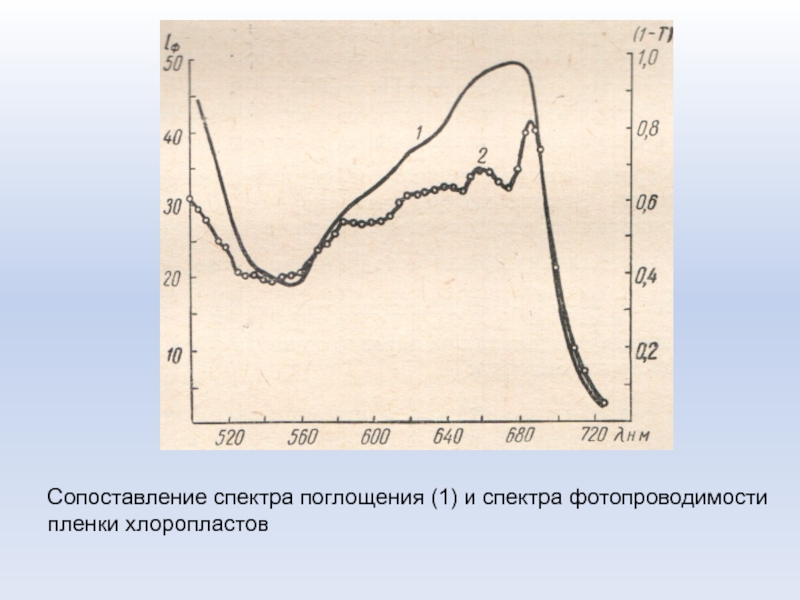
Слайд 40Сопоставление спектра поглощения (1) и спектра фотопроводимости пленки хлоропластов
Слайд 42ЭКСИТОН (от лат. excito - возбуждать)-мигрирующее в кристалле электронное возбуждение,
не связанное с переносом электрического заряда и массы.
Представление об ЭКСИТОНЕ
введено в 1931
Я. И. Френкелем
Яков Ильич Френкель
1894— 1952
Слайд 43В 1937-38 Дж. Ванье (G. Wannier) и H. Мотт (N.
Mott) ввели представление об ЭКСИТОНЕ как о перемещающихся по кристаллу
связанных состояниях электрона и дырки, которые могут находиться на различных узлах кристаллической решётки (Э. большого радиуса),
Экситон Френкеля можно представить как предельный случай, когда связанные электрон и дырка сидят на одном и том же узле (Э. малого радиуса).
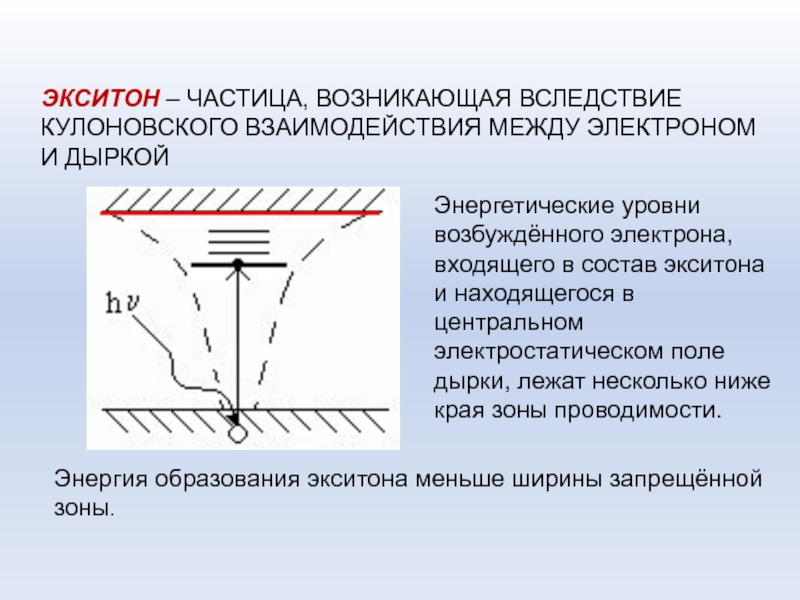
Слайд 44ЭКСИТОН – ЧАСТИЦА, ВОЗНИКАЮЩАЯ ВСЛЕДСТВИЕ КУЛОНОВСКОГО ВЗАИМОДЕЙСТВИЯ МЕЖДУ ЭЛЕКТРОНОМ И
ДЫРКОЙ
Энергетические уровни возбуждённого электрона, входящего в состав экситона и находящегося
в центральном электростатическом поле дырки, лежат несколько ниже края зоны проводимости.
Энергия образования экситона меньше ширины запрещённой зоны.
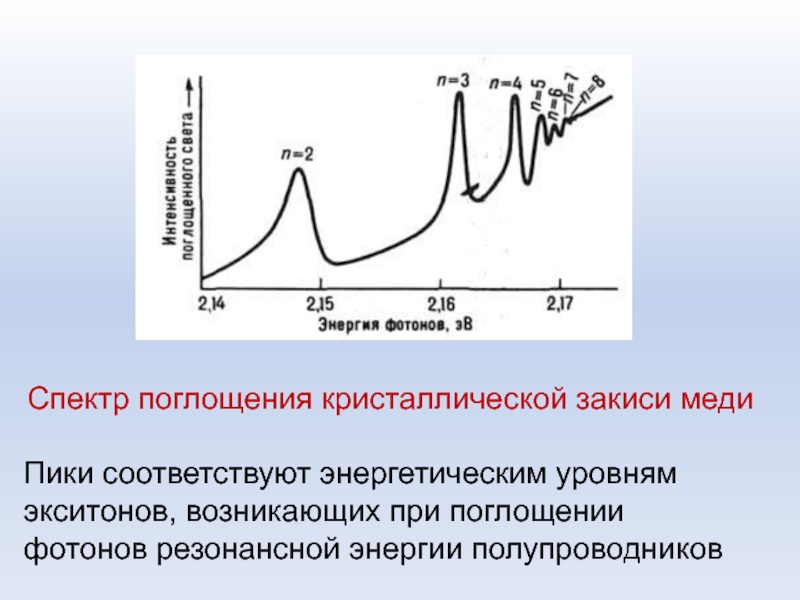
Слайд 45Спектр поглощения кристаллической закиси меди
Пики соответствуют энергетическим уровням экситонов, возникающих
при поглощении фотонов резонансной энергии полупроводников
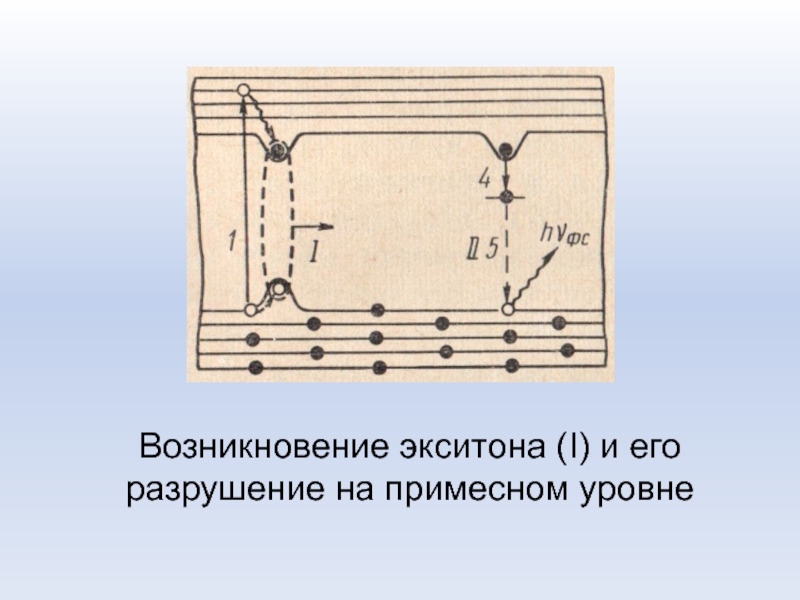
Слайд 46Возникновение экситона (I) и его разрушение на примесном уровне
Слайд 48ФОТОХИМИЧЕСКИЕ РЕАКЦИИ – реакции, которые происходят только под действием светового
излучения.
Для возбуждения таких реакций обычно используют видимое или УФ
излучение (длина волны λ от 200 до 700 нм).
Слайд 49При поглощении света происходит первичная реакция (фотохимическая активация) и молекула
переходит в возбужденное электронное состояние:
A + hν → A*.
Возбужденная молекула
может испытывать последующие превращения (вторичные реакции):
Слайд 50Фотодиссоциация- распад молекулы по какой-либо связи на радикалы, атомы или
ионы
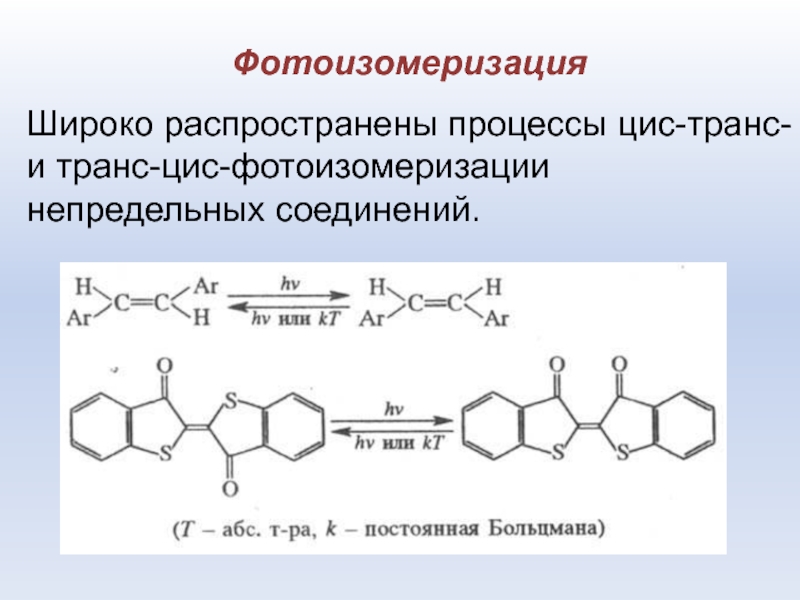
Слайд 51Фотоизомеризация
Широко распространены процессы цис-транс- и транс-цис-фотоизомеризации непредельных соединений.
Слайд 52Окислительно-восстановительные фотохимические реакции. В основе большинства из них лежит фотоперенос
электрона. В основе большинства из них лежит фотоперенос электрона. Образующиеся
в первичной стадии ион-радикалы вступают в дальнейшие превращения, давая продукты окисления. В основе большинства из них лежит фотоперенос электрона. Образующиеся в первичной стадии ион-радикалы вступают в дальнейшие превращения, давая продукты окисления или восстановления.
Слайд 53Характеристика фотохимической реакции - квантовый выход ϕ .
Квантовый выход фотохимической
реакции равен отношению числа прореагировавших молекул к числу поглощенных фотонов
.
Если каждый поглощенный фотон вызывает фотохимический акт, то ϕ =1.
В действительности ϕ <1 за счет вторичных процессов.
Слайд 551785 – 1822
Теодор фон ГРОТГУС
ЗАКОН ГРОТГУСА
ФОТОХИМИЧЕСКОЕ ДЕЙСТВИЕ
ОКАЗЫВАЕТ ТОЛЬКО ПОГЛОЩЕННЫЙ СВЕТ.
Слайд 56ЗАКОН ЭЙНШТЕЙНА
(ЗАКОН ЭКВИВАЛЕНТНОСТИ):
КАЖДЫЙ ПОГЛОЩЕННЫЙ КВАНТ СВЕТА hν ВЫЗЫВАЕТ ИЗМЕНЕНИЕ
ОДНОЙ МОЛЕКУЛЫ
АЛЬБЕРТ ЭЙНШТЕЙН
(1879-1955)
Слайд 57Концентрация продуктов фотохимической реакции пропорциональна общему количеству энергии излучения, поглощённого
светочувствительным веществом.
Это количество равно произведению мощности излучения на время
его действия.
Иными словами, увеличение времени и увеличение мощности излучения взаимозаместимы
Роберт Вильгельм БУНЗЕН
1811 – 1899
ЗАКОН БУНЗЕНА – РОСКО:
КОЛИЧЕСТВО ФОТОПРОДУКТА ЗАВИСИТ ОТ ДОЗЫ ОБЛУЧЕНИЯ (It)
Слайд 58Кинетика фотохимических реакций описывается обычными дифференциальными уравнениями, выражающими закон действующих
масс.
Единственное ОТЛИЧИЕ от обычных реакций в том, что скорость
фотохимических процессов определяется интенсивностью поглощенного света.
Слайд 59СКОРОСТЬ ФОТОХИМИЧЕСКИХ РЕАКЦИЙ
Скорость фотохимических реакций пропорциональна количеству квантов, поглощенных в
единицу времени:
Слайд 60Не все поглощенные кванты вызывают фотохимическую реакцию, поэтому следует учесть
квантовый выход реакции – ϕ .
Слайд 61Скорость поглощения квантов зависит от
интенсивности падающего света (I),
концентрации вещества
(c), участвующего в поглощении.
Коэффициент пропорциональности S - эффективное поперечное
сечение молекулы- площадь (S), при попадании в которую, квант поглощается:
Слайд 62С учетом квантового выхода реакции, уравнение примет вид:
Слайд 63Решая это дифференциальное уравнения имеем
Слайд 64Часто вводят величину σ - поперечное сечение фотореакции,
Площадь, при попадании
в которую квант не только поглощается, но и вызывает фотохимическую
реакцию:
Слайд 65Таким образом, концентрация реагирующего вещества убывает по экспоненциальному закону в
зависимости от дозы облучения It.
Тогда уравнение примет вид:
Слайд 66ФЛУОРЕСЦЕНТНАЯ СПЕКТРОСКОПИЯ БЕЛКОВ
Используется для изучения конформационных свойств белка в растворе.
Белки содержат три собственных флуоресцирующих хромофора – триптофан, тирозин и
фенилаланин.
Наиболее интенсивную ФЛ дают триптофан и тирозин.
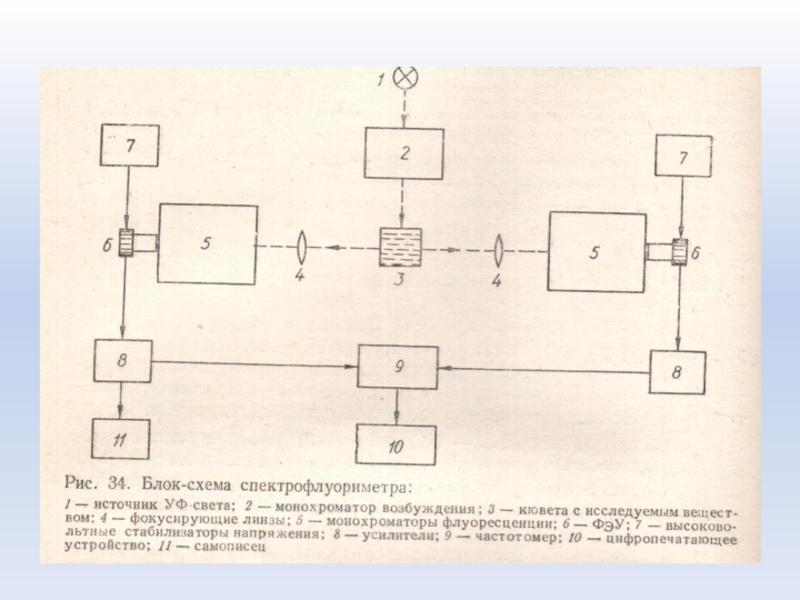
Флуоресценцию изучают на спектрофлуориметрах
Слайд 68Наиболее чувствительной к изменению конформации белка является ФЛ триптофановых остатков.
Положение максимума спектра ФЛ триптофановых остатков зависит от свойств микроокружения.
Триптофановые
остатки находятся на поверхности глобулы в полярном окружении, или в денатурированном белке: их спектр подобен спектру триптофана в воде.
Спектр остатков триптофана внутри глобулы смещен в более коротковолновую область, а его максимум варьирует в широких пределах (от 442 до 320 нм).
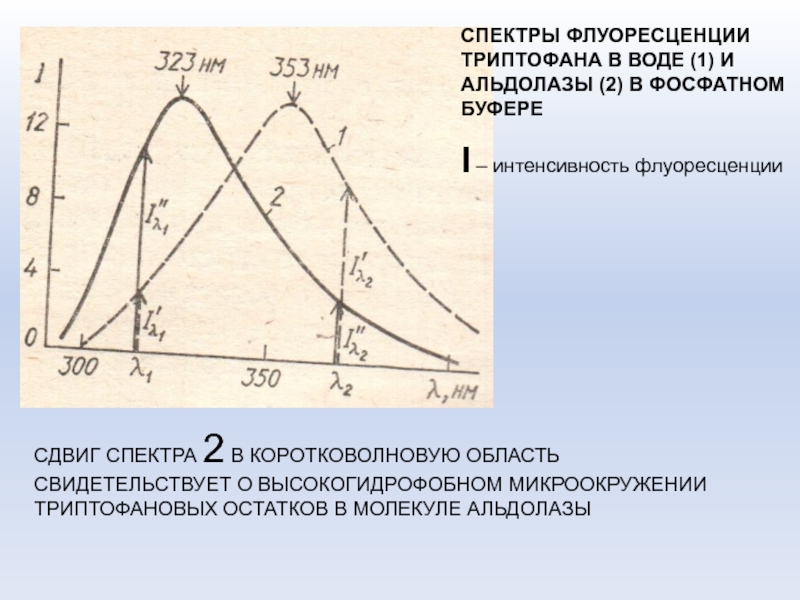
Слайд 69СПЕКТРЫ ФЛУОРЕСЦЕНЦИИ ТРИПТОФАНА В ВОДЕ (1) И АЛЬДОЛАЗЫ (2) В
ФОСФАТНОМ БУФЕРЕ
I – интенсивность флуоресценции
СДВИГ СПЕКТРА 2 В КОРОТКОВОЛНОВУЮ ОБЛАСТЬ
СВИДЕТЕЛЬСТВУЕТ О ВЫСОКОГИДРОФОБНОМ МИКРООКРУЖЕНИИ ТРИПТОФАНОВЫХ ОСТАТКОВ В МОЛЕКУЛЕ АЛЬДОЛАЗЫ
Слайд 70Измеряя спектры триптофановой ФЛ белка, можно оценить конформационные перестройки в
белке при действии факторов среды или в процессе функционирования белка
(ферментный катализ, транспорт ионов и др.)
Кроме изучения собственной ФЛ широко используют флуоресцентные зонды.
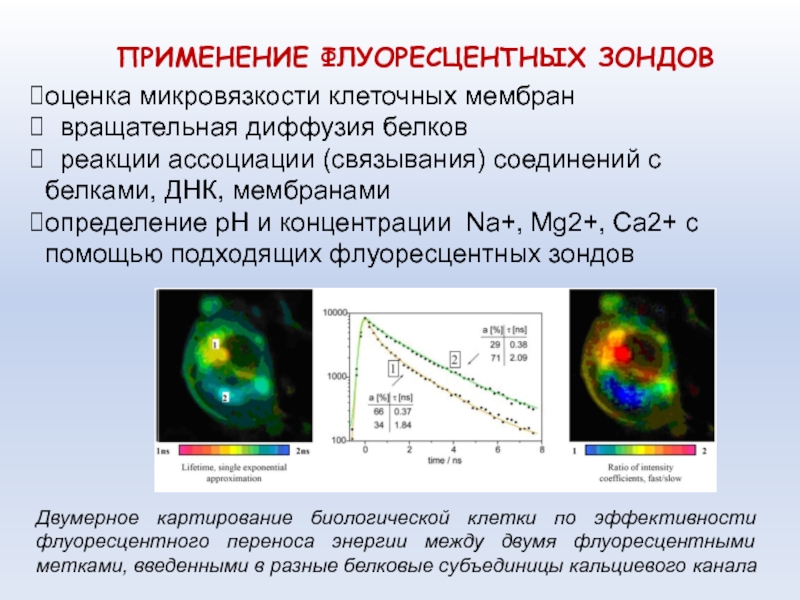
Слайд 71оценка микровязкости клеточных мембран
вращательная диффузия белков
реакции ассоциации (связывания)
соединений с белками, ДНК, мембранами
определение рН и концентрации Na+, Mg2+,
Ca2+ с помощью подходящих флуоресцентных зондов
ПРИМЕНЕНИЕ ФЛУОРЕСЦЕНТНЫХ ЗОНДОВ
Двумерное картирование биологической клетки по эффективности флуоресцентного переноса энергии между двумя флуоресцентными метками, введенными в разные белковые субъединицы кальциевого канала