Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Реферат на тему: Методы выделения, очистки и идентификации биологически
Содержание
- 1. Реферат на тему: Методы выделения, очистки и идентификации биологически
- 2. Основные методы выделения биологически активных веществ 1)Экстрагирование2)Перегонка водяным паром
- 3. Экстрагирование1.Теоретические основы экстрагирования.Процесс экстрагирования относится к массообменным
- 4. Экстрагирование3. Стадии процесса экстрагирования и их количественные характеристикиСтадии
- 5. Экстрагирование1.На первой стадии экстрагирование из обезвоженного сырья
- 6. Виды экстрагированияА) Мацерация. Мацерация – метод экстрагирования
- 7. Виды экстрагированияБ) Перколяция – метод основанный на
- 8. Виды перколяторов1)Конические перколяторы. Конические перколяторы удобны для
- 9. Виды перколяторов2)Цилиндрический перколятор. На рисунке представлена схема
- 10. Виды перколяторов3) Экстрактор-перколятор с паровой рубашкой для
- 11. Виды экстрагированияВ) Реперколяция – метод основанный на
- 12. Виды экстрагированияГ) Ускоренная дробная мацерация методом противотока.
- 13. Виды экстрагированияД) Циркуляционное экстрагирование. Сущность метода заключается
- 14. Виды экстрагированияЕ) Непрерывное противоточное экстрагирование с перемешиванием
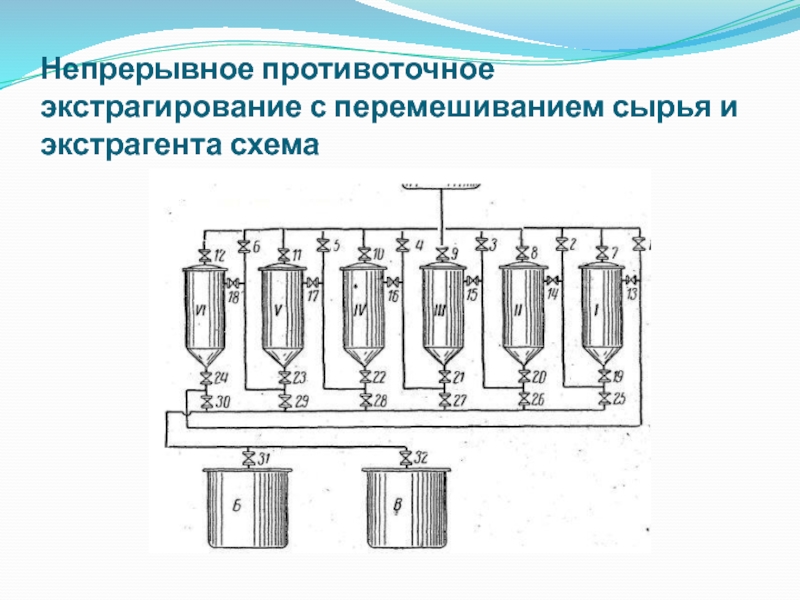
- 15. Непрерывное противоточное экстрагирование с перемешиванием сырья и экстрагента схема
- 16. Непрерывное противоточное экстрагирование с перемешиванием сырья и
- 17. Виды экстрагированияЖ) Экстракция сжиженными газами(низкотемпературная экстракция).Экстракция сжиженными
- 18. Интенсификация процессов экстрагированияА)Применение ультразвука. Ультразвуковой способ экстрагирования
- 19. Интенсификация процессов экстрагированияБ) Применение электрических зарядов. Ускорение
- 20. Интенсификация процессов экстрагированияВ) Применение электроплазмолиса. Электроплазмолиз — обработка
- 21. Интенсификация процессов экстрагированияПрименение электродиализа. Ускорение процесса экстрагирования
- 22. Перегонка с водяным паром 1)Гидродистилляция. Простейший вариант заключается
- 23. Перегонка с водяным паром 2)Паровая дистилляция. Наиболее
- 24. 2)Паровая дистилляция схема Схема установки для паровой
- 25. Перегонка с водяным паром Деструктивная дистилляция. Иногда
- 26. Основные методы очистки БАВ 1)Диализ. Диализ — освобождение коллоидных
- 27. Основные методы очистки БАВ2) Обратный осмос. Обратный
- 28. Основные методы очистки БАВ3) Микрофильтрация(МФ). Микрофильтрация позволяет
- 29. Основные методы очистки БАВ4) Ультрафильтрация(УФ). Ультрафильтрация позволяет
- 30. Основные методы очистки БАВ5) Нанофильтрация(НФ).Нанофильтрация позволяет удалять
- 31. Основные методы очистки БАВ6) Сорбция. Сорбция —
- 32. Основные методы очистки БАВ7) Адсорбционно - хроматографический
- 33. Основные методы очистки БАВ8) Гель-фильтрация. Гель-фильтрация –
- 34. Основные методы очистки БАВ9) Гидрофобная хроматография - жидкостная
- 35. Основные методы очистки БАВ10) Аффинная хроматография — разновидность лигандной.
- 36. Основные методы идентификации БАВ 1)Определение вещества по
- 37. Основные методы идентификации БАВ2)Определение вещества по спектрам,
- 38. Основные методы идентификации БАВ3)ХромотаграфияЭто способ анализа веществ, основанных
- 39. Основные методы идентификации БАВ4) Применение ферментовМожно воспользоваться
- 40. Основные методы идентификации БАВ5)Спектроскопия - разделы физики и аналитической химии,
- 41. Виды спектроскопииА) Микроволновая спектроскопия - методика определения
- 42. Виды спектроскопииБ) Инфракрасная спектроскопия (ИКС) — раздел спектроскопии, охватывающий
- 43. Виды спектроскопииВ) Ультрафиолетовая (электронная) спектроскопия — раздел оптической спектроскопии,
- 44. Виды спектроскопииГ) РЕНТГЕНОВСКАЯ спектроскопия, раздел спектроскопии, изучающий спектры испускания
- 45. Скачать презентанцию
Основные методы выделения биологически активных веществ 1)Экстрагирование2)Перегонка водяным паром
Слайды и текст этой презентации
Слайд 1Реферат
на тему: «Методы выделения, очистки и идентификации биологически активных веществ»
Выполнил
Студент
группы 21-ПБ
Слайд 2Основные методы выделения биологически активных веществ
1)Экстрагирование
2)Перегонка водяным паром
Слайд 3Экстрагирование
1.Теоретические основы экстрагирования.
Процесс экстрагирования относится к массообменным процессам и протекает
за счет диффузии =из зоны с высокой концентрацией. Это, как
правило, клетки животного или растительного материала, содержащие биологически активные вещества. Экстрагирование основано на диффузии биологически активных веществ из внутренних структур частиц материала в экстрагент и заканчивается при достижении равновесных концентраций. В равновесном состоянии из материала в экстрагент переходит такое же количество молекул, как и из экстрагента в материал, т. е. концентрация остается постоянной.2. Особенности экстрагирования из растительного сырья с клеточной структурой
При экстрагировании из лекарственного растительного сырья идет диффузия БАВ из внутренних структур частицы материала. При этом процессе извлечение имеет свои особенности. Прежде ч всего, наличие пористой перегородки, межклеточного пространства и клеточных ходов снижает скорость диффузии. Далее, через поры перегородки могут пройти только те вещества, частицы которых не превышают размеров пор. Наконец, имеется еще одна существенная особенность — явление десорбции, наблюдаемое в клетке после проникновения в нее экстрагента. Поскольку вещества внутри клетки связаны силами притяжения, то необходимо прежде всего преодоление этих адсорбционных сил. Весь сложный комплекс диффузионных явлений, протекающих внутри кусочков растительного материала, называютвнутренней диффузией.
Особенности извлечения биологически активных веществ из материалов с клеточной структурой связаны с тем, что на пути к веществам, содержащимся в клетке, находится клеточная стенка, физиологическое состояние которой может быть различным. Так, живая растительная клетка имеет пристенный слои протоплазмы определенной толщины. Он накладывает особый отпечаток на свойства клеточной стенки, как перегородки, отделяющей раствор внутри клетки (клеточный сок) от жидкости вне клетки.
Пока протоплазма жива, клеточная стенка является полупроницаемой перегородкой, не пропускающей наружу вещества, растворенные в клеточном соке. В данном случае возможно лишь проникновение экстрагента внутрь клетки (осмос).
Совершенно по-другому ведет себя мертвая клетка. Вследствие гибели протоплазмы (плазмолиза) клеточная стенка теряет характер полупроницаемой перегородки и начинает пропускать вещества в обе стороны (диализ). То есть клеточная стенка приобретает .свойства пористой перегородки, через нее могут диффундировать биологически активные вещества, молекулы которых не превышают размера пор.
Подавляющее большинство экстракционных препаратов получают из высушенного растительного сырья, т. е. обезвоженного путем тепловой сушки. В случае получения препаратов из свежих растений клетки умерщвляют этиловым спиртом. Он очень гигроскопичен и при соприкосновении с растительной клеткой обезвоживает ее, вызывая сильнейший плазмолиз. Умерщвлениеклеток сырья животного происхождения достигается теми же способами: сушкой или обезвоживанием спиртом и ацетоном.
При получении препаратов из свежего сырья, клетки которого не обезвожены, скорее имеет место вымывание клеточного сока из разрушенных клеток и открытых пор, чем процесс экстрагирования.
Слайд 4Экстрагирование
3. Стадии процесса экстрагирования и их количественные характеристики
Стадии процесса экстрагирования и
их количественные характеристики
Процесс экстрагирования проходит в три стадии:
1) смачивание
сырья (капиллярная пропитка);2) образование первичного сока;
3) массообмен. В процессе экстрагирования происходит массопередача, характеризуемая переходом одного или нескольких веществ из одной фазы (сырья) в другую (экстрагент). Массопередача из сырья с клеточной структурой — сложный процесс, в котором можно выделить три стадии:
1) «внутренняя диффузия», включающая все явления переноса веществ внутри частиц сырья; 2) перенос вещества в пределах непосредственно диффузионного пограничного слоя; 3) перенос вещества движущимся экстрагентом (конвективная диффузия).
Слайд 5Экстрагирование
1.На первой стадии экстрагирование из обезвоженного сырья с клеточной структурой
начинается с проникновения экстрагента в материал, смачивания веществ, находящихся внутри
клетки, растворения и десорбции их. Далее следует молекулярный перенос растворенных веществ, вначале в экстрагент, находящийся в межклеточном пространстве, затем в экстрагент, заполняющий микро-и макротрещины, и наконец, на поверхность кусочков материала. Представим в виде схемы (рис.) частичку материала, находящуюся в экстрагенте, и обозначим среднюю концентрацию экстрагируемых веществ внутри частицы С1 а на ее поверхности — С2.Рис1. Частичка сырья в экстрагенте 2.На второй стадии идет диффузия веществ от поверхности частицы (концентрация С2) к наружной поверхности диффузионного пограничного слоя (концентрация С3). В настоящее время общепризнанно существование на поверхности кусочков сырья пристенного слоя, экстрагента, называемого диффузионным пограничным слоем. Пограничный диффузионный слой оказывает большое сопротивление дальнейшему переносу экстрагируемых веществ в экстрагент. Толщина этого слоя зависит от гидродинамики процесса и, в основном, от скорости перемешивания экстрагента. Чем больше скорость перемешивания, тем меньше толщина пограничного слоя. В пределах диффузионного пограничного слоя перенос веществ осуществляется по закону свободнойдиффузии и может быть записан в виде первого закона Фика. 3.Далее, на третьей стадии процесса экстрагирования перенос действующих веществ осуществляется за счет движения экстрагента (конвективная диффузия) средняя концентрация экстрагента в объеме, омывающем частичку- С4, факторов.
Слайд 6Виды экстрагирования
А) Мацерация. Мацерация – метод экстрагирования заключающийся в настаивании
(является самым древним и приметивным).
Этот процесс заключается в следующем. Измельченный
до требуемой крупности материал помещают в настойник и заливают извлекателем— водой, спиртом и т. п. Количества растительного материала и извлекателя для каждого препарата устанавливаются регламентом.Для ускорения процесса экстрагирования образовавшийся вокруг растительного материала концентрированный слой извлечения необходимо постоянно удалять. Эта достигается двумя способами:
1) непрерывным перемешиванием всего экстрагируемого материала;
2) принудительным циркулированием получаемого извлечения либо чистого извлекателя, в то время как растительный материал остается без движения.
Все полученные после нескольких настаиваний жидкости сливают вместе и отстаивают в прохладном месте в течение четырех-пяти суток для того, чтобы взвешенные частицы осели на дно.
В основном для мацерации применяют настойник с мешалкой.
В бак 1 на ситовидное дно 8 с фильтровальным полотном 6 насыпают
измельченный материал, заливая его требуемым количеством извлекателя,
чтобы вся смесь стала достаточно жидкой. Для более
быстрого экстрагирования содержимое настойника перемешивают
мешалкой 5, приводимой в движение при помощи зубчатой
передачи 2 и шкивов 3 и 4. Выливают извлечение через кран 7.
Слайд 7Виды экстрагирования
Б) Перколяция – метод основанный на непрерывном вытеснении БАВ
чистым извлекателем из растительного сырья (заранее приготовленного к этому процессу).
Процесс производится в особых конусообразных или цилиндрических аппаратах, называемых вытеснителями или перколят орами. Перколяторы бывают различных размеров и формы. В большинстве случаев — это аппараты цилиндрической или конической формы, имеющие в нижней части кран и закрываемые сверху крышкой.Слайд 8Виды перколяторов
1)Конические перколяторы. Конические перколяторы удобны для загрузки и выгрузки
растительного материала, но процесс перколяции в них при очень большой
конусности протекает неравномерно. Поэтому чаще применяют цилиндрические перколяторы, в которых для выгрузки проэкстрагированного сырья имеются различные приспособления.. На рисунке а представлена схема маленького конического перколятора. Из опрокинутой склянки извлекатель наливается на растительный материал. После того, как уровень жидкости поднимется до конца стеклянной трубки 2, наполнение перколятора прекращается, а с уменьшением количества жидкости в перколяторе прежний уровень автоматически восстанавливается.
В перколяторе имеется ситовидное дно, на котором расстилают полотно и укладывают растительный материал 3. Перколят собирают в приемнике 5 через кран 4. Иногда, для предохранения от чрезмерного уплотнения мягкого или, смолистого растительного материала, в перколяторе устанавливается ряд ситовидных днищ.
Слайд 9Виды перколяторов
2)Цилиндрический перколятор. На рисунке представлена схема опрокидывающегося цилиндрического, экстрактора-перколятора,
установленного на стойках растительный материал 11 загружают в корпус 1
на ложное дно 8, на которое натянуто полотно 7, служащее для первого фильтрования перколята. Перколятор заполняют извлекателем через воронку 3, закрывают крышкой 2, завинчивают барашки и настаивают в течение 24—48 ч. После этого приступают к вытеснению, т. е. через нижний кран 9 сливают перколят, одновременно наливая через воронку в верхнем кране чистый извлекатель. Так продолжают до полного истощения растительного материала. Затем для выгрузки истощенного материала, Отвинчивают крышку 2 и при помощи рукоятки червяка 6 и червячного колеса 5 опрокидывают перколятор, поворачивающийся на осях 4.Слайд 10Виды перколяторов
3) Экстрактор-перколятор с паровой рубашкой для обогрева и барботе-ром
для отгонки спирта. На рисункке представлена схема такого перколятора из
нержавеющей стали емкостью 250 л.Перколятор состоит из корпуса 1; стальной паровой рубашки 2 с патрубками для входа пара в рубашку 3 и 6 и патрубком для конденсата 4; загрузочного люка 5; опорных лап 7; ложного днища 8; барботера 9 патрубка для выпуска перколята 10; гильзы для термометра 11; патрубка для паров 12; патрубка для сжатого воздуха 13; патрубка для наполнения перко-лятдра извлекателем 14; люка для выгрузки истощенного растительного материала 15: Экстрактор-перколятор с откидным дном. На рисунке дана схема перколятора, применяемого на крупном производстве. Этот перколятор сострит из цилиндрического корпуса 1 с коническими крышкой и днищем. В крышке устроен загрузочный люк 2, а в днище — откидной выгрузочный люк 3 и ситовидное ложное дно 4. Такие перколяторы часто устанавливают в виде батарей, связанных между собой специальным трубопроводом.
Слайд 11Виды экстрагирования
В) Реперколяция – метод основанный на приготовлении экстрактов многократной
перколяцией. Самой эффективной является реперколяция состоящая из 5 стадий перколяции.
При реперколяции экстракция происходит более эффективно и при этом расходуется примерно в 8 раз меньше экстракторов.Слайд 12Виды экстрагирования
Г) Ускоренная дробная мацерация методом противотока. Принцип работы заключается
в том, что растительный материал в сухом виде загружают поровну
в три экстрактора. Экстрагент подают в первый экстрактор и настаивают в течение 2ч. Полученную вытяжку переносят на сырье во второй экстрактор, одновременно в первый снова заливают чистый экстрагент». Сырье в обоих экстракторах настаивают 2ч, после этого вытяжку из второго экстрактора переносят на сырье в третий, а из первого — на сырье во второй экстрактор. В первый экстрактор заливают весь оставшийся экстрагент. Загруженные экстракторы оставляют для настаивания сырья на 24ч. Затем из третьего экстрактора получают первый слив готового продукта. Вытяжку из второго экстрактора переносят на сырье в третий, сливом из первого — заливают сырье во втором экстракторе. Оба экстрактора оставляют на 2ч для настаивания сырья. В это время первый экстрактор отключают, сырье выгружают и отжимают. Через 2ч из третьего экстрактора получают второй слив готового продукта. Вытяжкой из второго экстрактора заливают сырье в третьем, второй экстрактор разгружают, сырье отжимают. После двухчасового настаивания из третьего экстрактора получают третью порцию готового продукта, сырье выгружают и отжимают Все сливы и отжимы объединяют.Слайд 13Виды экстрагирования
Д) Циркуляционное экстрагирование. Сущность метода заключается в многократном экстрагировании
растительного сырья одной и той же порцией летучего экстрагента. (эфир,
хлороформ, метилен хлористый и т. д.). Экстрагирование осуществляется в замкнутом цикле в аппарате типа «Сокслет» .Лучшие условия экстрагирования сырья создаются в нижней части экстрактора (4), так как оно находится там в контакте с экстрагентом более длительное время, чем в верхней. В связи с этим конструируются экстракторы, снабженные специальными приспособлениями для перемещения сырья внутри аппарата. Основными узлами установки для проведения циркуляционного экстрагирования являются: испаритель (1), снабженный паровой рубашкой, экстрактор (4), конденсатор (2) и сборник (3).
Во избежание засорения трубопровода растительный материал загружают в полотняном мешке, заливают экстрагентом и оставляют для настаивания на несколько часов. После этого вытяжку переводят в испаритель (1) и доводят до кипения. Образующиеся пары поступают в конденсатор и в виде дистиллята возвращаются на сырье в экстрактор. Циркуляция экстрагента повторяется 10—15 раз до истощения растительного материала. Полученную вытяжку концентрируют отгонкой экстрагента в приемник. В испарителе остается концентрированный раствор экстрактивных веществ.
Слайд 14Виды экстрагирования
Е) Непрерывное противоточное экстрагирование с перемешиванием сырья и экстрагента.
Растительный материал при помощи транспортных устройств: шнеков, ковшей, дисков, лент,
скребков или пружинно-лопастных механизмов перемещается навстречу движущемуся экстрагенту. Сырье, непрерывно поступающее в экстракционный аппарат, движется противотоком к экстрагенту. При этом свежее сырье контактирует с выходящим, насыщенным экстрактивными веществами экстрагентом, который еще более насыщается, так как в сырье концентрация еще выше. Истощенное сырье экстрагируется свежем экстрагентом, который еще полнее извлекает оставшиеся экстрактивные вещества. С точки зрения теории экстрагирования этот способ наиболее эффективен, так как в каждый момент процесса и в любом поперечном сечении по длине (или высоте) аппарата имеет место разность концентраций БАВ в сырье и экстрагенте, что позволяет с наибольшим выходом и наименьшими затратами проводить процесс. Кроме того, непрерывные процессы поддаются автоматизации, что позволяет исключить трудоемкие работы по загрузке и выгрузки сырья из перколяторов. Экстрагирование по данному методу производят в многокорпусных экстракторах или батареях экстракторов (перколяторов, диффузоров). Эти установки состоят из нескольких (от 5 до 12) экстракторов одинакового объёма и конструкции, связанных между собой трубопроводами. Но отдельные батареи могут отличаться друг от друга типами экстракторов и их размерами. На рисунке представлена схема батареи экстракторов. Работа подобной установки разделяется на три основных периода: 1) пусковой, 2) рабочий и 3) остановочный в конце производства определенного препарата. Следует отметить, что чем продолжительнее рабочий период, тем рентабельнее производство, потому что при пусковом периоде из батареи экстракторов не получают никакой продукций, а в конце производственного цикла получают менее концентрированное извлечение, чем во время рабочего периода. Обычно рабочий период длится годами или месяцами.Слайд 16Непрерывное противоточное экстрагирование с перемешиванием сырья и экстрагента схема
Пусковой период
непродолжителен, он видоизменяется в зависимости от характера растительного сырья и
извлекателя. Обычно растительный материал, измельченный до требуемой крупности, загружают в один из экстракторов. При этом, если данный материал рыхлый, без мелкой крошки и хорошо пропускает извлекатель через весь слой экстрагируемого материала, то экстрактор загружают им на 0,8—0,9 рабочей емкости. На этот растительный материал сверху наливают извлекатель, который, пройдя через весь слой материала, постепенно заполняет весь экстрактор и, насыщаясь экстрактивными веществами, вытекает через нижний кран или поступает на растительный материал, находящийся в другом экстракторе. Но в тех случаях, если: 1) при разбавлении извлекателя выделяются смолы или другие вещества, которые закрывают, отверстая крана, находящиеся под экстрактором; 2) в растительном материале содержится много воздуха; 3) или извлечение становится легче, чем чистый извлекатель, — то загрузку экстрактора производят послойно, тщательйо перемешивая растительный материал с извлекателем, подавая последний снизу вверх, например: из напорного бака А через краны 2 и 19 этот материал заливают извлекателем. После того, как экстрактор будет заполнен на 0,9— 0,95 емкости, к нему герметически привинчивают крышку, закрывают кран 13 и открывают кран 7. Экстрактор 1 продолжают заполнять извлекателем до тех пор, пока из крана 7 не потечет жидкость. Это служит признаком того, что воздух из экстрактора вытеснен полностью и он заполнен извлекателем. Тогда закрывают краны 2 и 7, и смесь настаивается в экстракторе. Затем по предыдущему способу загружают растительным материалом экстрактор VI, куда из бака А через краны 2, 19, 13 и 24 поступает извлекатель. После заполнения экстрактора VI его закрывают крышкой, закрывают кран 18 и открывают кран 12, через который вытесняют воздух. После заполнения этого экстрактора жидкостью закрывают кран 12. Рабочий период (установившаяся работа) начинается со второго оборота экстрактора I. При этом его отключают от батареи, выгружая истощенный материал и выливая из него оставшийся извлекатель, который может содержать еще ничтожное количество лекарственных веществ. Если извлекатель недорогой, то его сразу спускают в канализацию. Ценный же извлекатель, например спирт или водно-спиртовую смесь, через краны 19, 25 и 32 спускают в бак В, а затем перекачивают в бак А и используют вместо чистого извлекателя. При экстрагировании сырья ценным извлекателем его необходимо возможно полнее регенерировать из отходов.Слайд 17Виды экстрагирования
Ж) Экстракция сжиженными газами(низкотемпературная экстракция).Экстракция сжиженными газами – один
из новейших и перспективных способов экстракции материала, содержащего летучие и
неустойчивые вещества, такие как эфирные масла, сердечные гликозиды, фитонциды, растительные гормоны и т.п. При использовании в качестве экстрагента сжиженных бутана, бутанпропана, азота, аммиака, углекислоты, фреонов, аргона и др., имеющих температуру кипения ниже комнатной, окисления, разложения и потери ценных веществ и их свойства при выпаривании не будет, т.к. эти экстрагенты улетучиваются при комнатной температуре. Преимущества метода:1)выход биологически активных веществ в полученном концентрате составляет 95-98% от их содержания в исходном сырье ;
2)вместе с маслом извлекают все жирорастворимые витамины, каратиноиды, токоферолы, хлорофиллы, фитостерины, эфирные масла, кумарины, активные комплексы макро- и микроэлементов и др. биологически активные вещества, которые не всегда попадают в растительные масла при холодном и горячем отжиме;
3)растительные экстракты, полученные по технологии низкотемпературной экстракции, обладают как высокими питательными, так и значительными лечебными свойствами;
4)сухой остаток из растительного сырья, подвергнутого низкотемпературной экстракции, представляет собой ценнейший продукт, содержащий очищенную клетчатку растительную, водорастворимые витамины, полисахариды, пектины, минеральные комплексы и слизеобразующие вещества.
Слайд 18Интенсификация процессов экстрагирования
А)Применение ультразвука. Ультразвуковой способ экстрагирования позволяет значительно сократить
длительность процесса и обеспечить более полное извлечение веществ. При воздействии ультразвуковых
волн нарушается пограничный диффузионный слой, улучшается проникновение экстрагента в материал. В результате сырьё набухает гораздо быстрее, возникают турбулентные и вихревые потоки, способствующие переносу масс, растворению веществ. Происходит интенсивное перемешивание содержимого даже внутри клетки (чего невозможно достичь другими способами экстракции). Всё это приводит к значительному ускорению процесса перехода действующих веществ из сырья в экстрагент.Слайд 19Интенсификация процессов экстрагирования
Б) Применение электрических зарядов. Ускорение процесса экстрагирования лекарственного
сырья может быть достигнуто применением электроимпульсивных разрядов в специальной установке.
Внутри экстрактора с обрабатываемым материалом помещают электроды, к которым поступает импульсивный ток высокой или ультравысокой частоты. Под воздействием электрического разряда в экстрагируемой смеси возникают ударные волны, создающие высокое импульсивное давление. Происходит интенсивное перемешивание обрабатываемой смеси, истончается или полностью исчезает диффузионный пристенный слой и возрастает коэффициент конвективной диффузии. Возникновение ударных волн способствует проникновению экстрагента внутрь клетки. Создаются условия для быстрого протекания внутриклеточной диффузии. В результате искрового разряда в жидкости образуются плазменные каверны, расширяясь, они достигают максимального объема и захлопываются. При этом за короткий промежуток времени в малом пространстве выделяется большое количество энергии и происходит микро взрыв, разрывающий клеточные структуры растительного материала. Процесс ускоряется за счет вымывания экстрактивных веществ из разрушенных клеток. Кроме того, образовавшиеся полости за время своего существования постоянно пульсируют, вызывая увеличение скорости движения жидкости около частиц сырья и ускоряя процесс экстрагирования за счет увеличения коэффициента конвективной диффузии.Импульсивная обработка материала с помощью высоковольтных разрядов имеет ряд преимуществ и достоинств, заключающихся в том, что электрическая |энергия непосредственно преобразуется в энергию колебательного движения жидкости. Возникающие в жидкости акустические колебания широкого спектра частот и амплитуд значительно сокращают время процесса экстрагирования и повышают выход биологически активных веществ.
Слайд 20Интенсификация процессов экстрагирования
В) Применение электроплазмолиса. Электроплазмолиз — обработка сырья электрическим током
низкой и высокой частоты. Электроплазмолиз перспективен при получении препаратов из
свежего растительного и животного сырья. Сущность метода заключается в разрушающем воздействии тока на белково-липоидные мембраны растительных тканей с сохранением целостности клеточных оболочек. При этом увеличивается выход сока, обогащенного действующими веществами и содержащего лишь небольшое количество сопутствующих веществ. Процесс проводят в специальных устройствах — электроплазмолизаторах, снабженных подвижными и неподвижными электродами.Слайд 21Интенсификация процессов экстрагирования
Применение электродиализа. Ускорение процесса экстрагирования растительного и животного
сырья может быть достигнуто при обработке его по принципу электродиализа. Движущей
силой процесса в данном случае является разность концентраций экстрагируемых веществ по обе стороны полупроницаемой перегородки, роль которой в материале, имеющем клеточную структуру, выполняют оболочки клеток. Под действием электрического тока изменяются электрические потенциалы поверхности материала, улучшается его смачиваемость, ускоряется движение ионов биологически активных веществ в полости клеток и в капиллярах клеточных оболочек. Вследствие этого увеличивается коэффициент внутренней диффузии.Слайд 22Перегонка с водяным паром
1)Гидродистилляция. Простейший вариант заключается в отгонке воды в
присутствии растительного материала. В промышленности применяется достаточно редко, например, при
получении розового масла. Часто используется в лабораторных и домашних условиях. В зависимости от давления гидродистилляцию проводят при нормальном давлении (наиболее часто) или в вакууме (вакуумная гидродистилляция - отгонка с паром при пониженном давлении). Есть предложения проводить гидродистилляцию при повышенном давлении до нескольких атмосфер, что существенно улучшает соотношение в дистилляте воды и отгоняющегося с ней вещества. Повышенная температура, необходимая для закипания воды способствует более быстрой отгонке. Выделенное таким образом масло несколько отличается от показателей масла, выделенного традиционным путем.Слайд 23Перегонка с водяным паром
2)Паровая дистилляция. Наиболее экономичный и технологически удобный
способ отгонки заключается в использовании перегретого пара (пара высокого давления).
При этом удается избежать местных перегревов растительного материала, наступающих при гидродистилляции и отогнать труднолетучие, часто весьма ценные компоненты эфирного масла. Таким методом получают преобладающее количество коммерческого эфирного масла.Образующийся пар увлекает с собой летучие компоненты эфирного масла. Пар охлаждают проточной водой, и жидкая смесь воды и эфирного масла расслаивается в приемнике. Устройство приемника зависит от удельного веса масла. Если масло легче воды, оно всплывает вверх, а вода удаляется через боковую трубку. Если масло тяжелее, то оно собирается на дне приемника, а избыток воды сливается через отверстие верхней части.
Слайд 242)Паровая дистилляция схема
Схема установки для паровой дистилляции:
1. Вход внутреннего пара
2.
Вход внешнего пара для нагрева воды
3. Выход внешнего пара
4. Сброс
воды5 и 6. Вход и выход охлаждающей воды
7. Выход эфирного масла
А. Емкость для растительного материала и воды
B. Отводной патрубок с изоляцией
C. Трубчатый конденсатор для охлаждения водно-паровой смеси
D. Склянка для сбора эфирного масла
E. Трубка для обратной дистилляционной воды
Слайд 25Перегонка с водяным паром
Деструктивная дистилляция. Иногда для получения эфирного масла
различные древесные материалы подвергают нагреванию в вакууме. При этом компоненты
аромата улетучиваются, часть древесины разрушается и образуются ряд фенольных соединений, которые придают полученному эфирному маслу запах «выделанной кожи». Такое эфирное масло обладает рядом целебных свойств, оно также применяется в парфюмерии при изготовлении духов для мужчин.Слайд 26Основные методы очистки БАВ
1)Диализ. Диализ — освобождение коллоидных растворов и растворов высокомолекулярных веществ
от растворённых в них низкомолекулярных соединений при помощи полупроницаемой мембраны. При
диализе молекулы растворенного низкомолекулярного вещества проходят через мембрану, а неспособные диализировать (проходить через мембрану) коллоидные частицы остаются за ней. Простейший диализатор представляет собой мешочек из коллодия(полупроницаемого материала), в котором находится диализируемая жидкость. Мешочек погружают в растворитель (например в воду). Постепенно концентрации диализирующего вещества в диализируемой жидкости и в растворителе становятся равными. Меняя растворитель, можно добиться практически полной очистки от нежелательных примесей. Скорость диализа обычно крайне низка (недели). Ускоряют процесс диализа увеличивая площадь мембраны и температуру, непрерывно меняя растворитель. Процесс диализа основан на процессах осмоса и диффузии, что объясняет способы его ускорения.Диализ применяют для очистки коллоидных растворов от примесей электролитов и низкомолекулярных неэлектролитов. Диализ применяют в промышленности для очистки различных веществ, например в производстве искусственных волокон, при изготовлении лекарственных веществ. Материал, прошедший через мембрану, называется диализат.
Слайд 27Основные методы очистки БАВ
2) Обратный осмос. Обратный осмос — процесс, в
котором с помощью давления принуждают растворитель (обычно вода) проходить черезполупроницаемую мембрану из более концентрированного в менее концентрированный раствор,
то есть в обратном для осмоса направлении. При этом мембрана пропускает растворитель, но не пропускает некоторые растворённые в нём вещества. Обратный осмос более экономичный процесс для повышения концентраций пищевых жидкостей, например фруктовых соков, чем термические процессы. Преимущество заключаются в низкой стоимости эксплуатации и возможности избежать термической обработки, что делает процесс пригодным для термочувствительных веществ, таких как белки и ферменты, в большинстве пищевых продуктов. Обратный осмос широко используется в молочной промышленности для производства порошков сывороточного белка и для концентрации молока — уменьшаются транспортные расходы.Слайд 28Основные методы очистки БАВ
3) Микрофильтрация(МФ). Микрофильтрация позволяет удалять частицы в
диапазоне приблизительно 0,1-1 мкм. В целом, взвешенные частицы и крупные
коллоидные частицы задерживаются, в тоже время макромолекулы и растворенные твёрдые частицы проходят через МФ мембрану. МФ применяется для удаления бактерий, хлопьевидных материалов или общей взвеси. Рабочее давление обычно составляет около 0.7 бар.Слайд 29Основные методы очистки БАВ
4) Ультрафильтрация(УФ). Ультрафильтрация позволяет удалять частицы в
диапазоне приблизительно от 20 до 1000 Ангстрем (до 0.1 мкм).
Все растворенные соли и более мелкие молекулы проходят через мембрану. Вещества, задерживаемые мембраной, включают коллоиды, белки, микробиологические загрязнения и крупные органические молекулы. Большая часть УФ мембран имеет рейтинг по молекулярной массе между 1000 и 100 000 Ангстрем. Рабочее давление обычно составляет около 1- 7 бар.Слайд 30Основные методы очистки БАВ
5) Нанофильтрация(НФ).Нанофильтрация позволяет удалять частицы в размером
в нанометры, отсюда и термин "нанофильтрация". Нанофильтрация представляет собой средний
процесс между ультрафильтрацией и обратным осмосом. Молекулы органических веществ с молекулярной массой 200-400 задерживаются. Кроме того, задерживаются растворенные соли на 20-98%. Соли, содержащие одновалентные ионы (например, хлорид натрия или кальция), задерживаются на 20-80%, в то время как соли с двухвалентными анионами (например, сульфат магния), задерживаются в большей степени (90-98%). НФ используется для удаления цветности и общего органического углерода из поверхностных вод, удаления жёсткости или радия из артезианской воды, общего снижения содержания растворенных веществ. Рабочее давление обычно составляет около 3.5 - 16 бар.Слайд 31Основные методы очистки БАВ
6) Сорбция. Сорбция — поглощение твёрдым телом
либо жидкостью различных веществ из окружающей среды. Поглощаемое вещество, находящееся
в среде, называют сорбатом (сорбтивом), поглощающее твёрдое тело или жидкость — сорбентом.Слайд 32Основные методы очистки БАВ
7) Адсорбционно - хроматографический медод – это
метод разделения и определения веществ, основанный на распределении компонентов между
двумя фазами – подвижной и неподвижной. Неподвижной (стационарной) фазой служит твердое пористое вещество (часто его называют сорбентом) или пленка жидкости, нанесенная на твердое вещество. Подвижная фаза представляетсобой жидкость или газ, протекающий через неподвижную фазу, иногда
под давлением.
Компоненты анализируемой смеси (сорбаты) вместе с подвижной
фазой передвигаются вдоль стационарной фазы. Ее обычно помещают в
стеклянную или металлическую трубку, называемую колонкой. В зависимости от силы взаимодействия с поверхностью сорбента (за счет адсорбции или по какому-либо другому механизму) компоненты будут перемещаться вдоль колонки с разной скоростью. Одни компоненты останутся в верхнем слое сорбента, другие, в меньшей степени взаимодействующие с сорбентом, окажутся в нижней части колонки, а некоторые и вовсе покинут колонку вместе с подвижной фазой (такие компоненты называются неудерживаемыми, а время их удерживания определяет “мертвое время” колонки).
Таким образом происходит быстрое разделение сложных смесей компонентов. Следует подчеркнуть следующие достоинcтва хроматографических методов:
1. Разделение носит динамический характер, причем акты сорбции-
десорбции разделяемых компонентов повторяются многократно. Этим
обусловлена значительно большая эффективность хроматографического
разделения по сравнению со статическими методами сорбции и
экстракции.
2. При разделении используют различные типы взаимодействия
сорбатов и неподвижной фазы: от чисто физических до хемосорбционных.
Это обуславливает возможность селективного разделения широкого круга
веществ.
3. На разделяемые вещества можно накладывать различные
дополнительные поля (гравитационное, электрическое, магнитное и др.),
которые, изменяя условия разделения, расширяют возможности
хроматографии.
4. Хроматография – гибридный метод, сочетающий одновременное
разделение и определения нескольких компонентов.
Слайд 33Основные методы очистки БАВ
8) Гель-фильтрация. Гель-фильтрация – разделение веществ при
помощи гелей, основанное на различиях в размере молекул. Наиболее часто
для этой цели применяют органические полимеры с трехмерной сетчатой структурой, придающей им свойства гелей.Слайд 34Основные методы очистки БАВ
9) Гидрофобная хроматография - жидкостная хроматография на неполярных
сорбентах, в которой п качестве подвижной фазы используются водные или
водно-органические буферные растворы и разделение смеси веществ происходит в результате различия в их взаимодействии с гидрофобными группами сорбента в условиях убывающего градиента солей в элюенте.Слайд 35Основные методы очистки БАВ
10) Аффинная хроматография — разновидность лигандной. В основе последней
лежит реакция взаимодействия разделяемых примесей с лигандом, связанным с инертным носителем. В
случае аффинной хроматографии в роли примесей выступают биологически активные вещества (белки, ферменты), вступающие с лигандом (тоже, как правило, органическим ) в специфическое биохимическое взаимодействие. Например: антитело-антиген, гормон-рецептор и т. д. Именно высокая специфичность подобного взаимодействия обуславливает высокую эффективность аффинной хроматографии и её широкое (по сравнению с другими видами лигандной хроматографии) распространение.Слайд 36Основные методы идентификации БАВ
1)Определение вещества по его физическим константам.
Каждое биологически
активное вещество характеризуется постоянными физическими свойствами в определенных условиях (температура
и давление).Основные физические свойства:
1) Температура плавления
2) Температура кипения
3) Показатель преломления
4) Удельное вращение
5) Плотность
6) Вязкость
7) Ультрафиолетовый спектр
8) Инфракрасный спектр
9) Протонно магнитный резонанс
Но этот способ не особо точен так как далеко не для всех соединений описаны константы , два разных вещества могут иметь одинаковую константу и к тому же вероятность совпадения констант приблизительно равна 2%.
Слайд 37Основные методы идентификации БАВ
2)Определение вещества по спектрам, цветным реакциям и
некоторым особенностям химического поведения.
Этот метод также не особо широко используется
так как не все вещества имеют отличные химические свойства или специфические реакции.Слайд 38Основные методы идентификации БАВ
3)Хромотаграфия
Это способ анализа веществ, основанных на их физическом
разделения. Например, при хроматографии на бумаге вещества двигаются по хроматограмме с током растворителя с
различными скоростями, индивидуальными и характерными для данного вещества в данных условиях. Последняя оговорка весьма существенна: в разных лабораториях и в разных руках точно воспроизвести абсолютные скорости – их называют хроматографическими подвижностями – весьма и весьма трудно. Поэтому здесь не обойтись литературными данными – нужно прямое сравнение двух образцов.Огромное достоинство хроматографических методов в том, что они позволяют работать с очень малыми количествами вещества(например, порядка микрограмма) и, что еще важнее, позволяют идентифицировать не только мало очищенные вещества, но даже вещества, присутствующие в качестве компонентов сложных смесей. Последнее особенно существенно для разбираемой нами задачи, так как, например гидролизат полисахарида может содержать несколько разных моносахаридов. И хроматография позволяет идентифицировать их без предварительного разделения.
Конечно, и хроматографические методы могут дать осечку: подвижности разных веществ могут и случайно совпасть. Однако хроматография – это очень гибкий метод. Можно использовать набор разных условий для анализа одной и той же пары веществ ,а совпадение подвижностей в нескольких различных условиях – это уже событие, вероятность которого ничтожно мала.
Слайд 39Основные методы идентификации БАВ
4) Применение ферментов
Можно воспользоваться ферментом катализирующим ту
или иную реакцию для определения вещества. Например можно определить D-
или L-галактозу мы имеем.Слайд 40Основные методы идентификации БАВ
5)Спектроскопия - разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения
(в том числе, электромагнитного излучения, акустических волн и др.) с веществом. В физике спектроскопические методы используются
для изучения всевозможных свойств этих взаимодействий. В аналитической химии — для обнаружения и определения веществ при помощи измерения их характеристических спектров, то есть методами спектрометрии. К существенным преимуществам спектроскопии можно отнести возможность диагностики in situ, то есть непосредственно в «среде обитания» объекта, бесконтактно, дистанционно, без какой-либо специальной подготовки объекта.Слайд 41Виды спектроскопии
А) Микроволновая спектроскопия - методика определения геометрического строения молекул
по микроволновым спектрам, обусловленным переходами между вращательными энергетическими уровнями. Определение таких
параметров молекул, как дипольный момент и момент инерции относительно главных осей методом микроволновой спектроскопии производится в подавляющем большинстве случаев путем анализа спектров поглощения электромагнитного излучения в диапазоне 10–40 ГГц, обусловленных переходами молекулы с одного вращательного энергетического уровня на другой. Метод микроволновой спектроскопии является очень точным для сравнительно простых молекул, но с ростом молекулярной массы на точность метода начинает влиять колебательно-вращательное взаимодействие. С помощью этого метода были определены с высокой точностью геометрические параметры многих двух-, трех- и четырехатомных молекул, а также был исследован такой интересный эффект, как инверсия. Метод плохо применим для неполярных молекул и используется для исследования веществ только в газовой фазе.Слайд 42Виды спектроскопии
Б) Инфракрасная спектроскопия (ИКС) — раздел спектроскопии, охватывающий длинноволновую область спектра
(>730 нм за красной границей видимого света). Инфракрасные спектры возникают в
результате колебательного (отчасти вращательного) движения молекул, а именно — в результате переходов между колебательными уровнями основного электронного состояния молекул. ИК излучение поглощают многие газы, за исключением таких как О2, N2, H2, Cl2 и одноатомных газов. Поглощение происходит на длине волны, характерной для каждого определенного газа, для СО, например, таковой является длина волны 4,7 мкм.По инфракрасным спектрам поглощения можно установить строение молекул различных органических (и неорганических) веществ с относительно короткими молекулами : антибиотиков, ферментов, алкалоидов, полимеров, комплексных соединений и др. Колебательные спектры молекул различных органических (и неорганических) веществ с относительно длинными молекулами (белки, жиры, углеводы, ДНК, РНК и др.) находятся в терагерцовом диапазоне, поэтому строение этих молекул можно установить с помощью радиочастотных спектрометров терагерцового диапазона. По числу и положению пиков в ИК спектрах поглощения можно судить о природе вещества (качественный анализ), а по интенсивности полос поглощения — о количестве вещества (количественный анализ). Основные приборы — различного типа инфракрасные спектрометры.
Слайд 43Виды спектроскопии
В) Ультрафиолетовая (электронная) спектроскопия — раздел оптической спектроскопии, который включает получение,
исследование и применение спектров испускания, поглощения и отражения в ультрафиолетовой области.
Энергия фотонов ультрафиолетового и видимого
диапазонов спектра достаточно высока (1,7—100 эВ или примерно от 10 до 730 нм) , чтобы перевести электроны органических молекул из основного состояния в возбужденное — со связывающей на разрыхляющие орбитали. Разность энергий между этими состояниями квантована, поэтому молекулы поглощают фотоны только строго определенной энергии.В УФ-области поглощают все органические вещества. Как правило, «рабочая» область составляет интервал 190—730 нм, главным образом от 200 до 380 нм. В этих областях прозрачны оптические материалы для изготовления призм и кювет. Длины волн менее 190 нм (вакуумный ультрафиолет) менее удобен для работы, так как в этой поглощают компоненты воздуха — кислород и азот. Поэтому для работы в этой области используются специальные вакуумные камеры, что усложняет лабораторную практику, однако часто бывает незаменимым, например, при исследовании диэлектриков с большой величиной запрещенной зоны.
Необходимые для исследования количества вещества невелики — около 0,1 мг. В связи с этим УФ-спектроскопия является одним из наиболее распространенных физико-химических методов исследования органических и неорганических соединений.
Слайд 44Виды спектроскопии
Г) РЕНТГЕНОВСКАЯ спектроскопия, раздел спектроскопии, изучающий спектры испускания (эмиссионные) и поглощения
(абсорбционные) рентгеновского излучения, т.е. электромагн. излучения в области длин волн
10-2-102 нм. Рентгеновскую спектроскопию используют для изучения природы хим. связей и количественного анализа в-в (рентгеновский спектральный анализ). С помощью рентгеновской спектроскопии можно исследовать все элементы (начиная с Li) с соединений, находящихся в любом агрегатном состоянии.Рентгеновские спектры обусловлены переходами электронов внутренних оболочек атомов. Различают тормозное и характеристическое рентгеновское излучение. Первое возникает при торможении заряженных частиц (электронов), бомбардирующих мишень в рентгеновских трубках, и имеет сплошной спектр. Характеристическое излучение испускают атомы мишени при столкновении с электронами (первичное излучение) или с рентгеновскими фотонами (вторичное, или флуоресцентное, излучение). В результате этих столкновений с одной из внутр. (К-, L- или М-) оболочек атома вылетает электрон и образуется вакансия, к-рую заполняет электрон с другой (внутр. или внеш.) оболочки. При этом атом испускает квант рентгеновского излучения.