Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Средняя кинетическая энергия хаотичного поступательного движения молекул газа
Содержание
- 1. Средняя кинетическая энергия хаотичного поступательного движения молекул газа
- 2. Зависимость давления от концентрации и температурыКонцентрация молекул
- 3. Наиболее вероятнаяСредняя арифметическаяСредняя квадратичнаяРаспределение молекул газа по
- 4. Вывод уравнения состояния идеального газаУниверсальная газовая постояннаяУравнение Менделеева-Клапейрона
- 5. если m=const и M=const, то …Уравнение КлапейронаГазовый
- 6. Соотношение было открыто в 1662 г. Робертом
- 7. Дыхание можно объяснить так: межреберные мышцы и
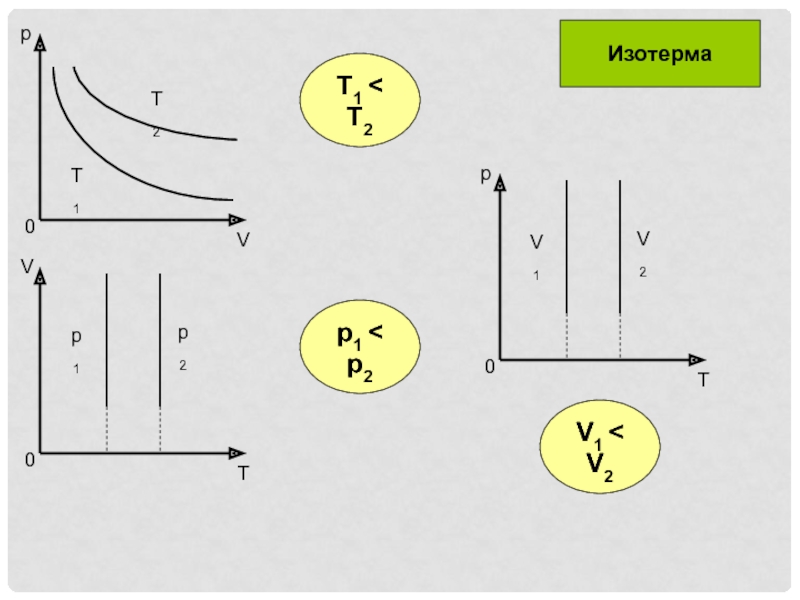
- 8. T1 < T2p1 < p2V1 < V2Изотерма
- 9. Равновесное состояние - состояние, при котором температура
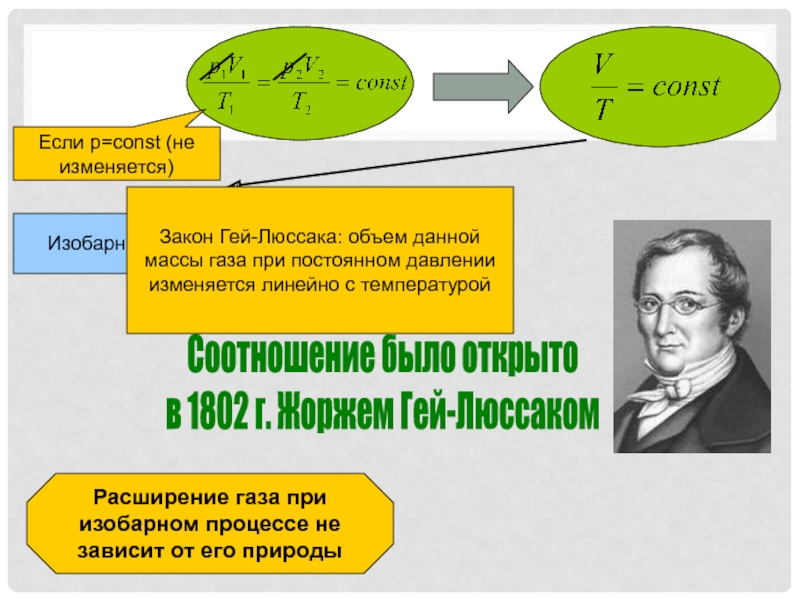
- 10. Соотношение было открыто в 1802 г. Жоржем
- 11. T1 < T2p1 < p2V1 < V2ИзобараВ
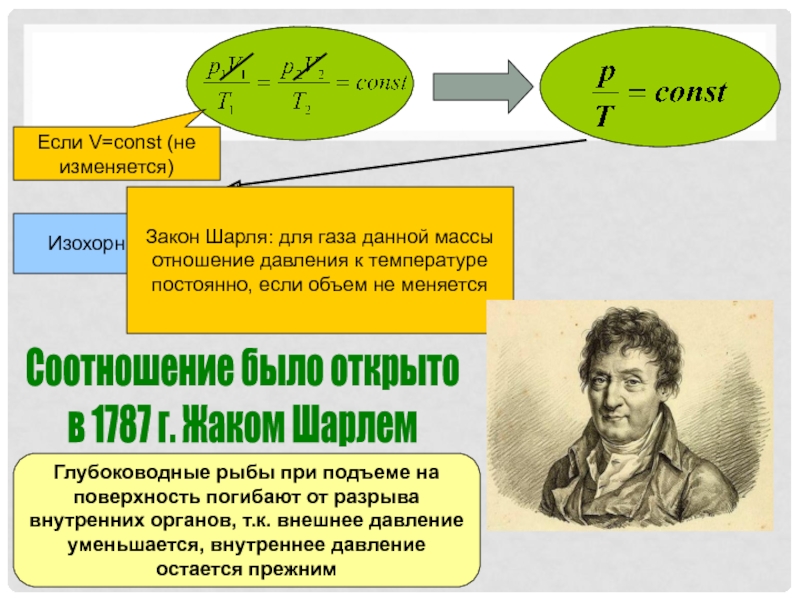
- 12. Соотношение было открыто в 1787 г. Жаком
- 13. T1 < T2p1 < p2V1 < V2ИзохораДавление идеального газа при абсолютном нуле равно 0
- 14. Слайд 14
- 15. Скачать презентанцию
Зависимость давления от концентрации и температурыКонцентрация молекул – число молекул в 1 м3k = 1,38*10-23 Дж/КПостоянная Больцмана
Слайды и текст этой презентации
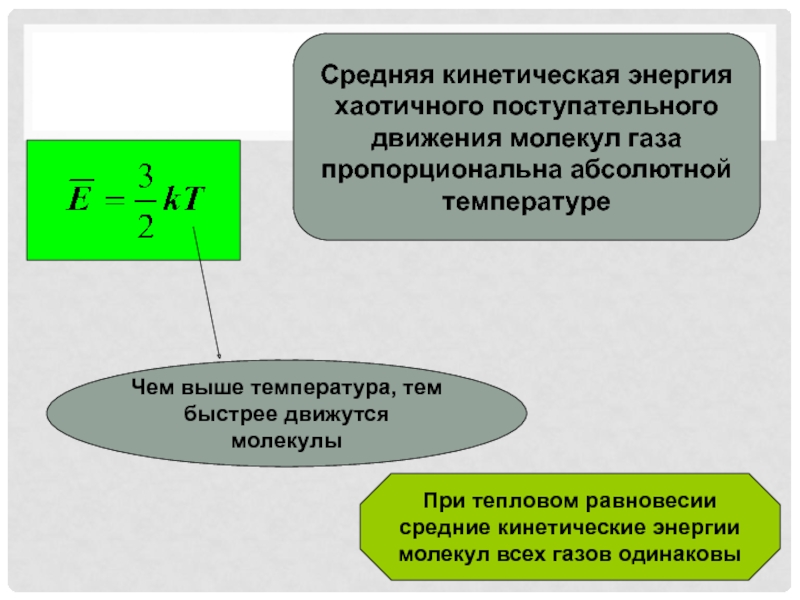
Слайд 1Средняя кинетическая энергия хаотичного поступательного движения молекул газа пропорциональна абсолютной
температуре
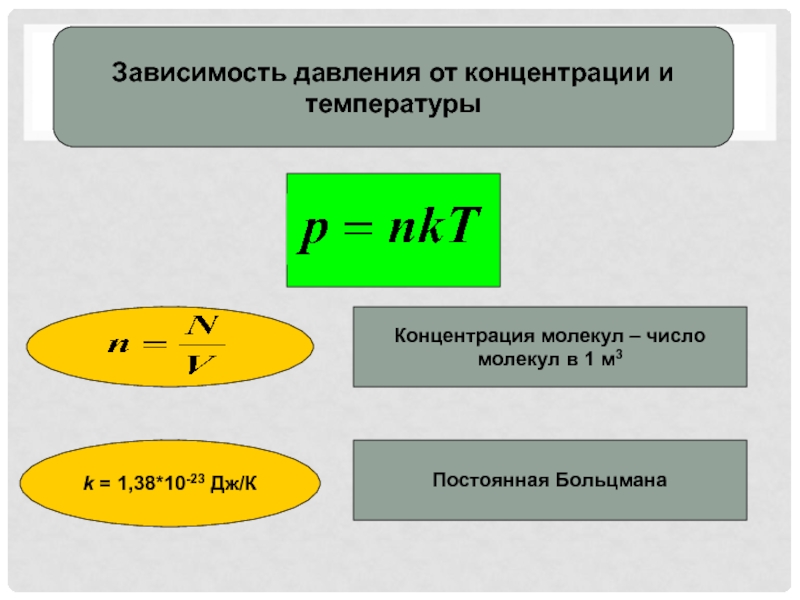
Слайд 2Зависимость давления от концентрации и температуры
Концентрация молекул – число молекул
в 1 м3
k = 1,38*10-23 Дж/К
Постоянная Больцмана
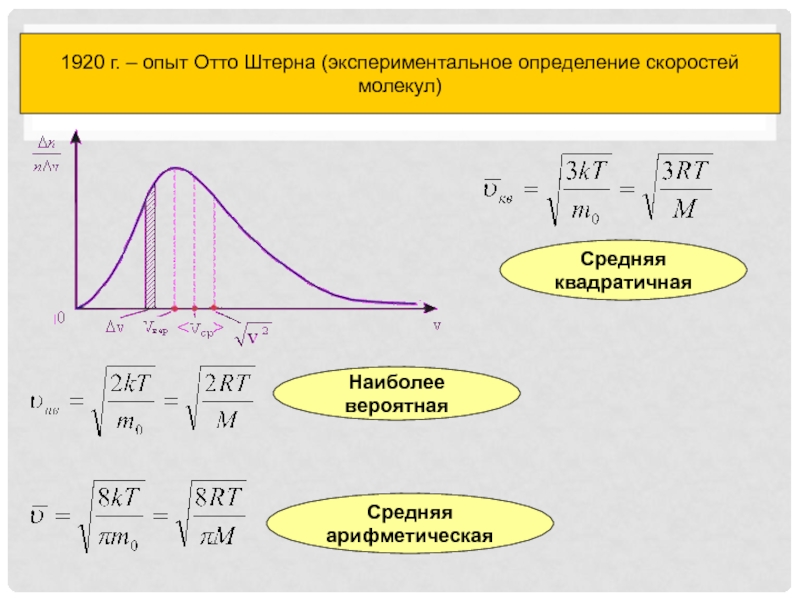
Слайд 3Наиболее вероятная
Средняя арифметическая
Средняя квадратичная
Распределение молекул газа по скоростям
1920 г. –
опыт Отто Штерна (экспериментальное определение скоростей молекул)
Слайд 4Вывод уравнения состояния идеального газа
Универсальная газовая постоянная
Уравнение Менделеева-Клапейрона
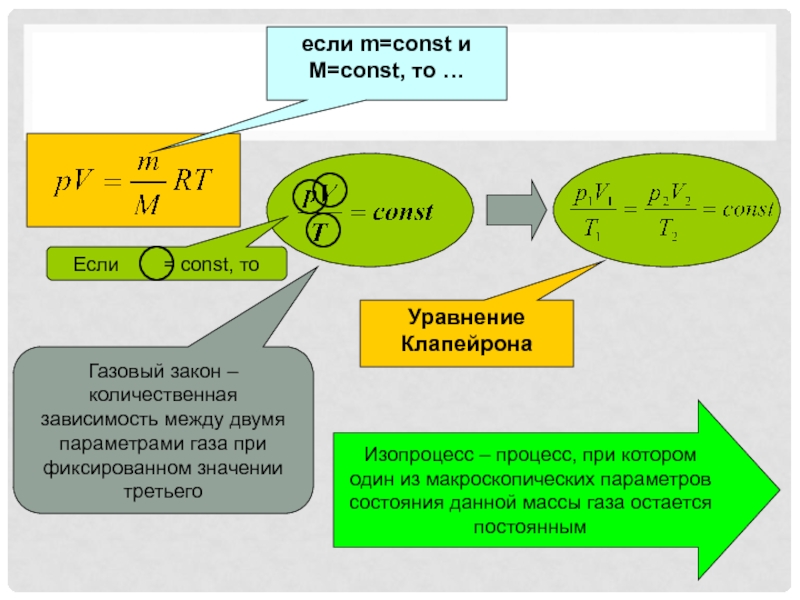
Слайд 5если m=const и M=const, то …
Уравнение Клапейрона
Газовый закон – количественная
зависимость между двумя параметрами газа при фиксированном значении третьего
Изопроцесс –
процесс, при котором один из макроскопических параметров состояния данной массы газа остается постояннымСлайд 6Соотношение было открыто
в 1662 г. Робертом Бойлем
Переоткрыто в 1676
г. Эдмоном Мариоттом
Если T=const (не изменяется)
Изотермический процесс
При изотермическом процессе плотность
газа изменяется прямо пропорционально давлениюСлайд 7Дыхание можно объяснить так: межреберные мышцы и диафрагма изменяют объем
грудной клетки. При ее расширении давление воздуха в легких уменьшается
и за счет перепада давления происходит вдохУвеличение объема пузырьков воздуха, когда они поднимаются в воде объясняется так: на глубине давление жидкости больше, чем у поверхности воды