Слайд 1Төмен молекулалық биологиялық заттар
Лектор: х.ғ.д., профессор Шоинбекова
Сабина Алимжановна
Слайд 2
1 дәріс. Кіріспе. Төменмолекулалық биологиялық қосылыстар. Түрлері, топтастыруы, негізгі кластары.
Химиялық байланыстар.
Табиғи биологиялық белсенді қосылыстар.
Органикалық қосылыстардың классификациясы;
Функционалды топтар, түрлері;
Химиялық
байланыстар;
Индуктивті және мезомерлі эффекттер.
Слайд 3«Төмен молекулалы биологиялық заттар» - ол тірі организмнің құрамындағы заттардың
құрамын, құрылысын, қасиеттерін, атқаратын қызметтерін, құбылыстарын зерттейтін пән.
«Төмен
молекулалы биологиялық заттар» органикалық химияның теориялық негіздерімен, биологиямен (биохимия, физиология) және физикамен (физикалық химия, биофизика) тығыз байланысты.
Слайд 4Органикалық химия органикалық қосылыстардың алу әдістерін, құрамын, құрылысын, қасиеттерін, құбылыстары
мен ыдырауын зерттейді.
Бұл терминді швед химигі Й.Я. Берцелиус 1808 жылы
енгізген, тарихи аты осы күнге дейін қолданылады (карбидтер, карбонаттар, оксидтер, СО2-бейорг. қос-р).
Слайд 5Органикалық химияның дамуы
Органикалық қосылыстардың ерекшеліктері:
Изомерия;
Молекулалардың конформациясы;
Органикалық қосылыстардың алуантүрлілігі және күрделі
құрылысы;
Молекулалардың төмен реакциялық қабілеттілігі;
Атомдардың өзара әсері және орынбасушылардың электронды эффекттері;
СС
, СН байланыстарындағы химиялық реакциялардың қайтымсыздығы;
Стериалық (кеңістік) факторлар;
Молекулаларда бос радикалды ыдырауы басымды келеді;
СС , СН байланыстардын төмен полярлығы.
Слайд 6«Төмен молекулалық биологиялық қосылыстар» органикалық химия пәнімен тікелей байланысты.
«Органикалық химия
адамды ақыл есінен айыра алады. Ол жұмбақ, ғажайыпқа толы, қызықтыратын
тропикалық орман секілді. Бұл сұмдық қорқынышты шексіз орманнан шығу мүмкін емес, оған кіру қорқынышты….».
Фридрих Велер (1835)
Фридрих Велер
(1800-1882)
Слайд 7Органикалық қосылыстардың құрылымдық теориясы.
Радикалдар теориясы (Л. Гей-Люссак (1815), Ф. Велер
(1832).
Типтер теориясы (Ш. Жерар, 1840-1854);
Фридрих Кекуле (1857) – көміртек –
төрт атомды.
Фридрих Август Кекуле
7. IX. 1829 – 13. VII.1896
ЖЕРАР Шарль Фредерик
(21.VIII.1816 - 19.VIII.1856)
Слайд 8Органикалық қосылыстардың құрылымдық теориясының негізгі қағидалары: (1861)
БУТЛЕРОВ
Александр Михайлович
3(15) қыркүйек 1828
ж. –
5(17) тамыз 1886 ж.
Слайд 9Органикалық қосылыстардың құрылымдық теориясының негізгі қағидалары
1) Атомдар молекулада өздерінің валенттілігіне
сәйкес химиялық байланыстармен байланысқан;
2) Атомдар органикалық қосылыстардың молекулаларында өзара белгілі
ретпен орналасады;
3) Органикалық қосылыстардың қасиеттері молекуланың құрамына кіретін тек атомдардың санына, табиғатына ғана емес, химиялық құрылысына тәуелді;
4) Молекулада тікелей байланысқан және байланыспаған атомдар бір біріне әсер етеді;
5) Заттың химиялық құрылысы оның қасиеттерін сиппаттайды, керісінше заттың химиялық алмасуларын зерттеп, заттың химиялық құрылысын анықтауға болады.
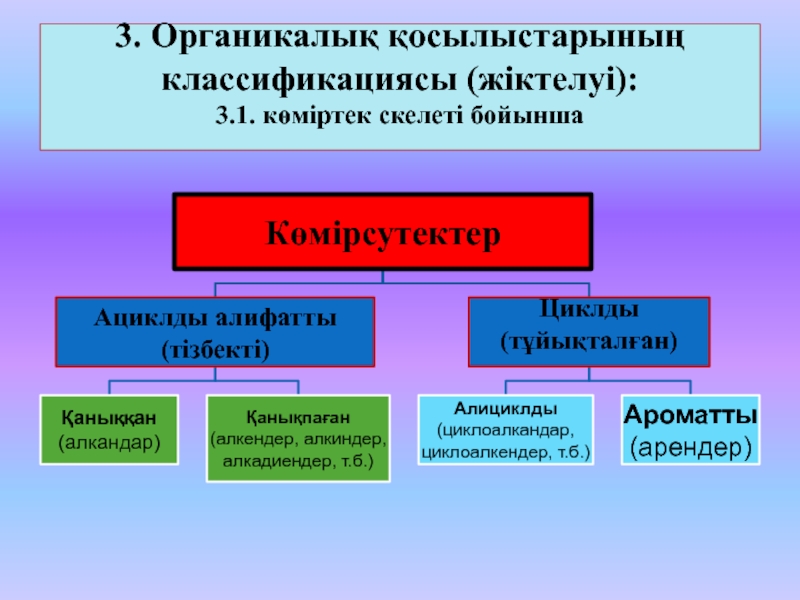
Слайд 103. Органикалық қосылыстарының классификациясы (жіктелуі):
3.1. көміртек скелеті бойынша
Слайд 11Функционалды топтар
Функционалды топтар – ол – қосылыстың химиялық қасиеттерін анықтайтын
және белгілі бір класқа жіктейтін атомдар немесе атом топтары.
Функционалды топтардың
құрамына: Н, О, N, Р, S элементтері және галогендер – олар -органогендер деп аталады.
Слайд 12
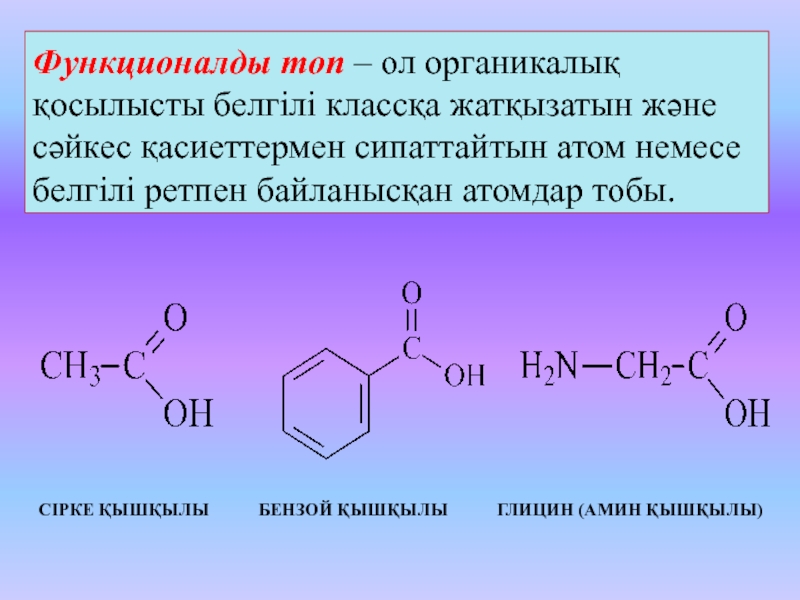
Функционалды топ – ол органикалық қосылысты белгілі классқа жатқызатын және
сәйкес қасиеттермен сипаттайтын атом немесе белгілі ретпен байланысқан атомдар тобы.
Сірке
қышқылы бензой қышқылы глицин (амин қышқылы)
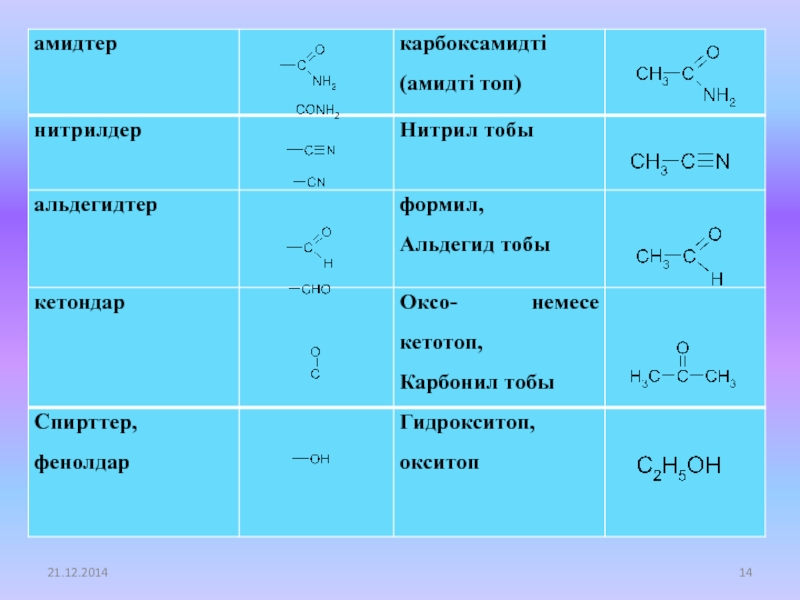
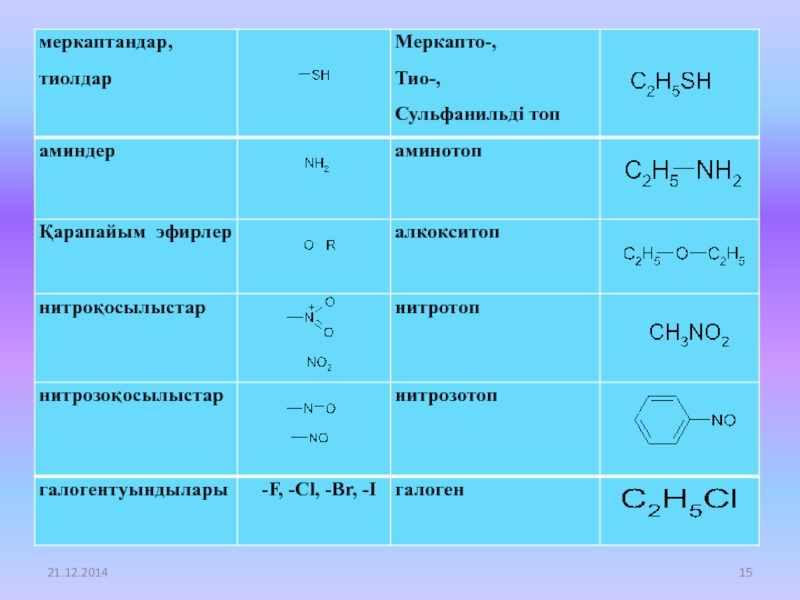
Слайд 133.2. функционалды топтары бойынша
Таблица 1. Классы органических соединений
Слайд 16Органикалық қосылыстарда бірнеше функционалды топтар болуы мүмкін:
Функционалды топтар бірдей болса,
олар полифункционалды деп аталады;
Функционалды топтар әртүрлі болса, олар гетерофункционалды қосылыстар
деп аталады.
Слайд 17
Органикалық қосылыстардағы химиялық байланыстар.
Химиялық байланыс – ол атомдар арасындағы
байланыстар. Байланыстардың түзілуінің нәтижесінде молекулалар мен кристаллдар пайда болады.
Слайд 19
Коваленттік байланыс
Коваленттік байланыс екі атомның арасындағы ортақ электрон жұбының
түзілуінің нәтижесінде пайда болады.
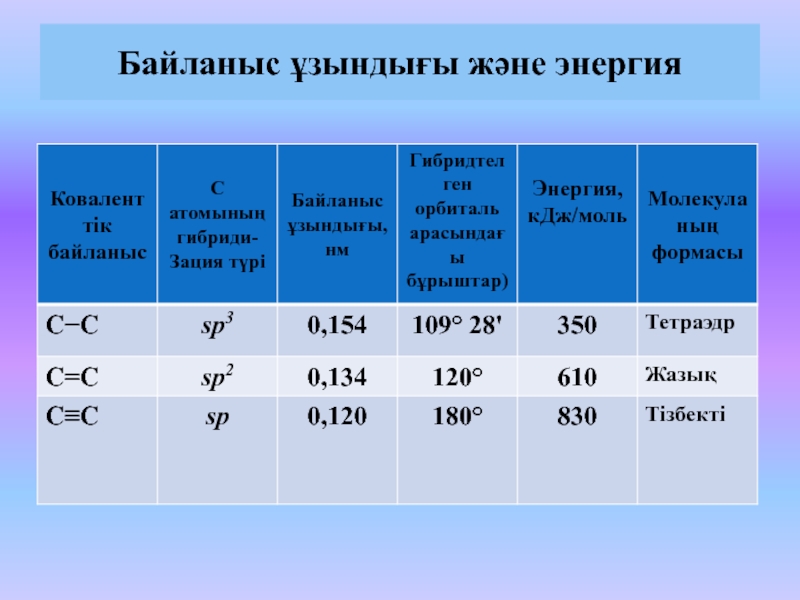
Коваленттік байланыс бірнеше параметрлермен: полярлық, байланыс,
энергиямен және кеңістіктегі бағытпен (байланыс арасындағы бұрыштар) сипатталады.
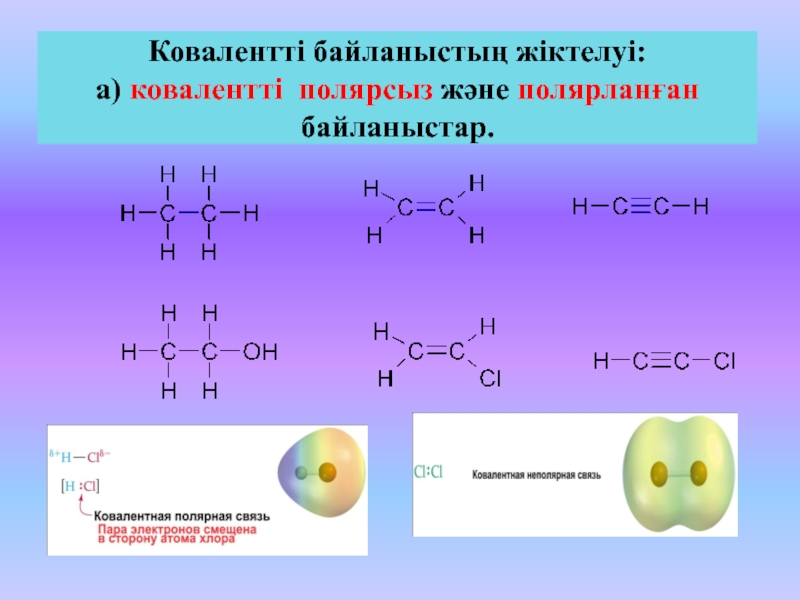
Слайд 20Ковалентті байланыстың жіктелуі:
а) ковалентті полярсыз және полярланған байланыстар.
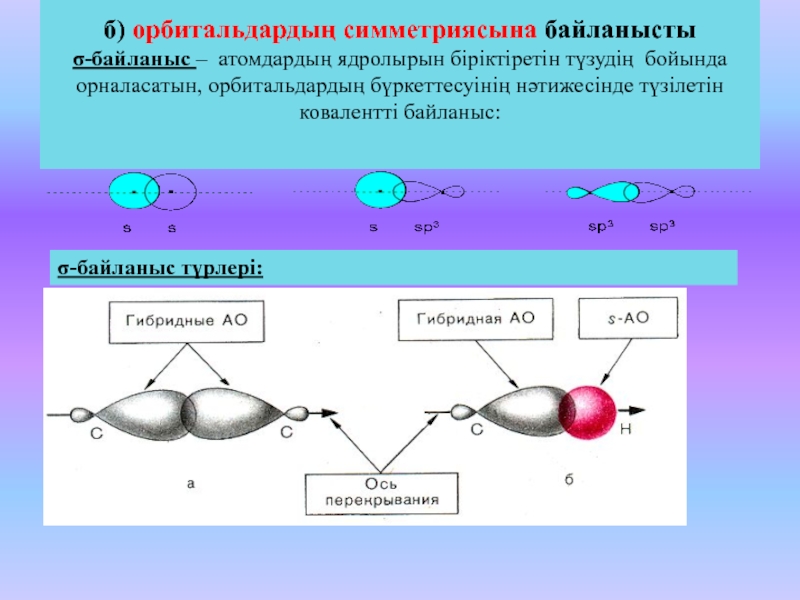
Слайд 21б) орбитальдардың симметриясына байланысты
-байланыс – атомдардың ядролырын біріктіретін түзудің бойында
орналасатын, орбитальдардың бүркеттесуінің нәтижесінде түзілетін ковалентті байланыс:
-байланыс түрлері:
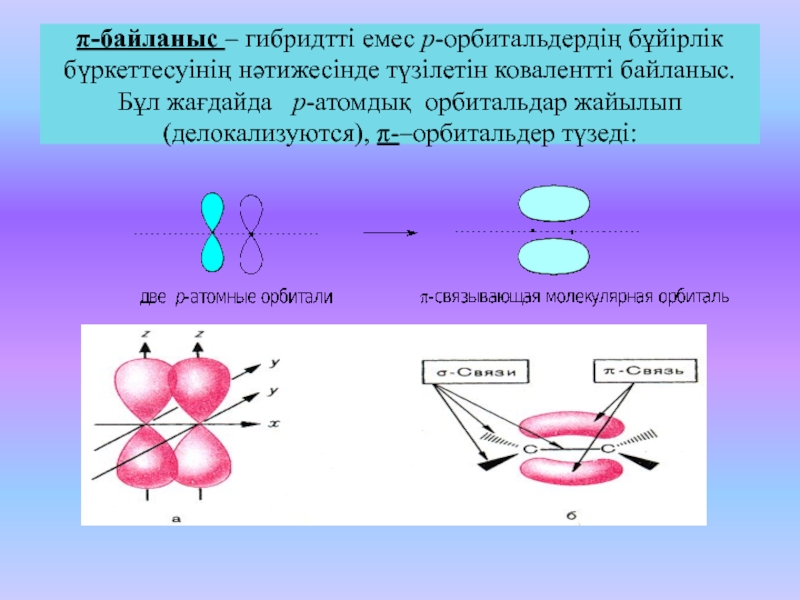
Слайд 22-байланыс – гибридтті емес p-орбитальдердің бұйірлік бүркеттесуінің нәтижесінде түзілетін ковалентті
байланыс. Бұл жағдайда p-атомдық орбитальдар жайылып (делокализуются), -–орбитальдер түзеді:
Слайд 23
Донор-акцепторлы механизм – донордың екі электроны мен акцептордың бос орбиталінің
есебінен пайда борлады.
Семиполярлы байланыс – ковалентті әрекеттесумен теріс зарядтардың тартылысының
нәтижесінде пайда болатын байланыс:
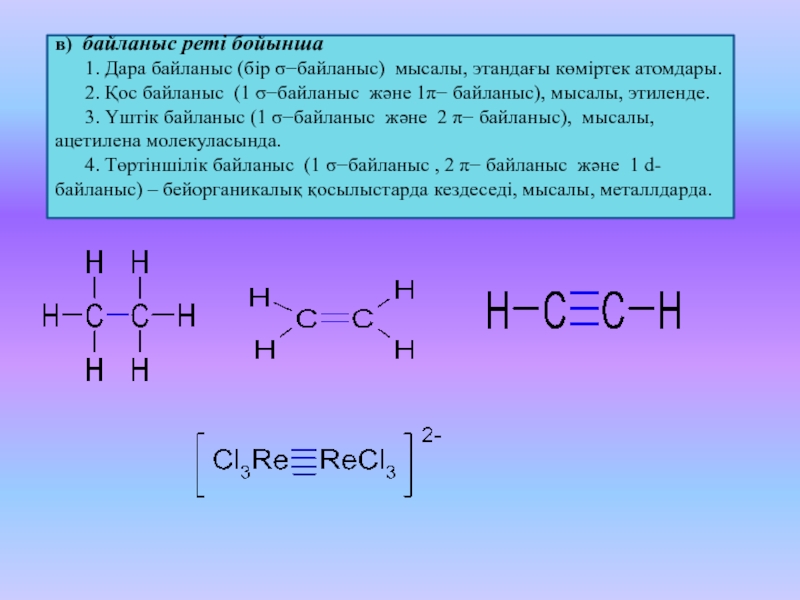
Слайд 24в) байланыс реті бойынша
1. Дара байланыс (бір
байланыс) мысалы, этандағы көміртек атомдары.
2. Қос байланыс
(1 байланыс және 1 байланыс), мысалы, этиленде.
3. Үштік байланыс (1 байланыс және 2 байланыс), мысалы, ацетилена молекуласында.
4. Төртіншілік байланыс (1 байланыс , 2 байланыс және 1 d-байланыс) – бейорганикалық қосылыстарда кездеседі, мысалы, металлдарда.
Слайд 25
Ковалентті байланыстың сипаттамалары:
Ι. Байланыс энергиясы. ΙΙ. Байланыстың ұзындығы.
ΙΙΙ.
Полярлығы. IV. Поляризациялануы.
F >O > Сl > N > Вг>
С > Н
Полярлығы:
Коваленттік байланыс поляриацияланумен сипатталады — сыртқы факторладың әсерінен полярлікті өзгерту қабілеті.
-байланыстар -байланыстарға қарағанда жылдам поляризацияланады.
Слайд 26
Көміртек атомының электронды құрылысы. Гибридизация.
Слайд 27Атомдық орбиталь — ол электронның кеңістікте орналасуының максималды ықтималдығы
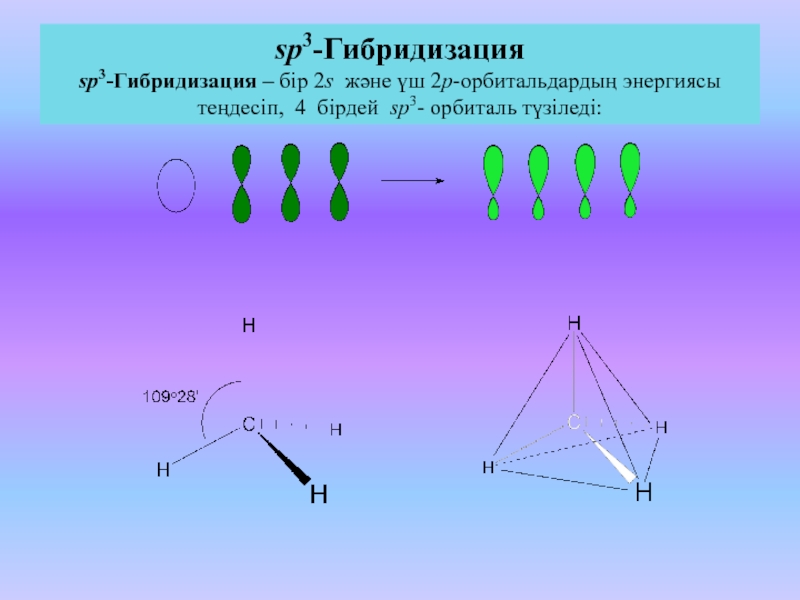
Слайд 28sp3-Гибридизация
sp3-Гибридизация – бір 2s және үш 2p-орбитальдардың энергиясы теңдесіп,
4 бірдей sp3- орбиталь түзіледі:
Слайд 29
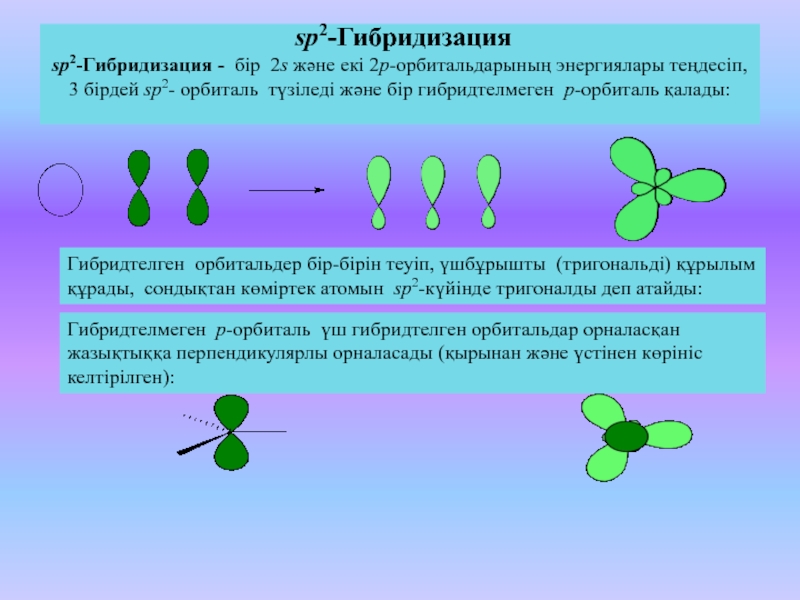
sp2-Гибридизация
sp2-Гибридизация - бір 2s және екі 2p-орбитальдарының энергиялары
теңдесіп, 3 бірдей sp2- орбиталь түзіледі және бір гибридтелмеген p-орбиталь
қалады:
Гибридтелген орбитальдер бір-бірін теуіп, үшбұрышты (тригональді) құрылым құрады, сондықтан көміртек атомын sp2-күйінде тригоналды деп атайды:
Гибридтелмеген p-орбиталь үш гибридтелген орбитальдар орналасқан жазықтыққа перпендикулярлы орналасады (қырынан және үстінен көрініс келтірілген):
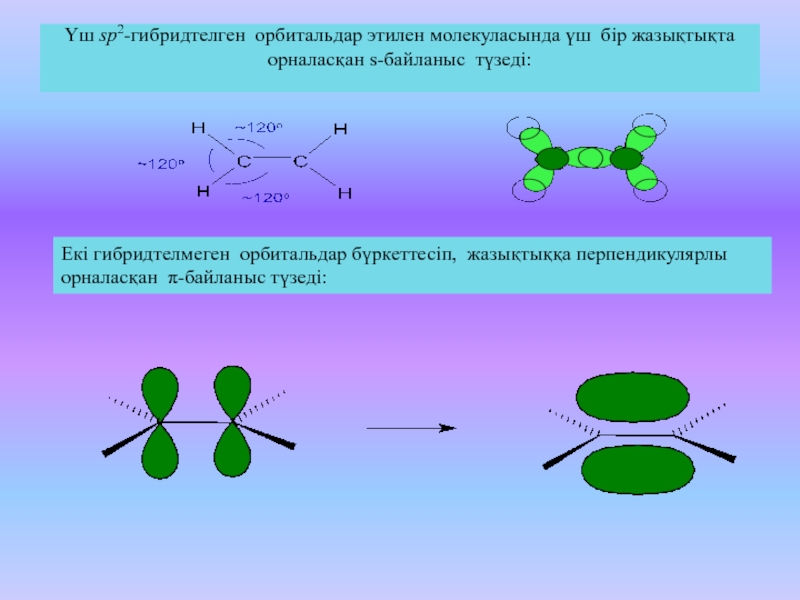
Слайд 30Үш sp2-гибридтелген орбитальдар этилен молекуласында үш бір жазықтықта орналасқан s-байланыс
түзеді:
Екі гибридтелмеген орбитальдар бүркеттесіп, жазықтыққа перпендикулярлы орналасқан -байланыс түзеді:
Слайд 31
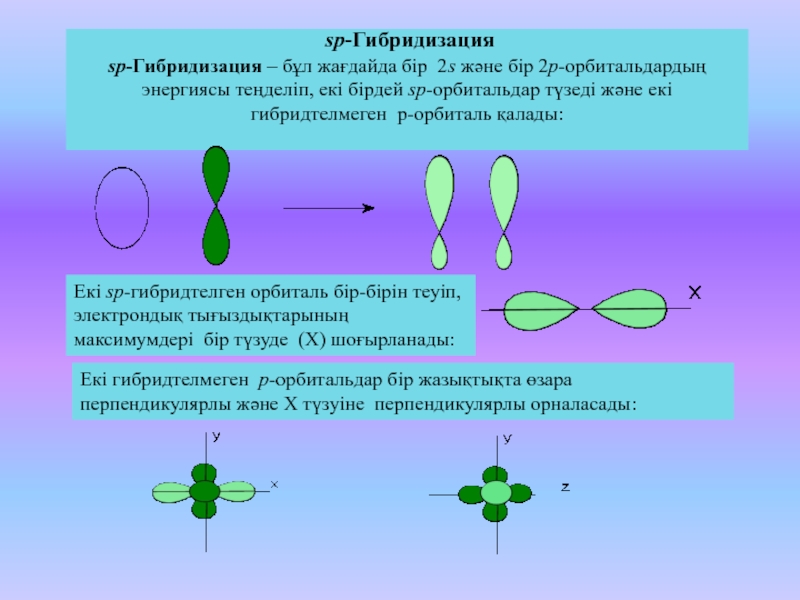
sp-Гибридизация
sp-Гибридизация – бұл жағдайда бір 2s және бір
2p-орбитальдардың энергиясы теңделіп, екі бірдей sp-орбитальдар түзеді және екі гибридтелмеген
p-орбиталь қалады:
Екі sp-гибридтелген орбиталь бір-бірін теуіп, электрондық тығыздықтарының максимумдері бір түзуде (Х) шоғырланады:
Екі гибридтелмеген p-орбитальдар бір жазықтықта өзара перпендикулярлы және Х түзуіне перпендикулярлы орналасады:
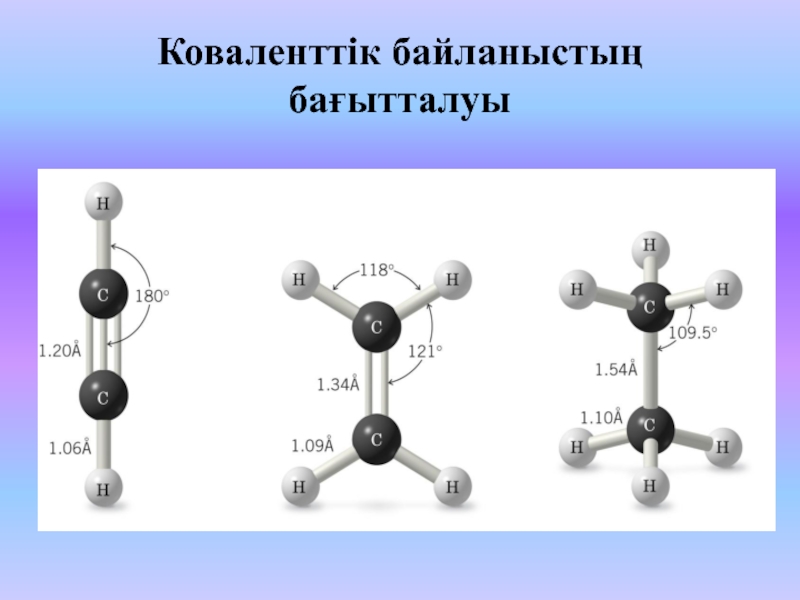
Слайд 33Коваленттік байланыстың бағытталуы
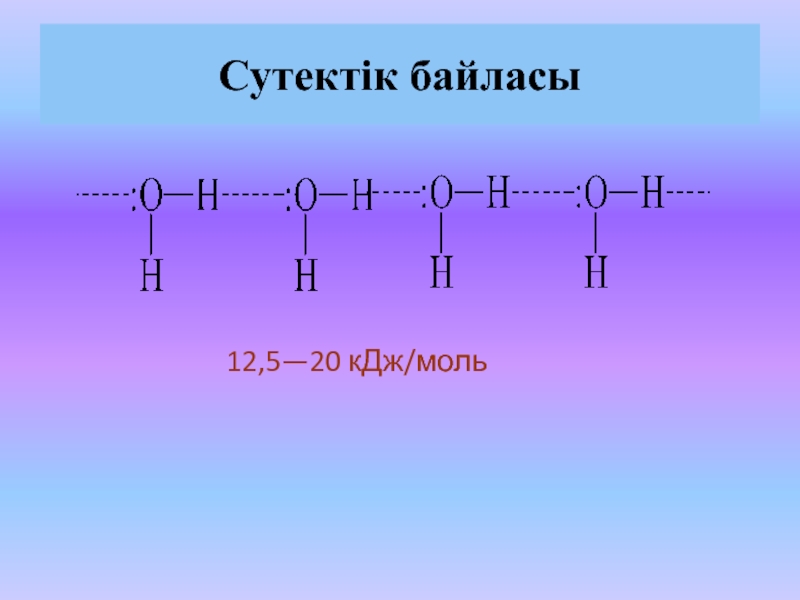
Слайд 34Сутектік байласы
12,5—20 кДж/моль
Слайд 35Молекуладағы атомдардың өзара әсері
Индуктивті эффект
Электрондық тығыздықтың -байланыс
бойында жылжуы индуктивті эффект деп аталады және I әріпімен белгіленеді.
Слайд 36Индуктивный эффект
Электронакцепторлы орынбасушылар, яғни -байланыстың электрондық тығыздығын көміртек атомынан
тартатын атом немесе атомдар тобы, теріс индуктивті эффектті көрсетеді (-I-эффект).
Электрондонорлы
орынбасушылар, яғни -байланыстың электрондық тығыздығын көміртек атомына тартатын атом немесе атомдар тобы, оң индуктивті эффект
(+I-эффект).
Слайд 37Индуктивті эффект
+I-Эффект алифатты көмірсутекті немесе алкилды радикалдар (–CH3, –C2H5,
т. б.) көрсетеді.
Функционалды топтар: –Hal, –NH2, –OH, >С=O, –COOH
көбіне -I-эффект көрсетеді.
пропен
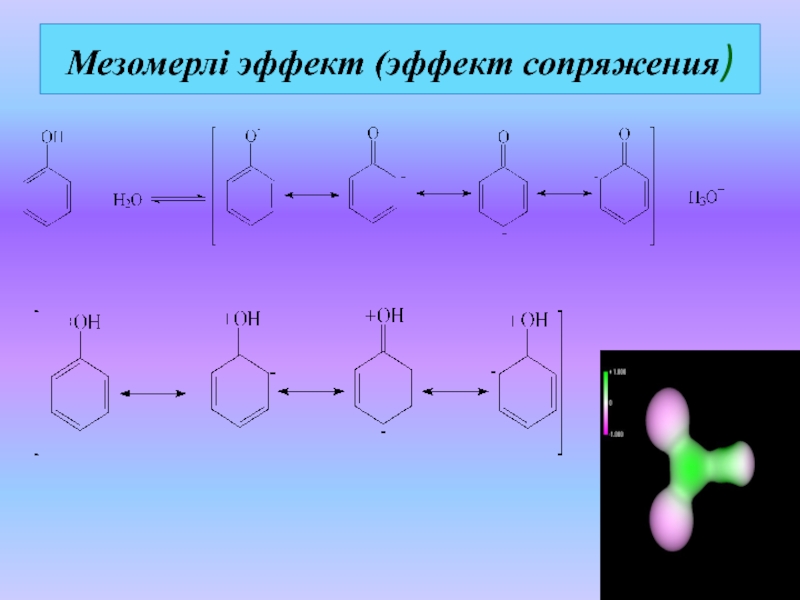
Слайд 38Мезомерлі эффект (эффект сопряжения)
Делокализацияланған байланыс
Слайд 39Мезомерлі эффект (эффект сопряжения)