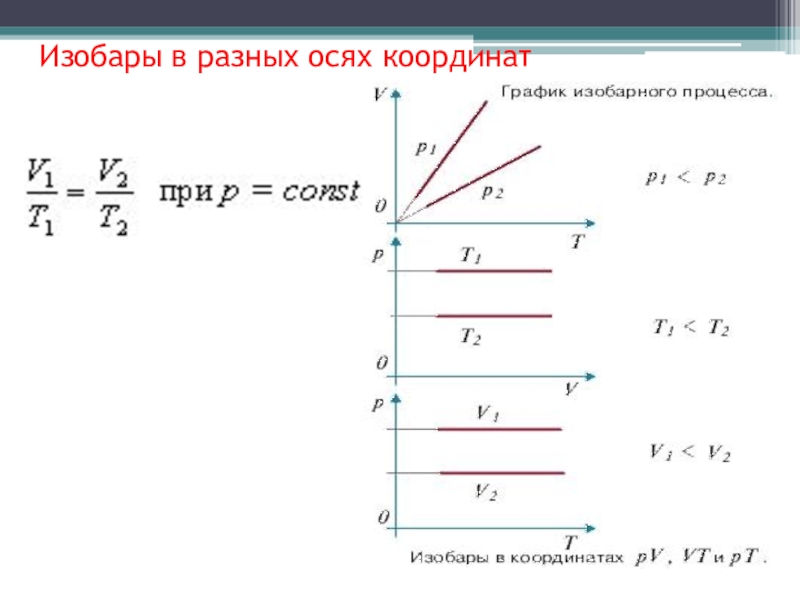
между p,V, T газа, которые называют параметрами газа.
Физические исследования Клапейрона
посвящены теплоте, пластичности и равновесию твердых тел.В 1834 г. вывел уравнение состояния идеального газа, объединяющее закон Бойля – Мариотта, закон Гей-Люссака и закон Авогадро, обобщенное Д. И. Менделеевым в 1874 г. (уравнение Менделеева – Клапейрона).