Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Витаминные комплексы в лечении нейропатий
Содержание
- 1. Витаминные комплексы в лечении нейропатий
- 2. Нейротропное действие тиамина (витамин В1)Участие в проведении
- 3. Нейротропное действие пиридоксина (витамин В6) Обеспечение синаптической
- 4. Нейротропное действие цианокобаламина (витамин В12) Участие
- 5. Влияние витаминов группы B на регенерацию поврежденных
- 6. ВОЗМОЖНЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ МИЛЬГАММЫСобственный антиноцицептивный эффект *
- 7. АНТИНОЦИЦЕПТИВНОЕ ДЕЙСТВИЕ МИЛЬГАММЫКомбинация В1, В6 и В12
- 8. Нейротропные свойства компонентов Мильгаммы-композитум1. Sanches-Ramirez G.M. et
- 9. МИЛЬГАММА - первый нейротропный комплекс• Восстанавливает структуру
- 10. МИЛЬГАММА композитум Сохраняет нервные волокна• Восстанавливает структуру
- 11. Сравнение биодоступности бенфотиамина и тиамина мононитратаДизайн исследования
- 12. Артамонов В.Е. 2007
- 13. Артамонов В.Е. 2007Преимущества БенфотиаминаВысокая абсорбция Бенфотиамина благодаря
- 14. В сравнении с тиамином Бенфотиамин не подавляет
- 15. ВСЕ ЛИ ВИТАМИНЫ В ОДИНАКОВЫ?Дополнительное введение цианкобаламина (В12) вредно:тромбозы, сердечная недостаточность, аллергиястимуляцмя роста новообразований
- 16. -липоевая (тиоктовая) кислота1948 - открыта О’ Кейн,
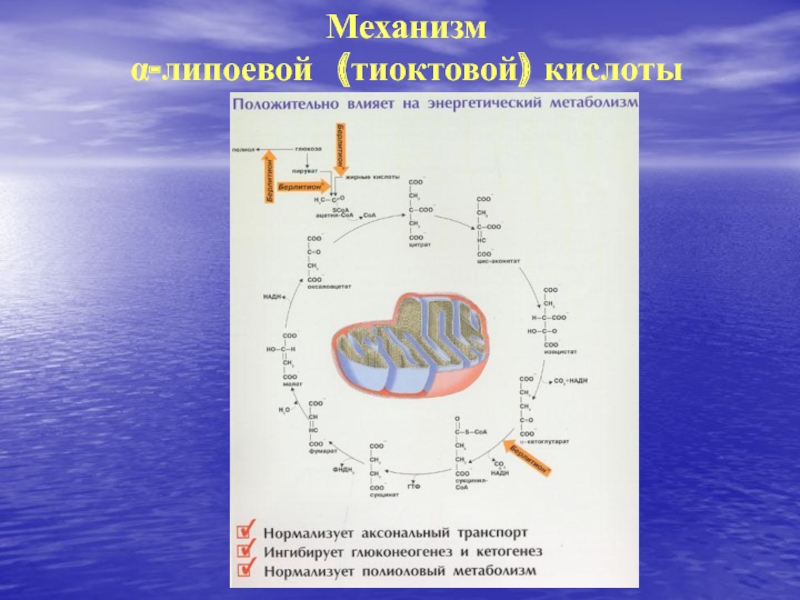
- 17. Механизм-липоевой (тиоктовой) кислоты
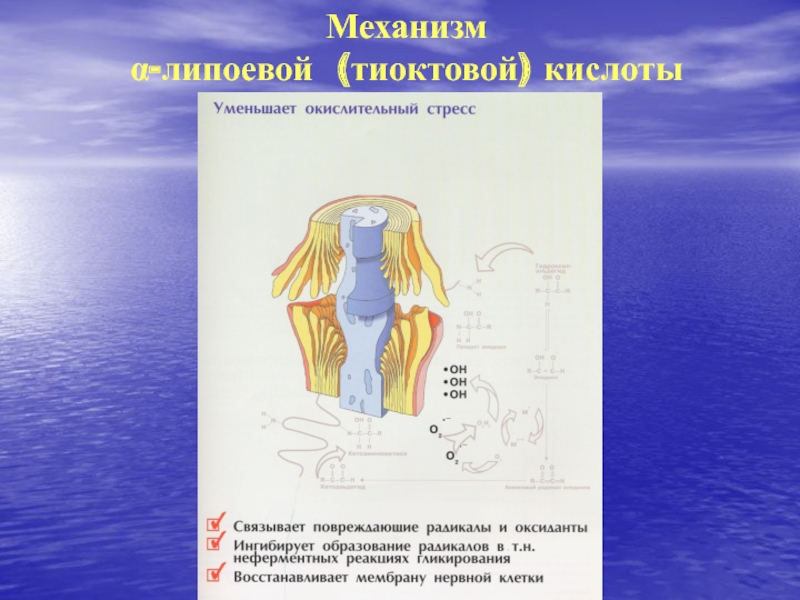
- 18. Механизм-липоевой (тиоктовой) кислоты
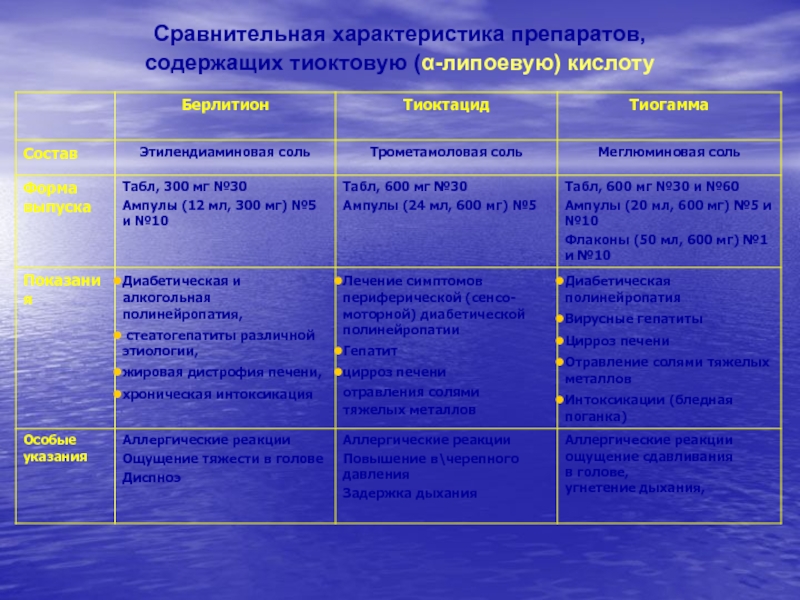
- 19. Сравнительная характеристика препаратов,содержащих тиоктовую (-липоевую) кислоту
- 20. ДИАБЕТИЧЕСКАЯ НЕЙРОПАТИЯПатогенетические предпосылки применения нейротропных комплексов Мильгамма композитум и Мильгамма
- 21. Гипогликемический или нейрометаболический контроль? Данные международных
- 22. Долгосрочное влияние гипергликемической памяти*Продолжительное снижение уровня глюкозы
- 23. Роль конечных продуктов гликирования (КПГ) в повреждении
- 24. КПГ активируют процесс окислительного стресса в митохондрияхПорочный
- 25. Возможный терапевтический подход: АКТИВАЦИЯ ТРАНСКЕТОЛАЗЫ Транскетолаза –фермент,
- 26. Потенциальные блокаторы образования КПГБенфотиамин защищает нервную ткань
- 27. Преимущества бенфотиаминаВысокая абсорбция благодаря липофильной структуре Почти 100% биодоступность Резистентность к тиаминазе кишечника
- 28. От феномена «гипергликемической памяти» к структурным повреждениям нервных волокон
- 29. Характер поражений нервных волокон при диабетической нейропатииНЕЗАВИСИМО
- 30. Характер поражений нервных волокон при диабетической нейропатииОба
- 31. «Гипергликемическая память» нервных волоконВ митохондриях нервных клеток
- 32. Патогенез развития ДПНГипергликемияна фоне СДМИЛЬГАММА КОМПОЗИТУМИзбыток свободных
- 33. Механизм действия Мильгаммы композитумАктивация транскетолазы (бенфотиамин) Блокирование
- 34. Бенфотиамин и пиридоксин – нейротропные факторы, препятствующие
- 35. Мильгамма композитум: блокатор КПГ1. Sanches-Ramirez G.M. et
- 36. Лечение диабетической нейропатии* ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ*последнее изданиеРедакция: И.И. Дедов, М.В. Шестакова 2009
- 37. Свойства тиоктовой кислоты (общее)Влияние на энергетический
- 38. Влияние на энергетический метаболизм, обмен глюкозы и
- 39. Антиоксидантное действиеИнактивировация свободных радикалов.Нормализация функции глутатионовой системы
- 40. Нейротропное и нейропротективное действиеПоложительное влияние на аксональный
- 41. Гепатопротективное действие тиоктовой кислотыСтимулирование накопление гликогена в
- 42. Детоксикационное действиеПротективная почечная и печёночная активность
- 43. Гиполипидемическое и гипогликемическое действияПовышает тропность инсулина к
- 44. ФОРМЫ ВЫПУСКА:Флаконы для инфузий (600 мг
- 45. ТИОГАММА®
- 46. Магний: биологическая рольМагний – регулятор биохимических процессов
- 47. Магний – антагонист кальция на всех субклеточных
- 48. Магний: биологическая рольМагний – регулятор внутриклеточных репаративных
- 49. Всасывание магния осуществляется во всем кишечнике, однако
- 50. Дефицит магнияДефицит магния – синдром, обусловленный снижением
- 51. Причины «Дефицита магния» Первичный (конституциональный, латентный) дефицит
- 52. Магнерот (оротат магния)Оротат магния служит предшественником пиримидиновых
- 53. МАГНЕРОТ®в кардиологии и терапии Инфаркт миокарда Хроническая сердечная недостаточность Магний-зависимые аритмии сердца Атеросклероз Дисплазия соединительной ткани
- 54. МАГНЕРОТ® при инфаркте миокардаГипомагниемия с уменьшением
- 55. МАГНЕРОТ® при ХСНПри ХСН недостаток магния в
- 56. МАГНЕРОТ® при аритмииАнтиаритмическая активность магния обусловлена электрической
- 57. Спасибо за внимание !
- 58. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Витаминные комплексы в лечении нейропатий
ФГБОУ ВПО «ОГУ»
Каф. фармакологии, клинической фармакологии
и фармации
Слайд 2Нейротропное действие тиамина (витамин В1)
Участие в проведении нервного импульса
Обеспечение аксонального транспорта, определяющего регенерацию нервной ткани
Модуляция нервно-мышечной
передачи в н-холинорецепторах Регуляция “болевой” активности нерва
Слайд 3Нейротропное действие пиридоксина (витамин В6)
Обеспечение синаптической передачи: участие
в синтезе нейротрансмиттеров (катехоламинов, гистамина)
Анальгетическое действие (подавление синтеза
медиаторов воспаления) системы Препятствует процессам гликирования на этапе "позднего гликозилирования" пиридоксамин способен эффективно ингибировать образование AGE-продуктов*.
Слайд 4Нейротропное действие цианокобаламина (витамин В12)
Участие в синтезе миелиновой оболочки
Уменьшение болевых ощущений, связанных с поражением периферической нервной системы
Слайд 5Влияние витаминов группы B на регенерацию поврежденных нервов
Бенфотиамин способствует
ремиелинизации через активацию фосфолипазы-A, что усиливает гидролиз эфиров жирных кислот.
Одновременное
применение тиамина, пиридоксина и кобаламина влияет на стимуляции аксоплазматической части транспорта структурных элементов мембраны или миелиновой оболочки, например холина. Бенфотиамин посредством усиления энергообеспечения в форме АТФ поддерживает аксоплазматический транспорт, в то время как пиридоксин участвует в синтезе транспортных белков, а цианокобаламин обеспечивает доставку жирных кислот для клеточных мембран и миелиновой оболочки.
Регенеративные свойства тиамина, пиридоксина и цианокобаламина основаны на фармакологических эффектах, характерных для высоких доз этих витаминов, и не зависящих от их дефицита
Слайд 6ВОЗМОЖНЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ МИЛЬГАММЫ
Собственный антиноцицептивный эффект *
(Franca D.
et al., 2001)Потенцирование действия аналгетиков и НПВП
(Wang ZB. et al., 2005)
Активация процессов регенерации, в частности, восстановление миелиновой оболочки
*Journal Schmerz 1998, 20; 12 (2), 136-41 Reyes-Garsia G.et al. J.Pharmacol.Toxicol Methods 1999, Oct 42 (2); 73-7
Слайд 7АНТИНОЦИЦЕПТИВНОЕ ДЕЙСТВИЕ МИЛЬГАММЫ
Комбинация В1, В6 и В12 обеспечивает торможение ноцицептивных
нейронов в дорсальных ядрах спинного мозга и в ядрах таламуса
за счет стимуляции норадренергических и серотонинергических антиноцицептивных систем**Journal Schmerz 1998, 20; 12 (2), 136-41 Reyes-Garsia G.et al. J.Pharmacol.Toxicol Methods 1999, Oct 42 (2); 73-7
Слайд 8Нейротропные свойства компонентов Мильгаммы-композитум
1. Sanches-Ramirez G.M. et al. European J.Pharmacol.2006,
530 (1-2), 48-53
2. Fu Q.-G., Carstens E., Stelzer B. Zimmermann
M. B vitamins supress spinal dorsal horn nociceptive neurons in the cat. Neurosci Lett 1988; 95: 192-197.Дополнительное введение цианкобаламина (В12) вредно!
Слайд 9МИЛЬГАММА
- первый нейротропный комплекс
• Восстанавливает структуру и функцию нерва при
радикулопатиях
• Снижает потребность пациентов с радикулопатией в НПВС
• Содержит
лидокаин• Имеет оптимальный объем ампулы – 2 мл
Слайд 10МИЛЬГАММА композитум
Сохраняет нервные волокна
• Восстанавливает структуру и функцию нерва при
радикулопатиях
• Снижает потребность пациентов с радикулопатией в НПВС
• Содержит
по 100 мг бенфотиамина и пиридоксина• Имеет 2 формы выпуска: №30,№60
Курс лечения хронической радикулопатии:
по 1 драже 3 раза в день
в течение 2-4 недель
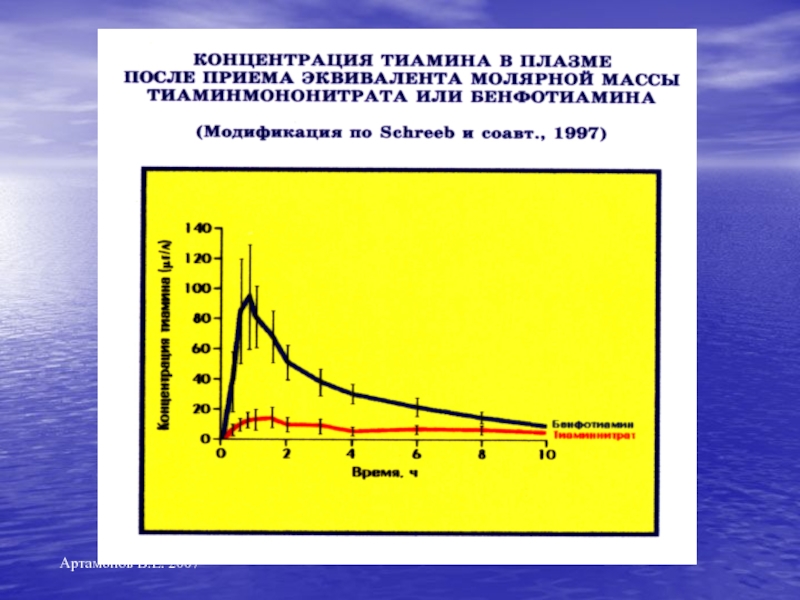
Слайд 11Сравнение биодоступности бенфотиамина и тиамина мононитрата
Дизайн исследования : двойное слепое
плацебо контролируемое
200 мг бенфотиамина
против 140,4 мг тиамина мононитрата (210 ммоль)
Перорально в 2 приема в течение 2 недель.
Результат:
Средняя площадь под кривой в 10 раз выше
Максимальная концентрация в 6,7 выше
Суточная экскреция в моче в 10 раз выше
у бенфотиамина, чем тиамина мононитрата
K.H. Shreeb et al. Eur J Pharmacol 1997
Слайд 13Артамонов В.Е. 2007
Преимущества Бенфотиамина
Высокая абсорбция Бенфотиамина благодаря липофильной структуре
Высокая
биодоступность (в 5 раз выше тиамина)
Резистентен к тиаминазе
Низкая тосичность (LD50
= 15 г/кг) после перорального приемаПерспективы терапии боли в спине
Слайд 14В сравнении с тиамином Бенфотиамин не подавляет абсорбцию через тонкий
кишечник
При применении Бенфотиамина отсутствует неприятный запах от тела
Бенфотиамин обладает
хорошей переносимостьюПерспективы терапии боли в спине
Преимущества Бенфотиамина
Слайд 15ВСЕ ЛИ ВИТАМИНЫ В ОДИНАКОВЫ?
Дополнительное введение цианкобаламина (В12) вредно:
тромбозы, сердечная
недостаточность, аллергия
стимуляцмя роста новообразований
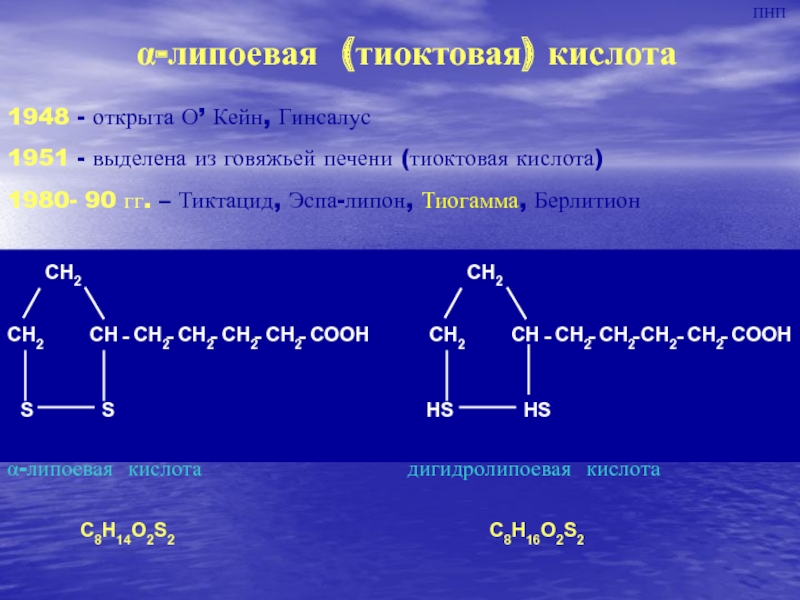
Слайд 16-липоевая (тиоктовая) кислота
1948 - открыта О’ Кейн, Гинсалус
1951 - выделена
из говяжьей печени (тиоктовая кислота)
1980- 90 гг. – Тиктацид, Эспа-липон,
Тиогамма, БерлитионCH2
CH
CH2
CH2
CH2
CH2
CH2
COOH
S
S
-липоевая кислота
CH2
CH
CH2
CH2
CH2
CH2
CH2
COOH
HS
HS
дигидролипоевая кислота
C8H14O2S2
C8H16O2S2
ПНП
Слайд 20ДИАБЕТИЧЕСКАЯ НЕЙРОПАТИЯ
Патогенетические предпосылки применения нейротропных комплексов Мильгамма композитум и Мильгамма
Слайд 21Гипогликемический или нейрометаболический контроль?
Данные международных рандомизированных исследований говорят о
недостаточной эффективности сахароснижающих препаратов (DCCT 1993, EDIC 2002)*
Концепция «гипергликемической
памяти» становится ведущей** Необходимость раннего лечения осложнений независимо от уровня глюкозы крови
*Ihnat et al.2007
**P.Thornelley 2009
Слайд 22Долгосрочное влияние гипергликемической памяти*
Продолжительное снижение уровня глюкозы крови не влияет
на скорость развития осложнений**
*Ihnat et al.2007
**P.Thornelley 2009
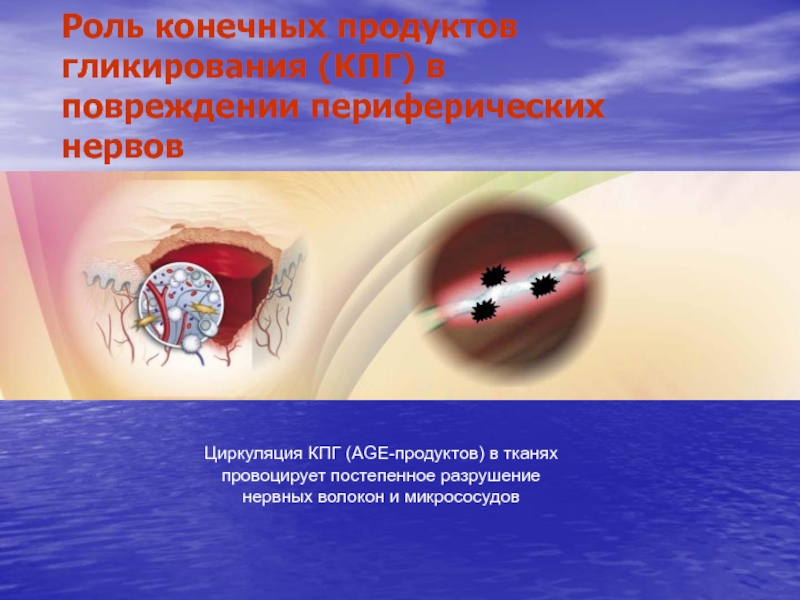
Слайд 23Роль конечных продуктов гликирования (КПГ) в повреждении периферических нервов
Циркуляция КПГ
(АGE-продуктов) в тканях провоцирует постепенное разрушение нервных волокон и микрососудов
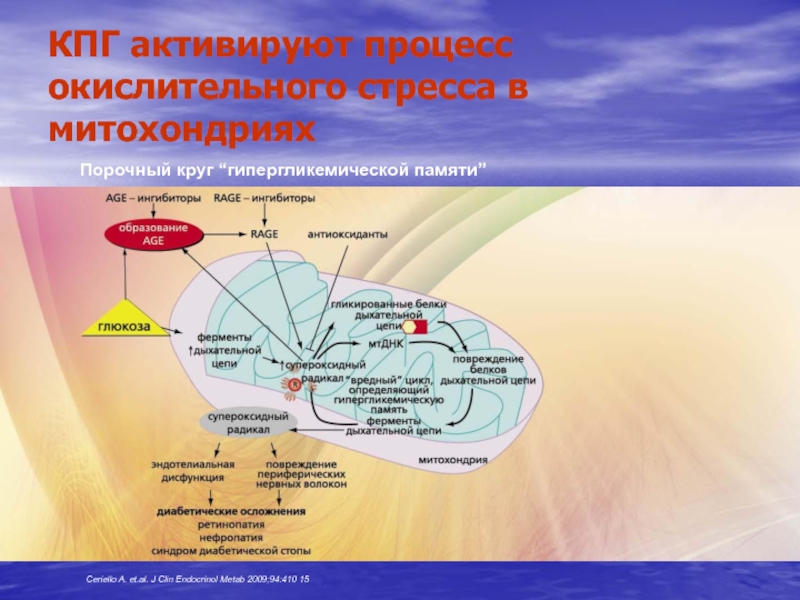
Слайд 24КПГ активируют процесс окислительного стресса в митохондриях
Порочный круг “гипергликемической памяти”
Ceriello
A. et.al. J Clin Endocrinol Metab 2009;94:410 15
Слайд 25Возможный терапевтический подход:
АКТИВАЦИЯ ТРАНСКЕТОЛАЗЫ
Транскетолаза –фермент, ограничивающий скорость реакций пентозофосфатного
пути
Кофактор транскетолазы –тиаминпирофосфат (активный метаболит бенфотиамина)
Слайд 26Потенциальные блокаторы образования КПГ
Бенфотиамин защищает нервную ткань от конечных продуктов
гликирования путем активации транскетолазы1,2
Активный метаболит В6 пиридоксамин напрямую препятствует
избыточному образованию КПГ1. V.Marchetti,R.Menghini Benfotiamine counteracts glucose toxicity effects on endothelial progenitor cell differentiation via Akt/FoxO Signaling, Department of Internal Medicine, University of Rome Tor Vergata
2. Stracke et al., A Benfotiamine-Vitamin B combination in the treatment of diabetic polyneuropathy.
Слайд 27Преимущества бенфотиамина
Высокая абсорбция благодаря липофильной структуре
Почти 100% биодоступность
Резистентность
к тиаминазе кишечника
Слайд 29Характер поражений нервных волокон при диабетической нейропатии
НЕЗАВИСИМО ОТ ЭТИОЛОГИЧЕСКОГО ФАКТОРА
ВЫДЕЛЯЮТ 2 ТИПА ПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ:
Поражение аксона
Демиелинизацию нервного волокна
Слайд 30Характер поражений нервных волокон при диабетической нейропатии
Оба процесса тесно взаимосвязаны:
при аксональном типе поражения возникает вторичная демиелинизация, при демиелинизирующем поражении
вторично присоединяется аксональный компонент. При аксональных нейропатиях страдает главным образом транспортная функция осевого цилиндра.Вывод:
необходимо назначение препаратов,
которые не только защищают нервную ткань от повреждений,
но и восстанавливают структуру нервных волокон
Слайд 31«Гипергликемическая память» нервных волокон
В митохондриях нервных клеток
остается память о
гипергликемических повреждениях,
несмотря на терапию ПССТ*
КПГ запускают каскад свободноокислительных реакций,
что
приводит к избытку образования свободных радикаловВывод: лечение надо начинать с активаторов
транскетолазы (Мильгамма композитум)
* Пероральная сахароснижающая терапия
Слайд 32Патогенез развития ДПН
Гипергликемия
на фоне СД
МИЛЬГАММА
КОМПОЗИТУМ
Избыток свободных радикалов
Полиоловый путь
метаболизма
глюкозы
Избыток КПГ
Na-K-АТФаза, нейротропных факторов,
вазоконстрикция
Гипоксия, снижение скорости
проведения нервных
импульсов Деградация
аксональной структуры
нервных волокон
Слайд 33Механизм действия
Мильгаммы композитум
Активация
транскетолазы
(бенфотиамин)
Блокирование синтеза КПГ (пиридоксин)
Разрушение конечных
продуктов гликирования
Восстановление структуры
нервных волокон
Профилактика развития
микро-и макроангиопатий
H.P.Hammes et.al.,Nature Med.
On line,2003Слайд 34Бенфотиамин и пиридоксин – нейротропные факторы, препятствующие формированию диабетической нейропатии
Оптимальная
нейротропная комбинация =
100 мг бенфотиамина
+ 100 мг пиридоксина
Слайд 35Мильгамма композитум:
блокатор КПГ
1. Sanches-Ramirez G.M. et al. European J.Pharmacol.2006, 530
(1-2), 48-53
2. Fu Q.-G., Carstens E., Stelzer B. Zimmermann M.
B vitamins supress spinal dorsal horn nociceptive neurons in the cat. Neurosci Lett 1988; 95: 192-197.3. Booth, A.A.; Khalifah, R.G.; Hudson, B.G. Thiamine pyrophosphate and pyridoxamine inhibit the formation of antigenic advanced glycation end-products: comparison with aminoguanidine.Biochem. Biophys. Res. Commun. 1996, 220, 113-119
Слайд 36Лечение диабетической нейропатии*
ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ
*последнее издание
Редакция: И.И. Дедов, М.В. Шестакова
2009
Слайд 37Свойства тиоктовой кислоты
(общее)
Влияние на энергетический метаболизм
Влияние на обмен глюкозы
и липидов
Антиоксидантный эффект
Нейротропное и нейропротективное действие
Гепатопротективное действие
Детоксикационное действие
Гиполипидемическое действие
Гипогликемическое
действиеСлайд 38Влияние на энергетический метаболизм, обмен глюкозы и липидов
усиление усвоения и
утилизации глюкозы
повышение основного обмена
нормализация глюконеогенеза
участие в окислительном декарбоксилировании -кетокислот
(пирувата и -кетоглютарата)
с активацией цикла КребсаСлайд 39Антиоксидантное действие
Инактивировация свободных радикалов.
Нормализация функции глутатионовой системы (выступает донором сульфргидрильных
групп и замещает восстановленный глутатион в реакциях, обеспечиваемых глутатионпероксидазой)
Уменьшение
оксидативного стрессаУвеличение эндогенного антиоксидантного потенциала
Слайд 40Нейротропное и нейропротективное действие
Положительное влияние на аксональный транспорт,
Уменьшение вредного влияния
на нервные клетки свободных радикалов;
Нормализация аномального поступления глюкозы к нерву
Предупреждение
повреждения нервов при инсулинорезистентностиУстранение симптомов диабетической нейропатии
Восстановление температурной, тактильной и болевой чувствительности
Влияние на автономную нервную систему
Уменьшение перекисного окисления липидов в периферических нервах
Улучшение эндоневрального кровотока (увеличение скорости проведения импульсов).
Нормализация уровня глутатиона в нервах.
Стимуляция роста аксонов и их разветвлений
Стимуляция роста новых нервных волокон.
Слайд 41Гепатопротективное действие тиоктовой кислоты
Стимулирование накопление гликогена в печени
(за счёт
повышения трансмембранного транспорта глюкозы в клетку)
Торможение накопления липидов в
печениОптимизация функции печени
Роль кофермента в белковом и углеводном обмене
Участие в окислении жирных кислот и ацетата (предупреждает развитие жирового стеатоза печени)
Подавление синтеза оксида азота гепатоцитами (профилактика и купирование реологических расстройств и сосудистых нарушений)
Тиоктовая кислота используется при алкогольном и неалкогольном стеатогепатите, при жировом стеатозе для профилактики прогрессирования и развития осложнений
Слайд 42Детоксикационное действие
Протективная почечная и печёночная активность
в восстановительном периоде после
лучевой болезни
ФОС, свинец, мышьяк, ртуть, сулема, цианиды, фенотиазиды аманитин, фаллоидин
(бледная поганка) и дрПри поражении радиоактивных веществ
Инактивирует соли тяжелых металлов
Слайд 43Гиполипидемическое и гипогликемическое действия
Повышает тропность инсулина к тканям
Повышает активность глюкозных
транспортеров
и внутриклеточный транспорт глюкозы
Тормозит процессы глюконеогенеза
Ингибирует процессы образования
холестерина Подавляет процессы липолиза
Снижает высвобождение жирных кислот из жировой ткани на 50%
Слайд 44ФОРМЫ ВЫПУСКА:
Флаконы для инфузий
(600 мг тиоктовой кислоты)
– №1 и
№10
Концентрат раствора
(600 мг тиоктовой кислоты)
– №5 и №10
Таблетки
(600 мг тиоктовой кислоты)– №30
– №60
ТИОГАММА®
Меглюминовая соль тиоктовой кислоты
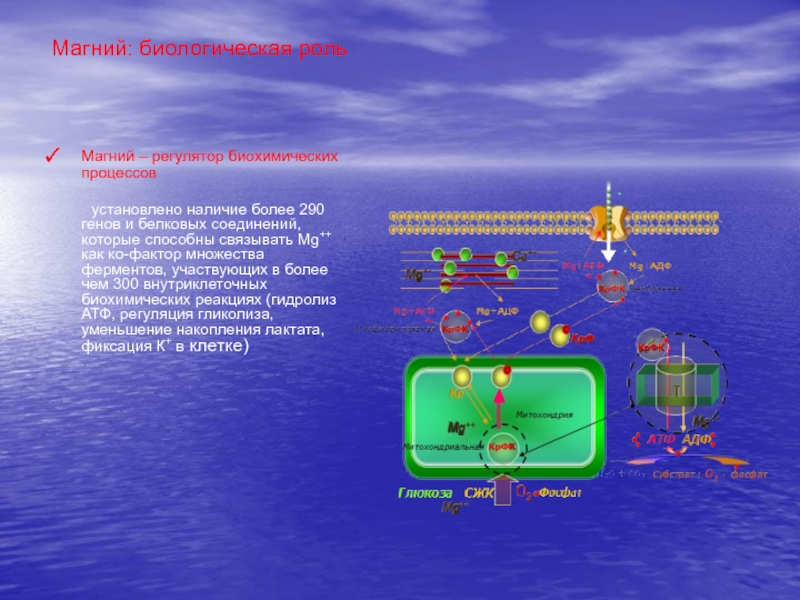
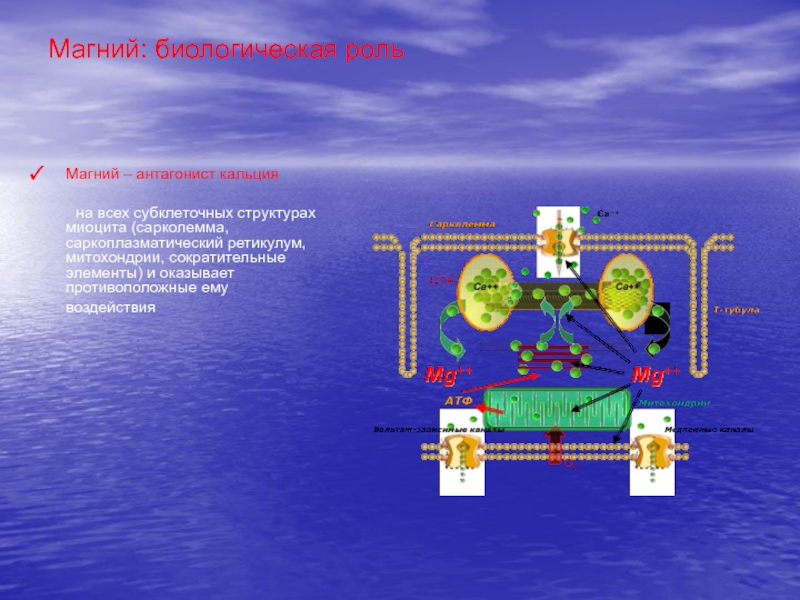
Слайд 46Магний: биологическая роль
Магний – регулятор биохимических процессов
установлено наличие более
290 генов и белковых соединений, которые способны связывать Mg++ как
ко-фактор множества ферментов, участвующих в более чем 300 внутриклеточных биохимических реакциях (гидролиз АТФ, регуляция гликолиза, уменьшение накопления лактата, фиксация К+ в клетке)Слайд 47Магний – антагонист кальция
на всех субклеточных структурах миоцита (сарколемма,
саркоплазматический ретикулум, митохондрии, сократительные элементы) и оказывает противоположные ему воздействия
Магний: биологическая роль
Слайд 48Магний: биологическая роль
Магний – регулятор внутриклеточных репаративных процессов
Ионы Mg++ стабилизируют
структуру транспортной РНК, контролирующей общую скорость ресинтеза белков
Магний – регулятор
физиологических функций: мембранного транспорта и электролитного баланса, требующих больших энергозатратОбеспечение нормальной структуры и функции нервных клеток, что позволяет ему контролировать деятельность центральной и периферической нервной системы, включая психо-эмоциональную сферу
Поддержание нормального липидного спектра
Участие в обеспечении ответа тканей на инсулин
Торможение гормона паращитовидной железы
Слайд 49Всасывание магния осуществляется во всем кишечнике, однако главной зоной абсорбции
служит 12-перстная кишка
Усвояемость магния из пищевых продуктов составляет
30 –
35%Вещества, препятствующие всасыванию магния: пища с высоким содержанием кальция, белков, жиров, фосфора
Препараты магния лучше принимать натощак
Обмен магния
Слайд 50Дефицит магния
Дефицит магния – синдром, обусловленный снижением внутриклеточного содержания магния
в различных органах и системах
С 1995 года ВОЗ классифицирует «недостаточность
магния» как заболевание, имеющее свой код (Е 61.3).По данным различных европейских исследований установлено, что дефицитом магния страдают от 25% до 40% населения*
*Whang R., Ryder KW. Frequency of hypomagnesemia and hypermagnesemia
Requested vs. routine. J Am Med Assoc 263, 3063-3064 (1990)
Слайд 51Причины «Дефицита магния»
Первичный (конституциональный, латентный) дефицит магния – обусловлен
дефектами в генах ответственных за трансмембранный обмен магния в организме
клинически проявляется судорожным синдромом (спазмофилия), «конституционной тетанией» или «нормокальциевой тетанией» на фоне нормального содержания Mg++ в сыворотке кровиВторичный дефицит магния – обусловлен социальными условиями жизни, заболеваниями и стрессом
Слайд 52Магнерот (оротат магния)
Оротат магния служит предшественником пиримидиновых оснований
– ДНК
и РНК
Оротат магния является кардиопротектором: ускоряет регенерацию миокарда, увеличивает устойчивость к
ишемии и выживаемость при инфарктеОротат магния оказывает защитное действие на ЦНС при гипоксии, травме, интоксикации, облегчает обучение и обработку информации, восстанавливает нормальный ответ на допамин
Оротат магния снижает количества общего холестерина и улучшает метаболические показатели, что тормозит развитие атеросклероза
Соединение – магниевая соль оротовой кислоты дает дополнительные преимущества: обеспечивает доставку ионов магния непосредственно в клетку, поскольку ее диссоциация происходит только внутри клетки
Оротат магния хорошо абсорбируется из желудочно-кишечного тракта
Слайд 53МАГНЕРОТ®
в кардиологии и терапии
Инфаркт миокарда
Хроническая сердечная недостаточность
Магний-зависимые
аритмии сердца
Атеросклероз
Дисплазия соединительной ткани
Слайд 54МАГНЕРОТ® при инфаркте
миокарда
Гипомагниемия с уменьшением внутриклеточного содержания Mg++ отмечается
в 92% среди больных ОИМ, поступивших в стационар в 1-е
сутки заболевания1Потеря Mg++ у больных с ОКС вызвана:
Выбросом катехоламинов в кровь (что всегда имеет место при ОИМ), влекущим за собой потерю клеточного Mg++ (особенно много Mg++ теряет миокард) и выведение его с мочой за счет снижения реабсорбции Mg++ в тубулярном аппарате
Усилением липолиза, в связи с чем повышается содержание свободных жирных кислот, связывающих ионизированный магний плазмы. Связывание магния плазмы еще более активирует выход внутриклеточного Mg++
Последствия дефицита магния при ИМ
Изменение Са++/Mg++ соотношения в клетках коры надпочечников, что вызывает усиление секреции минералокортикоидов и еще более усугубляет потерю Mg++ организмом.
Нарушение сократительной функции кардиомиоцитах ( Mg++ контролирует циклические колебания Са++ в цитоплазме): развивается диастолическая дисфункция, снижается сократительная способность миокарда, суммарно ухудшается насосная деятельность сердца
1Шилов А.М., Мельник М.В., 1998г.
Слайд 55МАГНЕРОТ® при ХСН
При ХСН недостаток магния в организме возникает в
результате
Нарушения нейрогуморальных взаимосвязей (активация
симпатоадреналовой и ренин-ангиотензин-альдостероновой систем)
Застоя в ЖКТ,
снижающего абсорбцию магнияУсугубляется приемом диуретических препаратов и сердечных
гликозидов, способствующих усиленному выведению Mg++ из клеток
У больных ХСН с «дефицитом магния» отмечается двукратное увеличение летальности от нарушений ритма сердечной деятельности и нарастания сердечной недостаточности.1
Гипомагнезиемия среди этих пациентов ассоциируется с латентной формой бронхообструкции, повышенной агрегацией тромбоцитов, сниженной подвижностью эритроцитов, что сопровождается увеличением работы дыхания, повышенным риском тромбозов и эмболий.2
1 Степура О.Б., Мартынов А.И., 2008
2 Шилов А.М., Бабченко П.К., 2004
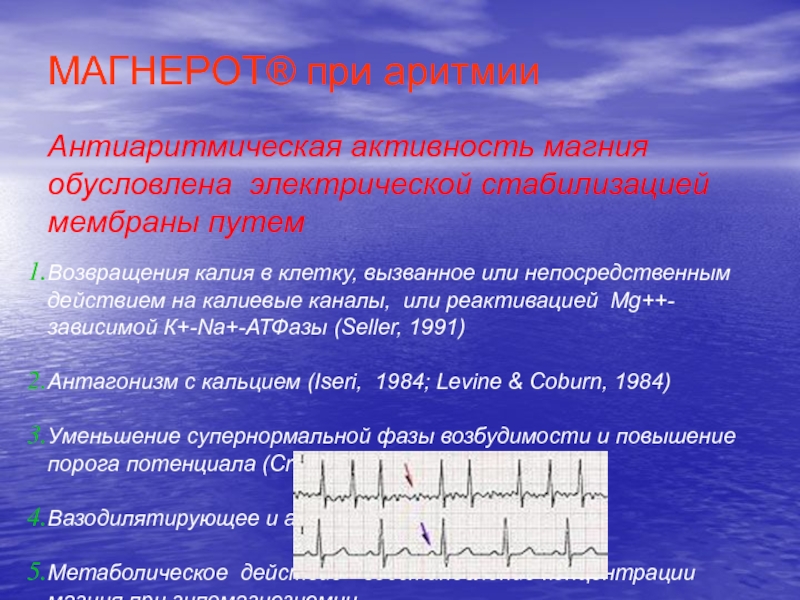
Слайд 56МАГНЕРОТ® при аритмии
Антиаритмическая активность магния обусловлена электрической стабилизацией мембраны путем
Возвращения калия в клетку, вызванное или непосредственным действием на калиевые
каналы, или реактивацией Мg++-зависимой К+-Na+-АТФазы (Seller, 1991)Антагонизм с кальцием (Iseri, 1984; Levine & Coburn, 1984)
Уменьшение супернормальной фазы возбудимости и повышение порога потенциала (Critelli et al., 1979)
Вазодилятирующее и антиишемическое действие
Метаболическое действие - восстановление концентрации магния при гипомагнезиемии