Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Воронежская государственная медицинская академия им. Н.Н.Бурденко кафедра Химии
Содержание
- 1. Воронежская государственная медицинская академия им. Н.Н.Бурденко кафедра Химии
- 2. Простые правила
- 3. Лекция 1. РАСТВОРЫ Якоб Хендрик Вант-Гофф1852-1911Сванте АвгустАррениус1859-1927Фридрих ВильгельмОствальд1853-1932Рихард АдольфЗигмонди1865-1929
- 4. Раствор - гомогенная (однородная) система переменного состава,
- 5. Классификация растворовПо взаимодействию между компонентами раствора (идеальные
- 6. 3. По размеру частиц растворенного вещества :истинные
- 7. концентрированные (с большим содержанием растворенного вещества) и
- 8. Подробнее о способах выражения состава растворов и
- 9. Растворение – физико-химический процесс, протекающий между твердой
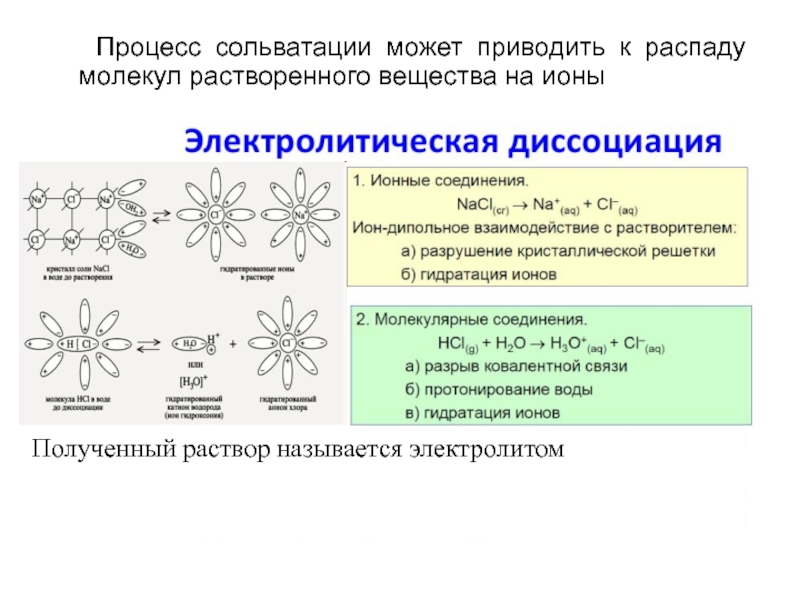
- 10. Процесс сольватации может приводить к распаду молекул растворенного вещества на ионы
- 11. Слабые и сильные электролиты
- 12. Полнота распада (сила электролита) характеризуется количественной величиной
- 13. Степень диссоциации зависит от:- природы электролита и
- 14. Константа диссоциации Электролитическая диссоциация слабых
- 15. Связь константы диссоциации и степени диссоциации (закон разведения Оствальда)Для очень слабых электролитов при α
- 16. Особенности растворов сильных электролитов Вследствие полной
- 17. В разбавленных растворах γ = 1, тогда
- 18. Ионная сила раствора (I) - величина, характеризующая
- 19. Слайд 19
- 20. Давление насыщенного пара (ДНП) над раствором Франсуа
- 21. Вторая формулировка закона Рауля: относительное понижение
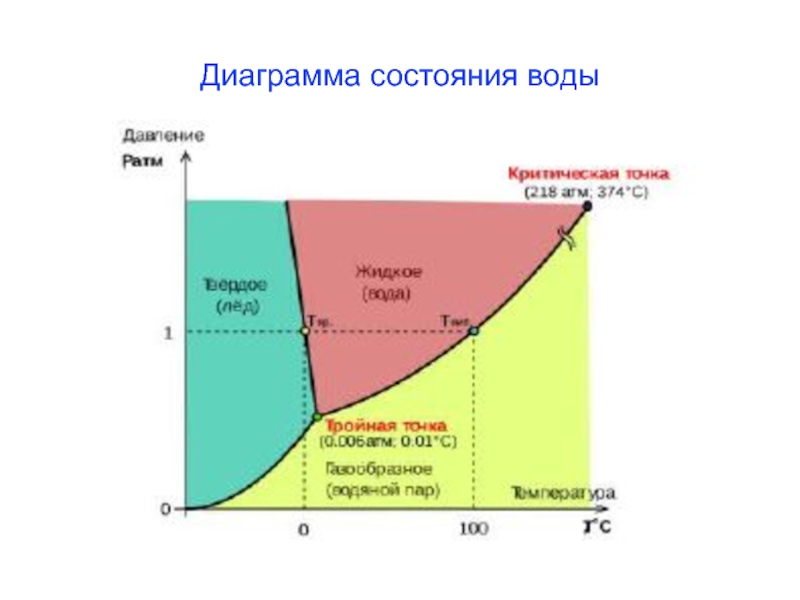
- 22. Диаграмма состояния воды
- 23. Следствия закона Рауля Любая жидкость закипает,
- 24. Понижение температуры замерзания и повышение температуры кипения
- 25. эти константы зависят от природы растворителя при
- 26. В растворах электролитов число частиц больше из-за
- 27. Осмос. Осмотическое давление Осмос – это
- 28. В организме осмотическое давление должно
- 29. Растворы, у которых больше,
- 30. Растворы, у которых меньше,
- 31. Значение осмоса упругость, тургор клеток
- 32. Методы, основанные на изучении коллигативных свойств растворовосмометрия
- 33. Применяются для определения : молекулярных
- 34. Криоскопическому методу исследования отдается предпочтение, поскольку температуру
- 35. СПАСИБО ЗА ВНИМАНИЕ
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Воронежская государственная медицинская академия им. Н.Н.Бурденко кафедра Химии Зав. кафедрой д.х.н., профессор
Пономарева Наталия Ивановна
Слайд 3Лекция 1. РАСТВОРЫ
Якоб Хендрик
Вант-Гофф
1852-1911
Сванте Август
Аррениус
1859-1927
Фридрих Вильгельм
Оствальд
1853-1932
Рихард Адольф
Зигмонди
1865-1929
Слайд 4Раствор - гомогенная (однородная) система переменного состава, состоящая из двух
и более компонентов.
Компоненты раствора
Растворитель
Растворенное вещество
Компонент, агрегатное состояние которого не изменяется
при образовании раствора, а при одинаковом агрегатном состоянии компонентов находится в избытке.вещество, равномерно распределенное в растворителе в виде молекул или ионов
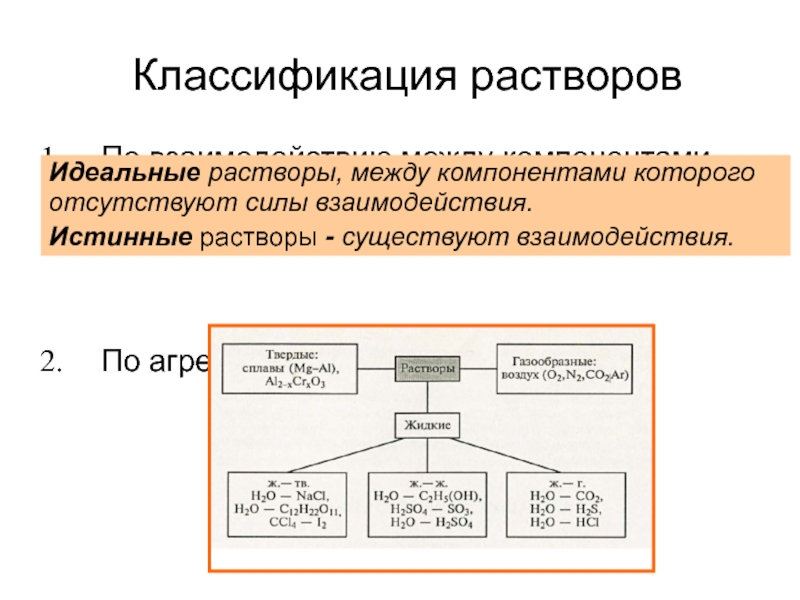
Слайд 5Классификация растворов
По взаимодействию между компонентами раствора (идеальные и истинные (реальные))
По
агрегатному состоянию
Идеальные растворы, между компонентами которого отсутствуют силы взаимодействия.
Истинные
растворы - существуют взаимодействия.Слайд 63. По размеру частиц растворенного вещества :
истинные растворы – однородные
(гомогенные) системы с размером частиц 10-10 – 10-9 м
растворы электролитов
(ионные)растворы неэлектролитов (молекулярные)
коллоидные растворы – неоднородные (гетерогенные) системы с размером частиц 10-9 – 10-6 м (мицеллярные).
4. По типу растворителя:
водные растворы (растворитель – вода) и
неводные растворы (растворители – спирт, эфир, бензол, толуол и т.д.).
Слайд 7концентрированные (с большим содержанием растворенного вещества) и разбавленные (с небольшим
содержанием).
5. По количеству растворенного вещества:
насыщенные (в которых данное вещество при
данной температуре больше не растворяется, т.е. такой раствор находится в равновесии с растворяемым веществом), ненасыщенные и пересыщенные.6. По состоянию равновесия:
Слайд 8Подробнее о способах выражения состава растворов и связи между ними
вы познакомитесь на лабораторных занятиях
Способы выражения состава растворов
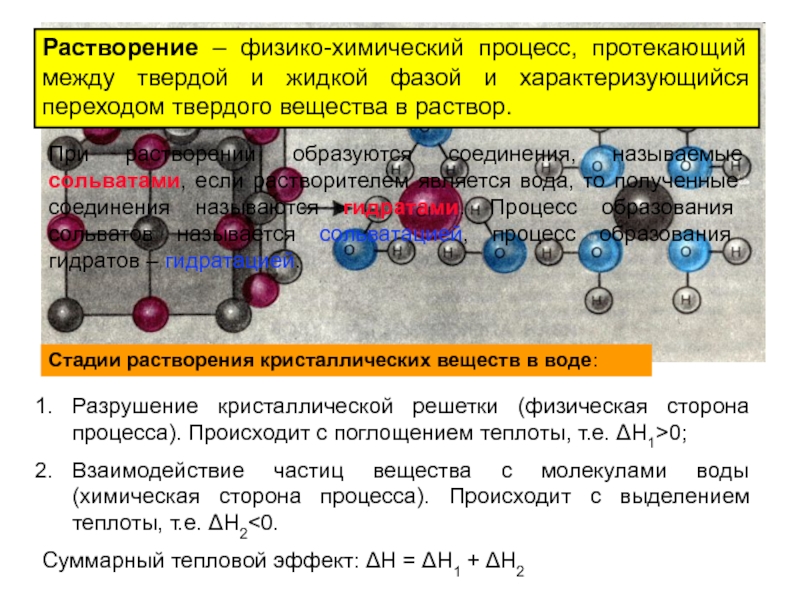
Слайд 9Растворение – физико-химический процесс, протекающий между твердой и жидкой фазой
и характеризующийся переходом твердого вещества в раствор.
При растворении образуются соединения,
называемые сольватами, если растворителем является вода, то полученные соединения называются гидратами. Процесс образования сольватов называется сольватацией, процесс образования гидратов – гидратацией.Стадии растворения кристаллических веществ в воде:
Разрушение кристаллической решетки (физическая сторона процесса). Происходит с поглощением теплоты, т.е. ΔН1>0;
Взаимодействие частиц вещества с молекулами воды (химическая сторона процесса). Происходит с выделением теплоты, т.е. ΔН2<0.
Суммарный тепловой эффект: ΔН = ΔН1 + ΔН2
Слайд 12Полнота распада (сила электролита) характеризуется количественной величиной – степенью диссоциации.
Степень
диссоциации (α – греческая буква альфа) - это отношение числа
молекул, распавшихся на ионы (n), к общему числу растворенных молекул (N):Основные характеристики электролитов
Слайд 13Степень диссоциации зависит от:
- природы электролита и растворителя: чем полярнее
химическая связь в молекуле электролита и растворителя, тем выше значение
α.- концентрации электролита: с уменьшением концентрации электролита (разбавление), α увеличивается.
- температуры: α возрастает при повышении температуры
Слайд 14
Константа диссоциации
Электролитическая диссоциация слабых электролитов, согласно теории Аррениуса,
является обратимой реакцией, например:
KA ↔ K+ + A−Константу равновесия такой реакции можно выразить уравнением:
Константу равновесия применительно к реакции диссоциации называют константой диссоциации (Кд).
.
На практике для характеристики слабого электролита часто используют показатель константы диссоциации (рК): рК = -lgКд . Чем больше рК, тем слабее электролит.
Слайд 15Связь константы диссоциации и степени диссоциации (закон разведения Оствальда)
Для очень
слабых электролитов при α
Слайд 16Особенности растворов сильных электролитов
Вследствие полной диссоциации число ионов
в растворе сильных электролитов больше, чем в растворе слабых той
же концентрации.При увеличении концентрации число ионов в растворе увеличивается, сила взаимодействия их между собой и с растворителем возрастает, что приводит к снижению подвижности ионов и создает эффект уменьшения их концентрации.
Количественно влияние межионного взаимодействия характеризуют:
Активность иона (а) – эффективная концентрация иона;
Коэффициент активности (γ) мера отклонения активности иона от его истинной концентрации.
Слайд 17В разбавленных растворах γ = 1, тогда а = С.
Коэффициент
активности иона (γ) зависит от температуры; общей концентрации всех ионов
в растворе (Г.Льюис ввел понятие ионной силы раствора)Слайд 18Ионная сила раствора (I) - величина, характеризующая силу электростатического взаимодействия
ионов в растворе, которая равна полусумме произведений молярных концентраций всех
ионов на квадрат их заряда:I = ½ Cizi2
Ионная сила плазмы равна 0,167; все кровезаменители готовят с I равной плазме.
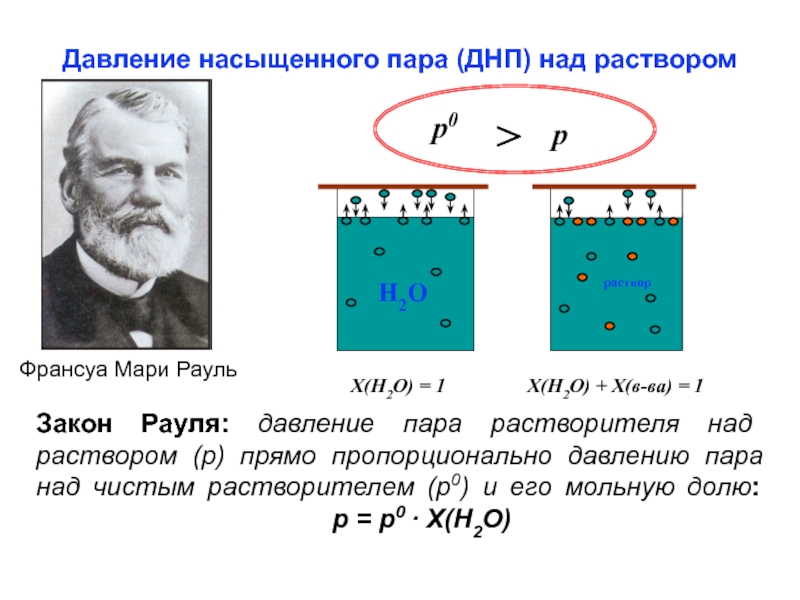
Слайд 20Давление насыщенного пара (ДНП) над раствором
Франсуа Мари Рауль
p0
>
p
Х(Н2О) = 1
Х(Н2О) + Х(в-ва) = 1
Закон Рауля: давление пара
растворителя над раствором (р) прямо пропорционально давлению пара над чистым растворителем (p0) и его мольную долю:
р = р0 · Х(Н2О) Слайд 21Вторая формулировка закона Рауля:
относительное понижение давления насыщенного пара
растворителя (p0) над раствором (p) нелетучего неэлектролита пропорционально мольной доле
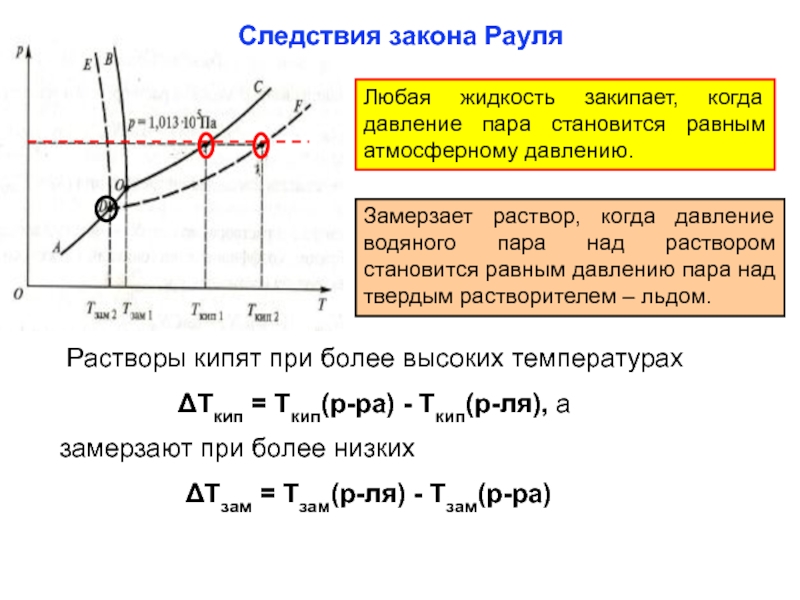
(Х) растворенного вещества:Слайд 23Следствия закона Рауля
Любая жидкость закипает, когда давление пара становится равным
атмосферному давлению.
Замерзает раствор, когда давление водяного пара над раствором становится
равным давлению пара над твердым растворителем – льдом. Растворы кипят при более высоких температурах
Ткип = Ткип(р-ра) - Ткип(р-ля), а
замерзают при более низких
Тзам = Тзам(р-ля) - Тзам(р-ра)
Слайд 24Понижение температуры замерзания и повышение температуры кипения прямопропорционально моляльной концентрации
раствора:
Т = К• mс,
где
ΔТ – понижение температуры замерзания и
повышения температуры кипения раствора;К – криоскопическая или эбулиоскопическая константа растворителя,
mс - моляльная концентрация раствора (моль/кг).
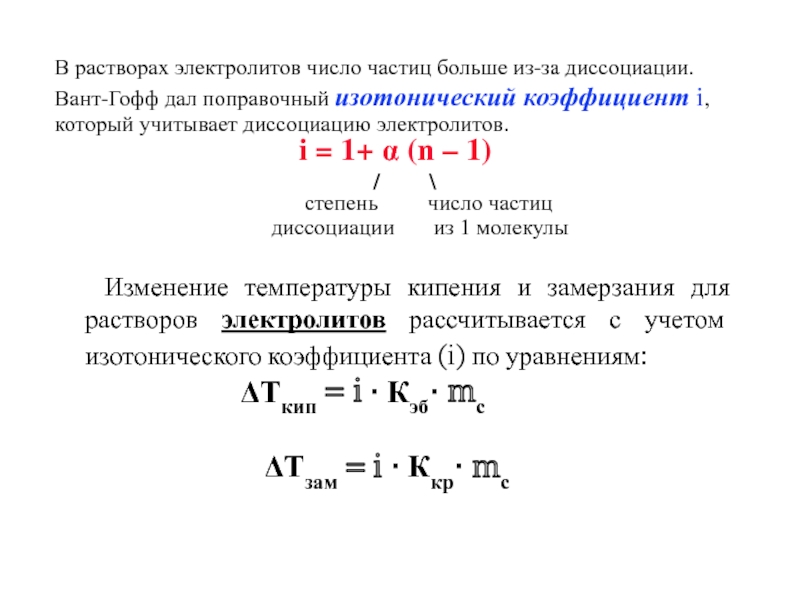
Слайд 26В растворах электролитов число частиц больше из-за диссоциации.
Вант-Гофф дал
поправочный изотонический коэффициент i,
который учитывает диссоциацию электролитов.
i = 1+
α (n – 1)/ \
степень число частиц
диссоциации из 1 молекулы
Изменение температуры кипения и замерзания для растворов электролитов рассчитывается с учетом изотонического коэффициента (i) по уравнениям:
Ткип = i · Кэб· mс
Тзам = i · Ккр· mс
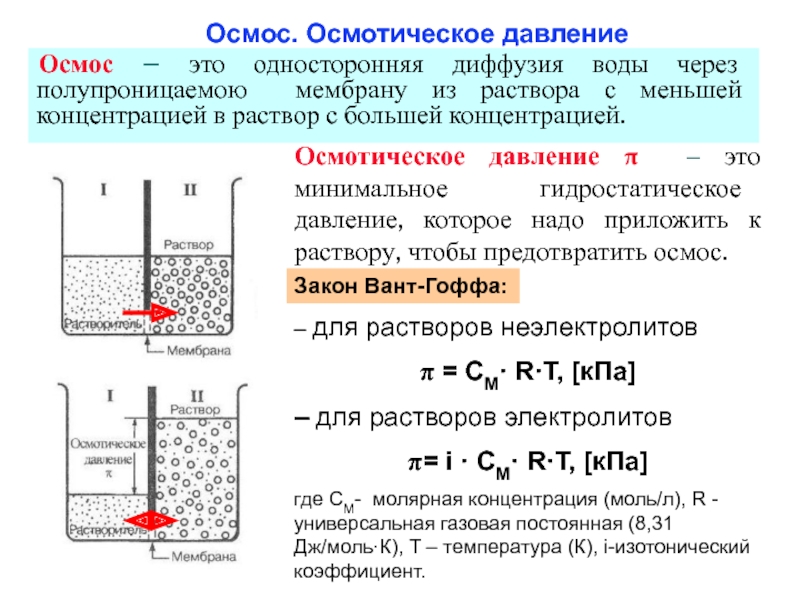
Слайд 27 Осмос. Осмотическое давление
Осмос – это односторонняя диффузия воды
через полупроницаемою мембрану из раствора с меньшей концентрацией в раствор
с большей концентрацией.Осмотическое давление π – это минимальное гидростатическое давление, которое надо приложить к раствору, чтобы предотвратить осмос.
– для растворов неэлектролитов
= СМ· R·T, [кПа]
– для растворов электролитов
= i · СМ· R·T, [кПа]
где СМ- молярная концентрация (моль/л), R - универсальная газовая постоянная (8,31 Дж/моль·К), T – температура (К), i-изотонический коэффициент.
Закон Вант-Гоффа:
Слайд 28 В организме осмотическое давление должно быть постоянным (изоосмия):
(плазмы)=7,7 атм= 740-780 кПа = 280-310 мОсм/л
Сосм = СM · i, [Осм/л]В медицинской практике применяют изотонические растворы. Это растворы, осмотическое давление которых равно (плазмы) (0,9 % NaCl – физраствор,
5 % раствор глюкозы).
1 = 2
Слайд 29 Растворы, у которых больше, чем у
(плазмы) , называются гипертоническими.
В медицине они применяются
для очистки ран от гноя (10 % NaCl), для удаления аллергических оттенков (10 % CaCl2, 20 % – глюкоза), в качестве слабительных лекарств (Na2SO4∙10H2O, MgSO4∙7H2O).
Экзоосмос (движение воды из клетки в плазму) приводит к сморщиванию оболочки клетки вызывая плазмолиз
1 < 2
Слайд 30 Растворы, у которых меньше, чем у
(плазмы) , называются гипотоническими. В медицине они практически не применяются.
Эндоосмос
(движение воды в клетку из плазмы) приводит к набуханию оболочки клетки с появлением напряженного состояния – тургора. Однако при большой разнице концентраций происходит разрушение клеточной мембраны и лизис клетки, что является причиной гемолиза.1 < 2
Слайд 31Значение осмоса
упругость, тургор клеток
эластичность тканей,
форма органов
усвоение пищи, образование лимфы, мочи, кала
действие
лекарствЗа счет осмоса вода в организме распределяется между кровью, тканями, клетками.
Слайд 32Методы, основанные на изучении коллигативных свойств растворов
осмометрия – измерение π,
криоскопия – измерение ΔТзам (р-ра),
эбулиоскопия – измерение ΔТкип (р-ра).
Слайд 33Применяются для определения :
молекулярных масс различных
веществ, чаще всего
биополимеров (белков);суммарной концентрации всех
растворенных частиц;
изотонического коэффициента, степени и
константы диссоциации.
Слайд 34Криоскопическому методу исследования отдается предпочтение, поскольку температуру замерзания можно измерить
с большой точностью и при низких температурах не происходит изменений
в структуре растворенных веществ и растворителя.При выборе растворителя предпочтение следует отдавать растворителю с большей криоскопической константой.