Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ВВЕДЕНИЕ В КЛИНИЧЕСКУЮ ИММУНОЛОГИЮ ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ
Содержание
- 1. ВВЕДЕНИЕ В КЛИНИЧЕСКУЮ ИММУНОЛОГИЮ ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ
- 2. ПЛАН ЛЕКЦИИКлиническая иммунология: определение, предмет и
- 3. КЛИНИЧЕСКАЯ ИММУНОЛОГИЯРаздел медицины, использующий знания об иммунной системе для обеспечения адекватной жизнедеятельности организма
- 4. ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ
- 5. ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ
- 6. ПРЕДМЕТ ИЗУЧЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИзаболевания, связанные с
- 7. ЗАДАЧИ КЛИНИЧЕСКОЙ ИММУНОЛОГИИОбследование, диагностика и лечение больных
- 8. РАЗДЕЛЫ КЛИНИЧЕСКОЙ ИММУНОЛОГИИПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯЛЕЧЕБНАЯ ИММУНОЛОГИЯТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯИММУНОЛОГИЯ РЕПРОДУКЦИИ
- 9. ПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯСПЕЦИФИЧЕСКАЯ ИММУНОПРОФИЛАКТИКА (ВАКЦИНАЦИЯ) – ПРОФИЛАКТИКА ОТНОСИТЕЛЬНО
- 10. ЛЕЧЕБНАЯ ИММУНОЛОГИЯИММУННАЯ НЕДОСТАТОЧНОСТЬ
- 11. ИММУННАЯ НЕДОСТАТОЧНОСТЬа) экзоантигенная – связанная с повреждающей
- 12. ИММУНОПАТОЛОГИЯИЗВРАЩЕНИЕ ФУНКЦИЙ КОМПОНЕНТОВ ИЛИ ИММУННОЙ СИСТЕМЫ В ЦЕЛОМАЛЛЕРГИЧЕСКИЕ ЗАБОЛЕВАНИЯАУТОИММУННЫЕ ЗАБОЛЕВАНИЯ
- 13. СОЧЕТАННЫЙ ПРОЦЕССЛИМФОПРОЛИФЕРАТИВНЫЙ СИНДРОМИММУНОПРОЛИФЕРАТИВНЫЕ ЗАБОЛЕВАНИЯГРАНУЛЕМАТОЗНЫЕ ПРОЦЕССЫ
- 14. ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯРАЗДЕЛ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ, ИЗУЧАЮЩИЙ МЕХАНИЗМЫ ТРАНСПЛАНТАЦИИ ТКАНЕЙ И ОРГАНОВ
- 15. ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТЭТО ИММУННЫЕ РЕАКЦИИ, РАЗВИВАЕМЫЕ ОРГАНИЗМОМ –
- 16. Судьба трансплантата - приживление или отторжение -
- 17. Пересадка органов и тканей в историческом аспектеИммунологическая
- 18. Пересадка органов и тканей в историческом аспекте3.
- 19. ГЕНЕТИЧЕСКИЕ ЗАКОНЫ ТРАНСПЛАНТАЦИИПри пересадки тканей внутри линии
- 20. При реципрокной трансплантации кожи у генетически идентичных
- 21. Механизмы трансплантационного иммунитета существует много генетических
- 22. Механизмы трансплантационного иммунитета Иммунный ответ на
- 23. ОТТОРЖЕНИЕ ТРАНСПЛАНТАТАСВЕРХОСТРОЕ (в первые часы после пересадки)ОСТРОЕ
- 24. ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТАРазвивается при наличии в
- 25. ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА Комплексы, состоящие
- 26. ПРЕДСУЩЕСТВУЮЩИЕ АНТИТЕЛАпри пересадке тканей обязательно исследуют наличие
- 27. ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТАПервичным механизмом распознавания является
- 28. ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА6. Цитокины Тh1 (ФНОα
- 29. Гистологическая картина острого отторжения трансплантированной почки -
- 30. ПАТОГЕНЕЗ ХРОНИЧЕСКОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТАРазвивается в случае, когда
- 31. Активированные АПК Тх-клетки выделяют цитокины, из которых
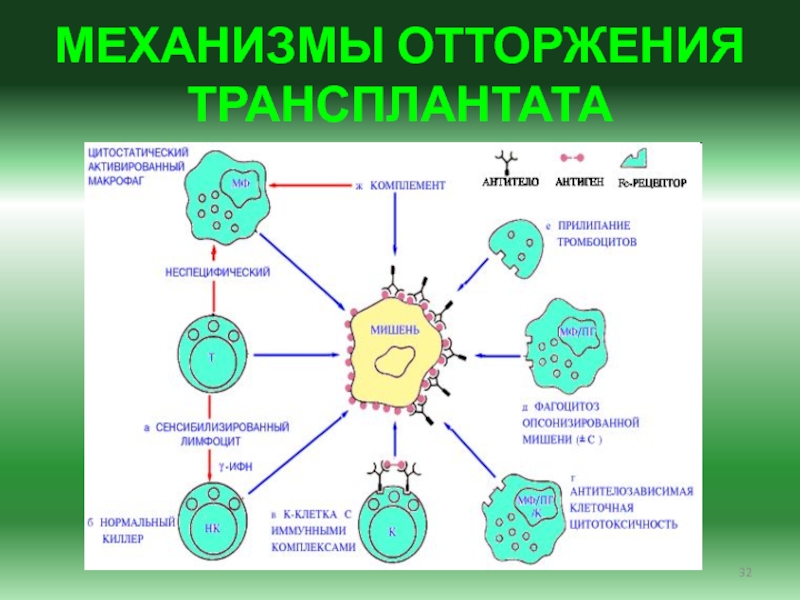
- 32. МЕХАНИЗМЫ ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
- 33. ВТОРИЧНАЯ РЕАКЦИЯ ОТТОРЖЕНИЯРеакцию на повторную подсадку ткани
- 34. Характер отторжения трансплантата зависит от развития иммунологической
- 35. Слайд 35
- 36. «ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА»Ткани трансплантатов содержат иммунокомпетентные и
- 37. Иммунокомпетентные клетки донора А введены реципиенту С,
- 38. КЛИНИЧЕСКАЯ КАРТИНА РТПХПроявляется у мышей через 7
- 39. ПОДХОДЫ К ПРЕОДОЛЕНИЮ ТРАНСПЛАНТАЦИОННОЙ РЕАКЦИИПОДБОР ДОНОРОВ ТРАНСПЛАНТАТОВ
- 40. Индекс гистосовместимости25% - если донор и реципиент
- 41. РЕЗЮМЕНе существует каких-либо специфических механизмов трансплантационного иммунитета,
- 42. ЭФФЕКТОРНЫЕ МЕХАНИЗМЫ ТРАНСПЛАНТАЦИОННОГО ИММУНИТЕТАПрямое действие цитотоксических Т-лфПрямое
- 43. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2
ПЛАН ЛЕКЦИИ
Клиническая иммунология: определение, предмет и задачи
Трансплантационная иммунология.
Механизмы трансплантационного
иммунитета.
тканей в клинике. Подходы к преодолению трансплантационной реакции.Слайд 3КЛИНИЧЕСКАЯ ИММУНОЛОГИЯ
Раздел медицины, использующий знания об иммунной системе для обеспечения
адекватной жизнедеятельности организма
Слайд 4ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ МЕДИЦИНЫ
Наработка большого количества
иммунных тестов и методов иммунологического обследования, способствующих лучшей и ранней
диагностике заболеваний, контролю эффективности их лечения.Расширение знаний о роли иммунных механизмов в развитии заболеваний и возможности влияния на систему иммунитета, что значительно изменяет течение этих заболеваний
Слайд 5ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ МЕДИЦИНЫ
3. Быстрое увеличение
уровня выявления больных с иммунной недостаточностью разного генеза.
4. Выявление заболеваний,
связанных с иммунными нарушениями на ранних этапах становления иммунной системы для своевременной иммунокоррекции и иммунореабилитации.5. Активное развитие иммунореабилитации и появление новых методов, основанных на современных представлениях о функционировании иммунной системы.
6. Расширение возможностей терапевтического воздействия на иммунную систему часто и длительно болеющих детей с целью уменьшения их количества.
Слайд 6ПРЕДМЕТ ИЗУЧЕНИЯ
КЛИНИЧЕСКОЙ ИММУНОЛОГИИ
заболевания, связанные с дисфункциями иммунной системы
и
заболевания, в которых иммунным реакциям принадлежит главенствующая роль
Слайд 7ЗАДАЧИ
КЛИНИЧЕСКОЙ ИММУНОЛОГИИ
Обследование, диагностика и лечение больных с заболеваниями или патологическими
процессами, развивающимися в результате нарушений иммунных механизмов
Обследование, диагностика и лечение
больных, у которых главной частью терапии или профилактики являются иммунологические манипуляцииСлайд 8РАЗДЕЛЫ
КЛИНИЧЕСКОЙ ИММУНОЛОГИИ
ПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯ
ЛЕЧЕБНАЯ ИММУНОЛОГИЯ
ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ
ИММУНОЛОГИЯ РЕПРОДУКЦИИ
Слайд 9ПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯ
СПЕЦИФИЧЕСКАЯ ИММУНОПРОФИЛАКТИКА (ВАКЦИНАЦИЯ) – ПРОФИЛАКТИКА ОТНОСИТЕЛЬНО НЕБОЛЬШОГО КОЛИЧЕСТВА ЭТИОЛОГИЧЕСКИ
КОНКРЕТНЫХ ЗАБОЛЕВАНИЙ
НЕСПЕЦИФИЧЕСКАЯ ИММУНОПРОФИЛАКТИКА (ПРОФИЛАКТИЧЕСКАЯ ИММУНОКОРРЕКЦИЯ) – ПРОФИЛАКТИКА ЭТИОЛОГИЧЕСКИ НЕКОНКРЕТНЫХ ЗАБОЛЕВАНИЙ
(ОРВИ) ИЛИ В СИТУАЦИИ, КОГДА СУММАРНОЕ КОЛИЧЕСТВО АНТИГЕНОВ ТАК ВЕЛИКО, ЧТО БЕССМЫСЛЕННО ВАКЦИНИРОВАТЬ ПРОТИВ КАЖДОГО ИЗ НИХ (ЭКОЛОГИЧЕСКОЕ НЕБЛАГОПОЛУЧИЕ)Слайд 11ИММУННАЯ НЕДОСТАТОЧНОСТЬ
а) экзоантигенная – связанная с повреждающей инициативой экзоантигенов (острые
или хронические воспалительные процессы)
б) эндоантигенная – при которой инициация развития
патологии принадлежит эндоантигенам (опухолевые и склеротические процессы)в) смешанная – когда экзогенная антигенная инициатива может вызвать эндогенную антигенную агрессию (вирус Эпштейна-Барра и лимфома Беркитта)
Слайд 12ИММУНОПАТОЛОГИЯ
ИЗВРАЩЕНИЕ ФУНКЦИЙ КОМПОНЕНТОВ ИЛИ ИММУННОЙ СИСТЕМЫ В ЦЕЛОМ
АЛЛЕРГИЧЕСКИЕ ЗАБОЛЕВАНИЯ
АУТОИММУННЫЕ ЗАБОЛЕВАНИЯ
Слайд 13СОЧЕТАННЫЙ ПРОЦЕСС
ЛИМФОПРОЛИФЕРАТИВНЫЙ СИНДРОМ
ИММУНОПРОЛИФЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ
ГРАНУЛЕМАТОЗНЫЕ ПРОЦЕССЫ
Слайд 14
ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ
РАЗДЕЛ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ, ИЗУЧАЮЩИЙ МЕХАНИЗМЫ ТРАНСПЛАНТАЦИИ ТКАНЕЙ И ОРГАНОВ
Слайд 15ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТ
ЭТО ИММУННЫЕ РЕАКЦИИ, РАЗВИВАЕМЫЕ ОРГАНИЗМОМ – РЕЦИПИЕНТОМ ПРОТИВ АНТИГЕНОВ
ПЕРЕСАЖЕННОЙ ТКАНИ ИЛИ ОРГАНА
В КЛИНИКЕ РЕАЛИЗАЦИЯ ТРАНСПЛАНТАЦИОННОГО ИММУНИТЕТА ПРОЯВЛЯЕТСЯ РЕАКЦИЕЙ
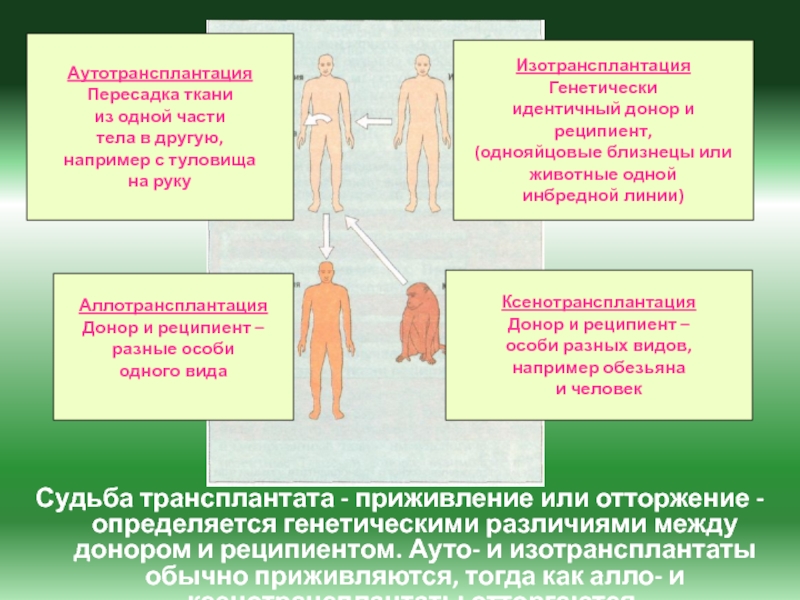
ОТТОРЖЕНИЯ ТРАНСПЛАНТАТАСлайд 16Судьба трансплантата - приживление или отторжение - определяется генетическими различиями
между донором и реципиентом. Ауто- и изотрансплантаты обычно приживляются, тогда
как алло- и ксенотрансплантаты отторгаются.Ксенотрансплантация
Донор и реципиент –
особи разных видов,
например обезьяна
и человек
Изотрансплантация
Генетически
идентичный донор и реципиент,
(однояйцовые близнецы или
животные одной
инбредной линии)
Аллотрансплантация
Донор и реципиент –
разные особи
одного вида
Аутотрансплантация
Пересадка ткани
из одной части
тела в другую,
например с туловища
на руку
Слайд 17Пересадка органов и тканей в историческом аспекте
Иммунологическая природа отторжения чужеродных
трансплантатов была доказана в 40-е годы ХХ века в серии
экспериментов Р.Medawar, который продемонстрировал возможность развития сенсибилизации и вторичного ответа, а также роль сенсибилизированных лимфоцитов в качестве ключевых факторов отторжения.Убедительные доказательства связи трансплантационного иммунитета с лимфоцитами были получены в опытах E.N.Mitchison по переносу состояния сенсибилизации к аллогенным тканям с лимфоцитами из лимфатических узлов.
Слайд 18Пересадка органов и тканей в историческом аспекте
3. С использованием генетически
чистых линий мышей были связаны основные успехи в анализе генетической
детерминации и механизмах трансплантационного иммунитета.4. Важный прорыв произошел после открытия и изучения системы ГКГС.
5. В связи с пересадками тканей мышей с использованием чистых линий и их гибридов G.D.Shell сформулировал генетические законы трансплантации.
Слайд 19ГЕНЕТИЧЕСКИЕ ЗАКОНЫ ТРАНСПЛАНТАЦИИ
При пересадки тканей внутри линии ткани приживаются, а
при пересадках между линиями – отторгаются
Ткани от гибридов F1, пересаженные
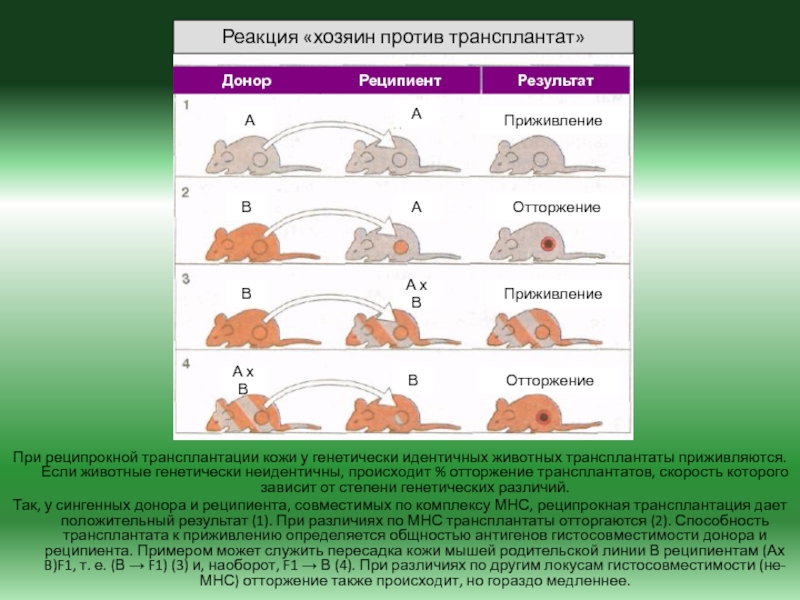
животным обеих родительских линий, не приживаются, тогда как пересадка тканей в обратном «направлении» не вызывает реакции отторжения (т.е. факторы, обусловливающие несовместимость тканей, наследуются кодоминантно)Слайд 20При реципрокной трансплантации кожи у генетически идентичных животных трансплантаты приживляются.
Если животные генетически неидентичны, происходит % отторжение трансплантатов, скорость которого
зависит от степени генетических различий.Так, у сингенных донора и реципиента, совместимых по комплексу МНС, реципрокная трансплантация дает положительный результат (1). При различиях по МНС трансплантаты отторгаются (2). Способность трансплантата к приживлению определяется общностью антигенов гистосовместимости донора и реципиента. Примером может служить пересадка кожи мышей родительской линии В реципиентам (Ах B)F1, т. е. (В → F1) (3) и, наоборот, F1 → В (4). При различиях по другим локусам гистосовместимости (не-МНС) отторжение также происходит, но гораздо медленнее.
Реакция «хозяин против трансплантат»
Донор
Реципиент
Результат
Приживление
Отторжение
Приживление
Отторжение
А
А
А
А х В
А х В
В
В
В
Слайд 21Механизмы трансплантационного иммунитета
существует много генетических локусов, обусловливающих гистосовместимость,
но только с одним локусом МНС (II класса) связано развитие
сильной трансплантационной реакции, приводящей к отторжению подсаженных тканей в течение 2 недель. При этом отторжение невозможно предотвратить и подавить иммунодепрессивными воздействиями. Это связано с развитием Th1- зависимого иммунного ответаСлайд 22Механизмы трансплантационного иммунитета
Иммунный ответ на трансплантат обусловлен распознаванием
антигенов HLA донора лимфоцитами реципиента.
Это вызывает активацию
Т-хелперов, которые, в свою очередь, стимулируют пролиферацию В-лимфоцитов и цитотоксических Т-лимфоцитов. Слайд 23ОТТОРЖЕНИЕ ТРАНСПЛАНТАТА
СВЕРХОСТРОЕ (в первые часы после пересадки)
ОСТРОЕ (в течение первых
2 – 3 недель)
ХРОНИЧЕСКОЕ (спустя месяцы, годы)
Слайд 24ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
Развивается при наличии в организме донора ПРЕДСУЩЕСТВУЮЩИХ
АНТИТЕЛ – иммуноглобулинов против некоторых «чужих» разновидностей молекул гистосовместимости. Наличие
таких антител свидетельствует о том, что данный организм уже встречался с чужеродными клетками представителя того же биологического вида: после переливания препаратов крови или беременности.Циркулирующие предсуществующие антитела практически немедленно связываются с соответствующими молекулами гистосовместимости трансплантата, что приводит к активации комплемента по классическому пути и оказанием повреждающего действия МАК на эндотелий, а также способствует развитию острого воспаления.
Слайд 25ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
Комплексы, состоящие из антигенов трансплантата
и антител реципиента, активируют свертывание крови и приводят к тромбозу
сосудов трансплантата.сверхострое отторжение трансплантата является результатом реализации иммунологической памяти
В первые часы после трансплантации еще отсутствует надежный медикаментозный иммуносупрессивный фон
Слайд 26ПРЕДСУЩЕСТВУЮЩИЕ АНТИТЕЛА
при пересадке тканей обязательно исследуют наличие предсуществующих антител в
организме реципиента к основыми разновидностям молекул гистосовместимости донора.
При обнаружении таких
антител пересадка тканей данного донора противопоказанаНаиболее опасными считаются тепловые антитела (лабораторно определяются при Т=370 С) – направлены против HLA I класса Т-лф
Холодовые антитела (Т=80 С) направлены против HLA II класса В-лф и наделены блокирующими свойствами (это хороший прогностический признак при трансплантации)
Слайд 27ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
Первичным механизмом распознавания является антигенная презентация иммуногенных
пептидов трансплантата дендритными клетками пересаженного органа, либо дендритными клетками организма-реципиента
Второй
механизм связан с деятельностью естественных киллеров, которые уничтожают клетки трансплантата, т.к. они не содержат молекул HLA I класса реципиента.После антигенной презентации происходит созревание и размножение Т-хелперов 1 типа, несущих специфические рецепторы к антигенам трансплантата.
Накапливаются Т-цитотоксические лимфоциты, которые атакуют клетки трансплантата, уничтожая их путем апоптоза
Апоптотические тельца фагоцитируются макрофагами, что способствует поддержанию иммунного ответа
Слайд 28ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
6. Цитокины Тh1 (ФНОα и ФНОβ) оказывают
прямое повреждающее действие на трансплантат.
7. ИФНγ повышает функциональную активность
NK и макрофагов, что способствует армированию этих клеток8. Все это обеспечивает разворачивание реакций антителозависимой клеточно-опосредованной цитотоксичности
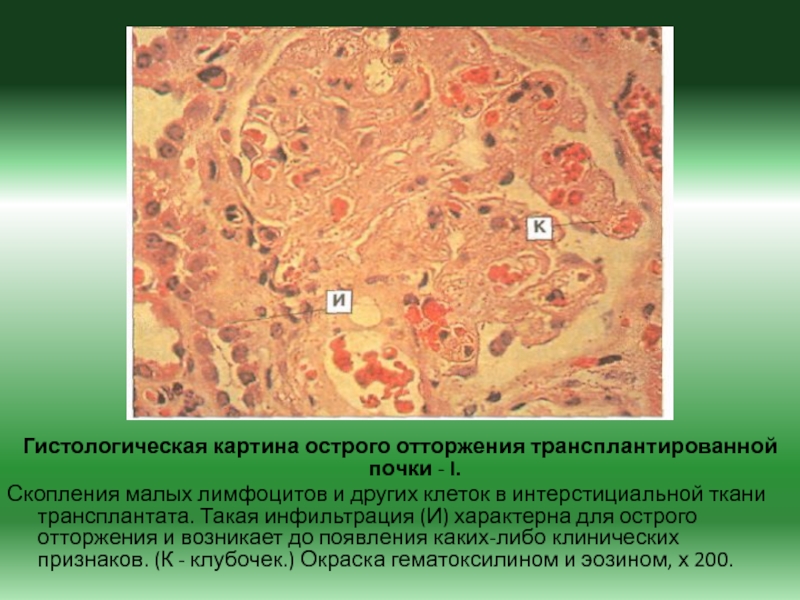
Слайд 29Гистологическая картина острого отторжения трансплантированной почки - I.
Скопления малых
лимфоцитов и других клеток в интерстициальной ткани трансплантата. Такая инфильтрация
(И) характерна для острого отторжения и возникает до появления каких-либо клинических признаков. (К - клубочек.) Окраска гематоксилином и эозином, х 200.Слайд 30ПАТОГЕНЕЗ ХРОНИЧЕСКОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
Развивается в случае, когда проводимая иммуносупрессивная терапия
предотвращает реализацию клеточных механизмов острого воспаления
Главную роль играют специфические антитела,
которые распознают антигены эндотелия трансплантата и вызывают активацию факторов врожденного иммунитета (комплемента)Это приводит к прямому повреждающему эффекту (комплемент-опосредованная цитотоксичность)
Хронический воспалительный процесс развивается и за счет высвобождения анафилотоксинов, хемоаттрактантов, кининов, свободных радикалов, медиаторов воспаления
Происходит постепенное склерозирование микроциркуляторного русла и отмирание клеток трансплантата
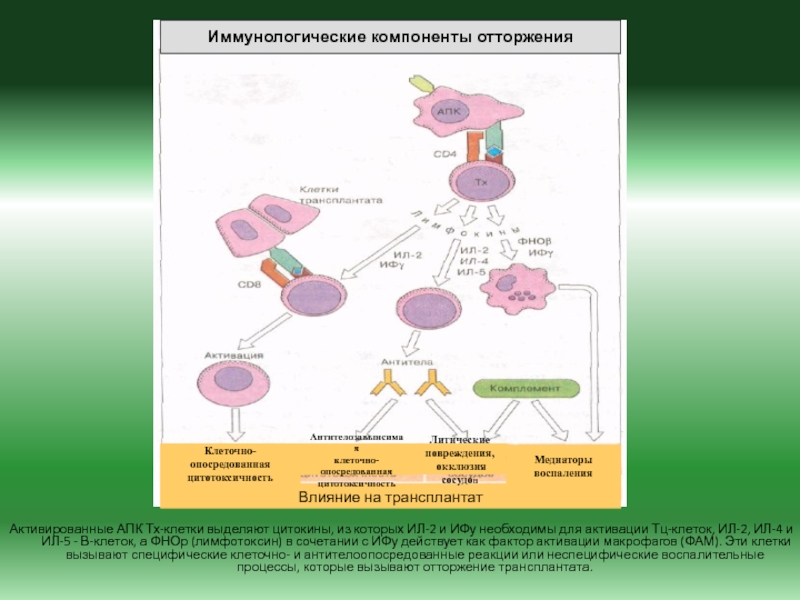
Слайд 31Активированные АПК Тх-клетки выделяют цитокины, из которых ИЛ-2 и ИФу
необходимы для активации Тц-клеток, ИЛ-2, ИЛ-4 и ИЛ-5 - В-клеток,
а ФНОр (лимфотоксин) в сочетании с ИФу действует как фактор активации макрофагов (ФАМ). Эти клетки вызывают специфические клеточно- и антителоопосредованные реакции или неспецифические воспалительные процессы, которые вызывают отторжение трансплантата.Иммунологические компоненты отторжения
Влияние на трансплантат
Клеточно-
опосредованная
цитотоксичность
Антителозавыисимая
клеточно-
опосредованная
цитотоксичность
Медиаторы
воспаления
Литические
повреждения,
окклюзия сосудов
Слайд 33ВТОРИЧНАЯ РЕАКЦИЯ ОТТОРЖЕНИЯ
Реакцию на повторную подсадку ткани от того же
донора называют second-set («второй заход»)
Основное отличие заключается в отсутствие продолжительной
индуктивной фазы с установлением кровоснабжения трансплантатаПри вторичной реакции отторжения, как правило, кровоснабжение не устанавливается, образуется «бледный трансплантат»
Эти сосудистые реакции связывают с действием цитокинов, освобождаемых активированными Т-лф, которые быстро формируются из клеток памяти при их контакте с клетками донора
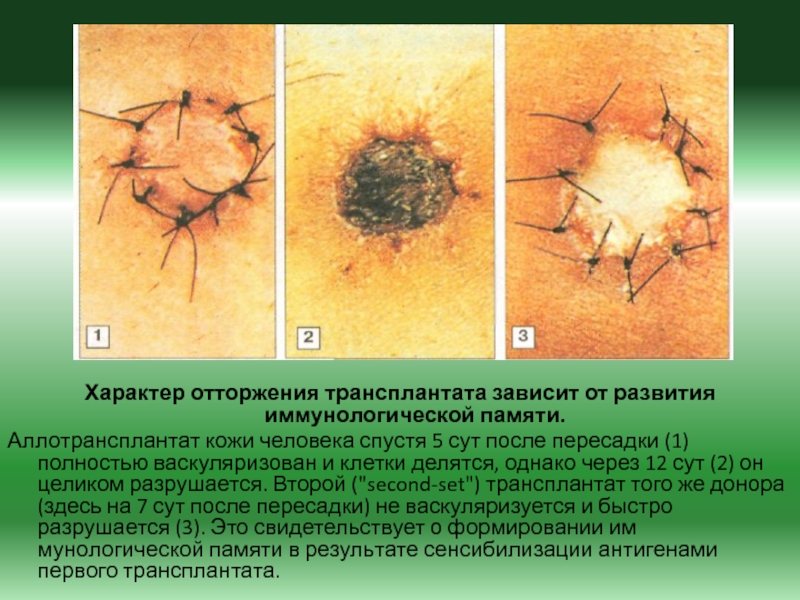
Слайд 34Характер отторжения трансплантата зависит от развития иммунологической памяти.
Аллотрансплантат кожи
человека спустя 5 сут после пересадки (1) полностью васкуляризован и
клетки делятся, однако через 12 сут (2) он целиком разрушается. Второй ("second-set") трансплантат того же донора (здесь на 7 сут после пересадки) не васкуляризуется и быстро разрушается (3). Это свидетельствует о формировании иммунологической памяти в результате сенсибилизации антигенами первого трансплантата.Слайд 35 ТРАНСПЛАНТАЦИЯ
КОСТНОГО
МОЗГАЗанимает обособленное место в практике трансплантации
Осуществляется в форме инфузии суспензированной ткани, а не подсадки солидной ткани
Мобилизируются иные иммунологические механизмы
Существует опасность иммунологической агрессии со стороны подсаженной ткани – развитие реакции «трансплантат против хозяина»
Слайд 36«ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА»
Ткани трансплантатов содержат иммунокомпетентные и антигенпредставляющие клетки («клетки-пассажиры»),
которые могут опосредовать иммунную агрессию против антигенов организма - реципиента
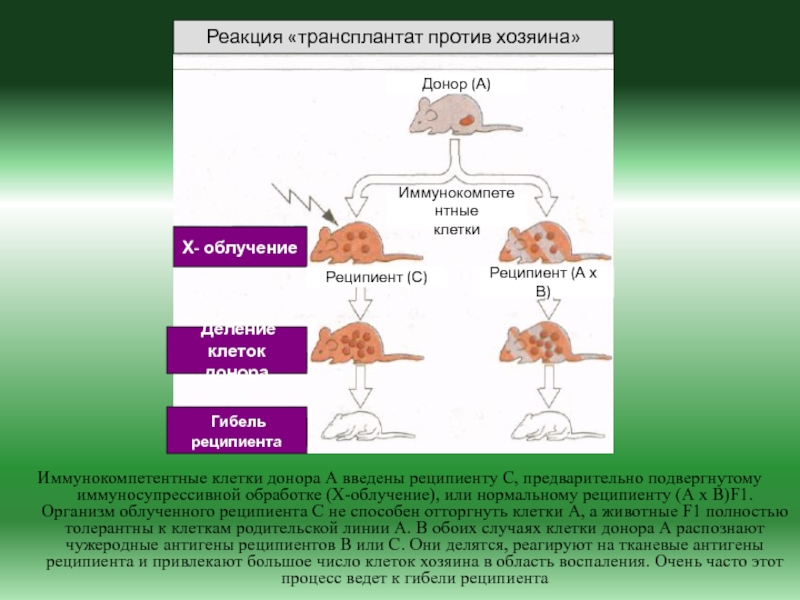
Слайд 37Иммунокомпетентные клетки донора А введены реципиенту С, предварительно подвергнутому иммуносупрессивной
обработке (Х-облучение), или нормальному реципиенту (А х B)F1. Организм облученного
реципиента С не способен отторгнуть клетки А, а животные F1 полностью толерантны к клеткам родительской линии А. В обоих случаях клетки донора А распознают чужеродные антигены реципиентов В или С. Они делятся, реагируют на тканевые антигены реципиента и привлекают большое число клеток хозяина в область воспаления. Очень часто этот процесс ведет к гибели реципиентаРеакция «трансплантат против хозяина»
Х- облучение
Деление клеток
донора
Гибель
реципиента
Реципиент (С)
Реципиент (А х В)
Донор (А)
Иммунокомпетентные
клетки
Слайд 38КЛИНИЧЕСКАЯ КАРТИНА РТПХ
Проявляется у мышей через 7 – 10 дней
, у человека на второй декаде после подсадки клеток (вторичная
болезнь)Происходит увеличение селезенки (при введении клеток внутривенно) или регионарных л/узлов (при введении клеток в стопу)
Системная острая РТПХ может закончиться летально из-за анемии, поражения почек, кахексии и инфекции
Хроническая РТПХ проявляется поражением кожи (дерматит, облысение, язвы) и кишечника (энтерит, колит), нарушением гемопоэза, функций тимуса и ИДС
Слайд 39ПОДХОДЫ К ПРЕОДОЛЕНИЮ ТРАНСПЛАНТАЦИОННОЙ РЕАКЦИИ
ПОДБОР ДОНОРОВ ТРАНСПЛАНТАТОВ ПО ПРИНЦИПУ МАКСИМАЛЬНОГО
СООТВЕТСТВИЯ ПО НАБОРУ МОЛЕКУЛ ГИСТОСОВМЕСТИМОСТИ ОРГАНИЗМУ-РЕЦИПИЕНТУ (особенно по локусам А,
В, С и DR)ИММУНОСУПРЕССИЯ
использование цитостатиков (азатиоприна, сандимуна и др.) и кортикостероидов
Слайд 40Индекс гистосовместимости
25% - если донор и реципиент содержат одинаковые молекулы
HLA одного локуса
50% - два одинаковых локуса HLA
75% - три
одинаковых локуса HLA100% - четыре одинаковых локуса HLA