Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
УРОК ФИЗИКИ ПО ТЕМЕ: СТРОЕНИЕ АТОМА
Содержание
- 1. УРОК ФИЗИКИ ПО ТЕМЕ: СТРОЕНИЕ АТОМА
- 2. Повторение ОРО. Самоконтроль.Объясните, что означают понятия: Запишите
- 3. Постановка цели урока.По структурно- логической схемеизучения сущности
- 4. Модель атома Томсона1903г. - Дж.Дж.Томсон выдвинул гипотезу
- 5. Опыт Резерфорда по определению строения атомаЗолото было
- 6. Некоторые альфа-частицы проходили сквозь фольгу, образуя на
- 7. Опыт показал, что положительный заряд атома сконцентрирован
- 8. Планетарная модель атома Резерфорда
- 9. В 1911г. - Резерфорд предложил современную ядерную
- 10. В 1911 г., спустя месяц после
- 11. Задание
- 12. Слайд 12
- 13. В 1919 году Резерфорд осуществил первое искусственное
- 14. ИренЖолио-Кюри (1897-1956)Фредерик Жолио-Кюри (1900-1958)Джон Чедвик(1920-1998)В 1920 году
- 15. Вернер КарлГейзенберг(1901-1976)Дмитрий Дмитриевич Иваненко (1904-1994)Советский физик Д.
- 16. Обозначение атомных ядерZ- заряд ядра А – массовое числоХ – символ химического элемента
- 17. Конспект по теме «Строение атома» Обязательный
- 18. В 1912 году была разгадана еще
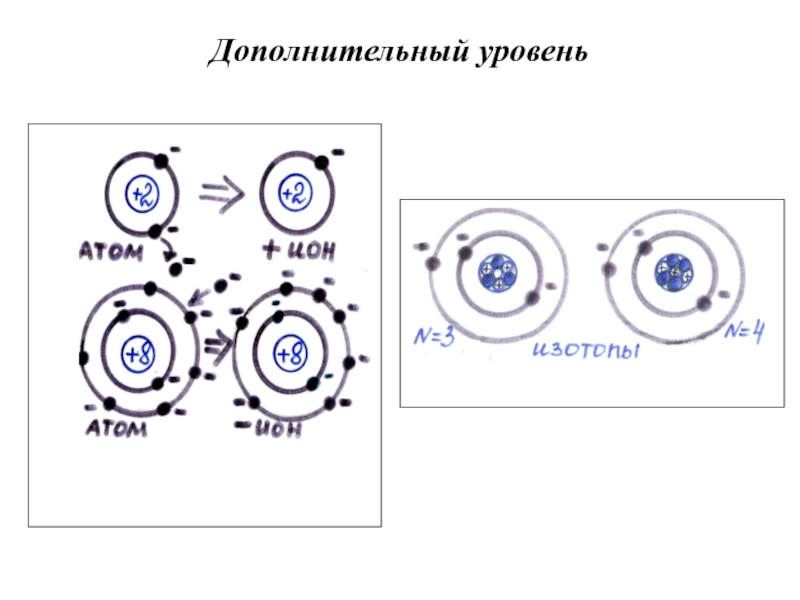
- 19. Дополнительный уровень
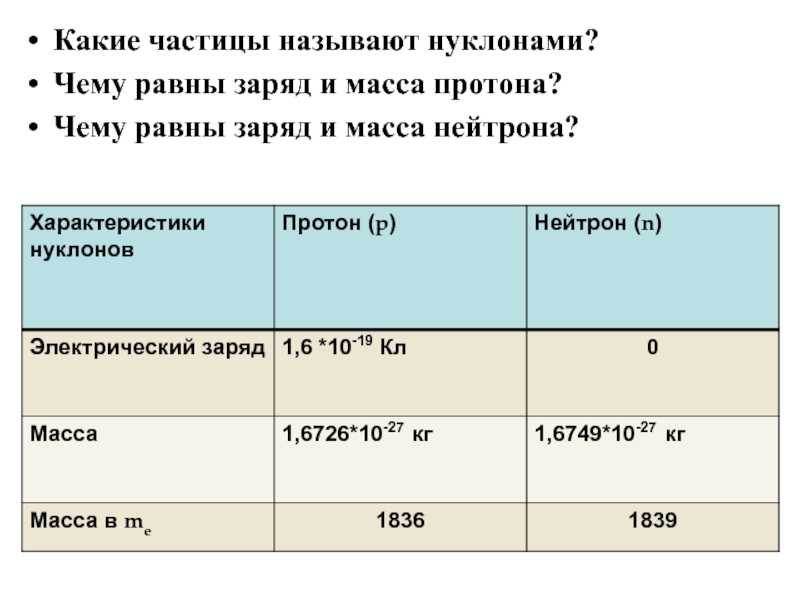
- 20. Какие частицы называют нуклонами?Чему равны заряд и масса протона?Чему равны заряд и масса нейтрона?
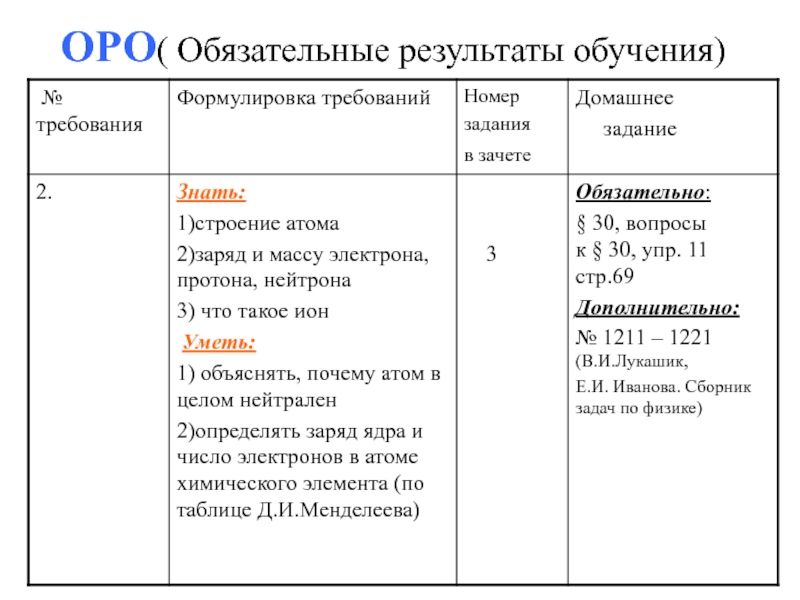
- 21. ОРО( Обязательные результаты обучения)
- 22. Домашнее задание: Обязательно:§ 30, вопросы к §
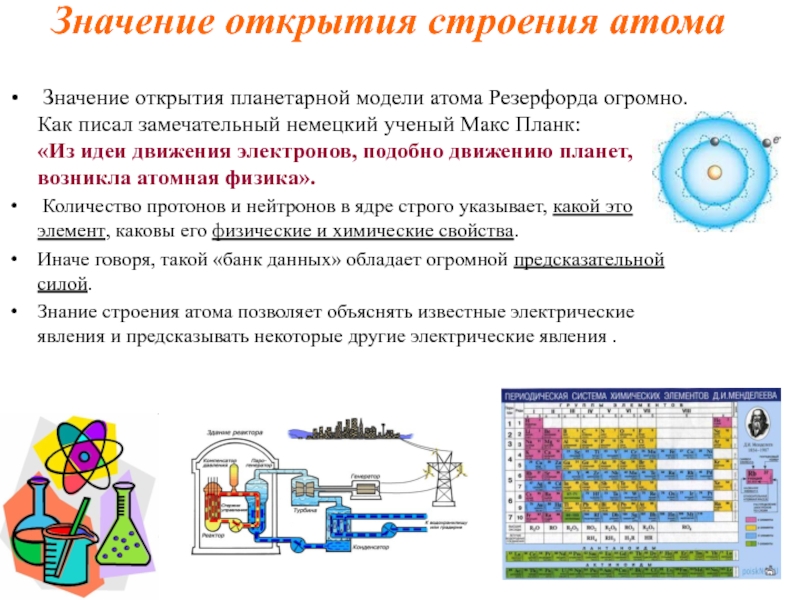
- 23. Значение открытия строения атома Значение открытия планетарной
- 24. ЗаключениеАтом скрывает в себе еще много тайн.
- 25. Скачать презентанцию
Слайды и текст этой презентации
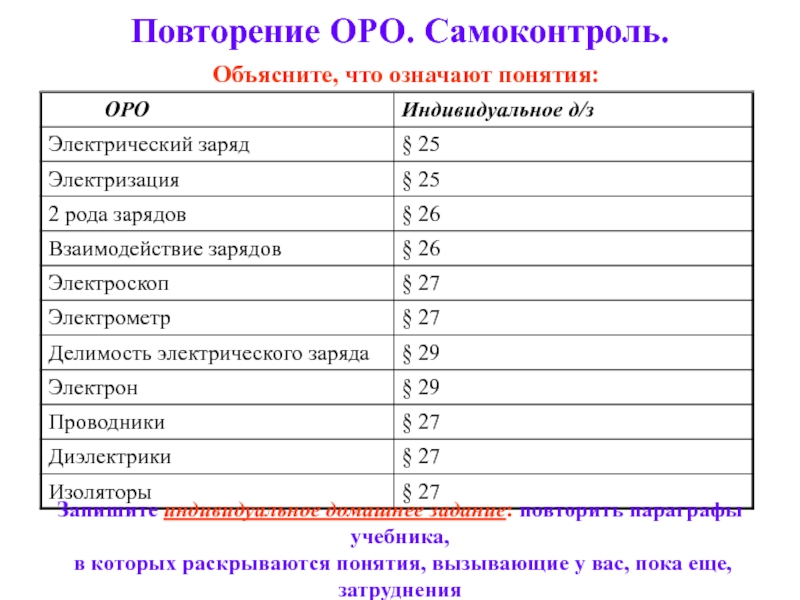
Слайд 2Повторение ОРО. Самоконтроль.
Объясните, что означают понятия:
Запишите индивидуальное домашнее задание:
повторить параграфы учебника,
в которых раскрываются понятия, вызывающие у вас,
пока еще, затрудненияСлайд 3Постановка цели урока.
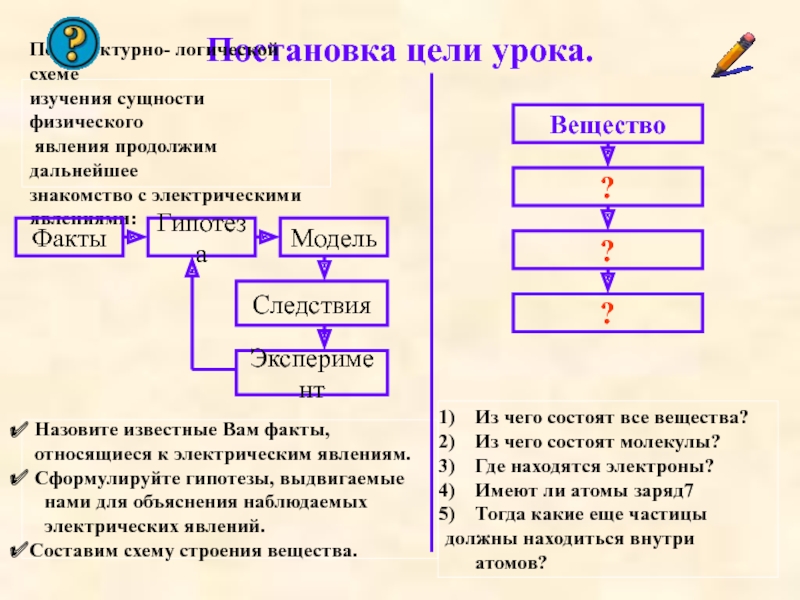
По структурно- логической схеме
изучения сущности физического
явления продолжим
дальнейшее
знакомство с электрическими
явлениями:
Факты
Гипотеза
Эксперимент
Следствия
Модель
Назовите известные Вам факты,
относящиеся к
электрическим явлениям.Сформулируйте гипотезы, выдвигаемые
нами для объяснения наблюдаемых
электрических явлений.
Составим схему строения вещества.
Вещество
?
?
?
Из чего состоят все вещества?
Из чего состоят молекулы?
Где находятся электроны?
Имеют ли атомы заряд7
Тогда какие еще частицы
должны находиться внутри атомов?
Слайд 4Модель атома Томсона
1903г. - Дж.Дж.Томсон выдвинул гипотезу о том, что
электрон находится внутри атома. Но атом в целом нейтральный, поэтому ученый
предположил, что отрицательныеэлектроны окружены в атоме положительно заряженным веществом. Атом,
по мысли Дж. Томсона, очень похож на "пудинг с изюмом", где "каша" –
положительно заряженное вещество атома., а электроны- " изюм" в ней.
«Истина – это то, что выдерживает проверку опытом»
А. Эйнштейн
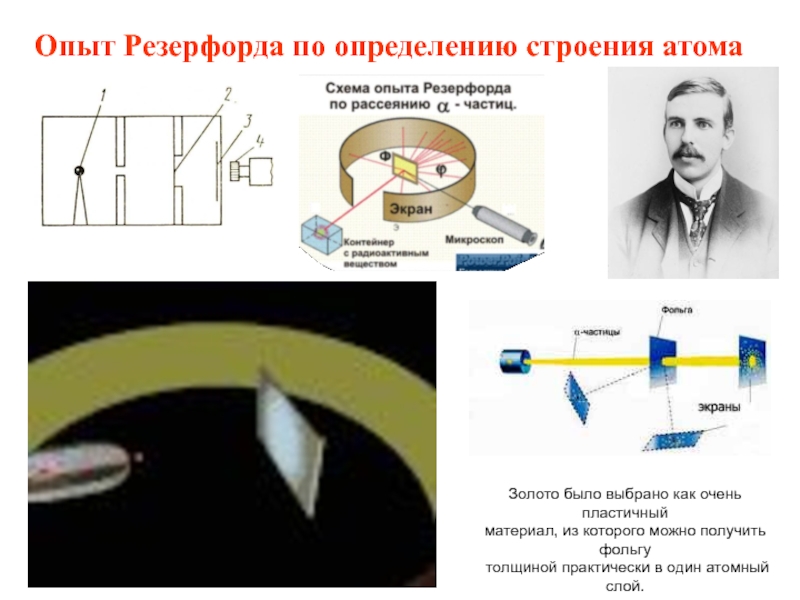
Слайд 5Опыт Резерфорда по определению строения атома
Золото было выбрано как очень
пластичный
материал, из которого можно получить фольгу
толщиной практически в
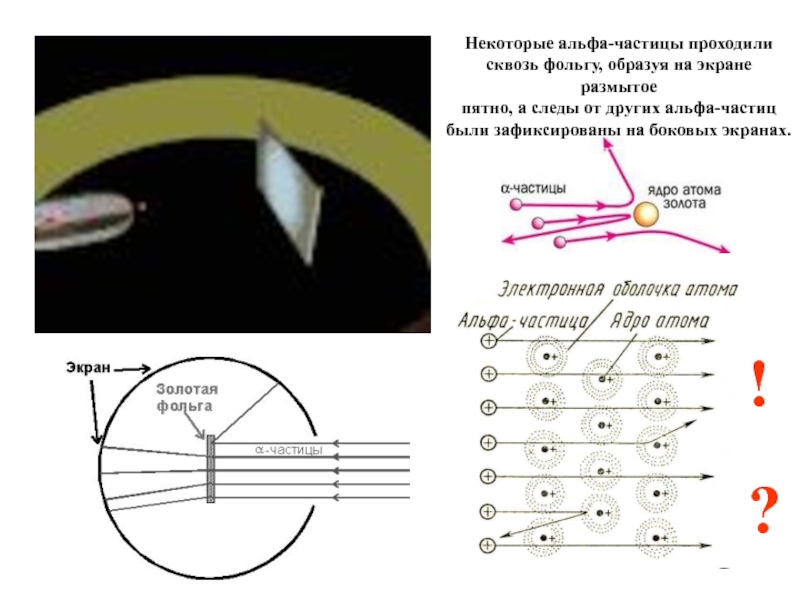
один атомный слой.Слайд 6Некоторые альфа-частицы проходили
сквозь фольгу, образуя на экране размытое
пятно,
а следы от других альфа-частиц
были зафиксированы на боковых экранах.
!
?
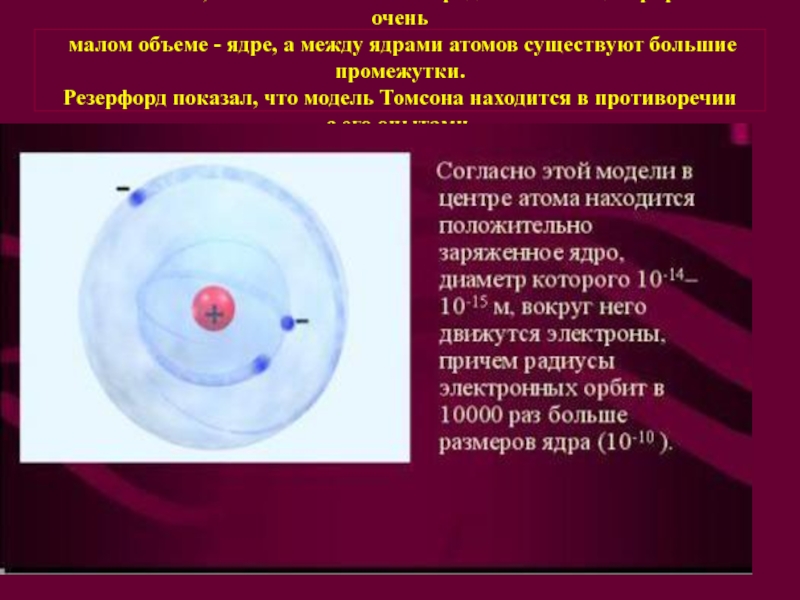
Слайд 7Опыт показал, что положительный заряд атома сконцентрирован в очень
малом
объеме - ядре, а между ядрами атомов существуют большие промежутки.
Резерфорд показал, что модель Томсона находится в противоречии
с его опытами.
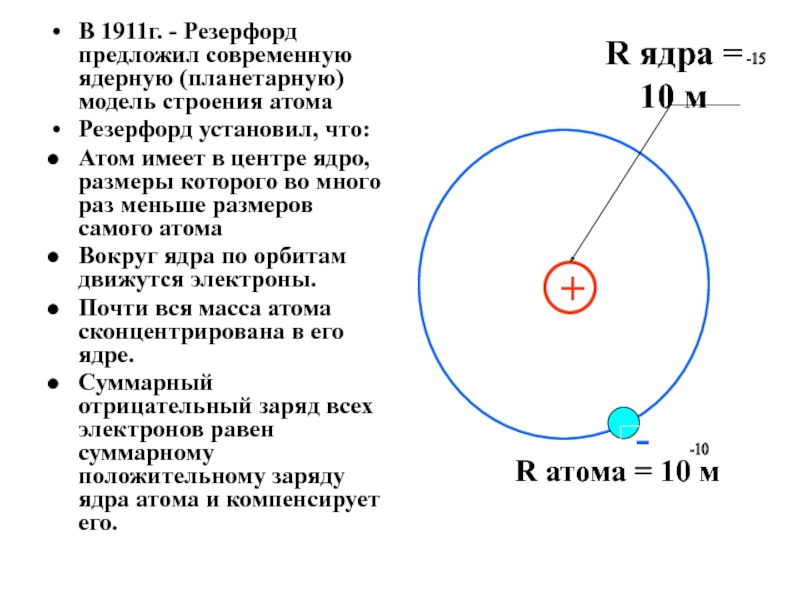
Слайд 9В 1911г. - Резерфорд предложил современную ядерную (планетарную) модель строения
атома
Резерфорд установил, что:
Атом имеет в центре ядро, размеры которого во
много раз меньше размеров самого атома Вокруг ядра по орбитам движутся электроны.
Почти вся масса атома сконцентрирована в его ядре.
Суммарный отрицательный заряд всех электронов равен суммарному положительному заряду ядра атома и компенсирует его.
+
-
R ядра = 10 м
-15
R атома = 10 м
-10
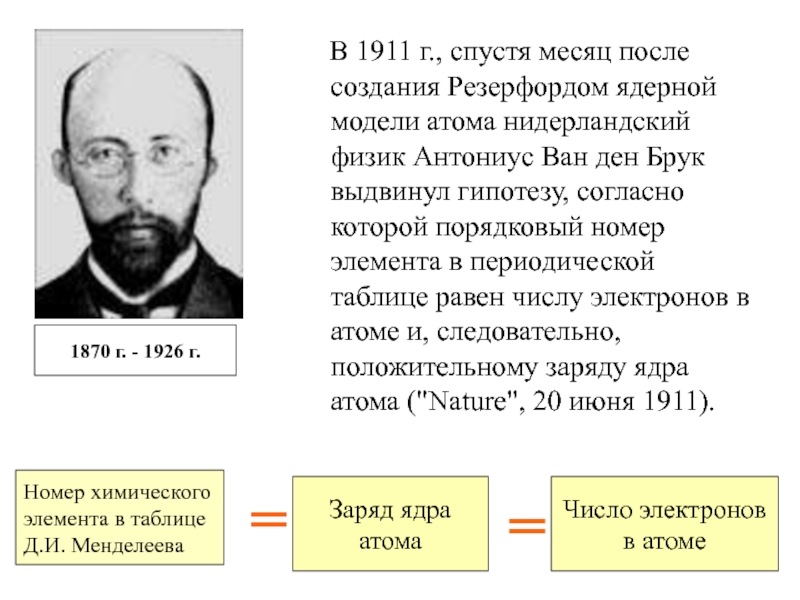
Слайд 10 В 1911 г., спустя месяц после создания Резерфордом ядерной модели
атома нидерландский физик Антониус Ван ден Брук выдвинул гипотезу, согласно
которой порядковый номер элемента в периодической таблице равен числу электронов в атоме и, следовательно, положительному заряду ядра атома ("Nature", 20 июня 1911).1870 г. - 1926 г.
Номер химического
элемента в таблице
Д.И. Менделеева
=
Заряд ядра атома
=
Число электронов
в атоме
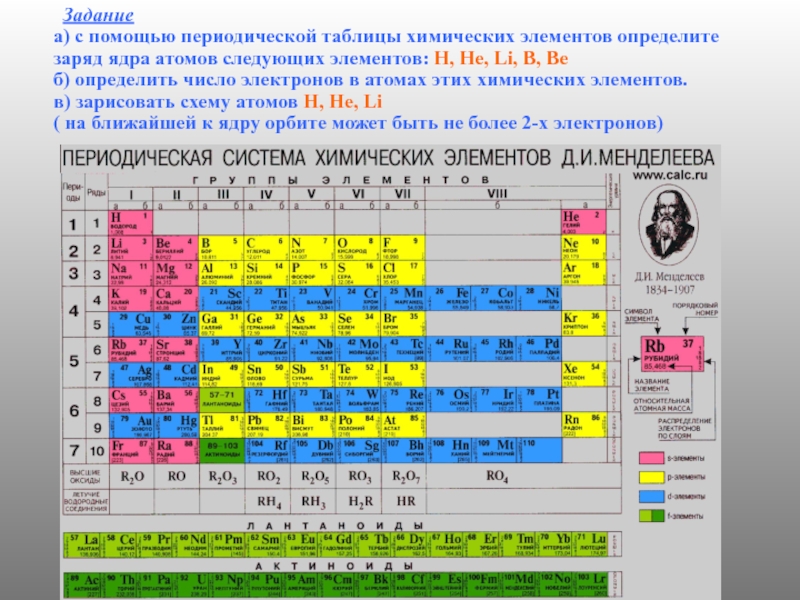
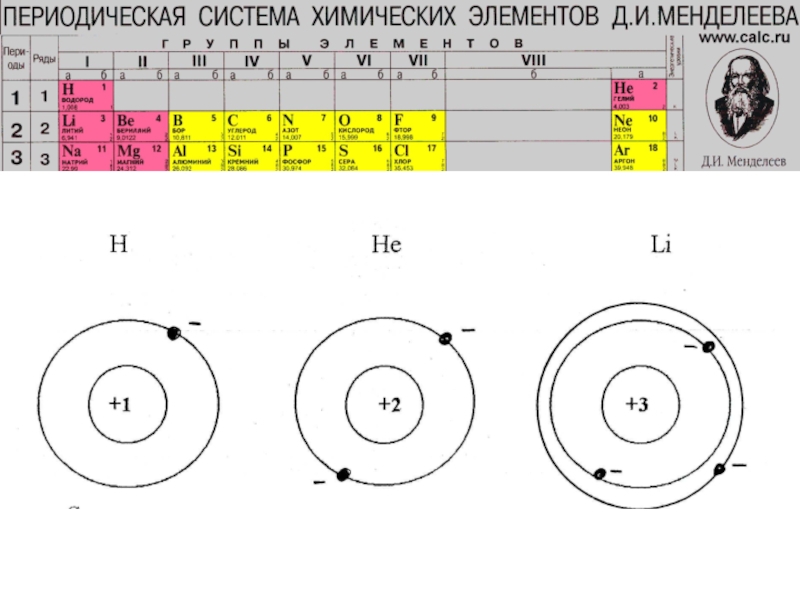
Слайд 11 Задание а) с помощью
периодической таблицы химических элементов определите заряд ядра атомов следующих элементов:
Н, Не, Li, В, Be б) определить число электронов в атомах этих химических элементов. в) зарисовать схему атомов Н, Не, Li ( на ближайшей к ядру орбите может быть не более 2-х электронов)Слайд 13В 1919 году Резерфорд осуществил первое искусственное расщепление атомного ядра,
экспериментально доказав, что в состав атомного ядра входят положительно заряженные
частицы. Их назвали протонами. Заряд протона по модулю равнялся заряду электрона. Но эти частицы имеют положительный заряд и массу приблизительно в 1840 раз больше, чем масса электрона.Строение атомного ядра
Слайд 14Ирен
Жолио-Кюри (1897-1956)
Фредерик Жолио-Кюри (1900-1958)
Джон Чедвик
(1920-1998)
В 1920 году Резерфорд высказал гипотезу
о существовании в атомном ядре частиц, не имеющих заряда с
массой, близкой к массе протона. В 1932 году английский физик Чедвик обнаружил эту частицу в атомном ядре и назвал нейтроном. Масса нейтрона приблизительно в 1840 разпревосходит массу электрона, т.е. близка к массе протона.
Слайд 15Вернер Карл
Гейзенберг
(1901-1976)
Дмитрий Дмитриевич Иваненко
(1904-1994)
Советский физик Д. Д. Иваненко и
немецкий физик
В. Гейзенберг предложили протонно-нейтронную модель ядра: ядра состоят из
элементарных частиц двух сортов: протонов и нейтронов. Число протонов в ядре равняется числу электронов в атомной оболочке, так как атом в целом нейтрален.
Протон и нейтрон – нуклоны -частицы, из которых состоит атомное ядро.
Строение атомного ядра
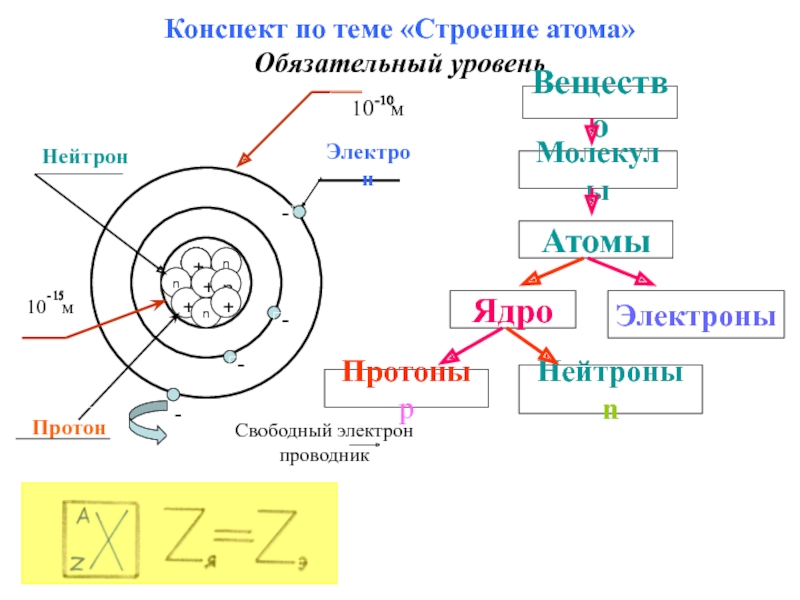
Слайд 17Конспект по теме «Строение атома»
Обязательный уровень
n
n
n
+
n
n
+
n
+
n
+
-
-
-
-
Электрон
Протон
Нейтрон
10 м
10
м
Свободный электрон проводник
-10
- 15
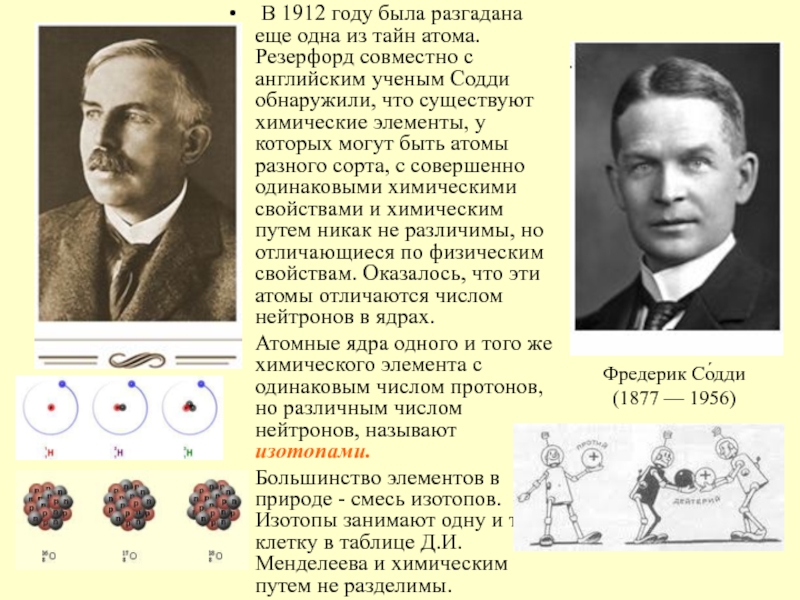
Слайд 18 В 1912 году была разгадана еще одна из тайн
атома. Резерфорд совместно с английским ученым Содди обнаружили, что существуют
химические элементы, у которых могут быть атомы разного сорта, с совершенно одинаковыми химическими свойствами и химическим путем никак не различимы, но отличающиеся по физическим свойствам. Оказалось, что эти атомы отличаются числом нейтронов в ядрах.Атомные ядра одного и того же химического элемента с одинаковым числом протонов, но различным числом нейтронов, называют изотопами.
Большинство элементов в природе - смесь изотопов. Изотопы занимают одну и ту же клетку в таблице Д.И. Менделеева и химическим путем не разделимы.
Фредерик Со́дди
(1877 — 1956)
Слайд 20Какие частицы называют нуклонами?
Чему равны заряд и масса протона?
Чему равны
заряд и масса нейтрона?
Слайд 22Домашнее задание:
Обязательно:
§ 30, вопросы к § 30, упр. 11 стр.69
Дополнительно:
№ 1211 – 1221(В.И.Лукашик,
Е.И. Иванова. Сборник задач по физике)
Слайд 23Значение открытия строения атома
Значение открытия планетарной модели атома Резерфорда
огромно. Как писал замечательный немецкий ученый Макс Планк:
«Из идеи движения электронов, подобно движению планет, возникла атомная физика».Количество протонов и нейтронов в ядре строго указывает, какой это элемент, каковы его физические и химические свойства.
Иначе говоря, такой «банк данных» обладает огромной предсказательной силой.
Знание строения атома позволяет объяснять известные электрические явления и предсказывать некоторые другие электрические явления .
Слайд 24Заключение
Атом скрывает в себе еще много тайн. Например, неизвестно, как
выглядит
электрон, его масса мала и находится он где-то внутри
атома. Считается, что это наименьший отрицательный заряд, меньше которого еще
никому наблюдать не удавалось. Вы, возможно, слышали о кварках
с электрическими зарядами, составляющими 1/3 и 2/3 от заряда электрона,
но в свободном состоянии их никто не наблюдал, поэтому электроны
считаются самыми малыми частицами в атоме.
Впереди у человечества много новых
открытий, и, как сказал Валерий Брюсов:
«Исканием тайн дух человека жил».
«Быть может эти электроны
Миры, где 5 материков?
Искусство, знанья, войны, троны
И память сорока веков!
Еще, быть может, каждый атом –
Вселенная, где сто планет,
Там все, что есть в объеме сжатом,
Но также то, чего здесь нет.»
( В.Я. Брюсов)