2. СН2 = СН2
3. СН
≡ СН 4. СН2 = СН - СН = СН2
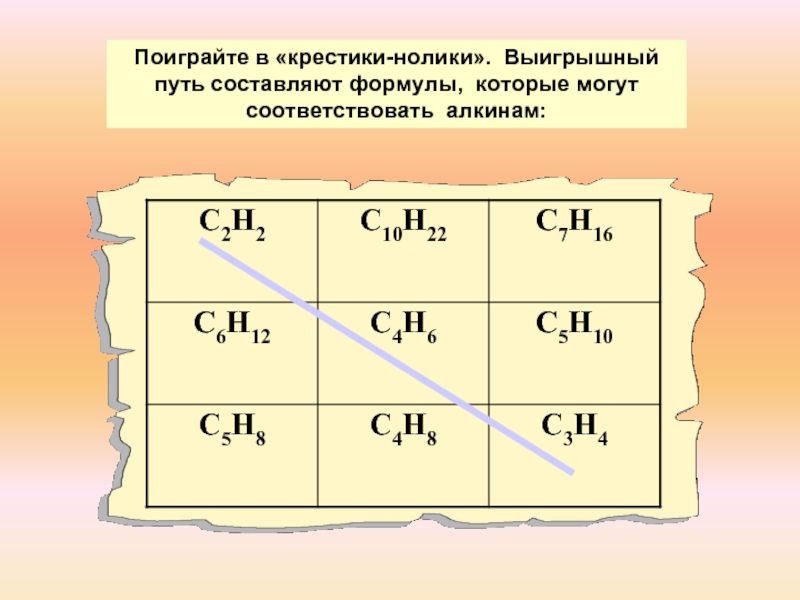
Среди указанных веществ выберите вещество, которое не относится ни к одному из изученных ранее классов углеводородов:
П. Бертло
1860г.
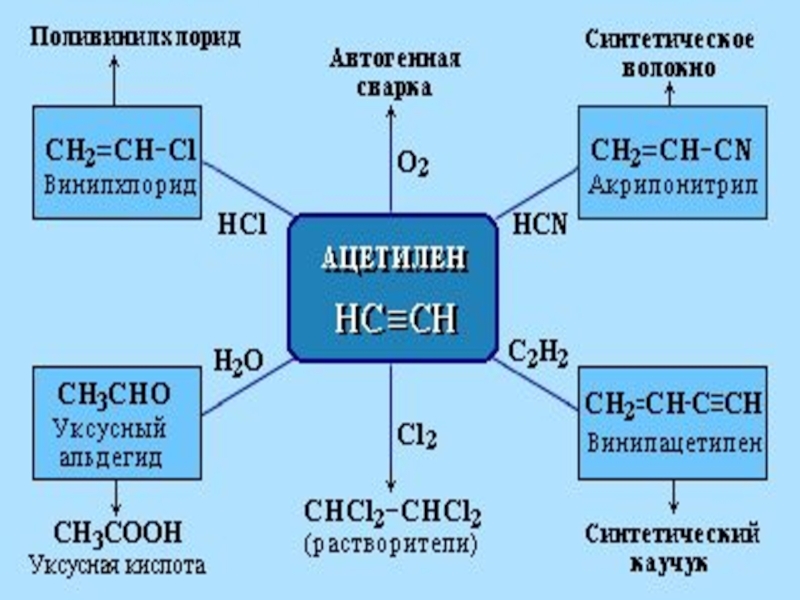
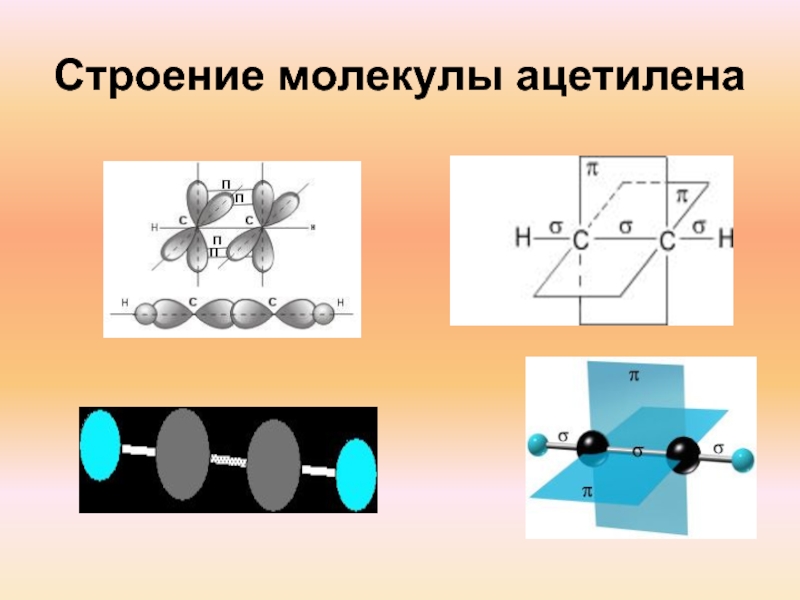
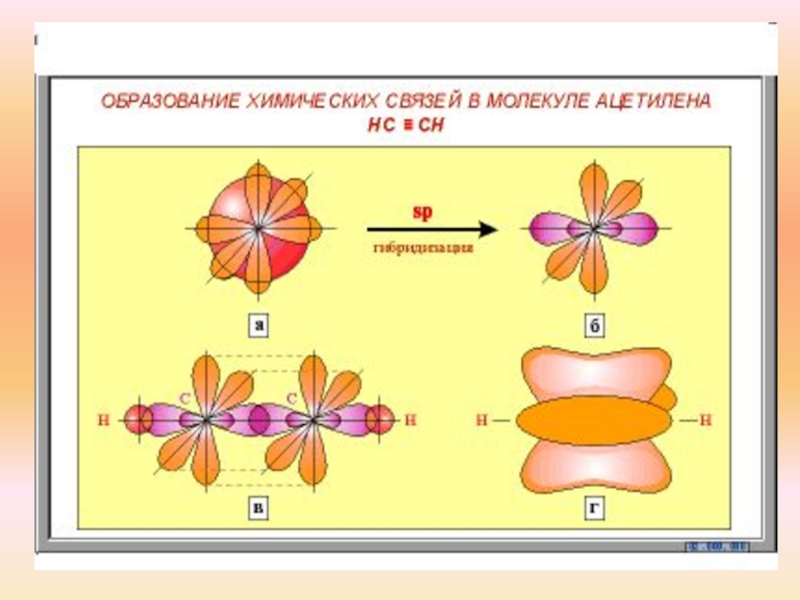
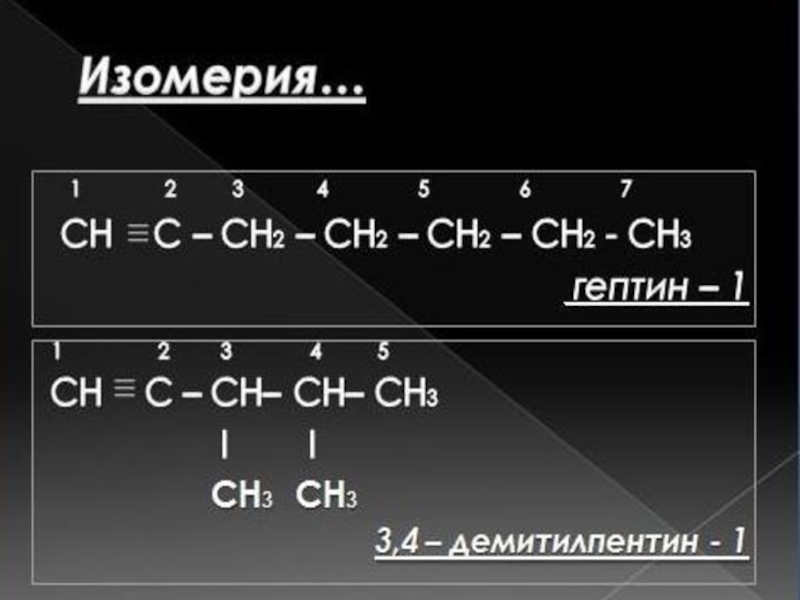
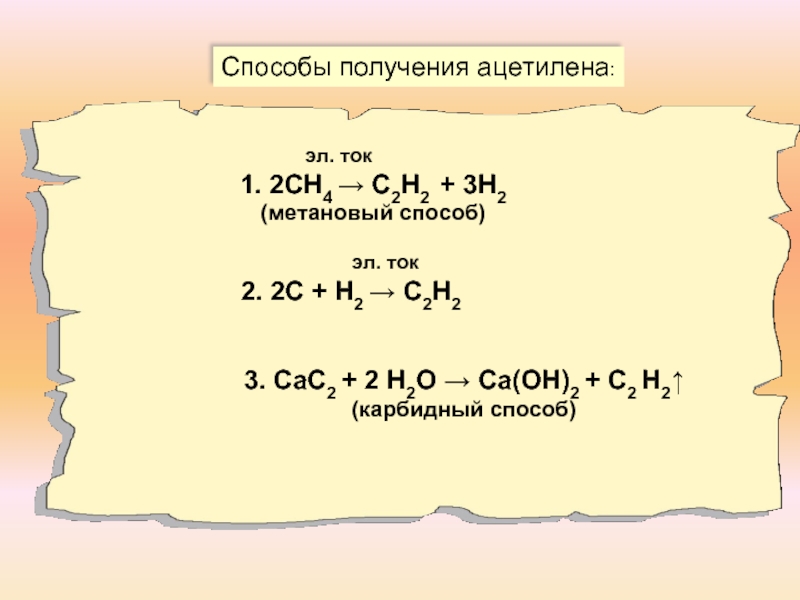
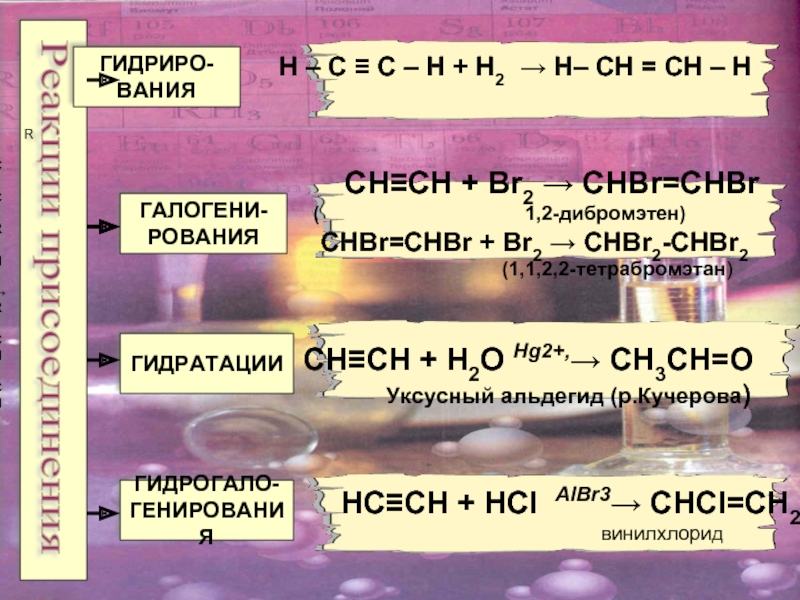
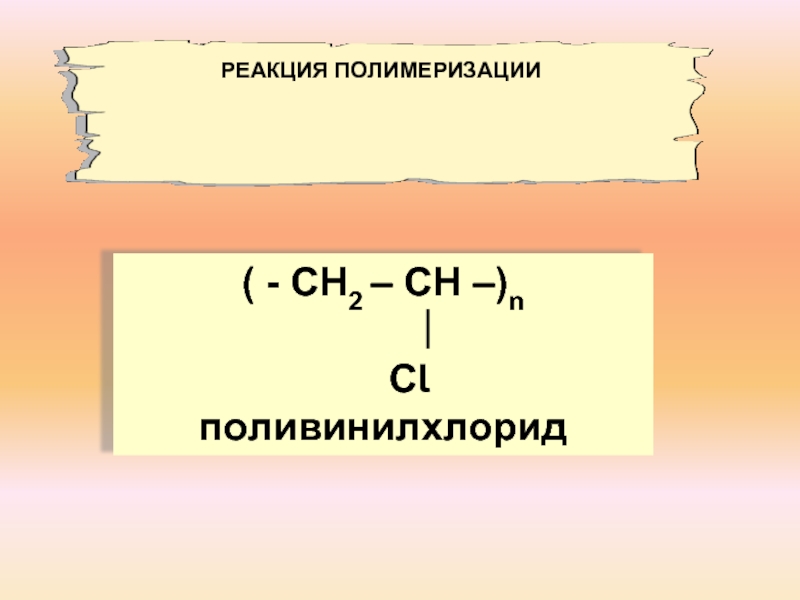
ацетилен






![Ацетилен и его гомологи Качественная реакция на алкины с тройной связью в конце цепи: НC≡CH Качественная реакция на алкины с тройной связью в конце цепи: НC≡CH + [Ag(NH3)2]OH → Аg-C≡C-Ag↓ +2NH3 +](/img/thumbs/b1eec1471787edc5f28059877ac5db08-800x.jpg)