Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Фенол
Содержание
- 1. Фенол
- 2. Фенол.
- 3. Девиз урока «Может тот, кто уверен , что может».
- 4. Цель урока: Изучить строение фенола,предсказать его свойства и на основе свойств рассмотретьзначение данного веществадля человека.
- 5. План урока. История открытия фенола.Строение фенола.Гомологический ряд фенолов.Физические свойства фенола.Применение фенолаХимические свойства фенола.
- 6. Найден в каменноугольной смоле Рунге в 1834.
- 7. Элементный состав его был установлен Лораном в
- 8. Какие фрагменты входили в состав вещества? (бензольное кольцо и группа OH)
- 9. Фенолы-органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксильными группами. ФЕНОЛHOHБЕНЗОЛС6Н50Н
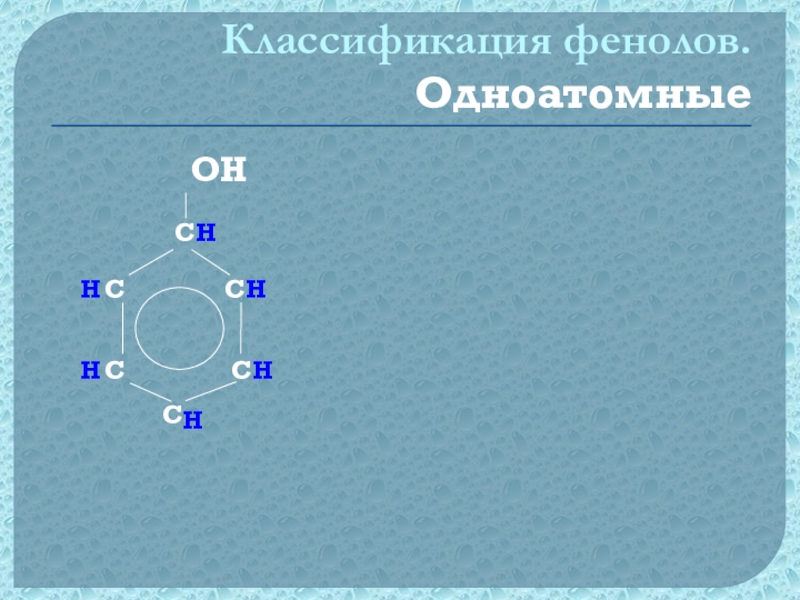
- 10. Классификация фенолов. Одноатомные ОH
- 11. ОHH ОHHHHДвухатомные. 4 - дигидроксибензол (гидрохинон)1,3 - дигидроксибензол (резорцин)1,2 - дигидроксибензол (пирокатехин)
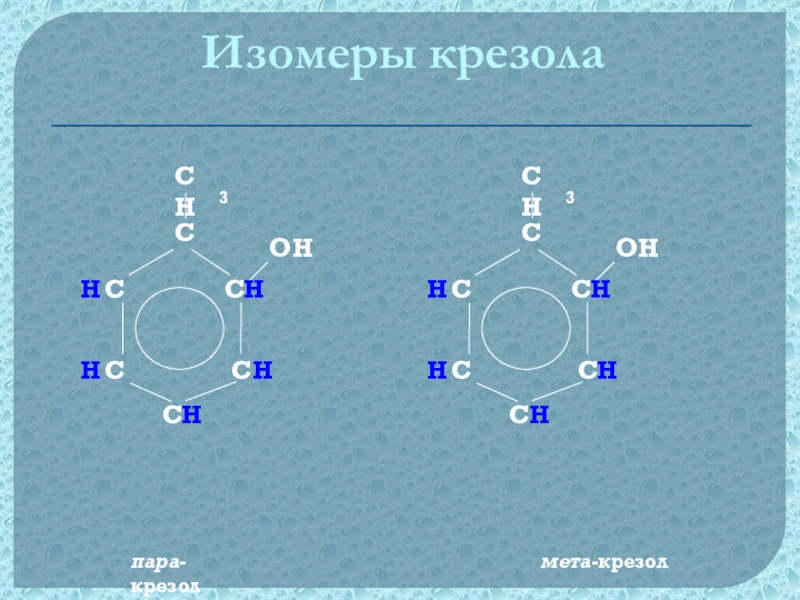
- 12. СH3HСH3HHHИзомеры крезолапара-крезолмета-крезол
- 13. Физические свойстваФенол бесцветное кристаллическоевещество. С водой дает гидрат – карболовуюкислоту.
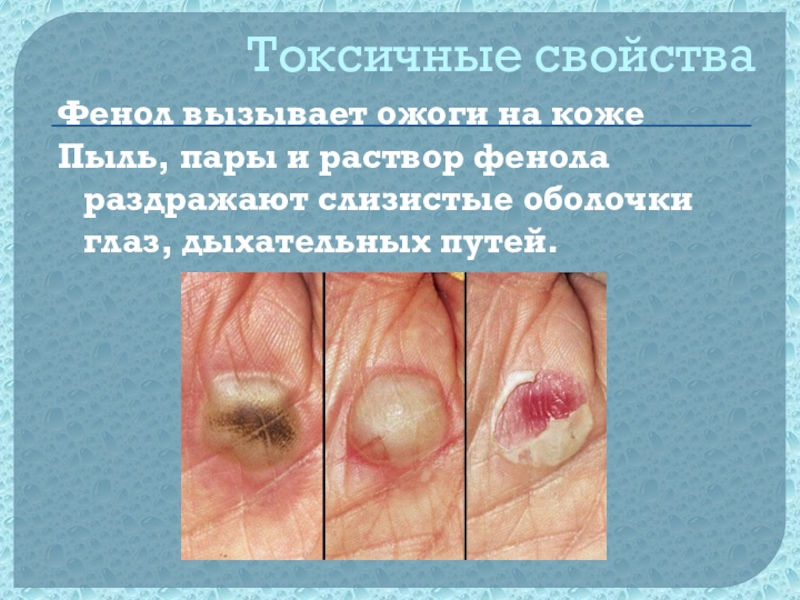
- 14. Токсичные свойстваФенол вызывает ожоги на кожеПыль, пары
- 15. Токсичные свойстваВызывает нарушение функций нервной системыБыстро всасывается
- 16. Фенолы применяются в производстве синтетических смол пластмасс полимеров
- 17. лекарственных препаратовкрасителей
- 18. поверхностно-активных веществ антиоксидантов антисептиковвзрывчатых веществ
- 19. средств защиты растенийпарфюмерных продуктов…
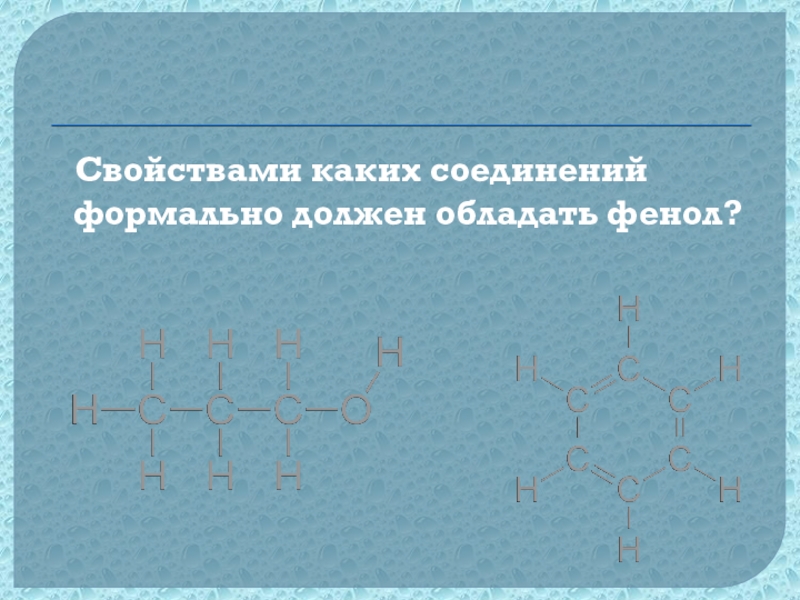
- 20. Свойствами каких соединений формально должен обладать фенол?
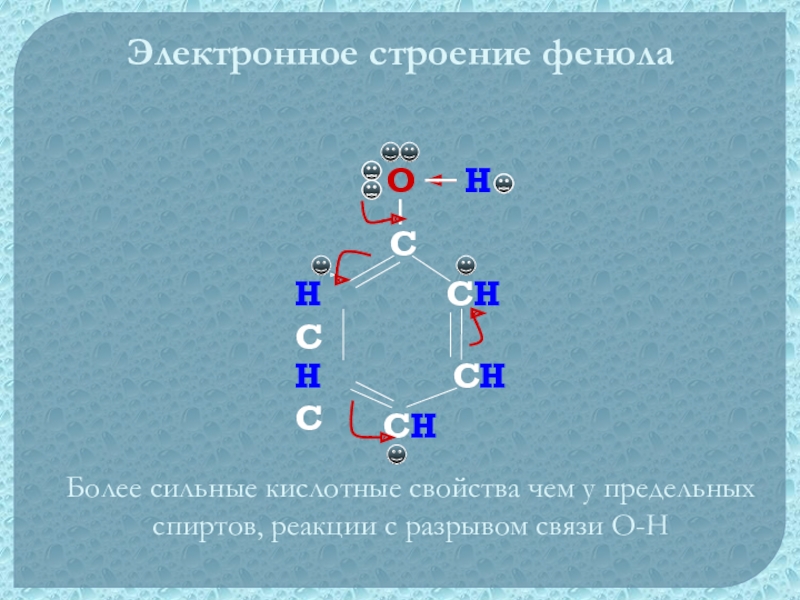
- 21. ССHСHH СH ССHOЭлектронное строение фенолаHБолее сильные кислотные
- 22. 1. Взаимодействие фенола с металлическим натрием КИСЛОТНЫЕ
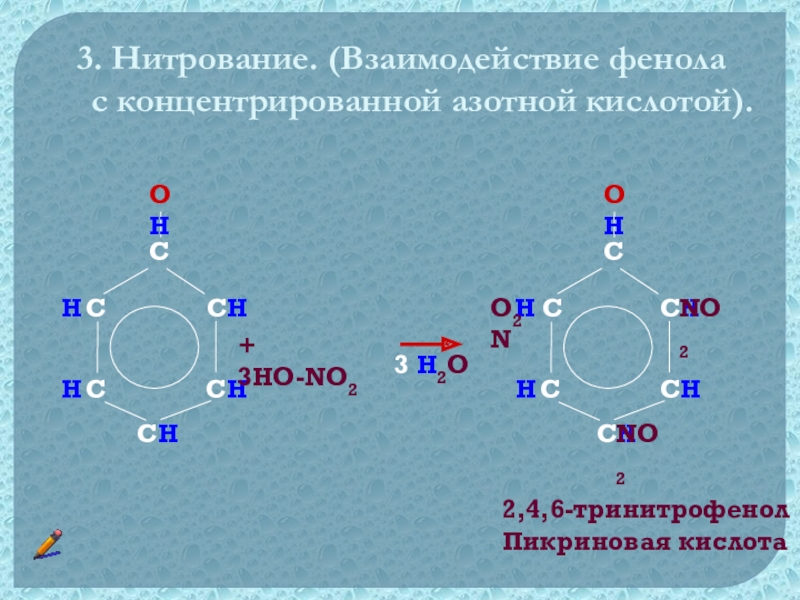
- 23. 3. Нитрование. (Взаимодействие фенола с концентрированной азотной кислотой).OHHHHO2N+ 3HO-NO2NO2NO23 H2O2,4,6-тринитрофенолПикриновая кислота
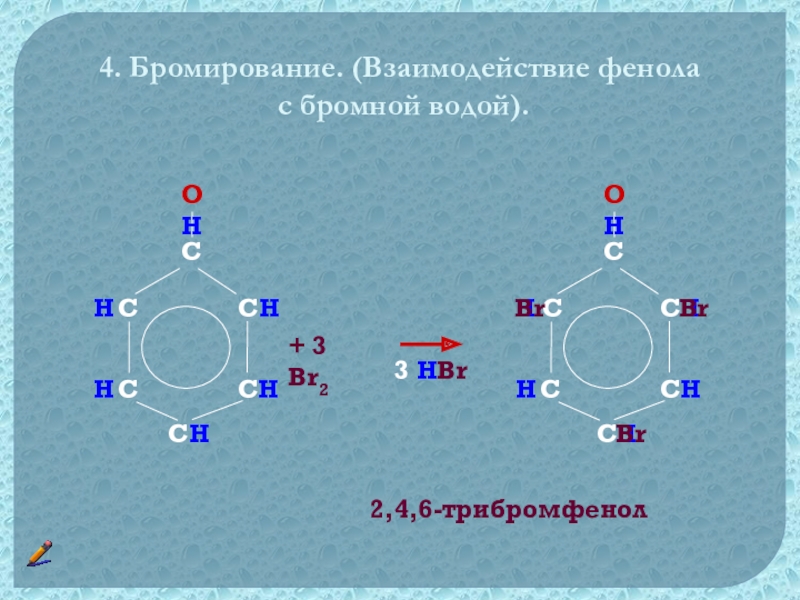
- 24. 4. Бромирование. (Взаимодействие фенола с бромной водой).OHHHHBr+ 3 Br2BrBr3 HBr2,4,6-трибромфенол
- 25. Вывод: 1) бензольное кольцо увеличивает полярность связи
- 26. Качественная реакция на фенол
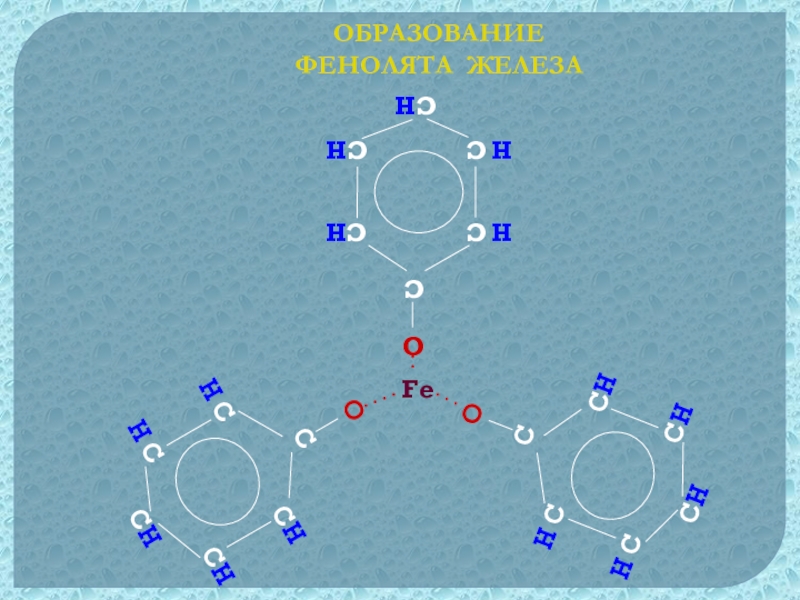
- 27. ОБРАЗОВАНИЕ ФЕНОЛЯТА ЖЕЛЕЗАFe
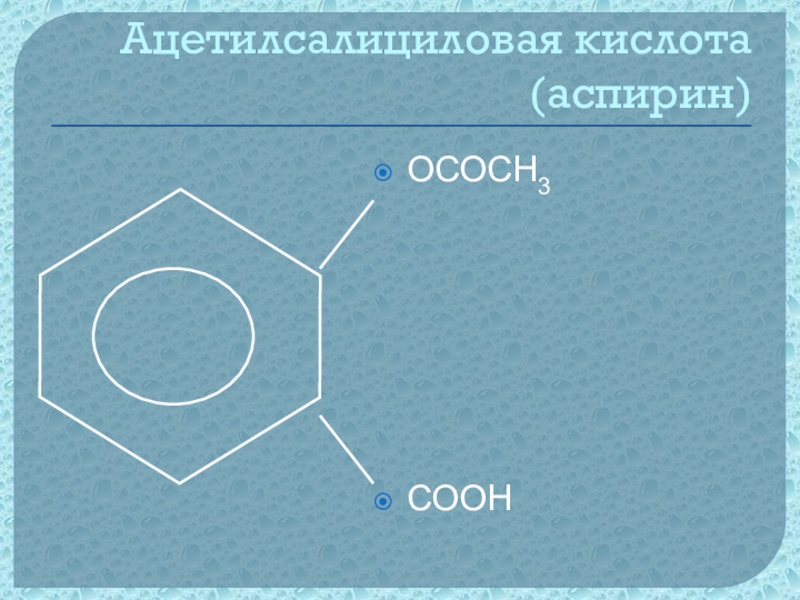
- 28. Ацетилсалициловая кислота (аспирин)
- 29. 1. Среди представленных веществ наиболее сильными кислотными свойствами обладает А)фенол Б)вода В)глицерин Г)метанол
- 30. 2. Фенол реагирует с каждым из веществ1)
- 31. 3. C помощью гидроксида меди(II) можно обнаружить в растворе1) пропилен2) пропанол3) фенол4) глицерин
- 32. 4. Влияние бензольного кольца на гидроксильного группу
- 33. 5. Наличие группы - OH в составе
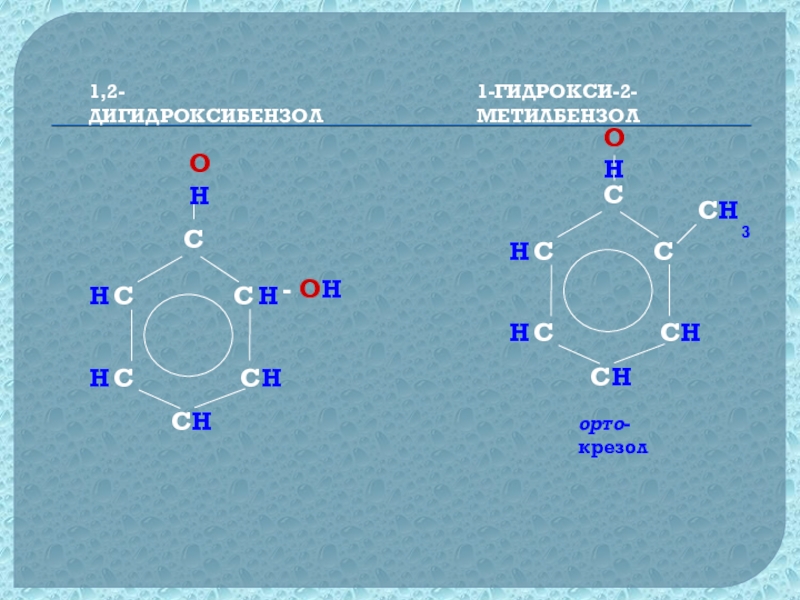
- 34. Составьте структурные формулы различных фенолов 1-ГИДРОКСИ-2-МЕТИЛБЕНЗОЛ1,2-ДИГИДРОКСИБЕНЗОЛ
- 35. 1,2-ДИГИДРОКСИБЕНЗОЛOH- OH1-ГИДРОКСИ-2-МЕТИЛБЕНЗОЛOHСH3орто-крезолH
- 36. Домашнее задание.§10. №6Подготовить сообщение о переработке каменного угля и получении фенола из него.
- 37. Два основных достояния человеческой Природы – это ум и рассуждение. Плутарх
- 38. Спасибо за урок!Учитесь хорошо!
- 39. Скачать презентанцию
Фенол.
Слайды и текст этой презентации
Слайд 5План урока.
История открытия фенола.
Строение фенола.
Гомологический ряд фенолов.
Физические свойства фенола.
Применение фенола
Химические
свойства фенола.
Слайд 7Элементный состав его был установлен Лораном в 1842 г.
Производное бензола
«Фениловая кислота»
В 1843г. Жерар
считал полученное вещество
спиртом-ОН
«фенол»
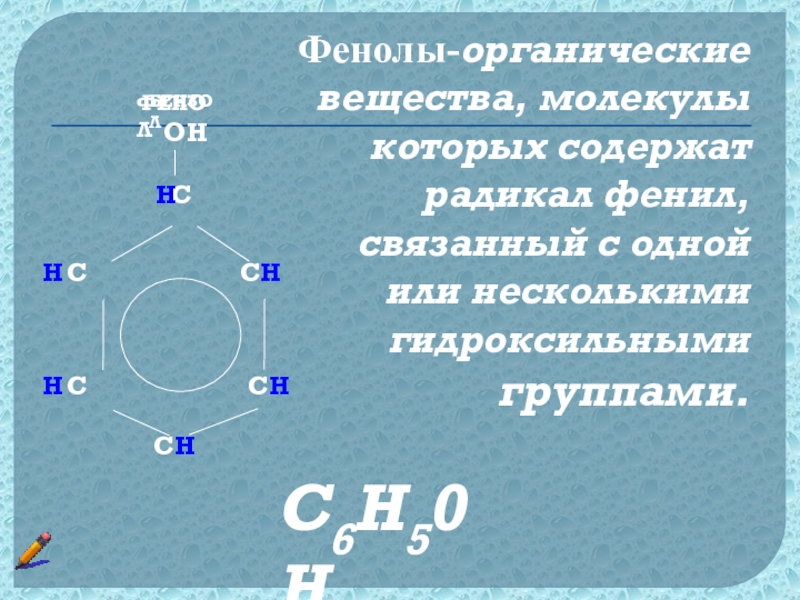
Слайд 9Фенолы-органические вещества, молекулы которых содержат радикал фенил, связанный с одной
или несколькими гидроксильными группами.
ФЕНОЛ
H
OH
БЕНЗОЛ
С6Н50Н
Слайд 11ОH
H
ОH
H
H
H
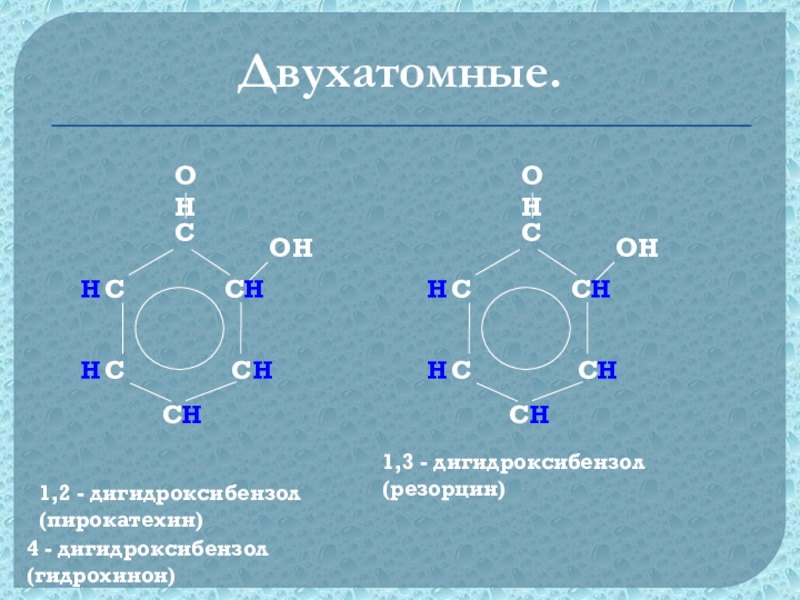
Двухатомные.
4 - дигидроксибензол (гидрохинон)
1,3 - дигидроксибензол (резорцин)
1,2 -
дигидроксибензол (пирокатехин)
Слайд 13Физические свойства
Фенол бесцветное кристаллическое
вещество. С водой дает гидрат – карболовую
кислоту.
Слайд 14Токсичные свойства
Фенол вызывает ожоги на коже
Пыль, пары и раствор фенола
раздражают слизистые оболочки глаз, дыхательных путей.
Слайд 15Токсичные свойства
Вызывает нарушение функций нервной системы
Быстро всасывается даже через неповрежденные
участки кожи и уже через несколько минут начинает воздействовать на
ткани головного мозга.Часто фенол является причиной
онкологических заболеваний.
Слайд 21С
СH
СH
H С
H С
СH
O
Электронное строение фенола
H
Более сильные кислотные свойства чем у
предельных спиртов, реакции с разрывом связи О-Н
Слайд 221. Взаимодействие фенола с металлическим натрием
КИСЛОТНЫЕ СВОЙСТВА
2. Взаимодействие фенола
с раствором щелочи
С6Н5ОН + Na = C6H5ONa + H2
C6H5OH +
NaOH = C6H5ONa + H2Oфенолят натрия
фенолят натрия
Слайд 233. Нитрование. (Взаимодействие фенола
с концентрированной азотной кислотой).
OH
H
H
H
O2N
+ 3HO-NO2
NO2
NO2
3 H2O
2,4,6-тринитрофенол
Пикриновая
кислота
Слайд 244. Бромирование. (Взаимодействие фенола
с бромной водой).
OH
H
H
H
Br
+ 3 Br2
Br
Br
3 HBr
2,4,6-трибромфенол
Слайд 25Вывод:
1) бензольное кольцо увеличивает полярность связи О-Н гидроксильной группы,
усиливая её кислотные свойства.
2) гидроксогруппа увеличивает подвижность атомов водорода бензольного
кольца в положениях 2,4,6.Слайд 291. Среди представленных веществ наиболее сильными кислотными свойствами обладает
А)фенол
Б)вода
В)глицерин
Г)метанол
Слайд 302. Фенол реагирует с каждым из веществ
1) бромная вода и
гидроксид натрия
2) гидроксид натрия и вода
3) вода и соляная кислота
4)
соляная кислота и бромная водаСлайд 313. C помощью гидроксида меди(II) можно обнаружить в растворе
1) пропилен
2)
пропанол
3) фенол
4) глицерин
Слайд 324. Влияние бензольного кольца на гидроксильного группу в молекуле фенола
доказывает реакция фенола с
1) гидроксидом натрия
2) формальдегидом
3) бромной водой
4) азотной
кислотойСлайд 335. Наличие группы - OH в составе фенола
1) облегчает протекание
реакции замещения
2) затрудняет протекание реакции замещения
3) не влияет на протекание
реакции замещения4) способствует протеканию реакции присоединения