Слайд 2Структура работы
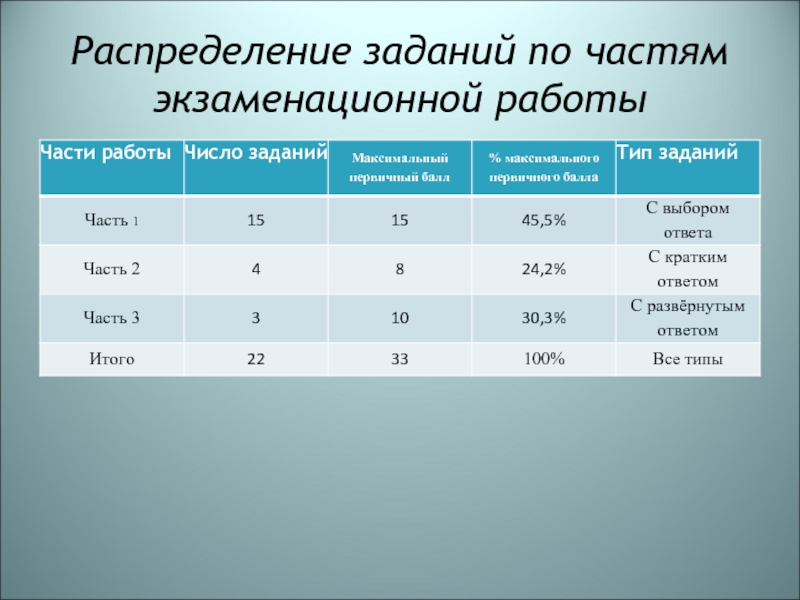
Часть 1 содержит 15 заданий с выбором ответа. Их
обозначение в работе: А1; А2; А3; А4 … А15.
Часть
2 содержит 4 задания с кратким ответом. Их обозначение в работе: В1; В2; В3, В4.
Часть 3 содержит 3 задания с развёрнутым ответом. Их обозначение в работе: С1, С2, С3.
Слайд 3Распределение заданий по частям экзаменационной работы
Слайд 4Распределение заданий по уровню сложности
Слайд 5
Распределение заданий экзаменационной работы по содержательным блокам (темам, разделам) курса
химии
Слайд 6Шкала пересчета первичного балла
Слайд 7Задания блока А
Задания с выбором ответа проверяют на базовом уровне
усвоение значительного количества элементов содержания (23 из 28) из всех
четырёх содержательных блоков курса:
знание языка науки,
основных химических понятий,
общих свойств классов неорганических и органических соединений, металлов, неметаллов;
признаков классификации элементов, неорганических и органических веществ, химических реакций; знания о видах химических связей и др.
Слайд 8А1. Строение атома
Распределение электронов по энергетическим уровням в атоме хлора
соответствует ряду чисел
1) 7,8,2
2) 2,8,7
3) 2,7
4) 2,8,8,7
Слайд 9А2. ПЗ и ПС
Наиболее выражены неметаллические свойства у элемента 3
периода
1) IIIА группы
2) VА группы
3) IVА группы
4)
VIА группы
Слайд 10А3. Строение молекул. Химическая связь
Химическая связь в оксиде калия
1) металлическая
2)
ионная
3) ковалентная полярная
4) ковалентная неполярная
Слайд 11А4. Валентность и степень окисления
Валентность серы в соединениях SO3 и
SO2 соответственно равна
1) III и II
2) VI и IV
3)
VI и II
4) III и IV
Слайд 12А5. Простые и сложные вещества. Классификация
Кислотным оксидом является
1) оксид
углерода(II)
2) оксид азота(I)
3) оксид азота(V)
4) оксид азота(II)
Слайд 13А6. Классификация химических реакций. Условия протекания реакций
Взаимодействие железа с раствором
серной кислоты относят к реакциям
1) обмена
2) соединения
3) замещения
4)
разложения
Слайд 14А7. Электролиты и неэлектролиты
Наибольшее количество катионов образуется при полной диссоциации
1 моль
1) фосфата натрия
2) нитрата алюминия
3) хлорида железа(III)
4) сульфата
железа(III)
Слайд 15А8. Реакции ионного обмена
Сокращённое ионное уравнение
Zn2+ + 2
OH– = Zn(OH)2
соответствует взаимодействию
1)оксида цинка и воды
2)хлорида цинка и
воды
3)хлорида цинка и гидроксида натрия
4)нитрата цинка и гидроксида железа (II)
Слайд 16А9. Химические свойства простых веществ
При комнатной температуре реагируют
1) сера
и кислород
2) азот и кислород
3) барий и вода
4) цинк и
вода
Слайд 17А10. Химические свойства оксидов
Оксид алюминия реагирует с
1) O2
2) NaOH
3) K3PO4
4) MgSO4
Слайд 18А11. Химические свойства гидроксидов
Гидроксид натрия реагирует с каждым из двух
веществ:
1) фосфорная кислота и вода
2) нитрат меди (II) и оксид
алюминия
3) хлорид железа (II) и сульфат калия
4) оксид кальция и соляная кислота
Слайд 19А12. Химические свойства солей
Раствор хлорида меди(II) реагирует с каждым из
двух веществ
1) Ва(NO3)2, KOH
2) Fe, AgNO3
3) SO2, Na3PO4
4) Al(OH)3
, Al
Слайд 20А13. Вещества и смеси. ТБ
Верны ли следующие суждения о чистых
веществах и смесях:
А. Молоко – это чистое вещество.
Б. При растворении
мела в воде образуется неоднородная смесь.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Слайд 21А14. Определение характера среды. Качественные реакции
Ион NH4+ можно обнаружить в
растворе с помощью
1) хлорида калия
2) гидроксида калия
3) нитрата бария
4)
сульфата калия
Слайд 22А15. Массовая доля элемента
Массовая доля кислорода в нитрате магния
равна
1) 55,8 %
2) 32,4 %
3) 10,8 %
4)
64,7%