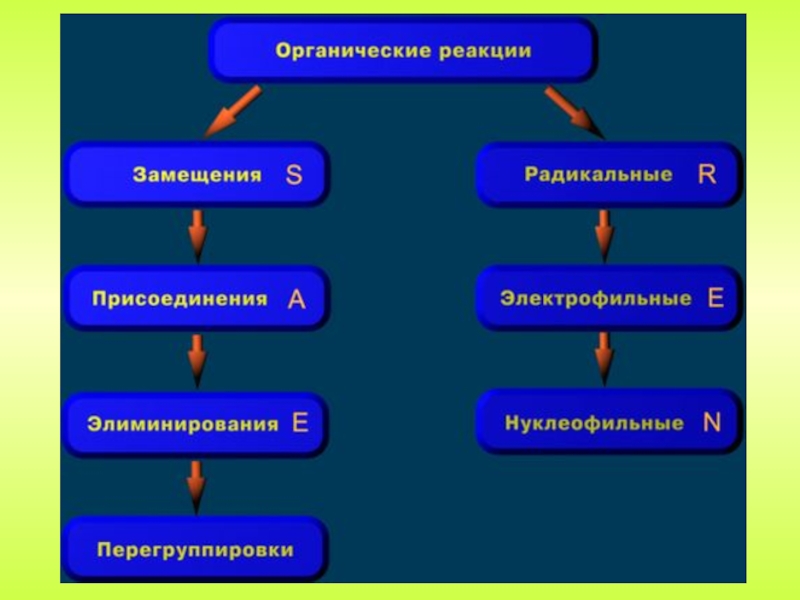
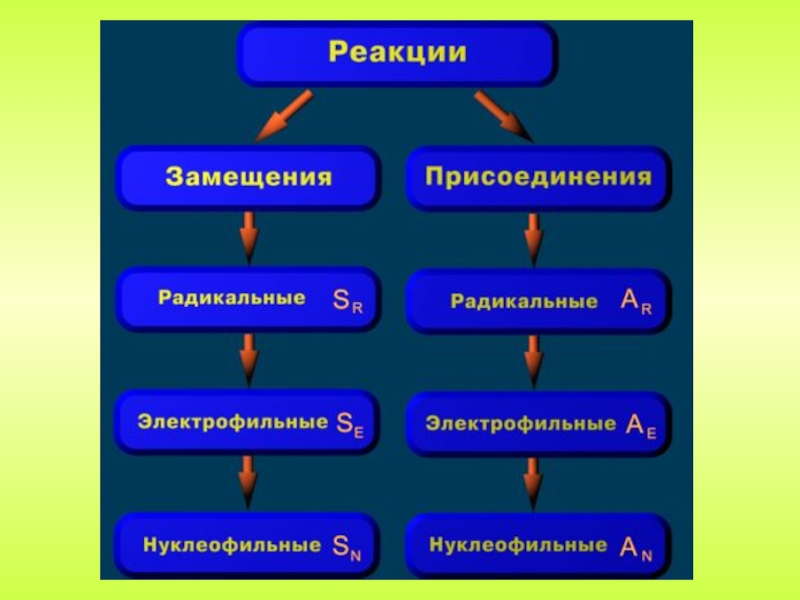
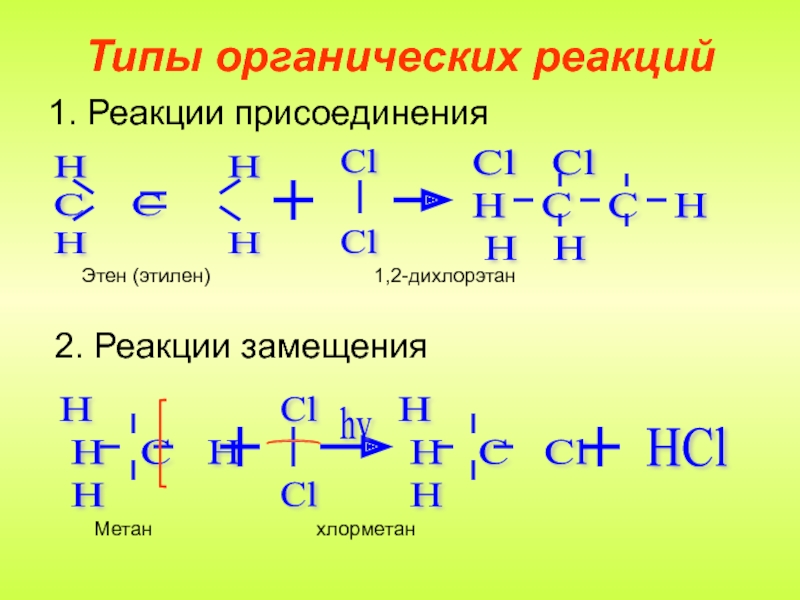
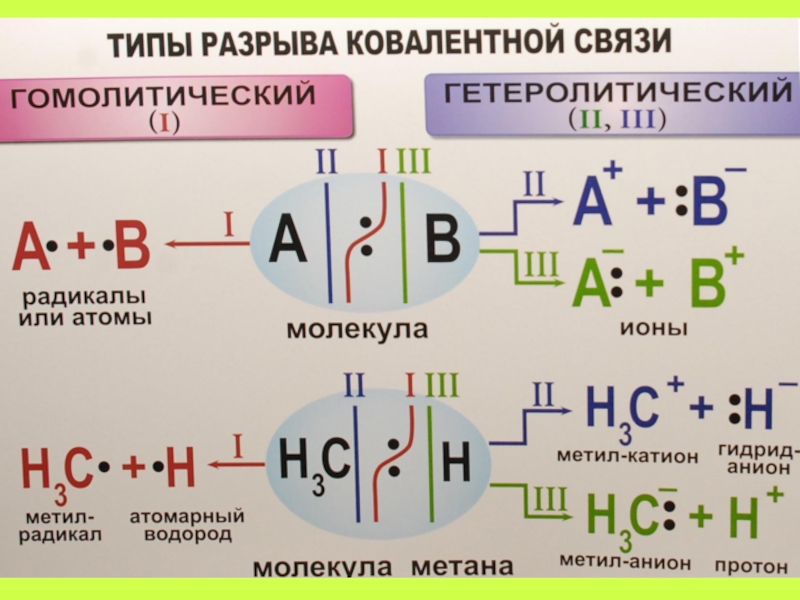
классификации реакций, в которых могут принимать участие органические вещества. Наиболее
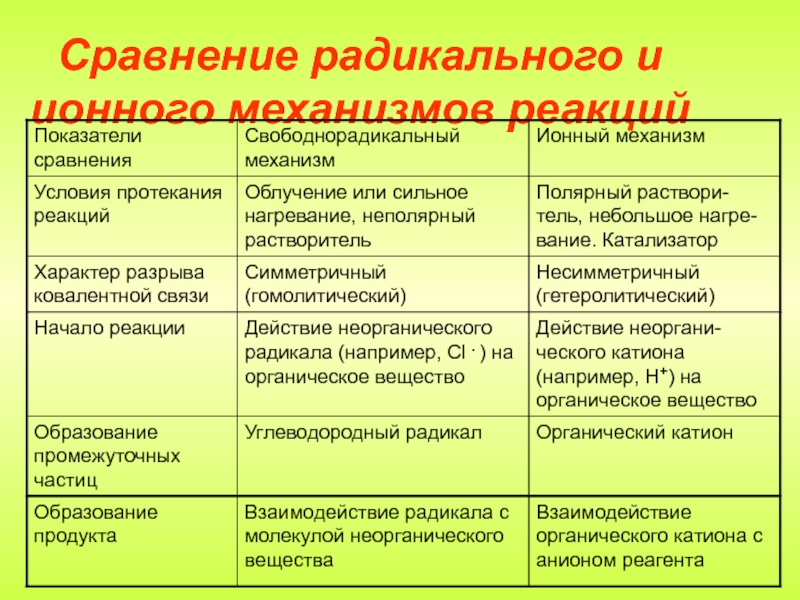
часто органические реакции различают по характеру происходящих изменений и по электронным характеристикам одного из компонентов реакции (реагента).Реакции замещения и присоединения, в соответствие с характером реагента, в свою очередь, делятся на – радикальные,- электрофильные и - нуклеофильные.