Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислоты органические и неорганические
Содержание
- 1. Кислоты органические и неорганические
- 2. Кисло́ты — сложные вещества, которые состоят из
- 3. По определению Льюиса, кислота — это электролит(вещество,
- 4. В рамках теории электролитической диссоциации кислота —
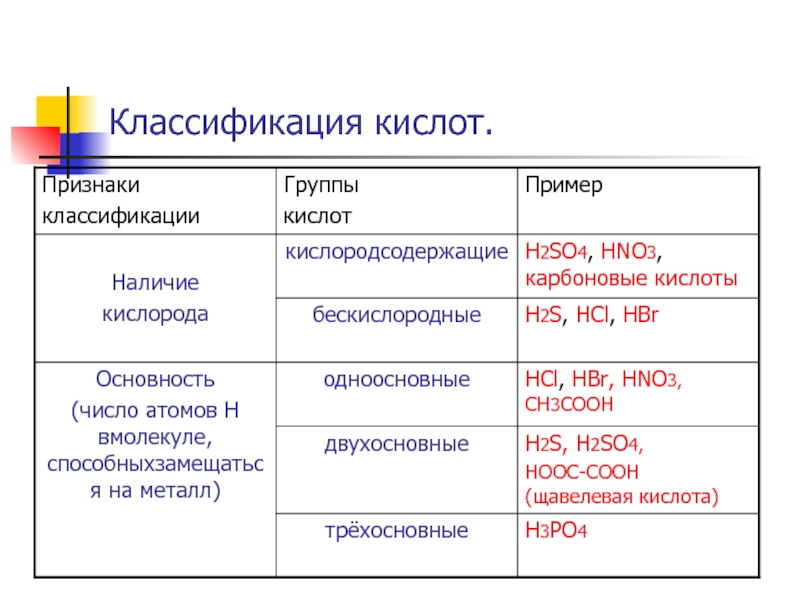
- 5. Классификация кислот.
- 6. Слайд 6
- 7. Слайд 7
- 8. Химические свойства.
- 9. Взаимодействие с нерастворимыми основаниямиВзаимодействие с нерастворимыми основаниями
- 10. Взаимодействие с солямиВзаимодействие с солями, если выпадает
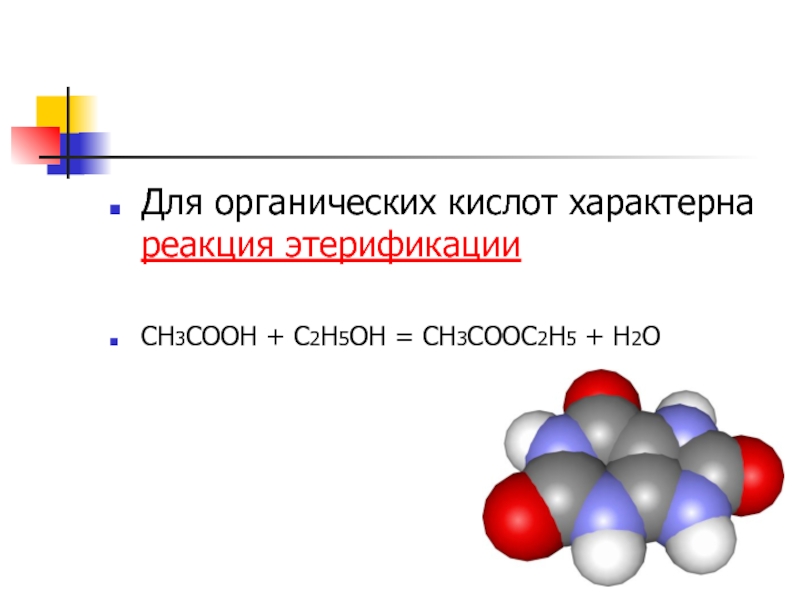
- 11. Для органических кислот характерна реакция этерификации CH3COOH + C2H5OH = CH3COOC2H5 + H2O
- 12. Слайд 12
- 13. Спасибо за работу!
- 14. Скачать презентанцию
Кисло́ты — сложные вещества, которые состоят из атомов водорода, способных замещаться на атомы металлов, и кислотных остатков. Они получили своё название из-за кислого вкуса большинства кислот. В водных растворах они диссоциируют
Слайды и текст этой презентации
Слайд 2Кисло́ты — сложные вещества, которые состоят из атомов водорода, способных
замещаться на атомы металлов, и кислотных остатков.
название из-за кислого вкуса большинства кислот. В водных растворах они диссоциируют на катион водорода (протон) и анион кислотного остатка.Слайд 3По определению Льюиса, кислота — это электролит(вещество, участвующее в реакциях
с переходом электрона), принимающий электронную пару в реакции с основанием,
то есть веществом, отдающим электронную пару.В теории Бренстеда-Лоури, кислота — вещество, отдающее протон (основание — вещество, принимающее протон).
Слайд 4В рамках теории электролитической диссоциации кислота — это электролит, при
электролитической диссоциации которого из катионов образуются лишь катионы водорода.
Слайд 9Взаимодействие с нерастворимыми основаниямиВзаимодействие с нерастворимыми основаниями с образованием солиВзаимодействие
с нерастворимыми основаниями с образованием соли и водыВзаимодействие с нерастворимыми
основаниями с образованием соли и воды, если полученная соль растворима:Cu(OH)2 + H2SO4 = CuSO4 + H2O
Слайд 10Взаимодействие с солямиВзаимодействие с солями, если выпадает осадокВзаимодействие с солями,
если выпадает осадок или выделяется газ:
BaCl2 + H2SO4 = BaSO4
+ 2HClМеталлы, стоящие в ряду активностиМеталлы, стоящие в ряду активности до водорода, вытесняют его из раствора кислоты
Mg + 2HCl = MgCl2 + H2
Теги