Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Массовая доля элемента в веществе. Решение задач.
Содержание
- 1. Массовая доля элемента в веществе. Решение задач.
- 2. Слайд 2
- 3. ЦЕЛИ УРОКА: - ОБОБЩИТЬ И
- 4. Актуализация опорных знаний Перед
- 5. Проверка домашнего задания Задание 1
- 6. Задание 2
- 7. Задание 3
- 8. Задание
- 9. вершина знань
- 10. Решение задач на нахождение массовой доли элемента
- 11. Задачи типа №1 малахит
- 12. Магнезит
- 13. И З
- 14. Слайд 14
- 15. Слайд 15
- 16. Вычисление массы элемента по
- 17. Задачи по типу 2
- 18. С
- 19. ГОРНЫЙ ХРУСТАЛЬ
- 20. Вычисление массы соединения
- 21. Задачи по типу 3
- 22. МРАМОР. МЕЛ. КАЛЬЦИТ
- 23. Нахождение формул веществ
- 24. Задачи по типу 4
- 25. Слайд 25
- 26. Слайд 26
- 27. Задачи по типу 5 Найти массовые соотношения елементов в нитрате аммония NH4 NO3
- 28. Слайд 28
- 29. Выведение формулы вещества
- 30. Задачи по типу 6 1.Найти простейшую формулу
- 31. Тестирование
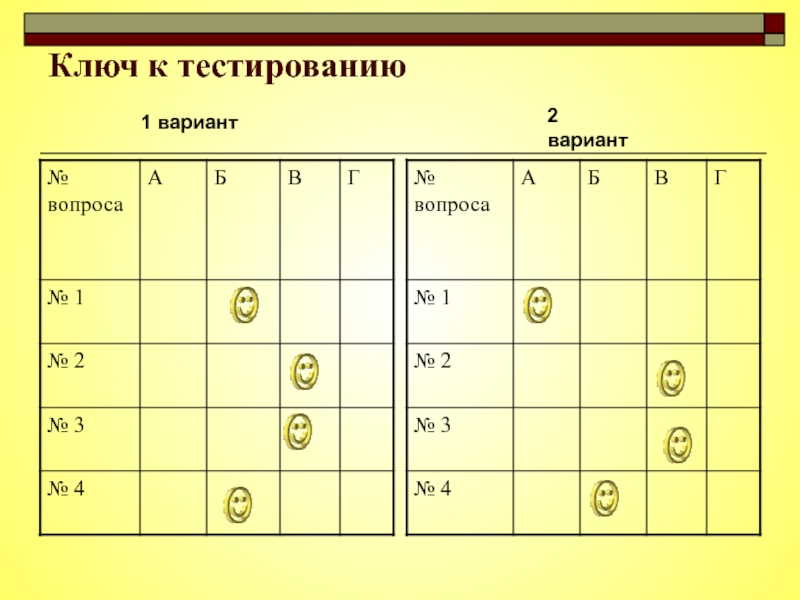
- 32. Ключ к тестированию 1 вариант2 вариант
- 33. Слайд 33
- 34. Вот и наша вершина знаний
- 35. Домашнее задание
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3 ЦЕЛИ УРОКА:
- ОБОБЩИТЬ И СИСТЕМАТИЗИРОВАТЬ ЗНАНИЯ ДЕТЕЙ
О ХИМИЧЕСКИХ ФОРМУЛАХ, КАЧЕСТВЕННОМ И КОЛИЧЕСТВЕННОМ СОСТАВЕ ВЕЩЕСТВ;
- РАЗВИВАТЬ УМЕНИЯ РЕШАТЬ ЗАДАЧИ С ИСПОЛЬЗОВАНИЕМ МАССОВОЙ ДОЛИ ЭЛЕМЕНТА В ВЕЩЕСТВЕ;- ПОЗНАКОМИТЬСЯ СО СПОСОБАМИ НАХОЖДЕНИЯ ФОРМУЛ ВЕЩЕСТВ ПО ДАННЫМ О МАССОВОЙ ДОЛЕ ЭЛЕМЕНТА
Слайд 4Актуализация опорных знаний
Перед нами вершина
знаний. На прошлом уроке мы уже изучили основные приемы решения
задач по формуле вещества, и каждый из вас достиг определенных высот на этой вершине. И сегодня мы должны подняться как можно выше, научиться находить массовые доли элементов в веществах, рассчитывать массы элементов по их массовым долям, находить формулы веществ по данным о массовых долях элементов.Слайд 5Проверка домашнего задания
Задание 1
Вычислить
массовые соотношения и массовые доли элементов в веществах
MgCl2
NaBr PH3 CrO3
Слайд 9вершина знань
Посмотрите на альпиниста у подножия скалы. Как вы думаете, ему
нужно приложить усилия , чтобы подняться на гору? А если он без усилий будет двигаться по горе, то куда он может попасть? Поэтому на уроке , для того, чтобы не скатиться вниз, нам необходимо будет приложить некоторые усилия для решения упражнений, быть внимательными и усердными в работе.
Слайд 10Решение задач на нахождение массовой доли элемента в веществе
Алгоритм
1.Записать краткое условие задачи.2.Рассчитать относительную молекулярную массу данного соединения. 3. Рассчитать массовую долю нужного элемента по формуле ω% (E)=
4.Записать ответ.
Слайд 11 Задачи типа №1
малахит
Малахит-хрупкий минерал зеленого цвета, имеет формулу CuCO3(OH)
2.Его считают русским камнем, слава его началась в 1635р. – после открытия уральских малахитовых рудников.
Рассчитайте массовую долю всех елементов в этом соединении.
Слайд 13 И З У М Р
У Д
Изумруд – камень зеленого цвета, имеет формулу Be3Al2(SiO3)6.
В изумрудную чашу, за библейской легендой, собрали кровь Христа. Римский император Нерон в изумрудный бинокль наблюдал за горящим Римом.
Рассчитайте массовую долю всех елементов в этом веществе.
Слайд 14 Б И
Р Ю З А
Бирюза имеет голубой цвет благодаря присутствию в этом соединении ионов меди.
Она химически неустойчивая: поглощает влагу , жиры, “боится” солнца, взаимодействует с углекислым газом, приобретая зеленый цвет.
Камышек массою 208г содержит 16г атомов меди.
Вичислить массовую долю меди в бирюзе.
Слайд 15
Р У Б И Н
Рубин, который в Стародавней Індии называли царем драгоценных камней, - разновидность минерала корунду ( Al2O3).
Его красный цвет обуславливают примеси атомов хрома.
Кристалл рубина массой 167 г содержит 15 г атомов хрома.
Вычислить массовую долю хрома в этом кристалле.
Слайд 16 Вычисление массы элемента по известной массовой
доле
Алгоритм1. Записать краткое условие задачи.
2. Рассчитать относительную молекулярную массу данного вещества. 3. Рассчитать массу элемента по формуле:
m(Э) = W• m(cп.)/100%
4. Записать ответ.
Слайд 17 Задачи по типу 2
Гематит
Гематит – полудрагаценный камень от черного до красного цвета, известный еще в Древнем Египте.
Массовая доля железа в нем составляет 70%.
Вычислить массу железа в камышке гематита массой 50 г
Слайд 18 С И Л Ь
В И Н
Минерал сильвин , химическая формула KCl, применяется как калийное удобрение.
Вычислить массу атомов калия, которая содержится в 50 г сильвина, если массовая доля его в минерале составляет 52%.
Слайд 19 ГОРНЫЙ ХРУСТАЛЬ
Горный хрусталь –
это кристаллический, прозрачный, бесцветный кварц с химической формулой SiO2. В Древней Греции считали, что это закаменевшая кристаллическая вода, которая совсем потеряла тепло.
Какая масса атомов кремния содержится в кристалле горного хрусталя массой 200 г, если массовая доля его составляет 46,7%.
Слайд 20 Вычисление массы соединения
по известной массовой доле элемента
Алгоритм1. Записать краткое условие задачи
2. Рассчитать относительную молекулярную массу 3.Рассчитать массу соединения по формуле
m(соед) = m(Э) •100% /W(Э)%
4.Записать ответ
Слайд 21 Задачи по типу 3
Сапфир
Сапфиры синего цвета издавна были “королевскими камнями ” – символами мудрости, власти, победы.
Это разновидность коррунду с массовой долей алюминия 53% и примесями титана и железа.
Рассчитать массу кристалла сапфира, в котором содержится 5,4г атомов алюминия.
Слайд 22МРАМОР. МЕЛ. КАЛЬЦИТ
Мрамор, мел, кальцит являются разновидностями соединения
с химической формулой СаСО3.Определить, в какой массе этого соединения содержится 120 г атомов углерода, если его массовая доля составляет 12%.
Слайд 23 Нахождение формул веществ
по известным массовым долям элементов
Алгоритм1. Записать краткое условие задачи
2. Рассчитать относительную молекулярную массу
3.По формуле n=W•Mr /Ar·100% можно определить количество атомов каждого элемента в формуле 4. Записать ответ
Слайд 24Задачи по типу 4
Минерал пирит это
руда, из которой получают железо. Он содержит 47% железа и
53% серы. Относительная формульная масса пирита равна 120. Выведите формулу пирита.Слайд 25 Галенит
Определить формулу галенита – соединения свинца с серой, в
котором массовая доля свинца 87%, а серы 13%. Относительная формульная масса галенита 239.Слайд 26 Алгоритм решения задач на
нахождение массових отношений элементов
в веществе 1. Записать краткое условие задачи 2.Записать формулу для расчета массовых
соотношений элементов, указав в скобках их
символы:
m (А) : m (В) : m (С) = хМ(А) : уМ(В) : zМ(С), где х, у, z – индексы.
3.Рассчитать массовые соотношения, подставивши
соответствующие значения в формулу.
4.Записать ответ.
Слайд 29 Выведение формулы вещества по массовым
соотношениям елементов
Алгоритм 1.Записываем краткое условие задачи. 2.Записываем формулу для вычисления массовых соотношений элементов, указав в скобках их символы: m (А) : m (В) : m (С) = Х: У : Z, 3. Перейти к массовым соотношениям , в которых бы содержалось целое количество атомов каждого вида
4. Записать формулу вещества
Слайд 30Задачи по типу 6
1.Найти простейшую формулу вещества, в состав
которого входят водород, углерод, кислород и азот в массовом соотношении
1:3:4:7.2. Массовые соотношения меди, серы и кислорода в веществе равны 2:1:2. Вывести формулу вещества.
Слайд 33 Итоги изучения
темы
Каждое вещество имеет свою, принадлежащую только ему формулу.
Что же можно
определить по формуле?∙ Качественный состав вещества (элементы, которые его образуют)
∙ Простое или сложное вещество
∙ Количественный состав(количество атомов каждого элемента в
формульной единице)
∙ Соотношения атомов разных элементов в веществе, массовые
соотношения элементов
∙ Относительную молекулярную или формульную массы веществ
∙ Массовую долю элементов в соединении
Слайд 34Вот и наша вершина знаний
Сегодня
каждый из вас одержал свою маленькую победу, овладев материалом темы.
Слайд 35 Домашнее задание
1.Повторить по
учебнику §10
2.Решить задачи по выбору за уровнем
сложности.3.Найти и презентовать интересный материал про минералы, которые не рассматривались сегодня на уроке