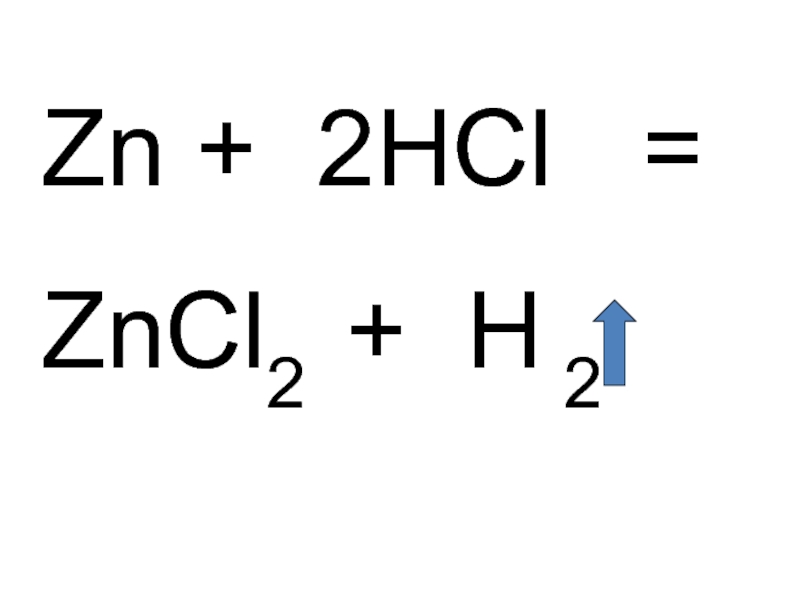Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Окислительно-востановительные реакции
Содержание
- 1. Окислительно-востановительные реакции
- 2. горение
- 3. сгорание топлива
- 4. Получение металлов
- 5. коррозия металлов и сплавов
- 6. БрожениеГниение
- 7. фотосинтез это единственно важный первичный источник энергии
- 8. ОВР- это такие реакции, при которых происходит
- 9. Cуть ОВР- переход электронов от одних атомов, молекул или ионов к другим.
- 10. ОКИСЛЕНИЕ – ОТДАЧА ЭЛЕКТРОНОВ(повышение с.о.)ВОССТАНОВЛЕНИЕ-ВЗЯТИЕ ЭЛЕКТРОНОВ(понижение с.о.)
- 11. Восстановители (отдающие электроны): металлы, водород, уголь, СO,сероводород,
- 12. Внимание!!! Самостоятельная работа...
- 13. Лабораторные опыты:
- 14. ЛАБОРАТОРНЫЙ ОПЫТ №1 Zn + HCl =КУСОЧЕК ЦИНКА ОПУСТИТЕВ ПРОБИРКУ С РАСТВОРОМ СОЛЯНОЙ КИСЛОТЫ
- 15. Zn + 2HCl =ZnCl2 + H 2
- 16. ЛАБОРАТОРНЫЙ ОПЫТ №2 Железный гвоздик опустите в
- 17. Fe + CuSO4 = Cu + FeSO4
- 18. Демонстрационный опыт РастворKMnO4(малиновый)H2SO4 Средакислаябесцветный Н2О Среданейтральнаябурый КOH Средащелочнаязелёный
- 19. (MnO4 )-Mn2+MnO2(MnO4) 2-БЕСЦВЕТНЫЙ РАСТВОРБУРЫЙ ОСАДОКЗЕЛЁНЫЙ РАСТВОР
- 20. СОСТАВЬТЕ УРАВНЕНИЯ овр МЕТОДОМ ЭЛЕКТРОННОГО БАЛАНСА: I
- 21. выводы: 4)среда оказывает влияние на процесс. 1)овр
- 22. Hg + KMnO4 + HCl= Hg Cl2
- 23. Скачать презентанцию
горение
Слайды и текст этой презентации
Слайд 7фотосинтез
это единственно важный первичный источник энергии для всего живого
6CO2 + 6H2O -> C6H12O6 + 6O2
Слайд 8ОВР- это такие реакции, при которых происходит изменение степеней окисления
атомов химических элементов или ионов, образующих реагирующие вещества.
Слайд 10ОКИСЛЕНИЕ – ОТДАЧА ЭЛЕКТРОНОВ
(повышение с.о.)
ВОССТАНОВЛЕНИЕ-ВЗЯТИЕ ЭЛЕКТРОНОВ
(понижение с.о.)
Слайд 11Восстановители (отдающие электроны): металлы, водород, уголь, СO,сероводород, аммиак.
Окислители(принимающие электроны): O2
,галогены, азотная и серная кислоты,KMnO4 , K2Cr2O7 .
Слайд 18Демонстрационный опыт
Раствор
KMnO4
(малиновый)
H2SO4
Среда
кислая
бесцветный
Н2О
Среда
нейтральная
бурый
КOH
Среда
щелочная
зелёный
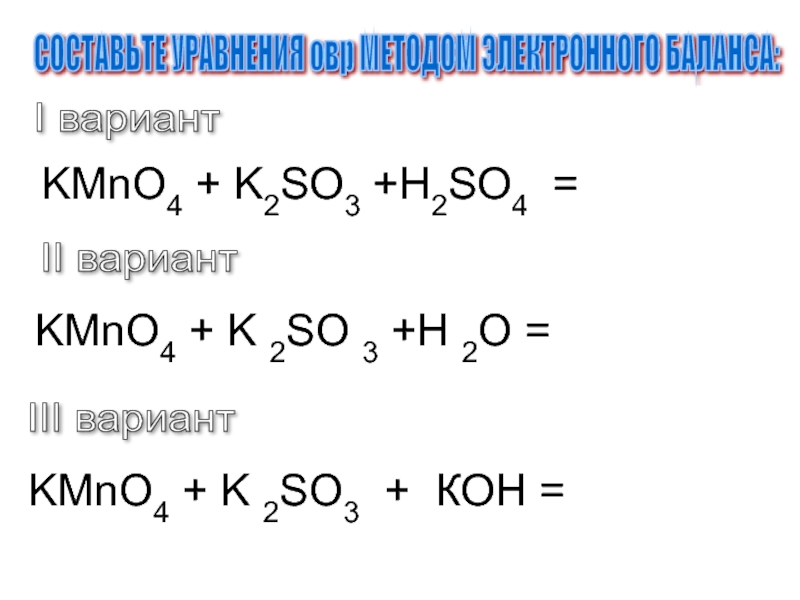
Слайд 20СОСТАВЬТЕ УРАВНЕНИЯ овр МЕТОДОМ ЭЛЕКТРОННОГО БАЛАНСА:
I вариант
KMnO4 +
K2SO3 +H2SO4 =
II вариант
KMnO4 + K
2SO 3 +H 2O =III вариант
KMnO4 + K 2SO3 + КOH =
Слайд 21выводы:
4)среда оказывает влияние на процесс.
1)овр чрезвычайно распространены;
2)суть
овр-переход электронов от одних
атомов,молекул или ионов к другим;
3)овр-единство
двух противоположных процессов-окисления и восстановления;