Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Периодическая система Д.И.Менделеева
Содержание
- 1. Периодическая система Д.И.Менделеева
- 2. Д.И.Менделеев (1834 – 1907 г.)Мир сложен, Он
- 3. Как все начиналось… Выдающийся шведский химик Берцелиус
- 4. Триады Деберейнера (1816 г.)Немецкий химик И.В. Деберейнер
- 5. Спираль Шанкуртуа (1862 г.)Профессор парижской высшей
- 6. Классификация Мейера (1864 г.) Немецкий исследователь Л.
- 7. Раздумья днем и ночью…До Д.И. Менделеева было
- 8. 17 февраля 1869 годаСтатья Менделеева "Опыт системы
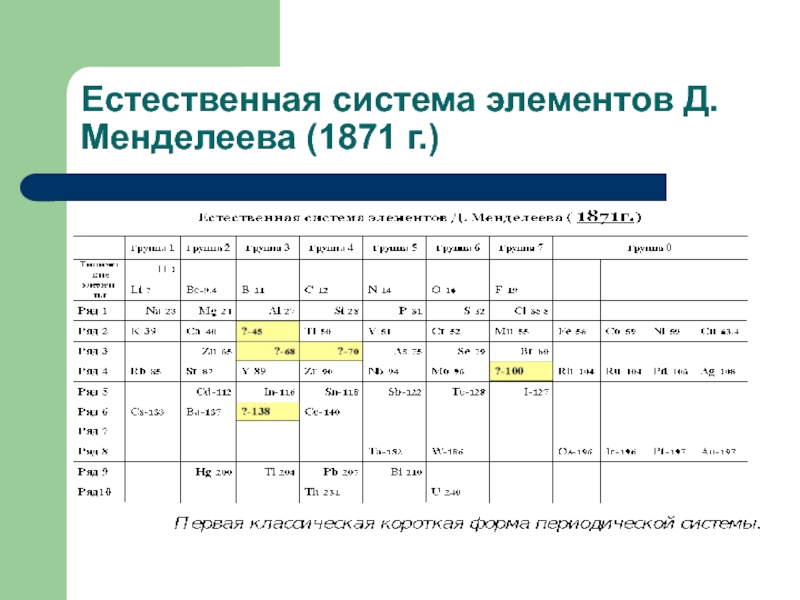
- 9. Естественная система элементов Д.Менделеева (1871 г.)
- 10. Таблица 1920 года
- 11. Периодический закон – основа современной химии.Периодический закон
- 12. Современная формулировка законаФормулировка 1: Свойства химических элементов
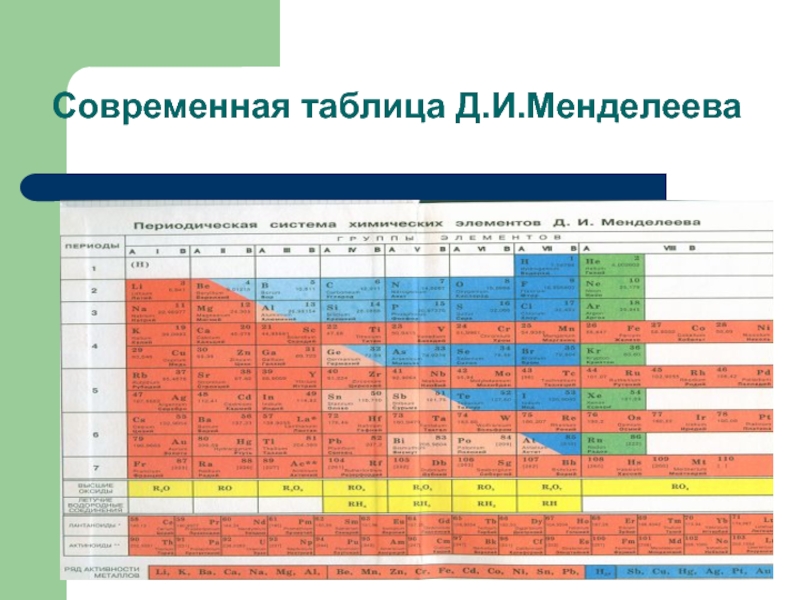
- 13. Современная таблица Д.И.Менделеева
- 14. Главный закон химииСовременная химия много привнесла в
- 15. Скачать презентанцию
Д.И.Менделеев (1834 – 1907 г.)Мир сложен, Он полон событий, сомнений,И тайн бесконечных, и смелых догадок.Как чудо Природы является генийИ в хаосе этом наводим порядок…Весь мир большой: жара и стужа,Планет круженье, свет
Слайды и текст этой презентации
Слайд 1Периодическая система Д.И.Менделеева.
Пропастина Любовь Сергеевна
11 класс
МОУ СОШ № 12
п.
Комсомолец
Слайд 2Д.И.Менделеев (1834 – 1907 г.)
Мир сложен, Он полон событий, сомнений,
И
тайн бесконечных, и смелых догадок.
Как чудо Природы является гений
И в
хаосе этом наводим порядок…Весь мир большой: жара и стужа,
Планет круженье, свет зари –
Все то, что видим мы снаружи,
Законом связано внутри.
Найдётся ль правило простое,
Что целый мир объединит?
Таблицу Менделеев стрит.
Природы ищет Алфавит.
Слайд 3Как все начиналось…
Выдающийся шведский химик Берцелиус разделил все элементы
на металлы и неметаллы на основе различий в свойствах, образованных
ими простых веществ и соединений. Он определил, что металлы соответствуют основные оксиды и основания, а неметаллам – кислотные оксиды и кислоты.Слайд 4Триады Деберейнера (1816 г.)
Немецкий химик И.В. Деберейнер разделил элементы по
три на основе сходства в свойствах образуемых веществ и так,
чтобы величина, которую мы сейчас понимаем как относительную атомную массу среднего элемента, была равна среднему арифметическому двух крайних. Пример триад:Li Ca Cl S Mn
Na Sr Br Se Sr
K Ba I Te Fe
Слайд 5Спираль Шанкуртуа (1862 г.)
Профессор парижской высшей
Li
Fшколы Шанкуртуа предложил
располагать элементы по спирали Na Cl
образующей цилиндр в
порядке возрастания их атомных K Br
масс и указал, что в этом случае
можно заметить сходство свойств Rb I
образуемых элементами веществ,
если они попадают на одну и ту же
вертикальную линию цилиндра,
располагаясь один под другим, например:
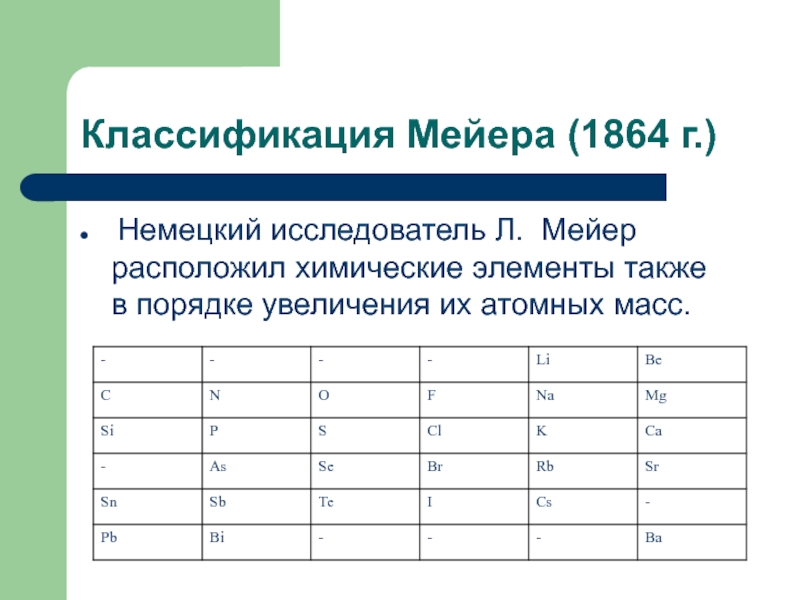
Слайд 6Классификация Мейера (1864 г.)
Немецкий исследователь Л. Мейер расположил химические
элементы также в порядке увеличения их атомных масс.
Слайд 7Раздумья днем и ночью…
До Д.И. Менделеева было предпринято более 50
попыток классифицировать химические элементы. Большинство учёных пытались выявить связь между
химическими свойствами и их соединений и атомной массой.Слайд 817 февраля 1869 года
Статья Менделеева "Опыт системы элементов, основанной на
их атомном весе и химическом сходстве" датирована "17 февраля 1869
года" (это по старому стилю).Так был открыт Периодический закон, современная формулировка которого такова:
«Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядер их атомов».
Слайд 11Периодический закон – основа современной химии.
Периодический закон является основным законом
современности. Выводы, сделанные Д.И.Менделеевым, находят свое подтверждение и в настоящее
время. Происходят открытия новых химических элементов, которые находят свое место в Периодической системе.Современные формулировки Периодического закона созвучны формулировкам Д.И.Менделеева. Периодическая система химических элементов, естественная система химических элементов, разработанная Д. И. Менделеевым на основе открытого им (1869) периодического закона.
Слайд 12Современная формулировка закона
Формулировка 1: Свойства химических элементов и образованных ими
веществ находятся в периодической зависимости от их относительных атомных масс.
Формулировка
2: Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от зарядов их атомных ядерФормулировка 3: Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от периодичности в изменении конфигураций внешних электронных слоёв атомов химических элементов.