Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Природный и попутный газ
Содержание
- 1. Природный и попутный газ
- 2. Классификация газовдобывают из газовых месторожденийрастворены в нефти и добываются вместе с ней
- 3. Классификация газов
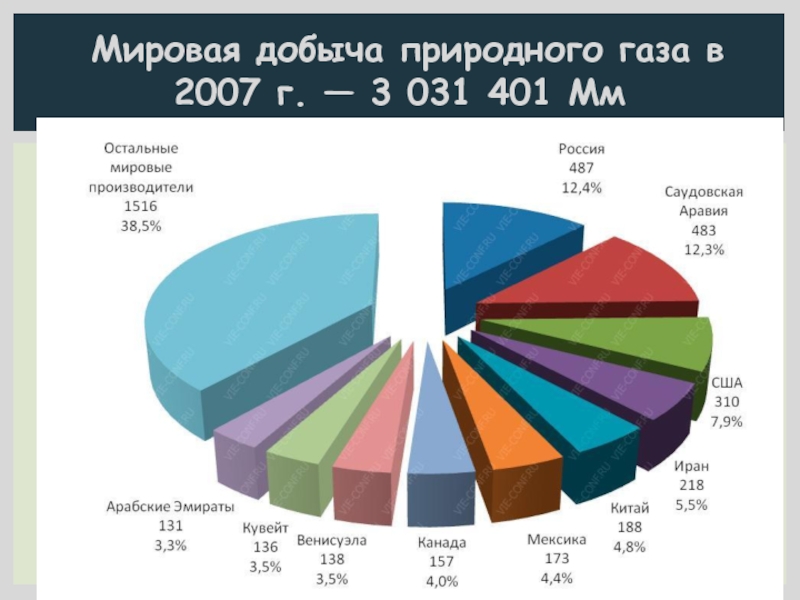
- 4. Мировая добыча природного газа в 2007 г. — 3 031 401 Мм
- 5. Россия занимает 1–е место в мире по
- 6. Газодобывающие регионы
- 7. Применение:
- 8. Природный газ - топливо
- 9. подачу газа в печь легко регулировать;теплота сгорания
- 10. Природный газзависит от месторождения
- 11. Гомология, номенклатураCnH2n+2 n≥1n=2 C2H6этанСН3─СН3n=3 C3H8СН3─СН2─СН3пропанn=4 C4H10СН3─СН2─СН2─СН3бутанn=5
- 12. IUPAC — International Union of Pure and Applied
- 13. Радикал - алкил СН4 метан
- 14. С2Н5 ― этил C3H7―
- 15. Гомология, изомериядля алканов характерны явления гомологии и
- 16. Как составить формулы гомологовНазовите вещество и составьте
- 17. Как составить формулы изомеровНазовите вещество; составьте и
- 18. Гомология, изомерия, номенклатура1 2
- 19. Гомология, изомерия, номенклатура1
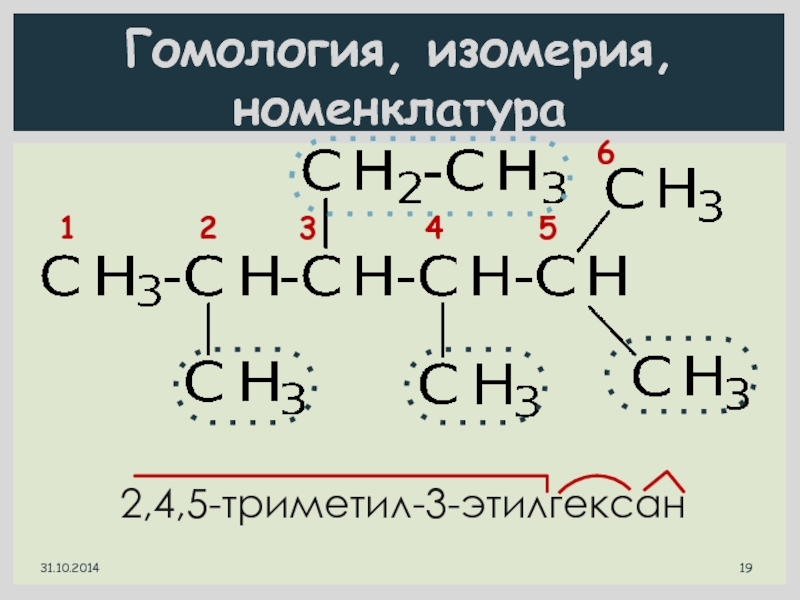
- 20. Гомология, изомерия, номенклатура2,3,4-триметилгексан45 6123
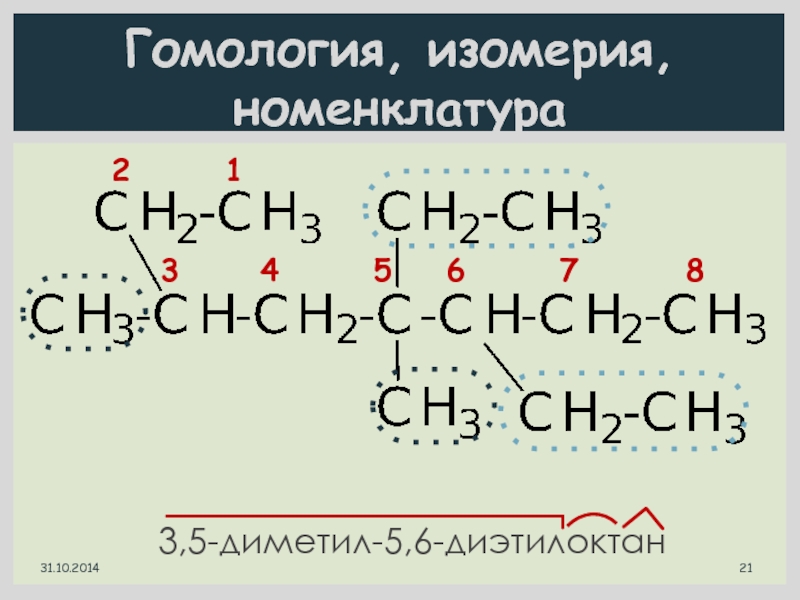
- 21. Гомология, изомерия, номенклатура3,5-диметил-5,6-диэтилоктан2 13
- 22. Физические и химические свойства алканов. Применение.Природный газ – химическое сырье
- 23. Физические свойстваС1-С4З, Ц, H2O С5-С15З,
- 24. Получение алканов в лабораторииCH3COONa + NaOH Na2CO3 + CH4прокаливание
- 25. Химические свойства Алканы - парафины (химически мало активные вещества): все реакции протекают в «жестких» условиях
- 26. CH4 + O2 → CO2 +
- 27. Реакции галогенирования – реакция, в результате которой происходит замещение атомов Н в молекулах алканов атомами галогенов.
- 28. Реакции галогенирования– ступенчатый процесс:
- 29. Реакции галогенирования H H
- 30. Реакции нитрования (Коновалова)-это реакция с азотной кислотой,
- 31. Термическое разложениеСН4 С
- 32. Слайд 32
- 33. Дегидроциклизация и ароматизациян-С6Н14t,Ptt,Pt-Н2-3Н2C6Н12C6Н6н-С7Н16t,PtCН3C6Н11-CH3-Н2t,Pt-3Н2CН3C6Н5-CH3
- 34. C32H66 → C16H34 + C16H32C16H34 → C8H18
- 35. §3, упр.1-12; Т.П.О.Самостоятельная работаДомашнее задание
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Классификация газов
добывают из газовых месторождений
растворены в нефти и добываются вместе
с ней
Слайд 5Россия занимает 1–е место в мире по добыче и экспорту
природного газа (35% мировой добычи газа);
Слайд 9подачу газа в печь легко регулировать;
теплота сгорания газа выше, чем
у др. видов топлива (при сгорании 1м3 газа выделяется 54400кДж);
при
его сгорании не образуется зола, его продукты сгорания являются максимально чистыми в экологическом отношении.Преимущества перед другими видами топлива
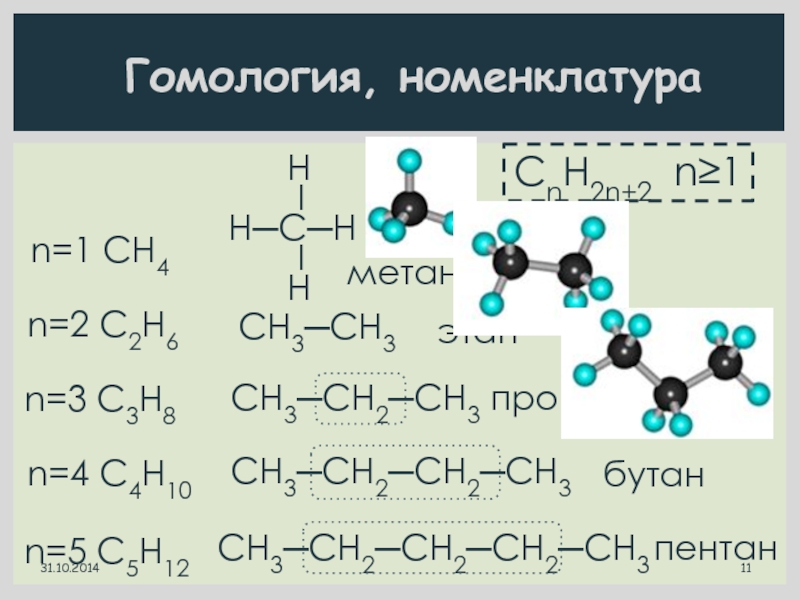
Слайд 11Гомология, номенклатура
CnH2n+2 n≥1
n=2 C2H6
этан
СН3─СН3
n=3 C3H8
СН3─СН2─СН3
пропан
n=4 C4H10
СН3─СН2─СН2─СН3
бутан
n=5 C5H12
СН3─СН2─СН2─СН2─СН3
пентан
n=1 CH4
метан
Н
I
Н─С─Н
I
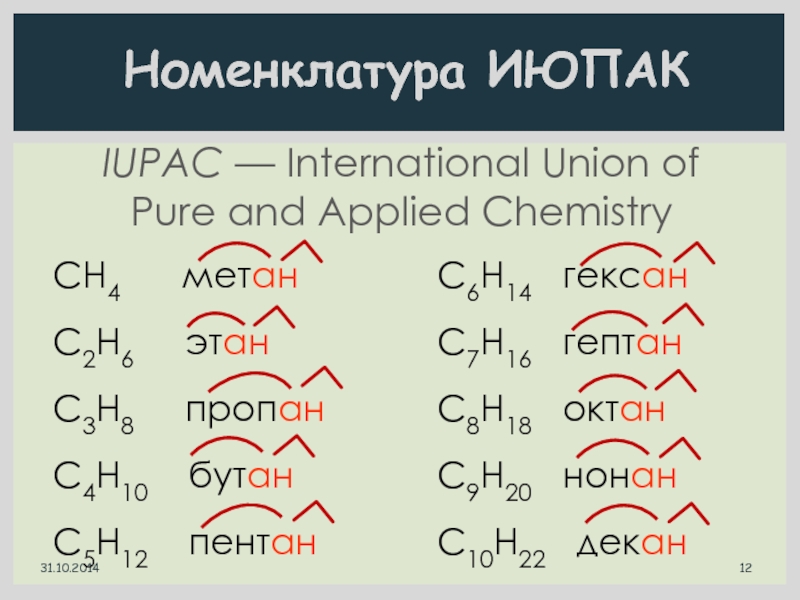
НСлайд 12IUPAC — International Union of Pure and Applied Chemistry
Номенклатура ИЮПАК
СН4
метан
С2H6 этан
C3H8
пропанC4H10 бутан
C5H12 пентан
C6H14 гексан
C7H16 гептан
C8H18 октан
C9H20 нонан
C10H22 декан
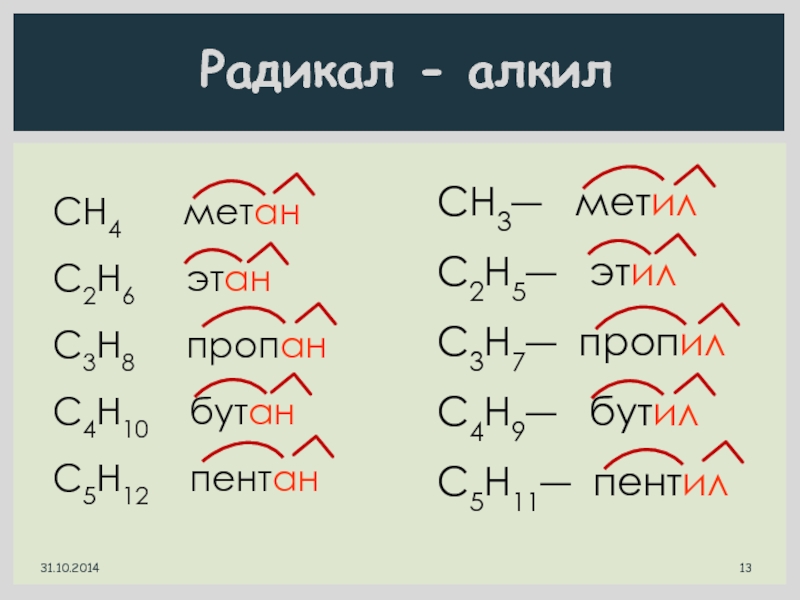
Слайд 13Радикал - алкил
СН4 метан
С2H6 этан
C3H8 пропан
C4H10 бутан
C5H12
пентанCH3― метил
C2H5― этил
C3H7― пропил
C4H9― бутил
C5H11― пентил
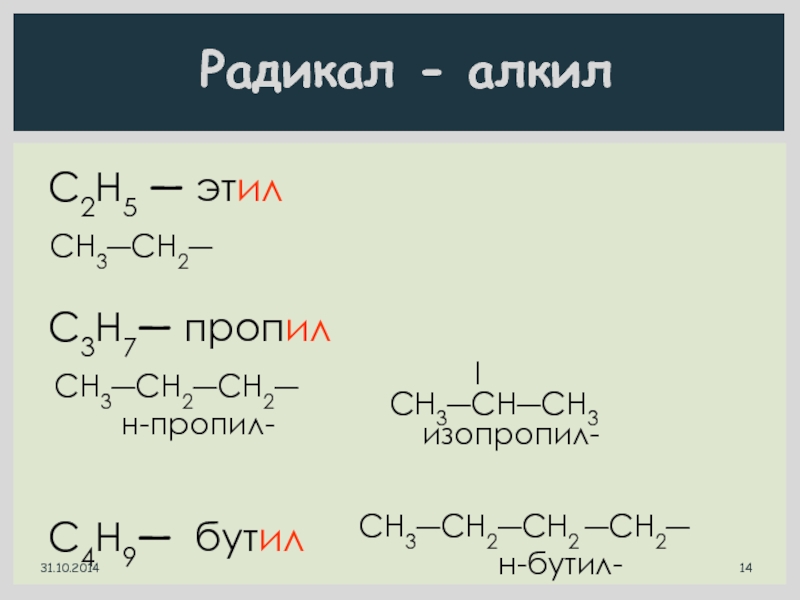
Слайд 14С2Н5 ― этил
C3H7― пропил
C4H9― бутил
CH3―CH2―
CH3―CH2―CH2―
н-пропил-
l
CH3―CH―CH3
изопропил-
CH3―CH2―CH2 ―CH2―
н-бутил-
Радикал - алкил
Слайд 15Гомология, изомерия
для алканов характерны явления гомологии и изомерии.
Гомологи - вещества,
имеющие сходное строение и свойства, но отличаются друг от друга
на одну или несколько (-СН2-)групп.Изомеры – вещества, имеющие одинаковый качественный и количественный состав, но разное строение, поэтому разные свойства.
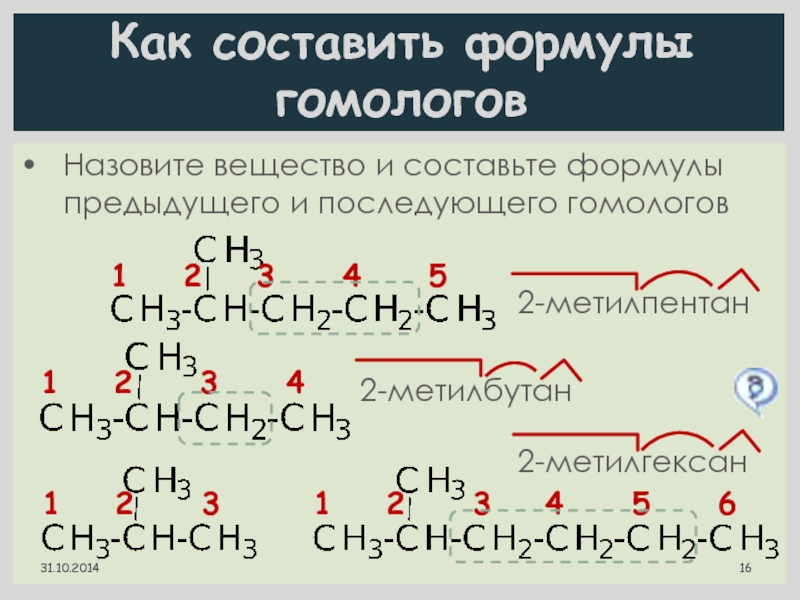
Слайд 16Как составить формулы гомологов
Назовите вещество и составьте формулы предыдущего и
последующего гомологов
1 2 3 4
52-метилпентан
1 2 3 4
1 2 3
1 2 3 4 5 6
2-метилбутан
2-метилгексан
Слайд 17Как составить формулы изомеров
Назовите вещество; составьте и назовите формулы трех
изомеров
1 2 3 4
5 62-метилгексан
С7Н16
C―C―C―C―C―C―C
1 2 3 4 5 6 7
CH3-CH2-CH2-CH2-CH2-CH2-CH3
1 2 3 4 5 6 7
гептан
1 2 3 4 5 6
3-метилгексан
1 2 3 4 5
2,4-диметилпентан
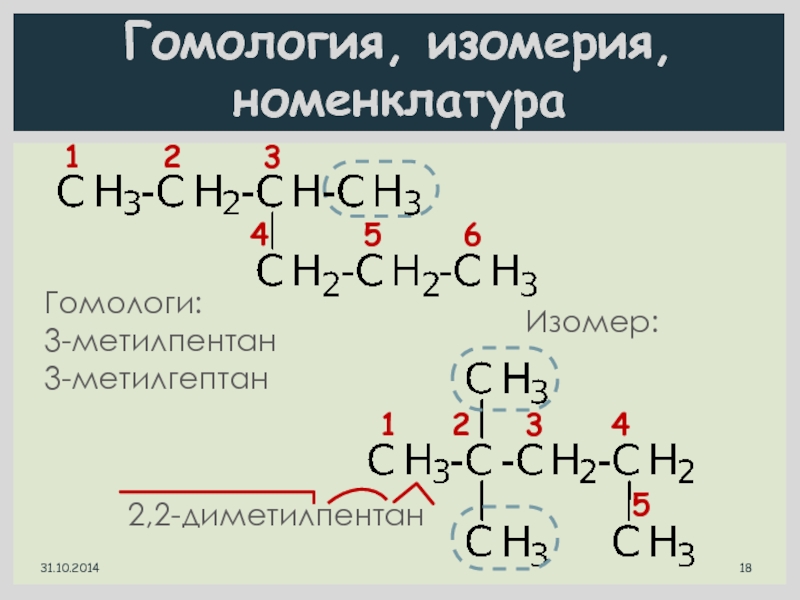
Слайд 18Гомология, изомерия, номенклатура
1 2 3
4
5 6
3-метилгексан
Гомологи:
3-метилпентан
3-метилгептан
Изомер:
1 2 3
45
2,2-диметилпентан
Слайд 23Физические свойства
С1-С4
З, Ц, H2O
С5-С15
З, H2O
С16-и выше
З,
Ц, H2O
жидкие ─
хорошие
растворители
Слайд 25Химические свойства
Алканы - парафины
(химически мало активные вещества): все
реакции протекают
в «жестких» условиях
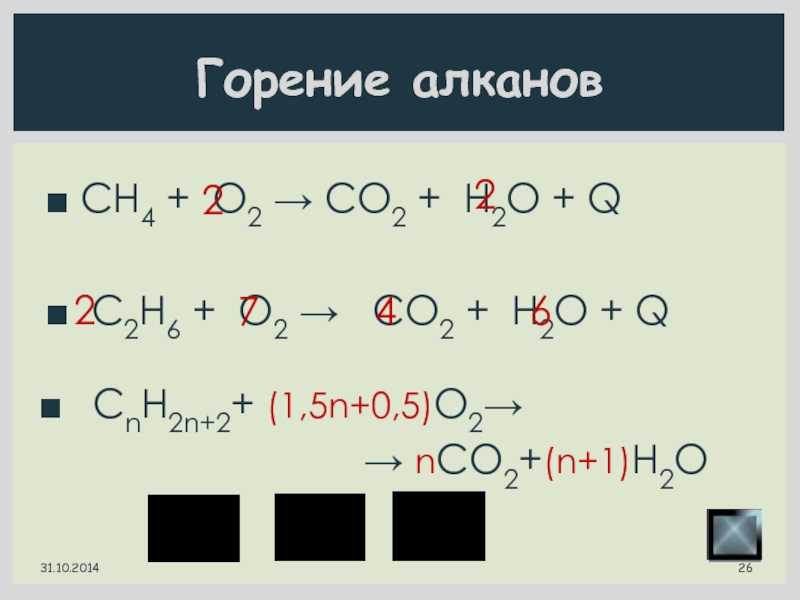
Слайд 26 CH4 + O2 → CO2 + H2O + Q
C2H6 + O2 → CO2 + H2O + Q
Горение
алканов2
2
2
7
4
6
CnH2n+2+ (1,5n+0,5)O2→
→ nCO2+(n+1)H2O
Слайд 27Реакции галогенирования
– реакция, в результате которой происходит замещение атомов
Н в молекулах алканов атомами галогенов.
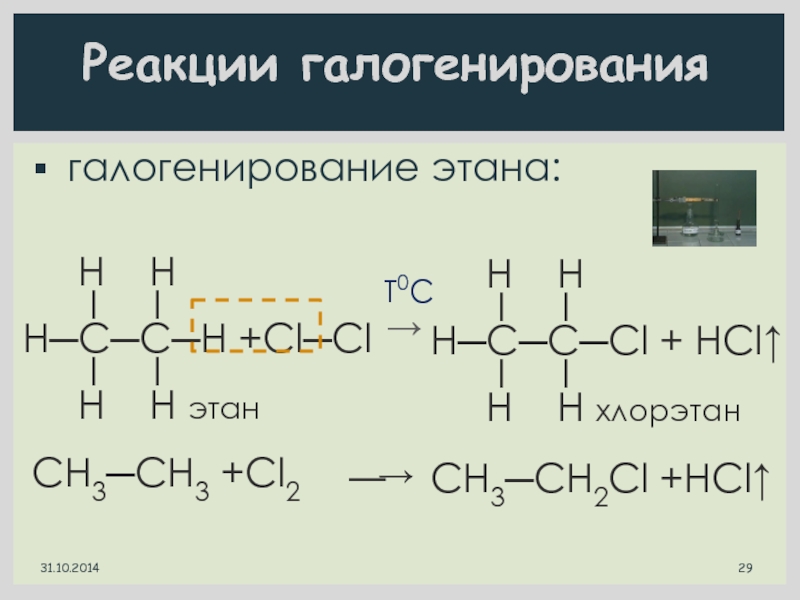
Слайд 29Реакции галогенирования
H H
I I
Н─С─С─Н +Cl─Cl
I
IH H этан
T0C
H H
I I
Н─С─С─Cl + НCl↑
I I
H H хлорэтан
СН3─СН3 +Cl2
СН3─СН2Cl +HCl↑
галогенирование этана:
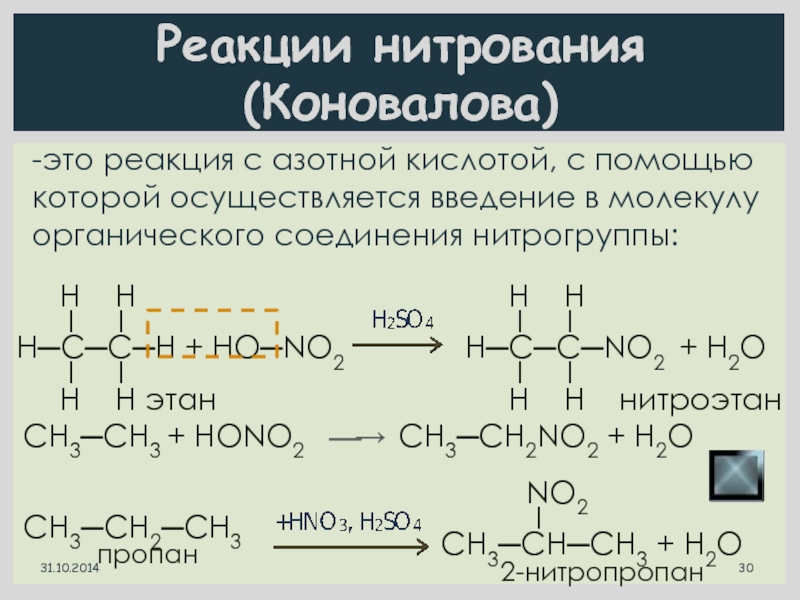
Слайд 30Реакции нитрования (Коновалова)
-это реакция с азотной кислотой, с помощью которой
осуществляется введение в молекулу органического соединения нитрогруппы:
СН3─СН2─СН3
пропан NO2
I
СН3─СН─СН3 + Н2O
2-нитропропан
H H
I I
Н─С─С─Н + HO─NO2
I I
H H этан
H H
I I
Н─С─С─NO2 + H2O
I I
H H нитроэтан
СН3─СН3 + HONO2
СН3─СН2NO2 + H2O
Слайд 31Термическое разложение
СН4 С + 2H2
сажа (полное разложение)
дегидрирование:
10000С
2СН4
С2H2 + 3H2ацетилен (неполное разложение)
15000С
СН3─СН3 CH2=CH2 + H2
этилен
8000С
Слайд 32
CН3
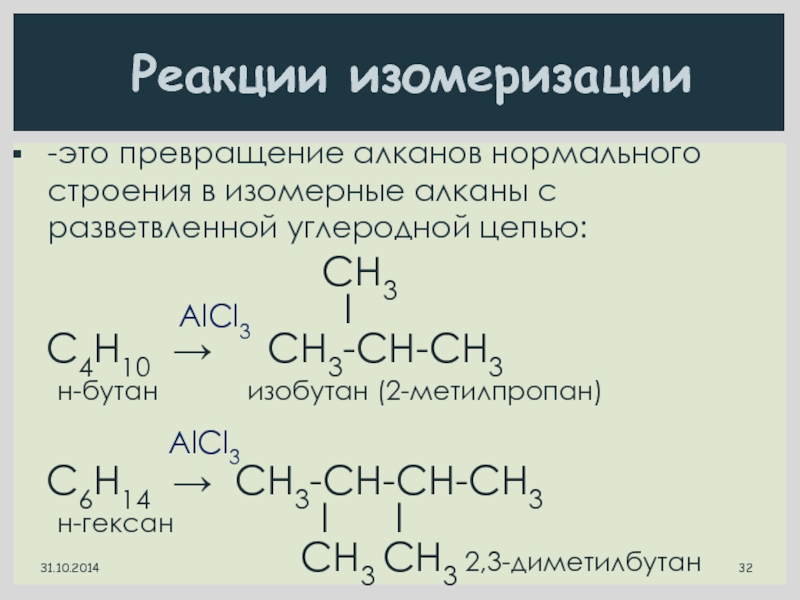
lC4H10 → CН3-СН-СН3
н-бутан изобутан (2-метилпропан)
C6H14 → CН3-СН-СН-СН3
н-гексан l l
CН3 CН3 2,3-диметилбутан
Реакции изомеризации
AlCl3
AlCl3
-это превращение алканов нормального строения в изомерные алканы с разветвленной углеродной цепью:
Слайд 33Дегидроциклизация и ароматизация
н-С6Н14
t,Pt
t,Pt
-Н2
-3Н2
C6Н12
C6Н6
н-С7Н16
t,Pt
CН3
C6Н11-CH3
-Н2
t,Pt
-3Н2
CН3
C6Н5-CH3
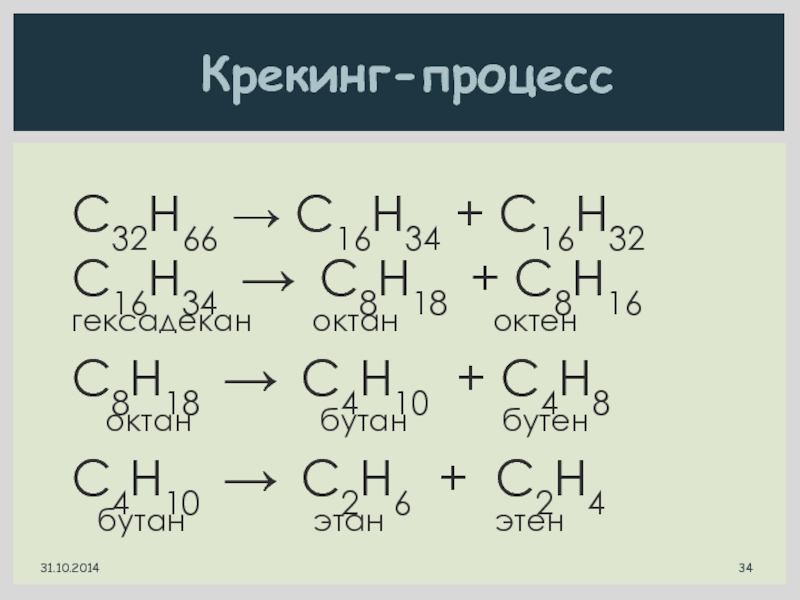
Слайд 34C32H66 → C16H34 + C16H32
C16H34 → C8H18 + C8H16
гексадекан
октан октен
C8H18 →
C4H10 + C4H8октан бутан бутен
C4H10 → C2H6 + C2H4
бутан этан этен
Крекинг-процесс