Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
СЕРА S
Содержание
- 1. СЕРА S
- 2. Девиз урока :« Жить – значит узнавать»S
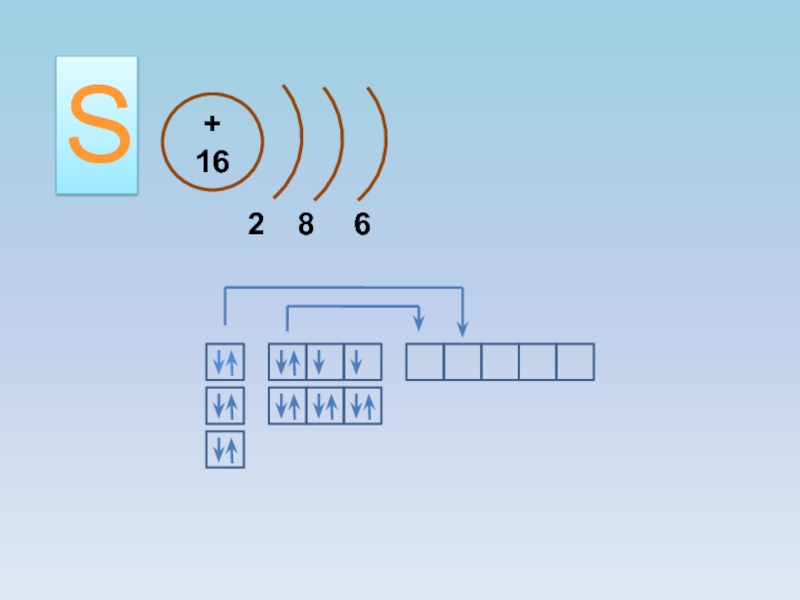
- 3. + 16286S
- 4. Для серы характерны степени окисления -2,
- 5. Сера ромбическаяСера пластическая Сера моноклиннаяЦвет –
- 6. У жёлтой серы есть корона,Но нет ни
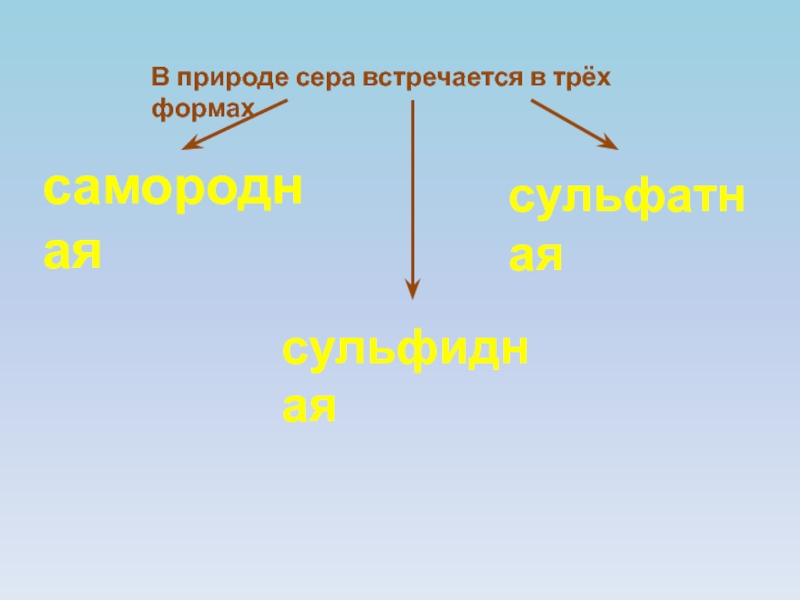
- 7. В природе сера встречается в трёх формахсамороднаясульфиднаясульфатная
- 8. О каких соединениях серы упоминал А.С.Пушкин в
- 9. Химические свойства серыS1. Взаимодействие с металлами.21восстановительокислитель
- 10. Взаимодействие серы с натрием (видеоопыт)http://files.school-collection.edu.ru/dlrstore/3e6b77cf-8fff-882a-d3c3-c50221c6eba9/index.htm
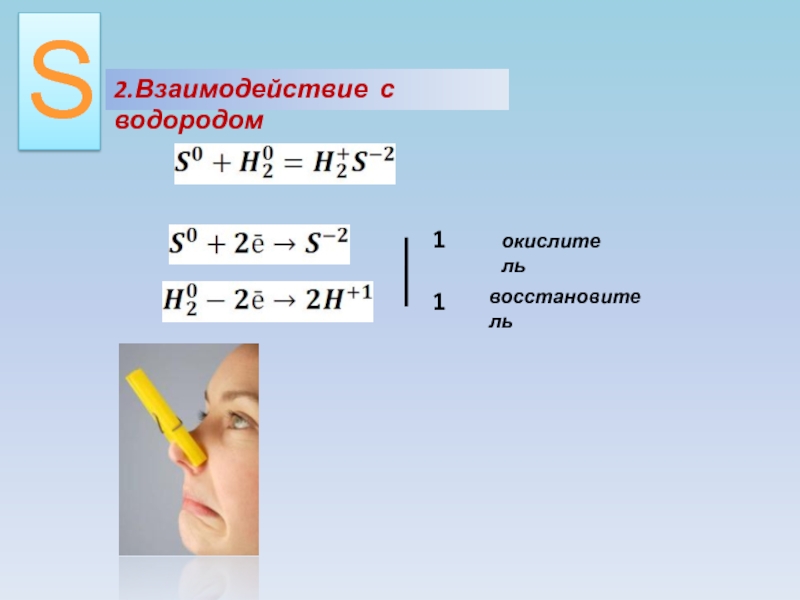
- 11. 2.Взаимодействие с водородом11окислительвосстановительS
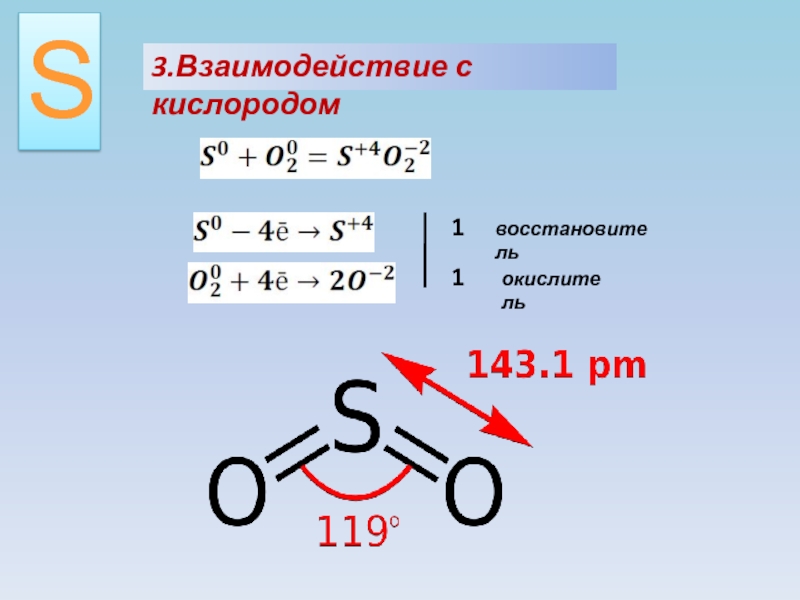
- 12. 3.Взаимодействие с кислородомS11восстановительокислитель
- 13. Диоксид серы – загрязнитель атмосферы
- 14. S
- 15. Уравнение реакции, в котором сера является окислителем:А.
- 16. ДОМАШНЕЕ ЗАДАНИЕ:§22, упр. 1, 2.
- 17. Скачать презентанцию
Слайды и текст этой презентации
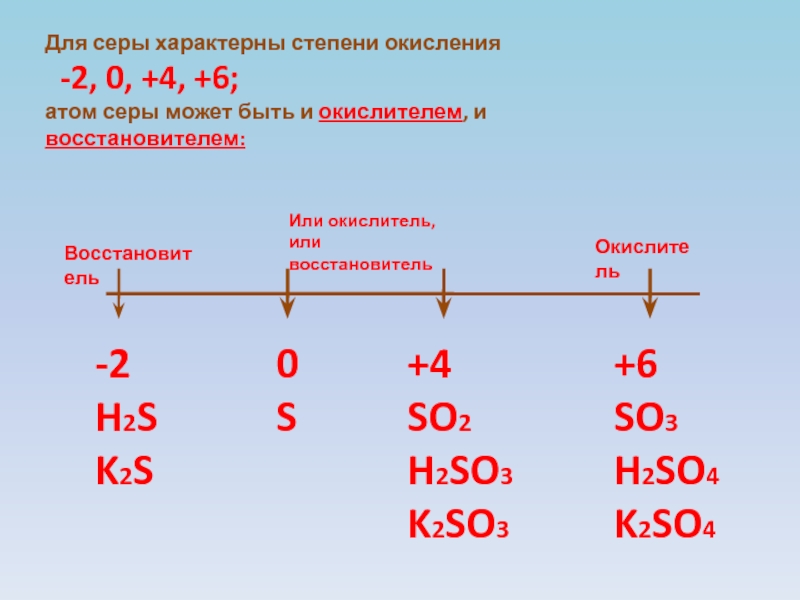
Слайд 4Для серы характерны степени окисления
-2, 0, +4, +6;
атом
серы может быть и окислителем, и восстановителем:
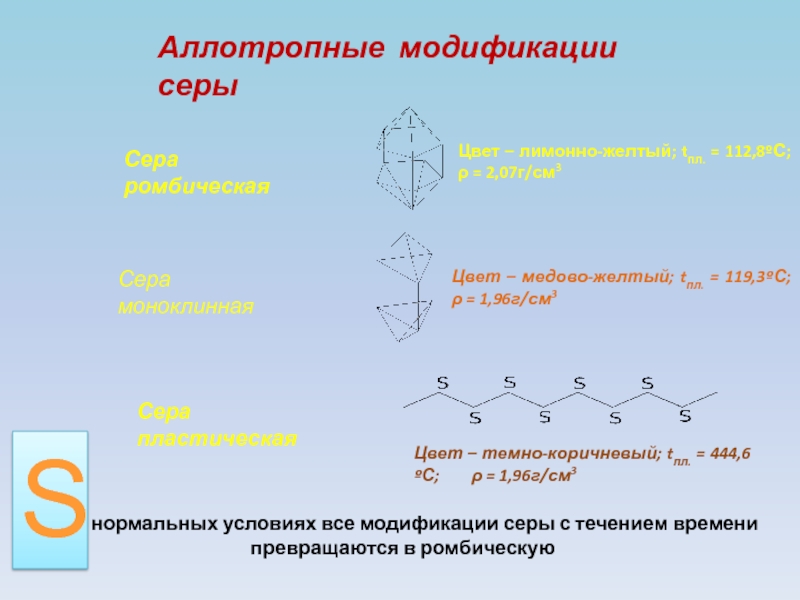
Слайд 5Сера ромбическая
Сера пластическая
Сера моноклинная
Цвет – лимонно-желтый; tпл. =
112,8ºС; ρ = 2,07г/см3
Цвет – медово-желтый; tпл.
= 119,3ºС; ρ = 1,96г/см3Цвет – темно-коричневый; tпл. = 444,6ºС; ρ = 1,96г/см3
При нормальных условиях все модификации серы с течением времени превращаются в ромбическую
S
Аллотропные модификации серы
Слайд 6У жёлтой серы есть корона,
Но нет ни подданных, ни трона.
Корону
сера надевает,
Когда устойчивой бывает.
Нагрев ведёт к кристаллам длинным
Бесцветной серы моноклинной.
S
Слайд 8О каких соединениях серы упоминал А.С.Пушкин в стихотворении,
написанном в 1832г.?
Тогда
услышал я (о диво) запах скверный,
Как будто тухлое разбилося яйцо
Иль
карантинный страж курил жаровней серной.Я, нос себе зажав, отворотил лицо…
Ответ: о сероводороде H2S и диоксиде серы SO2, который
с глубокой древности использовали для дезинфекции
(окуривание горящей серой).
S
Слайд 10Взаимодействие серы с натрием
(видеоопыт)
http://files.school-collection.edu.ru/dlrstore/3e6b77cf-8fff-882a-d3c3-c50221c6eba9/index.htm
Слайд 15Уравнение реакции, в котором сера является окислителем:
А. Zn + S
→ ZnS
Б. 2SO2 + O2 → 2SO3В. S + Cl2 → SCl2 Г. SO3 + H2O → H2SO4
Свойство, не характерное для серы:
А. Растворима в воде
Б. Не проводит электрический ток
В. твердое вещество желтого цвета
Г. Горит
Сумма всех коэффициентов в уравнении реакции:
MgS + O2 → MgO + SO2
А. 4 Б. 6 В. 9 Г. 12