Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соединения хрома в заданиях ЕГЭ уровня С
Содержание
- 1. Соединения хрома в заданиях ЕГЭ уровня С
- 2. «Мыслящий ум не чувствует себя счастливым, пока
- 3. Поведение соединений хрома в различных средахПроверка теоретических знаний
- 4. Зависимость свойств соединений хрома от степени окисления. Заполните таблицу.
- 5. Зависимость свойств соединений хрома от степени окисления.
- 6. Дихромат и хромат - окислителиK2Cr2O7 (кислая и
- 7. K2Cr2O7 (кислая и нейтральная среда), K2Cr
- 8. Изменение степени
- 9. Cr+3 + очень сильные
- 10. Дихроматы получаются при действии на хроматы ….?Na2CrO4
- 11. Превращение солей хромаДихроматы получаются при действии на
- 12. Поведение солей хрома в различных средах Работа с заданиями уровня С
- 13. Сr2(SO4)3 + KMnO4 + … = K2CrO4
- 14. Найдите в реакциях ошибочные продукты, объясните, почему
- 15. Работа экспертов :Найдите в реакциях ошибочные продукты,
- 16. не может получиться такое вещество, которое вступает
- 17. не может получиться такое вещество, которое вступает
- 18. Серо-зелёный порошок оксида хрома (III) сплавили с
- 19. 1. Cr2O3 + Br2 +NaOH→2. Cr(OH)3 +Cl2
- 20. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2«Мыслящий ум не чувствует себя счастливым, пока не удастся связать
воедино разрозненные факты, им наблюдаемые»
Д. Хевеши
Слайд 6Дихромат и хромат - окислители
K2Cr2O7 (кислая и нейтральная среда),
K2Cr O 4 (щелочная среда)
+ восстановители всегда
получается …..?кислая среда нейтральная среда щелочная среда
? в растворе …?.
?
в расплаве …?.
Слайд 7K2Cr2O7 (кислая и нейтральная среда),
K2Cr O 4 (щелочная
среда)
+ восстановители всегда получается Cr+3
кислая среда нейтральная
среда щелочная средаСоли тех кислот,
которые участвуют в в растворе
реакции:
в расплаве
Дихромат и хромат - окислители
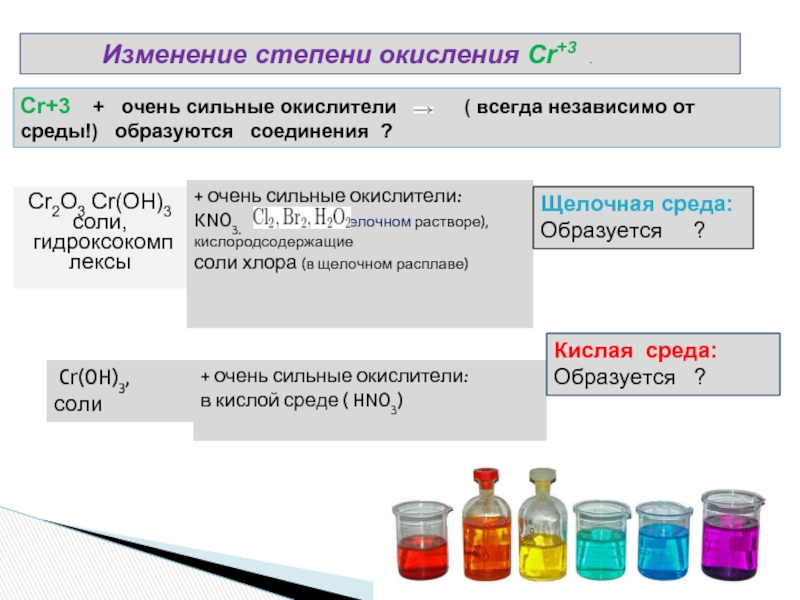
Слайд 8 Изменение степени окисления Cr+3 .
Cr+3
+ очень сильные окислители
( всегда независимо от среды!) образуются соединения ?+ очень сильные окислители:
KNO3. ( в щелочном растворе),кислородсодержащие
соли хлора (в щелочном расплаве)
Щелочная среда:
Образуется ?
Cr(OH)3,
соли
+ очень сильные окислители:
в кислой среде ( HNO3)
Кислая среда:
Образуется ?
Слайд 9
Cr+3 + очень сильные окислители
Cr+6 ( всегда независимо от среды!)
+ очень сильные окислители:
KNO3. ( в щелочном растворе),кислородсодержащие
соли хлора (в щелочном расплаве)
Щелочная среда:
Образуется хромат
K2CrO4
Cr(OH)3,
соли
+ очень сильные окислители:
в кислой среде ( HNO3)
Кислая среда:
Образуется дихромат
K2Cr2O 7
Изменение степени окисления Cr+3
Слайд 10Дихроматы получаются при действии на хроматы ….?
Na2CrO4 + ?= Na2Cr2O7
+ ?+ ?
Возможен и обратный переход при добавлении ….
? к растворам дихроматовNa2Cr2O7 + …? = Na2CrO4 + ?
Превращение солей хрома
Слайд 11Превращение солей хрома
Дихроматы получаются при действии
на хроматы кислот
2 Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + Н2О
Возможен и обратный переход при добавлении щелочей к растворам дихроматов
Na2Cr2O7 + 2NaOH = 2Na2CrO4 + Н2О
Равновесие в системе хромат-дихромат можно представить следующими уравнениями:
2СrО42- + 2Н+ = Сr2О72- + Н2О
Сr2О72- + 2ОН- = 2 CrO 42- + Н2О
Слайд 13Сr2(SO4)3 + KMnO4 + … = K2CrO4 + … K2SO4
+ H2O
К2Сr2О7 +Н2S + … = …+ Сr2(SО4)3 + …+
….K2Cr2O7 + SO2 +… = K2SO4 +… + H2SO4
KCrO2 + Br2 +… =Na2CrO4 + KBr +… + H2O
Cr(OH)3 + Ag2O + NaOH = Ag + ? +.. ?
С1 Используя метод электронного баланса, составьте уравнения реакций , определите окислитель и восстановитель.
Слайд 14Найдите в реакциях ошибочные продукты, объясните, почему они не могут
получаться в этих условиях:
Na3 [Сг(OH)6] + Вг2 + NaOH →Na2CrO4
+ HBr + Н2ОNa2SO3 + К2Сг2О7 + H2SO4 →Na2SO4+Cr2(SO4)3 + КOH + H2O
K2Cr2O7 + H2O2 +H2SO4→ Cr2(SO4)3+ КOH + O2 + H2O
Работа экспертов :
Слайд 15Работа экспертов :
Найдите в реакциях ошибочные продукты, объясните, почему они
не могут получаться в этих условиях:
Na3 [Сг(OH)6] + Вг2 +
NaOH →Na2CrO4 + HBr + Н2ОNa2SO3 + К2Сг2О7 + H2SO4 →Na2SO4+Cr2(SO4)3 + КOH + H2O
K2Cr2O7 + H2O2 +H2SO4→ Cr2(SO4)3+ КOH + O2 + H2O
Слайд 16не может получиться такое вещество, которое вступает во взаимодействие со
средой!
а) в …среде не может получиться оксид металла,
основание, аммиак;
б) в …..среде не получится кислота или кислотный оксид;
в) оксид или тем более металл, бурно реагирующие с водой, не образуются в …. растворе. Неверные с химической точки зрения продукты:
Слайд 17не может получиться такое вещество, которое вступает во взаимодействие со
средой!
а) в кислой среде не может получиться оксид
металла, основание, аммиак;
б) в щелочной среде не получится кислота или кислотный оксид;
в) оксид или тем более металл, бурно реагирующие с водой, не образуются в водном растворе. Неверные с химической точки зрения продукты:
Слайд 18Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное
вещество растворили в воде, при этом получился тёмно-зелёный раствор. К
полученному щелочному раствору прибавили пероксид водорода. Получился раствор желтого цвета, который при добавлении серной кислоты приобретает оранжевый цвет. При пропускании сероводорода через полученный подкисленный оранжевый раствор он мутнеет и вновь становится зелёным.составьте уравнения 4-х реакций
Практическая часть С2
Слайд 19
1. Cr2O3 + Br2 +NaOH→
2. Cr(OH)3 +Cl2 +NaOH→
3. CrCl3 +Br2
+KOH→
4. CrCl3 +H2O2 +NaOH→
5. Cr2(SO4)3 + Br2 +NaOH→
6. Cr2(SO4)3 +KMnO4
+KOH→7. K2Cr2O7 + H2O2 +H2SO4→
8. K2Cr2O7 + Fe +H2SO4 →
Домашнее задание.
ОВР. Соединения хрома.
Закончить уравнения реакций.












![Соединения хрома в заданиях ЕГЭ уровня С Найдите в реакциях ошибочные продукты, объясните, почему они не могут получаться Найдите в реакциях ошибочные продукты, объясните, почему они не могут получаться в этих условиях:Na3 [Сг(OH)6] + Вг2](/img/thumbs/a198918a9a230a78e9749d0a27aeb6e9-800x.jpg)
![Соединения хрома в заданиях ЕГЭ уровня С Работа экспертов :Найдите в реакциях ошибочные продукты, объясните, почему они не Работа экспертов :Найдите в реакциях ошибочные продукты, объясните, почему они не могут получаться в этих условиях:Na3 [Сг(OH)6]](/img/thumbs/fa2728f195d72c058ef5bceba3b2b1ed-800x.jpg)























