Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Все о спиртах
Содержание
- 1. Все о спиртах
- 2. Спирты (алканолы) — органические соединенияСпирты (алканолы) —
- 3. СОДЕРЖАНИЕ:☺НОМЕНКЛАТУРА СПИРТОВ;☺КЛАССИФИКАЦИЯ СПИРТОВ;☺СТРОЕНИЕ СПИРТОВ;☺ФИЗИЧЕСКИЕ СВОЙСТВА;☺ХИМИЧЕСКИЕ СВОЙСТВА;☺ИСТОРИЯ ОТКРЫТИЯ
- 4. НОМЕНКЛАТУРА СПИРТОВПо номенклатуре ИЮПАК названия простых спиртов
- 5. НОМЕНКЛАТУРА СПИРТОВ2) Если в молекуле содержится несколько
- 6. КЛАССИФИКАЦИЯ СПИРТОВ☺ по числу гидроксильных групп☺ по
- 7. ПО ЧИСЛУ гидроксильных групп☺ одноатомные спирты (например:
- 8. ПО ХАРАКТЕРУ УГЛЕВОДОРОДНОГО РАДИКАЛА☺ предельные или насыщенные
- 9. В зависимости от того, при каком атоме
- 10. Строение спиртовСпирты имеют геометрическое строение молекулы, похожее
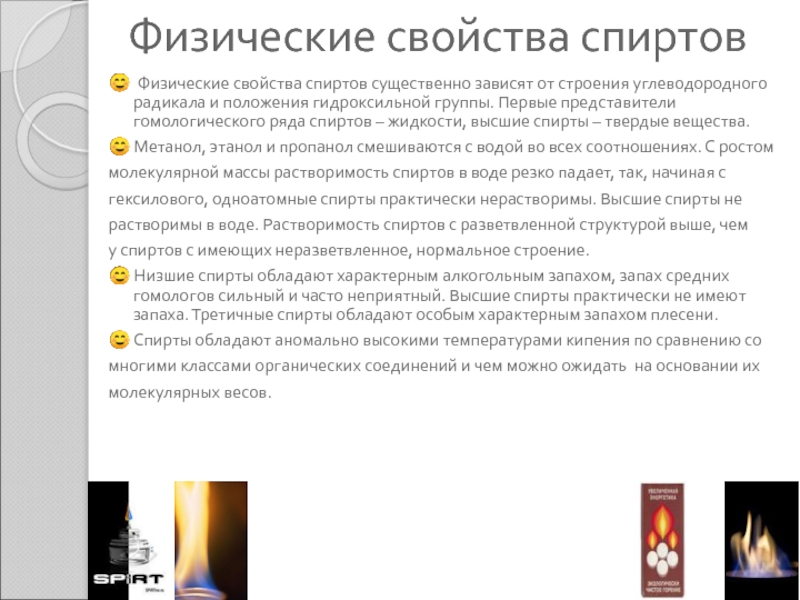
- 11. Физические свойства спиртов☺ Физические свойства спиртов существенно
- 12. Химические свойства спиртов1) Кислотные свойства:
- 13. ИСТОРИЯ ОТКРЫТИЯ СПИРТОВ☺ Считается, что не менее
- 14. НАХОЖДЕНИЕ В ПРИРОДЕ☺ Спирты имеют самое широкое
- 15. Получение спиртов
- 16. Получение спиртов☺ При домашнем и промышленном производстве
- 17. Применение спиртов
- 18. Физиологическое действие и токсичность спиртов☺ Одноатомные предельные
- 19. Действие алкоголя на организм человекаАлкоголь в организме
- 20. Действие алкоголя на организм человека☺ Умеренное потребление
- 21. Действие алкоголя на организм человека☺ Но, если
- 22. Действие алкоголя на организм человека☺ДЕЙСТВИЕ АЛКОГОЛЯ НА
- 23. Список используемой литературы: Алкоголь. Этимологический словарь Фасмера.
- 24. Работу выполнила ученица 10 «А» класса
- 25. Скачать презентанцию
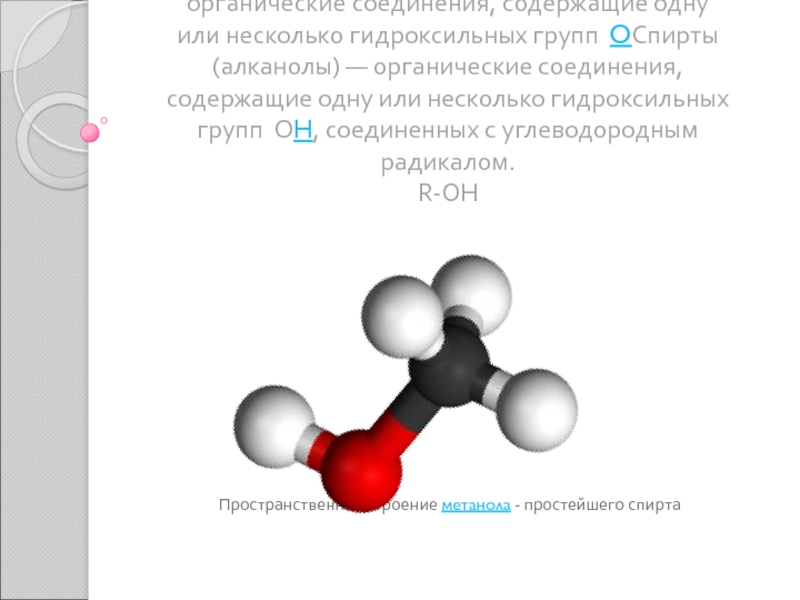
Спирты (алканолы) — органические соединенияСпирты (алканолы) — органические соединения, содержащие одну или несколько гидроксильных группСпирты (алканолы) — органические соединения, содержащие одну или несколько гидроксильных групп OСпирты (алканолы) — органические соединения, содержащие
Слайды и текст этой презентации
Слайд 2Спирты (алканолы) — органические соединенияСпирты (алканолы) — органические соединения, содержащие
Слайд 3СОДЕРЖАНИЕ:
☺НОМЕНКЛАТУРА СПИРТОВ;
☺КЛАССИФИКАЦИЯ СПИРТОВ;
☺СТРОЕНИЕ СПИРТОВ;
☺ФИЗИЧЕСКИЕ СВОЙСТВА;
☺ХИМИЧЕСКИЕ СВОЙСТВА;
☺ИСТОРИЯ ОТКРЫТИЯ СПИРТОВ;
☺НАХОЖДЕНИЕ В ПРИРОДЕ;
☺ПОЛУЧЕНИЕ
СПИРТОВ;
☺ПРИМЕНЕНИЕ СПИРТОВ;
☺ физиологическое действие и токсичность спиртов;
☺ДЕЙСТВИЕ АЛКОГОЛЯ НА ЧЕЛОВЕЧЕСКИЙ
ОРГАНИЗМ;☺ список литературы;
Слайд 4НОМЕНКЛАТУРА СПИРТОВ
По номенклатуре ИЮПАК названия простых спиртов образуются от названий
соответствующих алканов с добавлением суффикса «-ол».
Правила
построения названия спиртов (функциональная группа -OH) :1) в основе названия соединений любого вещества лежит родоначальная структура. Название родоначальной структуры составляет основу названия, корень слова.
Слайд 5НОМЕНКЛАТУРА СПИРТОВ
2) Если в молекуле содержится несколько гидроксильных групп, то
используют умножительную приставку: ди- (этандиол-1,2), три- (пропантриол-1,2,3) и т. д.
3)
Нумерацию главной цепи начинают с того конца, ближе к которому находится гидроксильнаягруппа. По радикально-функциональной номенклатуре название производят от
названия углеводородного радикала, связанного с гидроксильной группой, с
прибавлением слова спирт.
Структурная изомерия спиртов определяется изомерией углеродного скелета и
изомерией положения гидроксильной группы.
☺ Имена заместителей ставятся перед именем родительского углеводорода, а суффикс функциональной группы — после. ИЮПАК рекомендует цифру, характеризующую положение функциональной группы, писать сразу после имени углеводородного радикала перед суффиксом функциональной группы.
Слайд 6КЛАССИФИКАЦИЯ СПИРТОВ
☺ по числу гидроксильных групп
☺ по хар-ру углеводородного радикала
☺ по хар-ру атома углерода, с которым связана гидроксильная группа.
Слайд 7ПО ЧИСЛУ гидроксильных групп
☺ одноатомные спирты (например: метанол);
☺ двухатомные спирты
(например: этиленгликоль);
☺ трехатомные спирты (например: глицерин);
☺ четырёхатомные спирты (например: пентаэритрит);
☺
многоатомные спирты (например: пятиатомный спирт ксилит).Слайд 8ПО ХАРАКТЕРУ УГЛЕВОДОРОДНОГО РАДИКАЛА
☺ предельные или насыщенные спирты (например: бутанол);
☺
непредельные или ненасыщенные спирты (например: аллиловый спирт);
☺ ароматические спирты (например:
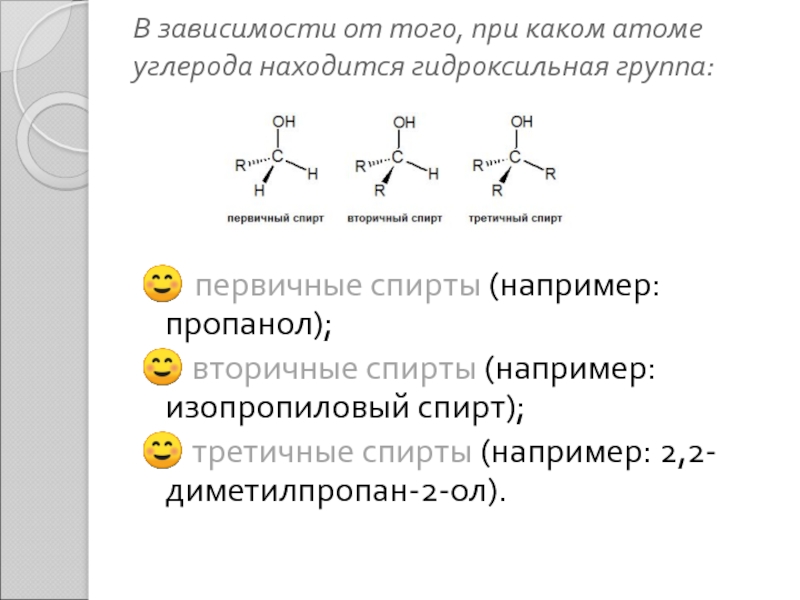
бензиловый спирт).Слайд 9В зависимости от того, при каком атоме углерода находится гидроксильная
группа:
☺ первичные спирты (например: пропанол);
☺ вторичные спирты (например: изопропиловый спирт);
☺
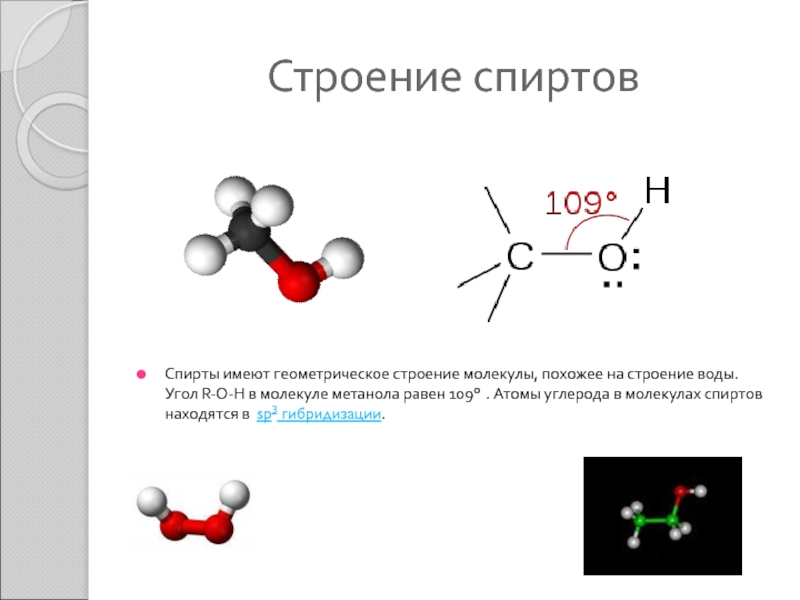
третичные спирты (например: 2,2-диметилпропан-2-ол).Слайд 10Строение спиртов
Спирты имеют геометрическое строение молекулы, похожее на строение воды.
Угол R-O-H в молекуле метанола равен 109° . Атомы углерода
в молекулах спиртов находятся в sp3 гибридизации.Слайд 11Физические свойства спиртов
☺ Физические свойства спиртов существенно зависят от строения
углеводородного радикала и положения гидроксильной группы. Первые представители гомологического ряда
спиртов – жидкости, высшие спирты – твердые вещества.☺ Метанол, этанол и пропанол смешиваются с водой во всех соотношениях. С ростом
молекулярной массы растворимость спиртов в воде резко падает, так, начиная с
гексилового, одноатомные спирты практически нерастворимы. Высшие спирты не
растворимы в воде. Растворимость спиртов с разветвленной структурой выше, чем
у спиртов с имеющих неразветвленное, нормальное строение.
☺ Низшие спирты обладают характерным алкогольным запахом, запах средних гомологов сильный и часто неприятный. Высшие спирты практически не имеют запаха. Третичные спирты обладают особым характерным запахом плесени.
☺ Спирты обладают аномально высокими температурами кипения по сравнению со
многими классами органических соединений и чем можно ожидать на основании их
молекулярных весов.
Слайд 12Химические свойства спиртов
1) Кислотные свойства:
Спирты — слабые кислоты, могут образовывать соли
и комплексы с активными металлами. Например: СН3-ОН + Na —> СН3—О—Na + Н2 .Соли одноатомных спиртов называются алкоголятами. Алкоголяты представляют собой твердые вещества, растворимые в спирте. Они легко гидролизуются водой с образование соответствующего спирта и щелочи: СН3-ОNa + H2O—> СН3—ОH + NaOH .2) Взаимодействие с галогеноводородами:
Для проведения этой реакции ипользуют реактив Лукаса: безводный хлорид цинка, растворенный в концентрированной соляной кислоте. Реакция протекает быстрее всего с третичными спиртами, медленнее всего - с первичными. Данная реакция отображает способность спирта образовывать карбокатион.
3) Межмолекулярная дегидратация(образование простых эфиров):
Катализатором данной реакции служит кислота. Чаще всего используют серную кислоту. Легче всего реагируют третичные спирты.
4) Внутримолекулярная дегидратация:
C2H5OH -> CH2=CH2 + H2O Спирты дегидратируются по правилу Зайцева. Легче всего отщепляют воду третичные спирты. Межмолекулярная и внутримолекулярная дегидратация являются конкурирующими реакциями. Но вторая протекает при более высокой температуре.
5) Окисление спиртов:
Спирты окисляются легче, чем углеводороды. Первичные и вторичные спирты окисляются легче третичных. Первичные окисляются до альдегидов, вторичные — до кетонов. В случае первичных спиртов может протекать дальнейшее окисление образующихся альдегидов до соответствующих карбоновых кислот. R-OH -> R-CHO -> R-COOH Третичные спирты устойчивы к окислению, но сильные окислители расщепляют молекулу. При этом образуется кетон и кислота.
Слайд 13ИСТОРИЯ ОТКРЫТИЯ СПИРТОВ
☺ Считается, что не менее чем за 8000
лет до новой эры люди изготавливали легкие спиртные напитки из
фруктов и мёда .☺ Впервые спирт из вина получили в 6-7 веках арабские химики, а первую бутылку крепкого алкоголя (прообраза современной водки) изготовил персидский алхимик Ар-Рази в 860 году.
☺ В Европе этиловый спирт был получен из продуктов брожения в 11-12 веке, в Италии.
☺ В Россию спирт впервые попал в 1386 году, когда генуэссское посольство привезло его с собой под названием «аква вита» и презентовала царскому двору.
☺ Первое исследование метилового спирта было сделано в 1834 году французскими химиками Жаном-Батистом Дюма и Эженом Пелиго; они назвали его «метиловым или древесным спиртом», так как он был обнаружен в продуктах сухой перегонки древесины.
☺ Впервые третичный спирт (2-метил-пропан-2-ол) синтезировал в 1863 году известный русский ученый А. М. Бутлеров, положив начало целой серии экспериментов в этом направлении.
☺ Двухатомный спирт — этиленгликоль — впервые был синтезирован французским химиком А.Вюрцем в 1856 году. Трехатомный спирт — глицерин — был обнаружен в природных жирах ещё в 1783 году, шведским химиком Карлом Шееле, однако его состав был открыт только в 1836 году, а синтез осуществлен из ацетона в 1873 году Шарлем Фриделем.
Слайд 14НАХОЖДЕНИЕ В ПРИРОДЕ
☺ Спирты имеют самое широкое распространение в природе,
особенно в виде сложных эфиров, однако и в свободном состоянии
их можно встретить достаточно часто.☺ Метиловый спирт в небольшом количестве содержится в некоторых растениях, например: борщевике.
☺ Этиловый спирт — естественный продукт спиртового брожения органических продуктов, содержащих углеводороды, часто образующийся в прокисших ягодах и фруктах без всякого участия человека. Этанол содержится в тканях и крови животных и человека.
☺В эфирных маслах зеленых частей многих растений содержится «спирт листьев», придающий им характерный запах.
☺ Фенилэтиловый спирт — душистый компонент розового эфирного масла.
☺ Очень широко представлены в растительном мире терпеновые спирты, многие из которых являются душистыми веществами, например:
☺ Линалоол — содержится во многих цветочных эфирных маслах.
☺ Бисаболол — входит в состав эфирного масла ромашки, тополя .
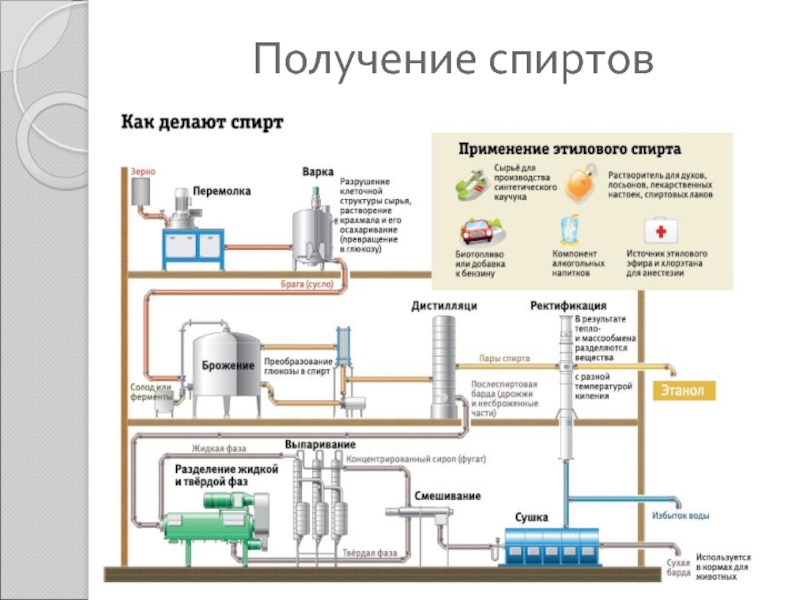
Слайд 16Получение спиртов
☺ При домашнем и промышленном производстве спиртных напитков этиловый
спирт вырабатывается путем ферментизации, т.е. разложения углеводсодержащих продуктов (маис, ячмень,
рис, картофель. виноград) под действие дрожжей. Получаемый напиток зависит от использованного сырья :Солод и ячмень – пиво;
Виноград – вино;
Пиво и вино образуется только путем ферментизации, уровень алкоголя не выше 15%.
☺ «Крепкие» спиртные напитки (водка, джин, виски, ликеры) требуют дистилляции. Это значит, что спирт перегоняется в новую емкость, оставляя воду в старой, получается повышенная концентрация алкоголя в будущем напитке.
Слайд 18Физиологическое действие и токсичность спиртов
☺ Одноатомные предельные спирты оказывают на
организм наркозоподобное, гипнотическое и токсическое действие. Введение в качестве заместителей
галогенов значительно повышает наркотический эффект.☺ Пары спиртов оказывают раздражающее действие на слизистые оболочки; поражают зрение — метиловый, гексиловый, гептиловый, нониловый спирты.
☺ Метиловый спирт — сильный яд (особенно при приеме внутрь) нервного и сердечнососудистого действия; поражает органы зрения вплоть до полной слепоты. В больших дозах (30 мл. и более) вызывает смерть.
☺ Этиловый спирт — быстро всасывается через слизистую оболочку желудка и тонкого кишечника, достигая максимальной концентрации в крови через 20-60 минут после его приёма, вызывая вначале возбуждение, а затем резкое угнетение центральной нервной системы; его употребление приводит к нарушению важнейших функций организма, тяжелому поражению органов и систем.
☺ Аллиловый спирт — вызывает острое отравление, в больших количествах при приеме внутрь — потеря сознания, тяжелая кома и смерть. Пары оказывают сильное раздражающее действие на глаза и верхние дыхательные пути.
☺ Этиленгликоль — очень токсичен при пероральном попадании в организм; поражает ЦНС и почки.
Слайд 19Действие алкоголя на организм человека
Алкоголь в организме оказывает 4 основных
эффекта :
☺ Обеспечение организма энергией ( спирт имеет высокую энергетическую
ценность, но не содержит питательных веществ).☺ Действует как анестезирующее средство на центральную нервную систему.
☺ Стимулирует производство мочи ( обезвоживание клеток).
☺ Временно выводит из строя печень при большом употреблении алкоголя.
Слайд 20Действие алкоголя на организм человека
☺ Умеренное потребление алкоголя не вредит
здоровью. Статистика показывает, что потребление умеренного(до 50 мл) количества спирта
может оказывать благотворительный эффект на весь организм:☺ самогон – лечение язвы желудка;
☺ спирт – улучшение роста и аппетита, общее укрепление здоровья, согревание, настойки успокаивающих трав и лекарств;
☺ вино ( кагор ) – образование красные кровяные тельца;
Слайд 21Действие алкоголя на организм человека
☺ Но, если употребление алкоголя будет
больше нормы, то можно достигнуть хронического алкоголизма за 5- 25
лет.☺ Конечная стадия алкоголизма наступает, если алкоголик отказывается от лечения или срывается вновь после лечения. Необратимые психические и физические нарушения обычно заканчиваются смертью.
☺ особенно хочу выделить женский алкоголизм, который не поддается лечению!
Слайд 22Действие алкоголя на организм человека
☺ДЕЙСТВИЕ АЛКОГОЛЯ НА ОТДЕЛЬНЫЕ ОРГАНЫ ОРГАНИЗМА:
☺
кровь: угнетение выработки тромбоцитов, белых и красных кровяных телец (
малокровие, кровотечения).☺ мозг: голодание и разрушение клеток мозга, дегенерация нервных клеток ( белая горячка, пневмония, сердечная и почечная недостаточность).
☺ сердце: повышение уровня холестерина в крови, сердечнососудистая недостаточность, алкогольная кардиомиопатия( гипертония, дистрофия миокарда).
☺ кишечник: изменение структуры стенки кишечника, клетки теряют способность всасывать питательные вещества ( истощение организма, цинга, бери-бери, воспаление желудка, кишечника, с повышенным риском появления язвы).
☺ печень: воспалительный процесс (гепатит), рубцовое перерождение (цирроз). Печень перестает обезвреживать токсические вещества ( смерть).
☺ поджелудочная железа: разрушение поджелудочной железы ( диабет).
☺ также алкоголь влияет на деторождаемость, поэтому во многих странах мира запрещено употреблять алкоголя молодым людям в возрасте 18 – 30 лет.
Слайд 23Список используемой литературы:
Алкоголь. Этимологический словарь Фасмера. Тезуарус.
Спирт. Этимологический
словарь Фасмера. Тезуарус.
История алкоголя. Спиртные напитки.
Этиловый спирт
// Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 5. — С. 994-997. Похлёбкин В.В. Терминология русских спиртных напитков в XIV – XV веках. История водки. Проверено 25 августа 2009.
Соловьев Ю. И. История химии: Развитие химии с древнейших времен до конца XIX в. Пособие для учителей. — 2-е изд., перераб. — М.: «Просвещение», 1983. — С. 32, 174-175, 240.
Фигуровский Н.А. История химии: Учеб. пособие для студентов пед. ин-тов по хим. и биол. спец. — М.: «Просвещение», 1979. — С. 132, 145, 176.
Метиловый спирт. Энциклопедический Словарь Ф.А.Брокгауза и И.А.Ефрона. Библиотека «Вехи».
Метиловый спирт // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 3. — С. 118-119.
Андреас Ф., Грабе К. Химия и технология попилена = Propylenchemie / Под редакцией Полякова З.Н.. — Л.: «Химия», 1973. — С. 53.
Рахманкулов Д.Л., Кимсанов Б.X., Чанышев Р.Р. Физические и химические свойства глицерина. — М.: «Химия», 2003. — С. 8. — ISBN 5-7245-1228-9
Васильев А.А., Черкаев Г.В., Никитина М.А. Новый подход к душистым веществам с запахом зелени. Англо-русскоязычный общественный химический журнал «Бутлеровские сообщения».
b-Фенилэтиловый спирт. Большая советская энциклопедия. Яндекс.Словари.
Борнеокамфорное дерево (Dryobalanops aromatica Coleb.). Получение, состав, свойства и применение эфирных масел.