Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Общая характеристика металлов
Содержание
- 1. Общая характеристика металлов
- 2. Положение металлов в периодической системе1. Определите местоположение
- 3. ВFrAtI-III группа (кроме Н и В)IV-VIII группа ( в конце группы)Побочные подгруппы
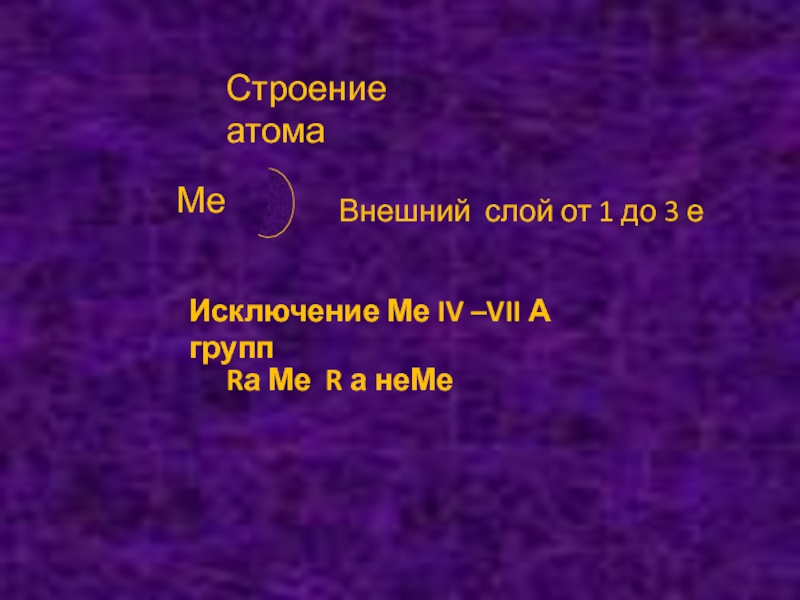
- 4. Строение атомаМе Внешний слой от 1 до
- 5. Окислительно-восстановительные свойстваА)Ме - neМе (окисление)восстановитель0+nБ) Возможные степени
- 6. В) Изменение восстановительных свойств металлов в периодической системеуменьшаютсяв периодеувеличиваются
- 7. Соединения металловМеС.о +1,+2С.о +3С.о +4 и большеМе2ОМеООсновные оксидыМеОНМе(ОН)2основанияМе2О3Ме2 О3Амфотерный оксидМе(ОН)3Амфотерное основаниеМеО2Ме2 О5Кислотные оксидН2МеО3НМеО3кислоты
- 8. Летучие водородные соединения не образуют, но с
- 9. Нахождение в природеАктивные Ме – только в
- 10. Характеристика простых веществ -металлов1.Строение молекулыА)Молекулы Ме -
- 11. Б) Изменение физических свойств в периодической таблицеВ
- 12. Самый лёгкий металл P˂5 г/см3Li p=0,53 г/см3
- 13. МелёгкиетяжёлыеМемягкиетвёрдые
- 14. МелегкоплавкиеТугоплавкие t пл˃1000 0СHg t пл= -38,9 0СW t пл= 33900С
- 15. Химические свойства металловМе вос-стано-вительНеМеО2Н2ООксид МеОксид неМекислотасоль?? Основной
- 16. Скачать презентанцию
Положение металлов в периодической системе1. Определите местоположение металлов в периодической системе2. Назовите самые распространённые на ваш взгляд металлы, ответ обоснуйте.
Слайды и текст этой презентации
Слайд 2Положение металлов в периодической системе
1. Определите местоположение металлов в периодической
системе
Слайд 5Окислительно-восстановительные свойства
А)Ме - ne
Ме (окисление)
восстановитель
0
+n
Б) Возможные степени окисления МЕ
Низшая 0,+1,+2,+3
Высшая
+4,+5,+6,+7,+8
Приведите пример соединений металлов с указанными степенями окисления металлов
Слайд 6В) Изменение восстановительных свойств
металлов в периодической системе
уменьшаются
в периоде
увеличиваются
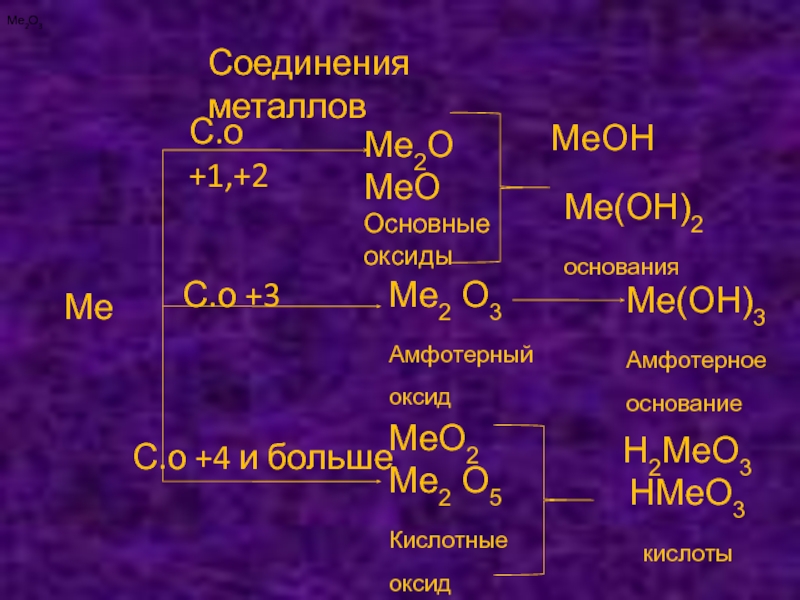
Слайд 7Соединения металлов
Ме
С.о +1,+2
С.о +3
С.о +4 и больше
Ме2О
МеО
Основные оксиды
МеОН
Ме(ОН)2
основания
Ме2О3
Ме2 О3
Амфотерный оксид
Ме(ОН)3
Амфотерное
основание
МеО2
Ме2 О5
Кислотные оксид
Н2МеО3
НМеО3
кислоты
Слайд 8Летучие водородные соединения не образуют, но с водородом образуют твёрдые
вещества гидриды
МеН IА группа
МеН2 II А группа и т.д
Слайд 9Нахождение в природе
Активные Ме – только в виде соединений NaCl,
Ca3(PO4)2
Менее активные Ме – в виде соединений и
в свободном виде (Sn,Pb, Cu)Неактивные Ме –в свободном виде (Pt,Au)
Слайд 10Характеристика простых веществ -металлов
1.Строение молекулы
А)Молекулы Ме - одноатомны
Металлическая связь
Металлическая кристаллическая
решётка
Твёрдые (кроме ртути), пластичные, тепло- и электропроводные, имеют металлический блеск
Слайд 11Б) Изменение физических свойств
в периодической таблице
В периоде
Твёрдость, температура плавления
и кипения –
уменьшаются( причина: увеличение числа электронов
на внешнем
слое, увеличивается порядковый номер, частично уменьшается радиус атома)
В группе главной подгруппе эти свойства увеличиваются
Слайд 12Самый лёгкий металл P˂5 г/см3
Li p=0,53 г/см3
Самый тяжёлый металл Р ˃ 5 г/см3
Os p=22,6 г/см3
Слайд 15Химические свойства металлов
Ме
вос-
стано-
витель
НеМе
О2
Н2О
Оксид Ме
Оксид неМе
кислота
соль
?
? Основной оксид
?
? Амфотерный оксид
?
?
R(OH)n
+H2↑
?
? RO
+H2↑
Mg+CuO
Al+Fe2O3
Mg+CO2
C+?
Fe+HCl
Особые свойства азотной кислоты- пример
Zn+CuCl2
? +?