Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
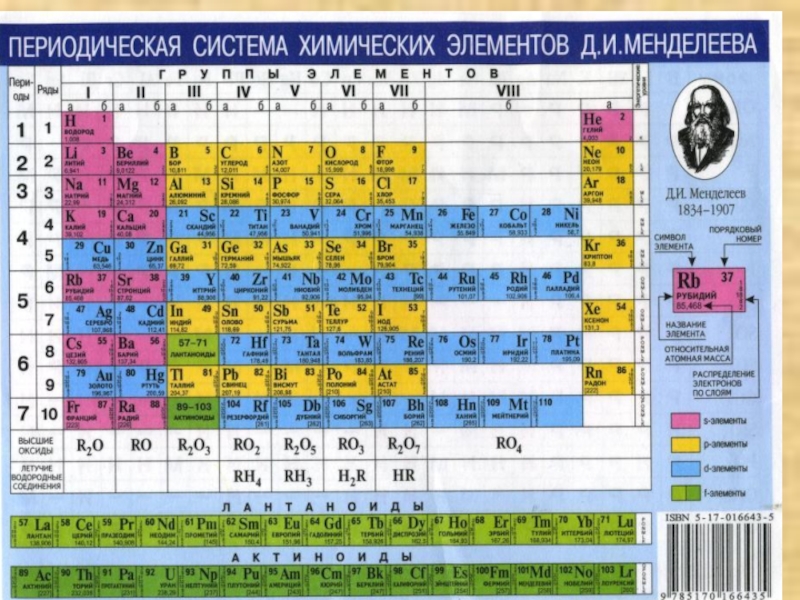
Значение Периодического закона Д.И.Менделеева
Содержание
- 1. Значение Периодического закона Д.И.Менделеева
- 2. Слайд 2
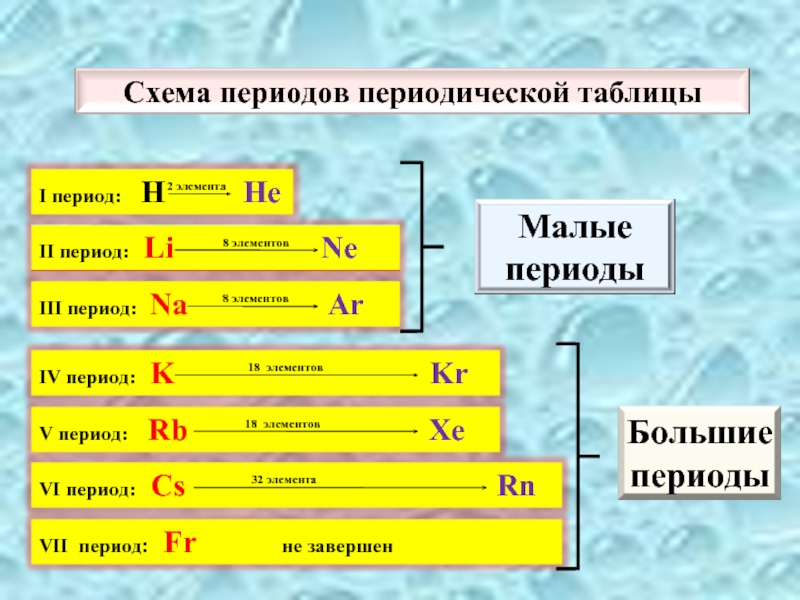
- 3. 2 элемента 8 элементов
- 4. H 1водородLi 3литийNa 11натрий K 19калийRb
- 5. Слайд 5
- 6. Слайд 6
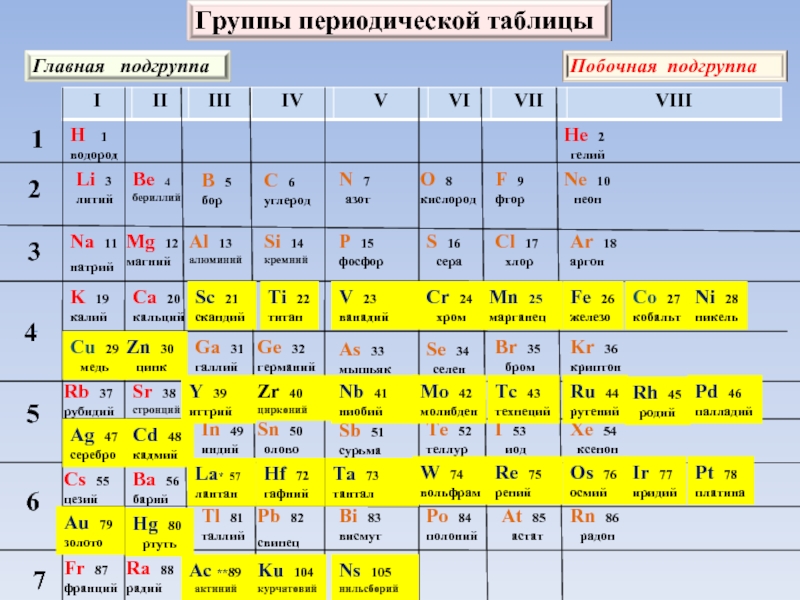
- 7. Г р у п п ыПериодыIIIIIIIVVVIVIIVIIIIIIIIIIVVVIVIIFrЩелочные металлыГалогеныИнертные
- 8. III IIIIV VVIVIIVIIIIIIIIПериодыLi2OBeOB2O3CO2N2O5Na2OAl203SiO2P2O5SO3Cl2O7MgOIIIIIIIVVVIVIIVIIIIIIIIПериодыCH4NH3H2OHFSiH4РН3H2SHClСтепень окисления высших оксидов возрастает
- 9. IIIIIIIVVVIVIIVIIIIIIIILi2O Be
- 10. В главных подгруппах периодической системы химических элементов
- 11. Слайд 11
- 12. До новых встреч, друзья мои
- 13. Скачать презентанцию
Слайды и текст этой презентации
Слайд 4H 1
водород
Li 3
литий
Na 11
натрий
K 19
калий
Rb 37
рубидий
Cs 55
цезий
1
2
3
4
5
6
7
Fr 87
франций
Be
4
бериллий
Mg 12
магний
Ca 20
кальций
Sr 38
стронций
Ba 56
барий
Ra 88
радий
B 5
бор
Al 13
алюминий
Ga 31
галлий
In 49
индий
Tl
81таллий
C 6
углерод
Si 14
кремний
Ge 32
германий
Sn 50
олово
Pb 82
свинец
N 7
азот
P 15
фосфор
As 33
мышьяк
Sb 51
сурьма
Bi 83
висмут
O 8
кислород
S 16
сера
Se 34
селен
Te 52
теллур
Po 84
полоний
F 9
фтор
Cl 17
хлор
Br 35
бром
I 53
иод
At 85
астат
He 2
гелий
Ne 10
неон
Ar 18
аргон
Kr 36
криптон
Xe 54
ксенон
Rn 86
радон
Cu 29
медь
Ag 47
серебро
Au 79
золото
Zn 30
цинк
Cd 48
кадмий
Hg 80
ртуть
Sc 21
скандий
Y 39
иттрий
La* 57
лантан
Ac **89
актиний
Ti 22
титан
Zr 40
цирконий
Hf 72
гафний
Ku 104
курчатовий
V 23
ванадий
Nb 41
ниобий
Ta 73
тантал
Ns 105
нильсборий
Cr 24
хром
Mo 42
молибден
W 74
вольфрам
Mn 25
марганец
Tc 43
технеций
Re 75
рений
Fe 26
железо
Co 27
кобальт
Ni 28
никель
Ru 44
рутений
Rh 45
родий
Pd 46
палладий
Os 76
осмий
Ir 77
иридий
Pt 78
платина
Слайд 7Г р у п п ы
П
е
р
и
о
д
ы
I
II
III
IV
V
VI
VII
VIII
I
II
III
IV
V
VI
VII
Fr
Щелочные металлы
Галогены
Инертные (благородные газы)
F
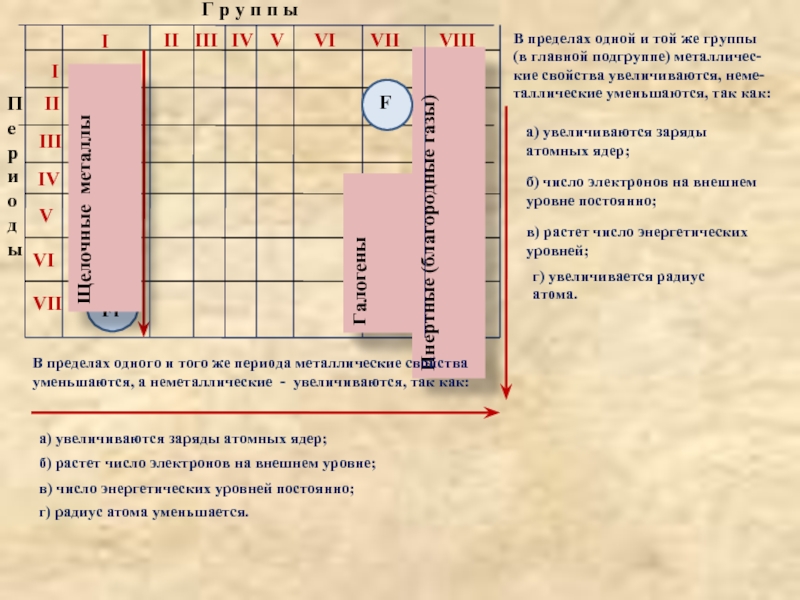
В пределах
одного и того же периода металлические свойства
уменьшаются, а неметаллические -
увеличиваются, так как:а) увеличиваются заряды атомных ядер;
б) растет число электронов на внешнем уровне;
в) число энергетических уровней постоянно;
г) радиус атома уменьшается.
В пределах одной и той же группы
(в главной подгруппе) металличес-
кие свойства увеличиваются, неме-
таллические уменьшаются, так как:
а) увеличиваются заряды
атомных ядер;
б) число электронов на внешнем
уровне постоянно;
в) растет число энергетических
уровней;
г) увеличивается радиус
атома.
Слайд 8I
II
III
IV
V
VI
VII
VIII
II
III
Периоды
Li2O
BeO
B2O3
CO2
N2O5
Na2O
Al203
SiO2
P2O5
SO3
Cl2O7
MgO
I
II
III
IV
V
VI
VII
VIII
II
III
Периоды
CH4
NH3
H2O
HF
SiH4
РН3
H2S
HCl
Степень окисления высших оксидов возрастает от + 1
до + 7
Степень окисления в летучих водородных соединениях возрастает от
-4 до -1Слайд 9I
II
III
IV
V
VI
VII
VIII
II
III
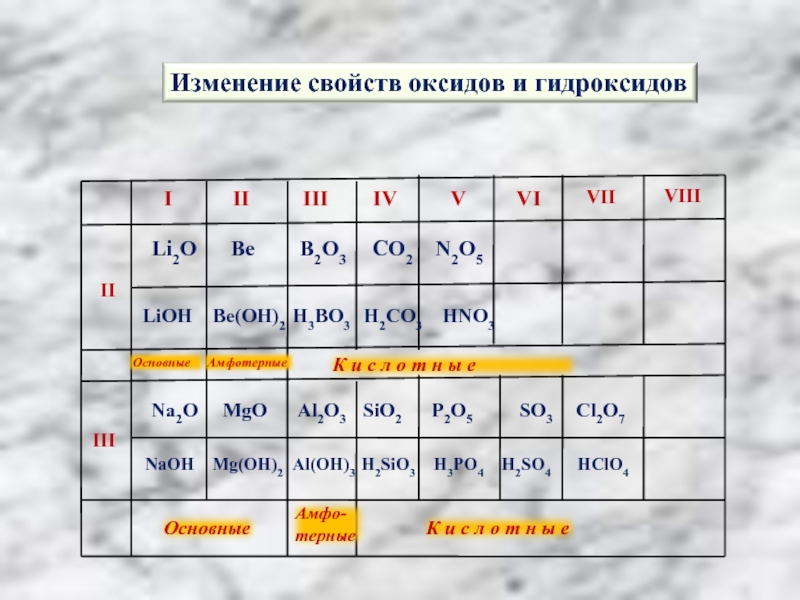
Li2O Be B2O3
CO2 N2O5
LiOH Be(OH)2 H3BO3
H2CO3 HNO3 Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7
NaOH Mg(OH)2 Аl(ОН)3 H2SiO3 H3PO4 H2SO4 HClO4
Слайд 10В главных подгруппах периодической системы химических элементов
Д.И.Менделеева с увеличением
заряда ядра радиус атомов, как правило:
1) увеличивается
2) уменьшается3) не изменяется
4) изменяется периодически
ОТВЕТ:
Наиболее ярко выраженные неметаллические свойства среди элементов
2-го периода периодической системы химических элементов Д.И.Менделеева
проявляет:
1) бор
2) углерод
3) азот
4) кислород
ОТВЕТ:
В периодах периодической системы химических элементов
Д.И.Менделеева с увеличением заряда ядер атомов не изменяется:
1) масса атомов
2) число энергетических уровней
3) общее число электронов
4) число электронов на внешнем энергетическом уровне
ОТВЕТ:
В ряду элементов Na → Mg → Al → Si → Cl:
1) неметаллические свойства ослабевают
2) металлические свойства усиливаются
3) металлические свойства не изменяются
4) металлические свойства ослабевают
ОТВЕТ: