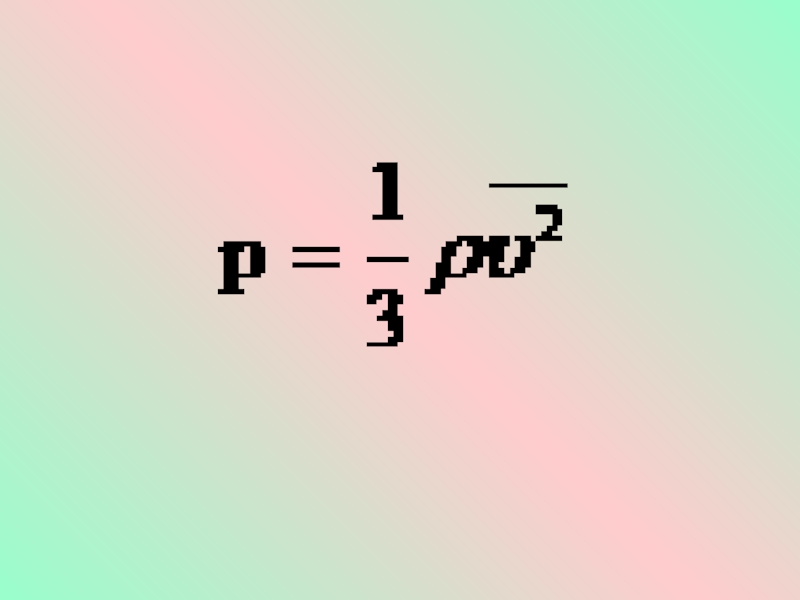Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основное уравнение МКТ
Содержание
- 1. Основное уравнение МКТ
- 2. Цель урока:Установить взаимосвязь между макроскопическими и микроскопическими параметрамиНаучиться решать вычислительные задачи с использованием основного уравнения МКТ
- 3. Макроскопические – параметры, которые можно измерить с помощью приборов.Микроскопические – параметры, которые измеряются косвенным путем.
- 4. m – масса газа V – объем газаt – температура газаp – давление газаn - концентрация
- 5. Слайд 5
- 6. Модель идеального газа1. Межмолекулярные силы притяжения отсутствуют
- 7. Слайд 7
- 8. Это уравнение, выведенное впервые немецким физиком Р.
- 9. Учитывая, что
- 10. Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения молекул, содержащихся в единице объема газа.
- 11. Слайд 11
- 12. Задача №1.Каково давление азота, если средняяквадратичная скорость
- 13. Слайд 13
- 14. Задача №2. Имеются два одинаковых сосуда. В
- 15. Слайд 15
- 16. Скачать презентанцию
Цель урока:Установить взаимосвязь между макроскопическими и микроскопическими параметрамиНаучиться решать вычислительные задачи с использованием основного уравнения МКТ
Слайды и текст этой презентации
Слайд 2Цель урока:
Установить взаимосвязь между макроскопическими и микроскопическими параметрами
Научиться решать вычислительные
задачи с использованием основного уравнения МКТ
Слайд 3Макроскопические – параметры, которые можно измерить с помощью приборов.
Микроскопические –
параметры, которые измеряются косвенным путем.
Слайд 6Модель идеального газа
1. Межмолекулярные силы притяжения отсутствуют (можно пренебречь потенциальной
энергией)
2. Взаимодействия молекул газа происходят только при их соударениях и
являются упругими 3. Молекулы газа не имеют объема - рассматриваются как материальные точки
Слайд 8Это уравнение, выведенное впервые немецким физиком Р. Клаузиусом, называется основным
уравнением молекулярно-кинетической теории идеального газа. Оно устанавливает связь между микроскопическими
параметрами и макроскопическими (измеряемыми) величинами.Слайд 10
Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения
молекул, содержащихся в единице объема газа.
Слайд 12Задача №1.
Каково давление азота, если средняя
квадратичная скорость его молекул
500
м/с, а его плотность 1,36 кг/м3 ?
Слайд 14Задача №2.
Имеются два одинаковых сосуда. В одном из них
находится кислород, а в другом азот. Число молекул каждого газа
и средние квадраты их скоростей одинаковы. Давление кислорода равно 32 кПа. Чему равно давление азота?
Теги