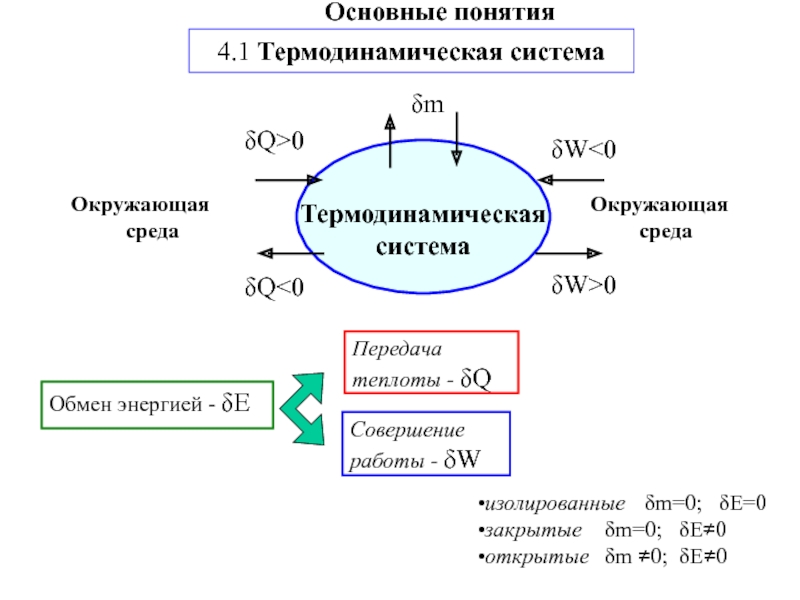
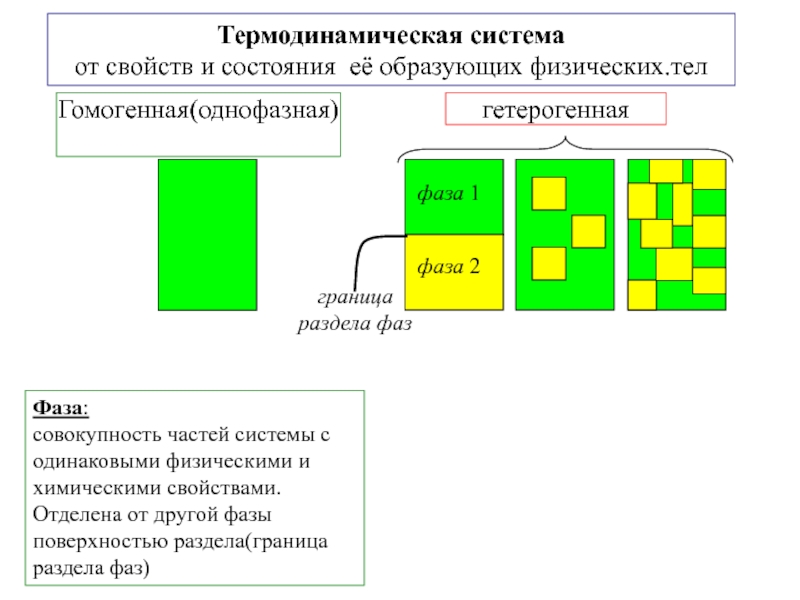
другую, от одной части системы к другой
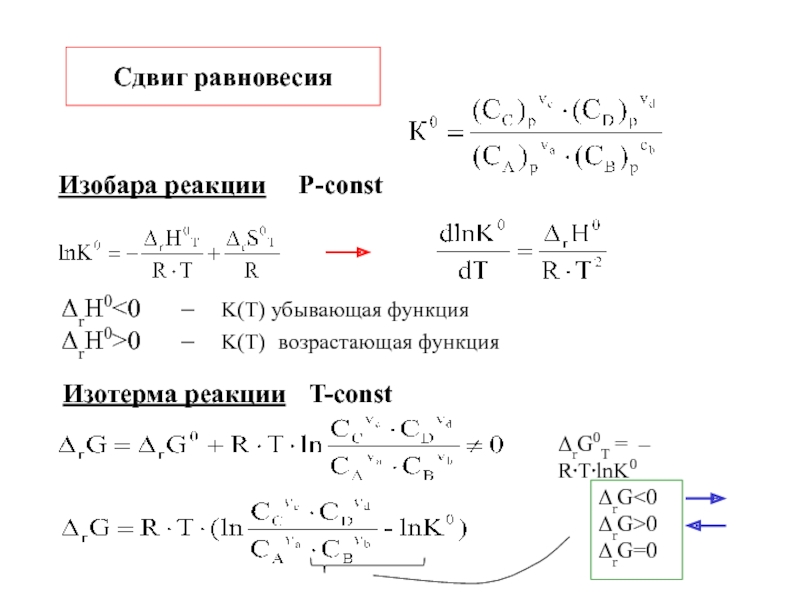
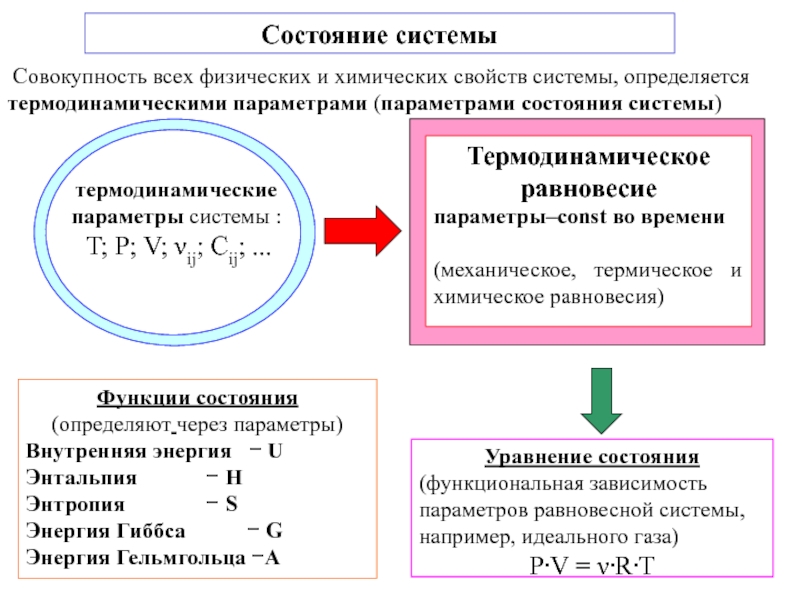
Химическая термодинамика -
термодинамика
химических процессов.Описывает статистически значимые процессы (большое число частиц)
энергетические эффекты, сопровождающие физические и химические процессы
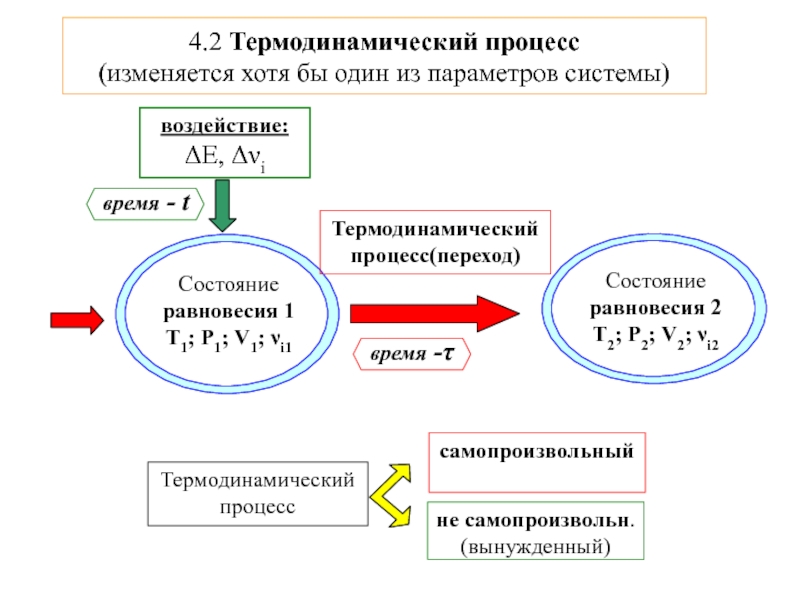
возможность, направления и предел самопроизвольного протекания процессов.










![4-ТЕРМОДИНАМИКА.ppt S [Дж/К] S0298 [Дж/моль⋅К] Факторы влияющие на величину энтропии S [Дж/К] S0298 [Дж/моль⋅К] Факторы влияющие на величину энтропии](/img/thumbs/c80039c8c24aa84ab9cfef2c2cc2a344-800x.jpg)