Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
5-КИНЕТИКА.ppt
Содержание
- 1. 5-КИНЕТИКА.ppt
- 2. 5.1 Элементарный акт химической реакции(10-13-10-15 с)AB +
- 3. Сложная химическая реакция AB + CD
- 4. Частицы, участвующие в элементарной химической реакции: Молекулы
- 5. 5.2 Элементарная(одностадийная) химическая реакция(совокупность элементарных хим.актов)
- 6. Скорость элементарной реакции число элементарных актов(r)
- 7. 5.3 Зависимость скорости реакции от концентрации в-в.
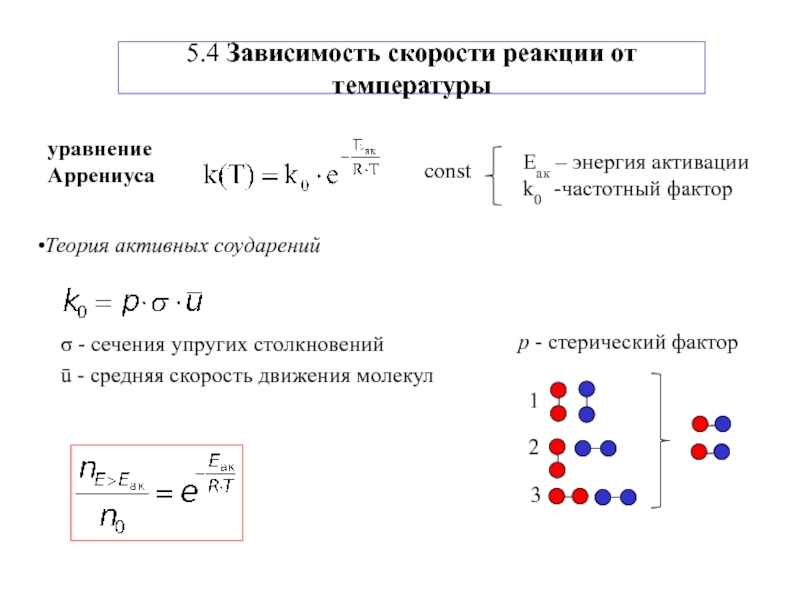
- 8. 5.4 Зависимость скорости реакции от температурыТеория активных соударений
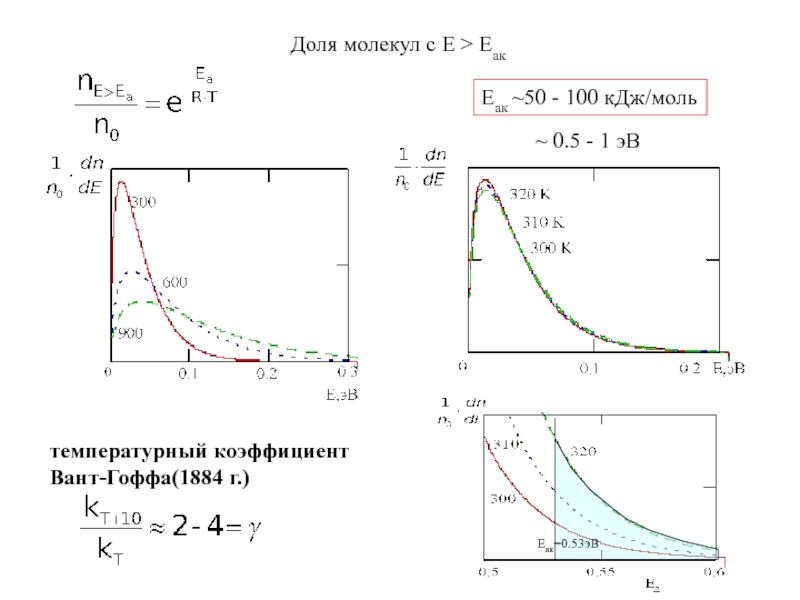
- 9. Доля молекул с Е > Еак
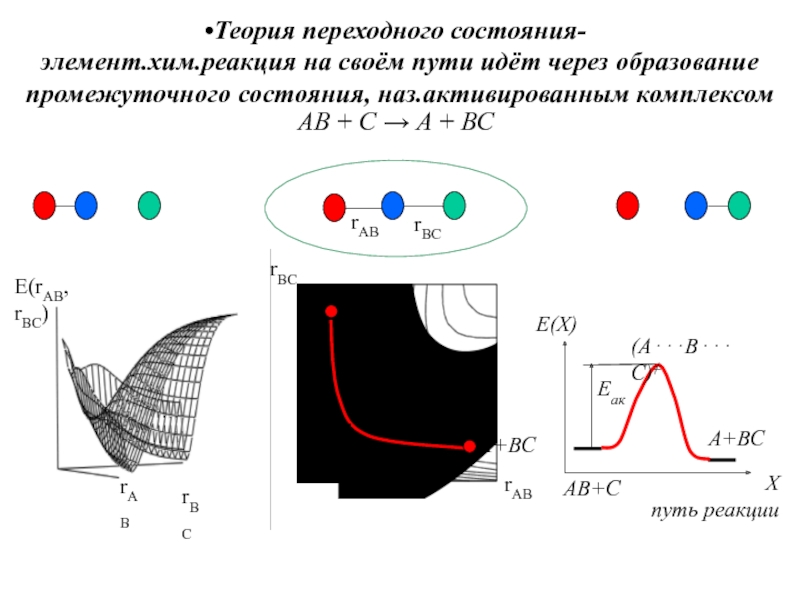
- 10. Теория переходного состояния- элемент.хим.реакция на своём пути идёт через образование промежуточного состояния, наз.активированным комплексом
- 11. 5.5 Сложные химические реакции(формальная кинетика) νAA + νBB → νDDЛимитирующая стадия
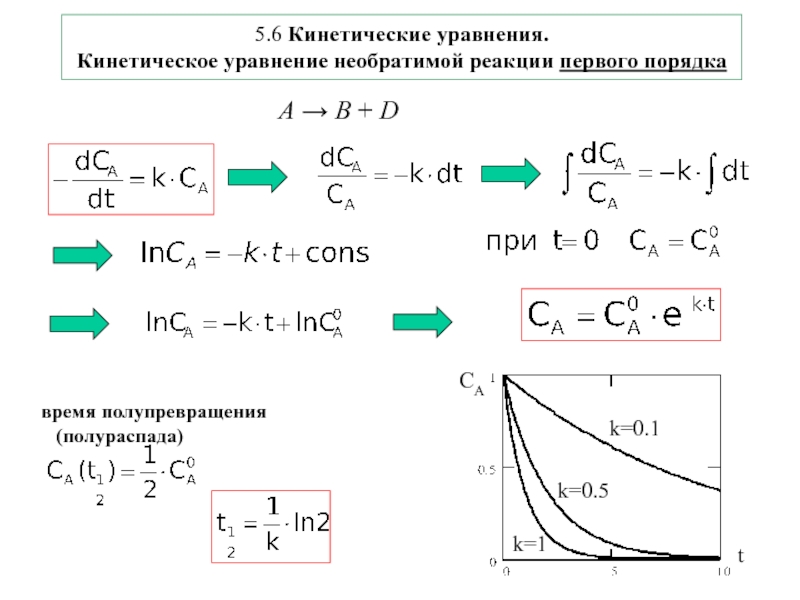
- 12. 5.6 Кинетические уравнения. Кинетическое уравнение необратимой реакции первого порядка
- 13. Кинетическое уравнение необратимой реакции второго порядка
- 14. 5.7 Цепной механизм химической реакцииЦепные реакции -
- 15. Примеры1. Неразветвленный цепной процесс
- 16. 5.8 Индуцированные реакции
- 17. 5.9 Гетерогенные реакцииνА A(тв) + νВ B(газ) → νD D2. химическая реакция на поверхности
- 18. Диффузионный режим(J-диффузионный поток)νА A(тв) + νВ B(газ) → νD D
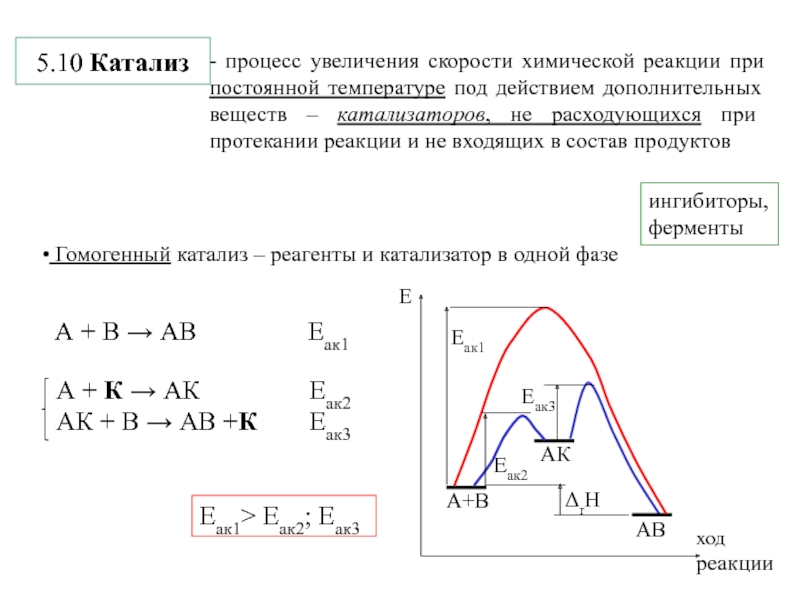
- 19. 5.10 Катализингибиторы,ферменты Гомогенный катализ – реагенты и
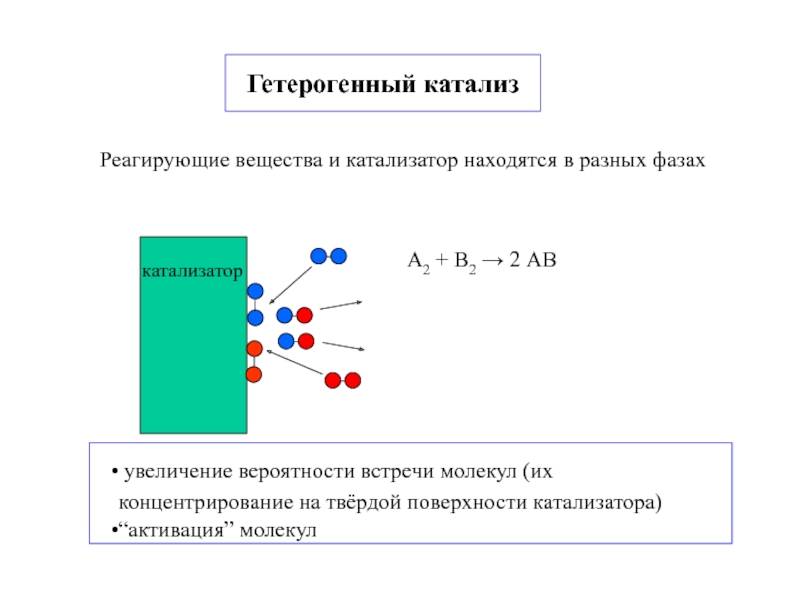
- 20. Гетерогенный катализРеагирующие вещества и катализатор находятся в разных фазахА2 + В2 → 2 АВ
- 21. 5.11 Горение и взрыв(взрывчатые превращения)
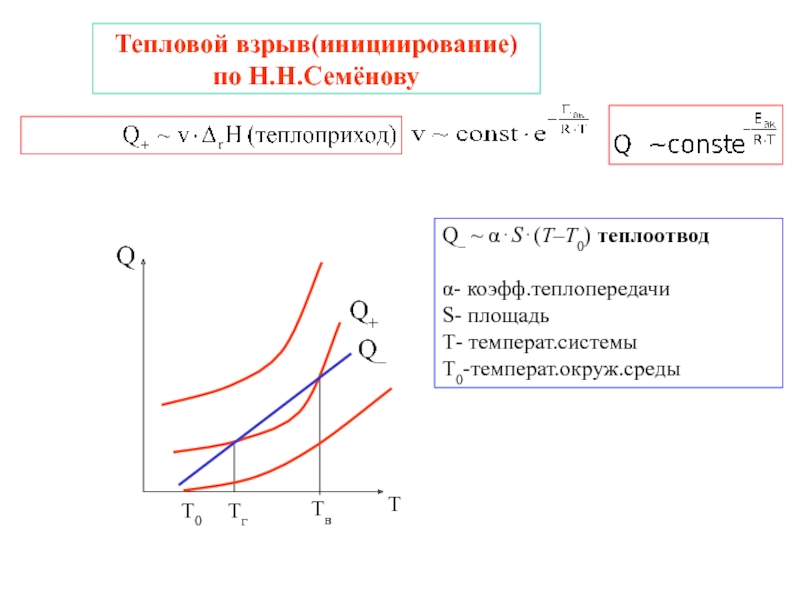
- 22. Тепловой взрыв(инициирование) по Н.Н.СемёновуQ– ~ α⋅S⋅(T–T0) теплоотводα- коэфф.теплопередачиS- площадьТ- температ.системыТ0-температ.окруж.среды
- 23. Скачать презентанцию
Слайды и текст этой презентации
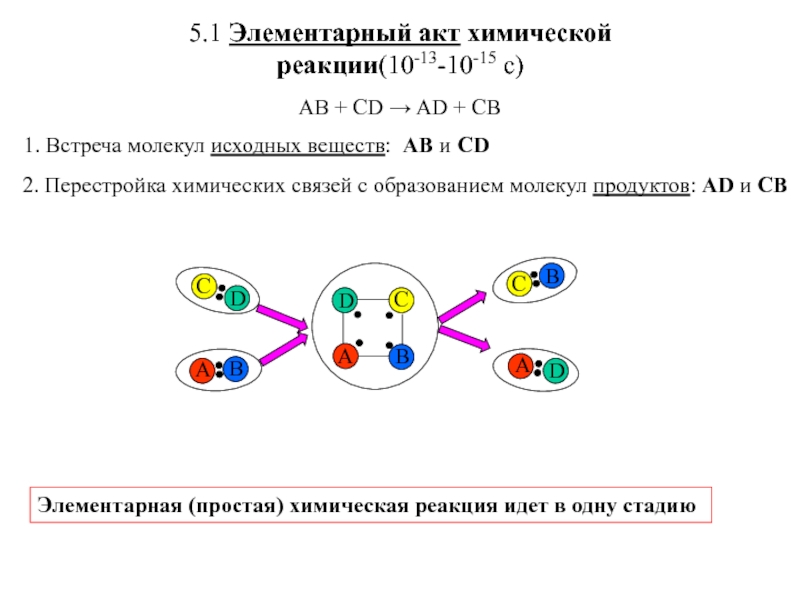
Слайд 25.1 Элементарный акт химической реакции(10-13-10-15 с)
AB + CD → AD
+ CB
Элементарная (простая) химическая реакция идет в одну стадию
1. Встреча
молекул исходных веществ: AB и CD2. Перестройка химических связей с образованием молекул продуктов: AD и CB
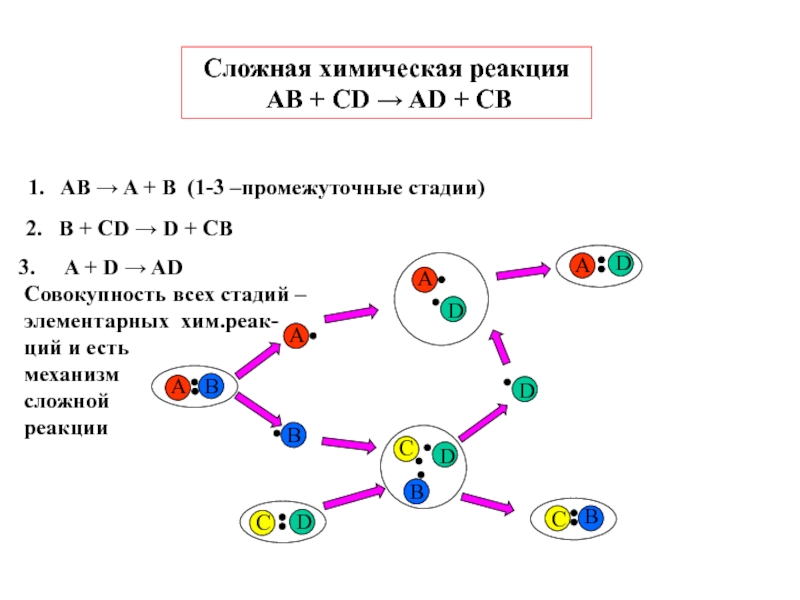
Слайд 3Сложная химическая реакция
AB + CD → AD + CB
1.
AB → A + B (1-3 –промежуточные стадии)
2.
B + CD → D + CBA + D → AD
Совокупность всех стадий –
элементарных хим.реак-
ций и есть
механизм
сложной
реакции
Слайд 4Частицы, участвующие в элементарной химической реакции:
Молекулы 2
NO + O2 → 2 NO2
макромолекулы (~102 –106 атомов)поверхностные атомы или молекулы
Классификация хим.реакций
Простые, сложные, гомогенные, гетерогенные, необратимые, обратимые, моно(би, три)молекулярные[распад, диссоциация, фрагментация, изомеризация, присоединение(ассоциация), димеризация, рекомбинация, отрыв, замещение], полимеризация,
окислительно-восстановительные, гомо(гетеро)литические, термические, фото-, радиационно-,электро, механохимические
Ионы H+ + OH- → H2O
Радикалы H∙ + Cl∙ → HCl
Слайд 55.2 Элементарная(одностадийная) химическая реакция(совокупность элементарных хим.актов) νAA + νBB →
νDD
реакционное пространство → V – объем(гомогенн.процесс)
реакционная
поверхность S - пов-ть (гетерогенн.процесс) Слайд 6Скорость элементарной реакции число элементарных актов(r) в единицу времени t
в единице реакционного объёма V νAA + νBB →
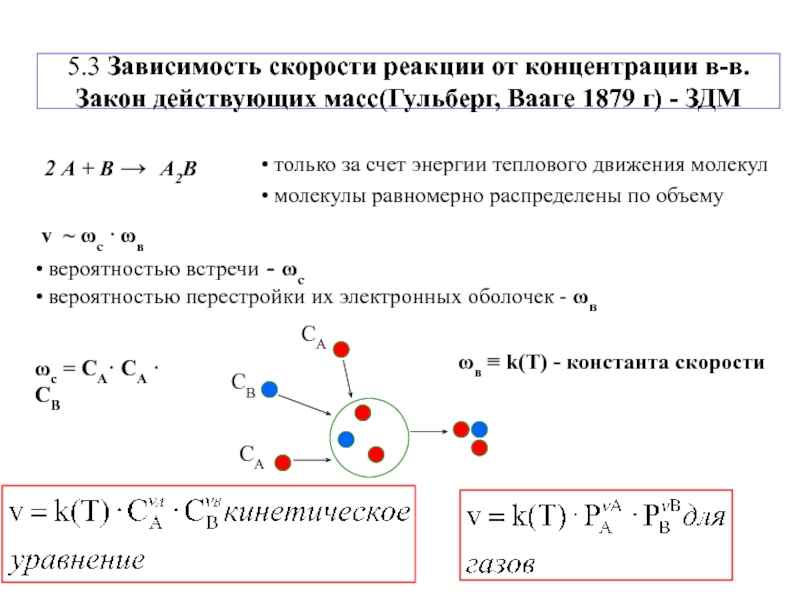
νDDСлайд 75.3 Зависимость скорости реакции от концентрации в-в. Закон действующих масс(Гульберг, Вааге
1879 г) - ЗДМ
ωс = СА· СА · СВ
ωв ≡
k(T) - константа скоростиСлайд 10Теория переходного состояния- элемент.хим.реакция на своём пути идёт через образование промежуточного
состояния, наз.активированным комплексом
Слайд 145.7 Цепной механизм химической реакции
Цепные реакции - ряд регулярно повторяющихся
многостадийных элементарных реакций с участием активных частиц (радикалов R∙), которые
взаимодействуют с молекулами реагентов с образованием продуктов реакции и новых активных частиц.Стадия зарождения цепи А → R∙ + R∙
Развитие цепи* А + R∙1 → R∙2+ В
Обрыв цепи R∙ + R∙ → А
А → В