Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
липидный обмен
Содержание
- 1. липидный обмен
- 2. План лекции: Синтез и катаболизм кетоновых тел.Регуляция
- 3. Синтез кетоновых тел (кетогенез) Это вынужденный метаболический
- 4. Кетоновые тела выступают дополнительным источником энергии для
- 5. Ход процесса Из 2-х молекул ацетил-КоА образуется
- 6. Большая часть ацетоацетил-КоА присоединяет 3-ю молекулу ацетил-КоА.
- 7. Ацетоуксусная к-та может восстанавливаться до β-гидроксибутирата. Фермент
- 8. Слайд 8
- 9. Катаболизм КТ β-гидроксибутират окисляется в ацетоуксусную к-ту.
- 10. 2. Свободный HSКоА (с затратой АТФ). Фермент
- 11. Слайд 11
- 12. Слайд 12
- 13. Регуляция липидного обмена.1. Субстратная2. Гормональная
- 14. Субстратная регуляция Регуляторные ферменты:1. Ацетил-КоА-карбоксилаза активируется цитратом
- 15. Слайд 15
- 16. Гормональная регуляция инсулин – активирует липогенез.глюкагон, адреналин,
- 17. Слайд 17
- 18. Слайд 18
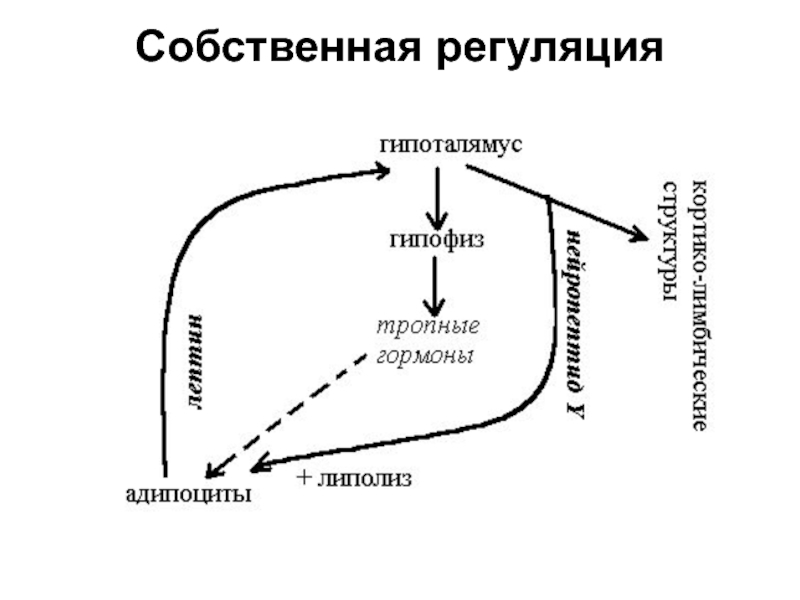
- 19. Собственная регуляция
- 20. Метаболизм холестерина (ХЛ) ХЛ – важнейший компонент
- 21. ХЛ выступает предшественником для стероидов (кортикостероиды, минералокортикоиды,
- 22. Синтез ХЛ 1. Образование мевалоновой кислоты.2. Образование сквалена. 3. Конденсация сквалена.
- 23. Образование мевалоновой кислоты.1. Две молекулы ацетил-КоА превращаются в
- 24. Слайд 24
- 25. Образование сквалена. мевалоновая к-та фосфорилируется образуется
- 26. часть изопентилпирофосфата изомеризуется в диметилалилпирофосфат;изопентилпирофосфат вместе с
- 27. Конденсация сквалена Сквален ⇒ ланостерин ⇒ зимостерин ⇒ десмостерин ⇒ ХЛ.
- 28. Регуляция синтеза ХЛ ГМГ-КоА-редуктаза ингибируется:ХЛ (механизм отрицательной
- 29. Катаболизм ХЛ Ферментов окисляющих ХЛ –
- 30. Транспорт ХЛ ХЛ из клеток в
- 31. НарушенияНарушения ХЛ-го баланса приводит к отложению ХЛ
- 32. Гиперлипопротеидемии (ГЛП). (по классификации ВОЗ)I. ↑ ХМ
- 33. IV. ↑ ЛПОНП (нарушена утилизация) – атеросклероз,
- 34. Другая важная причина атеросклероза – скэвенджер-путь утилизации липопротеидов.Он происходит при модификации ЛП в крови.
- 35. Причины модификации ЛП: 1. Гликозилирование ЛП
- 36. Жировая инфильтрация печени (стеатоз)Стеатоз – накопление липидов
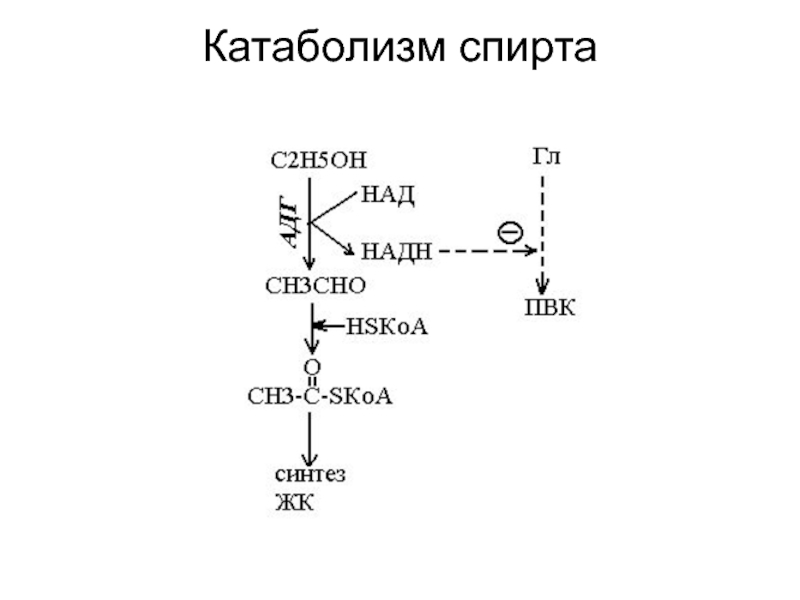
- 37. Катаболизм спирта
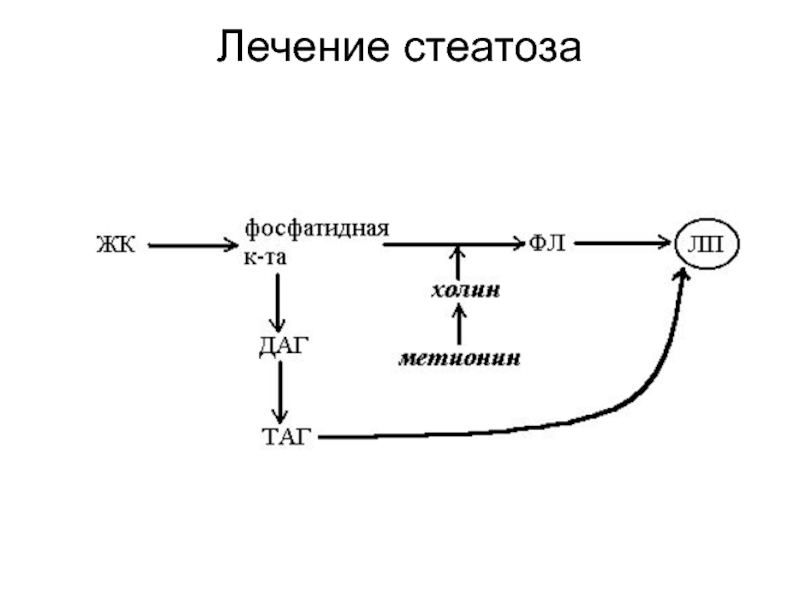
- 38. Лечение стеатоза
- 39. Скачать презентанцию
План лекции: Синтез и катаболизм кетоновых тел.Регуляция липидного обмена.Синтез и катаболизм ХЛ.Транспорт ХЛ и его нарушения.Жировая инфильтрация печени.
Слайды и текст этой презентации
Слайд 2План лекции:
Синтез и катаболизм кетоновых тел.
Регуляция липидного обмена.
Синтез и катаболизм
ХЛ.
Слайд 3Синтез кетоновых тел (кетогенез)
Это вынужденный метаболический путь (идет при сахарном
диабете или голодании).
Проходит в печени (в митохондриях).
Кетоновые тела (ацетоуксусная к-та,
β-гидроксимасляная к-та, ацетон) образуются из ацетил-КоА.Слайд 4
Кетоновые тела выступают дополнительным источником энергии для большинства клеток.
При избытке
возникает кетонемия и кетонурия (т.е. кетоз) которые истощает щелочные резервы
и приводят к кетоацидозу. Опасное состояние – кетоацидотическая кома (при сахарном диабете).Слайд 5Ход процесса
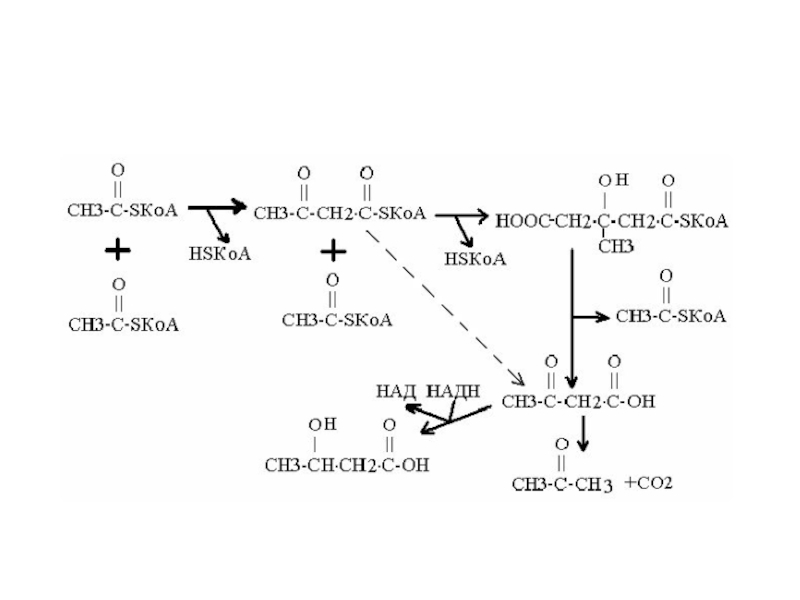
Из 2-х молекул ацетил-КоА образуется ацетоацетил-КоА. Фермент – ацетоацетил-КоА-тиолаза.
Ацетоацетил-КоА
(небольшая часть) может гидролизоваться до ацетоацетата и НSКоА. Фермент –
деацилаза.Слайд 6
Большая часть ацетоацетил-КоА присоединяет 3-ю молекулу ацетил-КоА. Образуется 3-гидрокси-3-метил-глутарил-КоА
(ГМГ-КоА). Фермент – гидроксиметилглутарил-КоА-синтаза.
ГМГ-КоА распадается на ацетоуксусную к-ту и ацетил-КоА.
Фермент – гидроксиметил-КоА-лиаза. Слайд 7
Ацетоуксусная к-та может восстанавливаться до
β-гидроксибутирата. Фермент – гидроксибутиратдегидрогеназа.
Ацетоуксусная
к-та в крови может спонтанно декарбоксилироваться. Образуется ацетон.
Слайд 9Катаболизм КТ
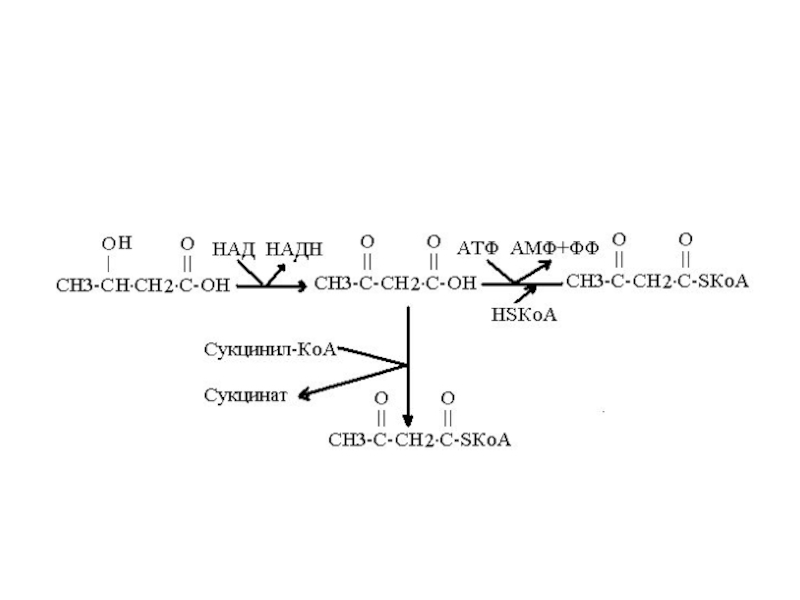
β-гидроксибутират окисляется в ацетоуксусную к-ту. Фермент – гидроксибутиратдегидрогеназа.
Ацетоуксусная к-та
принимает – КоА и превращается в ацетоацетил-КоА.
1. С сукцинил-КоА. Фермент
– сукцинилКоА-ацетоацетатКоА-трансфераза.Слайд 10
2. Свободный HSКоА (с затратой АТФ). Фермент – ацетоацетил-КоА-синтетаза.
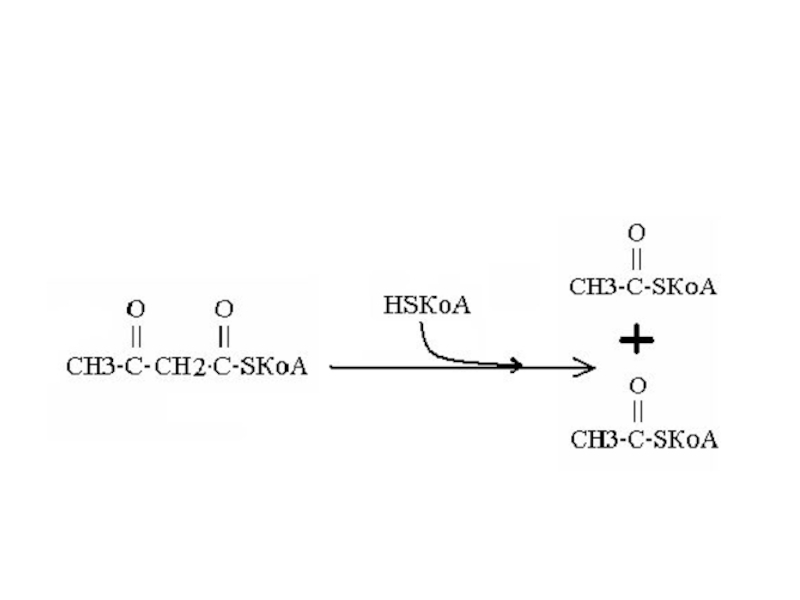
Ацетоацетил-КоА распадается
на 2 ацетил-КоА. Фермент – ацетоацетил-КоА-тиолаза.
Ацетил-КоА сгорает в цикле Кребса.
Слайд 14Субстратная регуляция
Регуляторные ферменты:
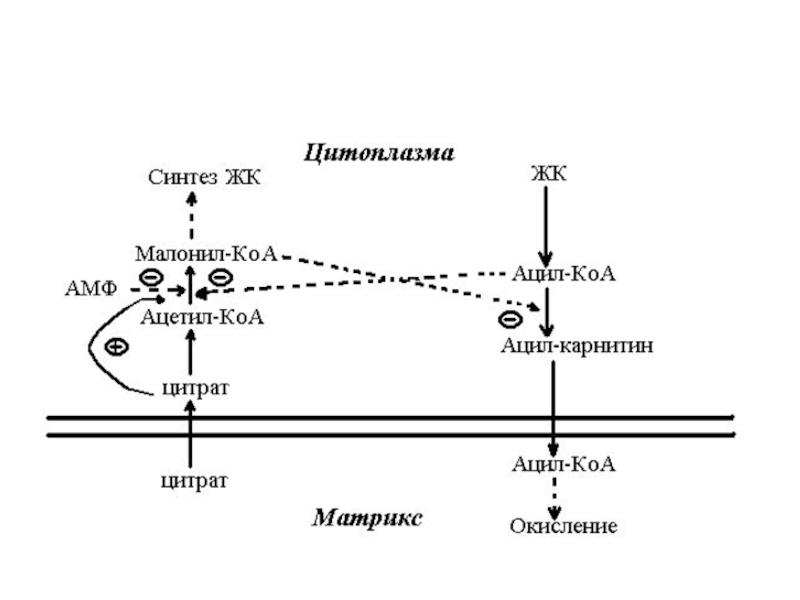
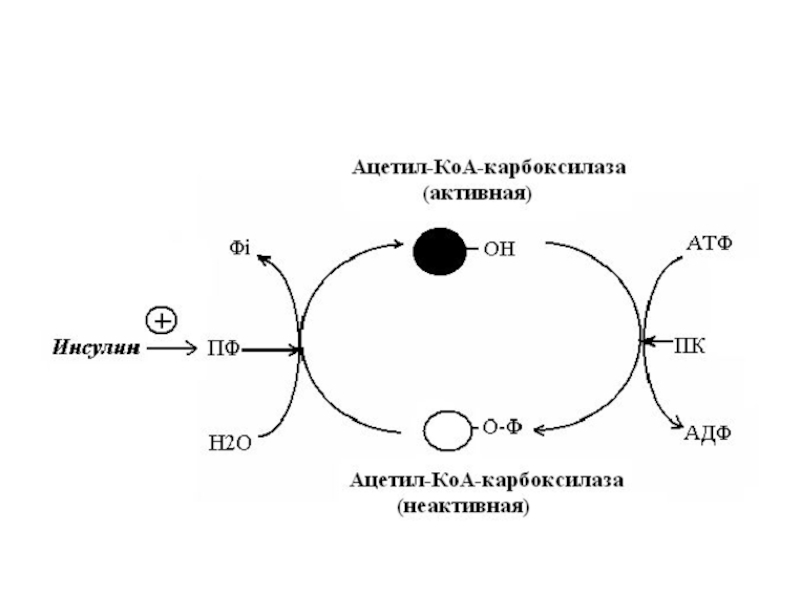
1. Ацетил-КоА-карбоксилаза
активируется цитратом (выходит из митохондрий)
ингибируется
ацил-КоА и АМФ (АМФ образуется из 2 АДФ ⇒ АМФ
+ АТФ. Фермент -- аденилаткиназа).2.Карнитинацилтрансфераза ингибируется малонил-КоА.
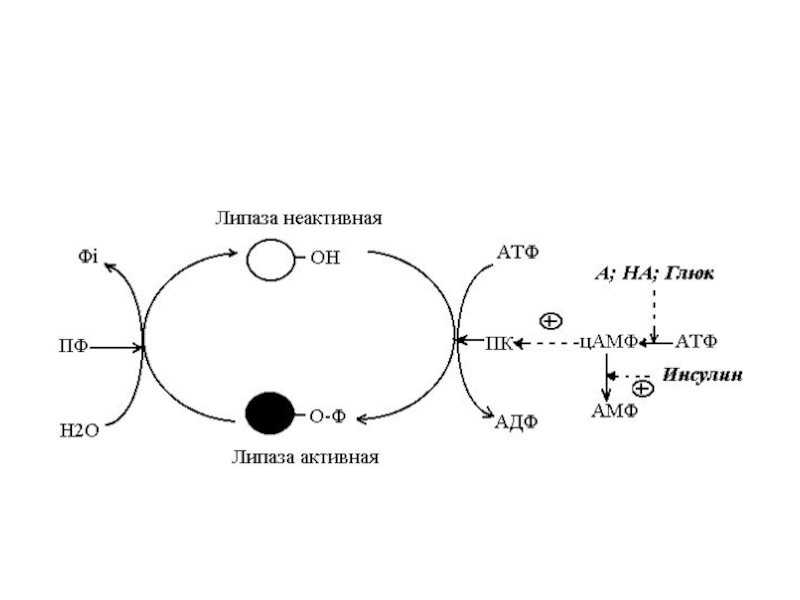
Слайд 16Гормональная регуляция
инсулин – активирует липогенез.
глюкагон, адреналин, норадреналин – активируют липолиз.
другие
гормоны также влияют на липолиз и липогенез.
Слайд 20Метаболизм холестерина (ХЛ)
ХЛ – важнейший компонент плазматических мембран. Включаясь в
состав мембранных фосфолипидов он изменяет реологические свойства мембраны. Мембрана содержащая
ХЛ переходит из жидкокристаллического состояния в гелевое.Слайд 21
ХЛ выступает предшественником для стероидов (кортикостероиды, минералокортикоиды, половые гормоны, желчные
кислоты, Вит Д).
ХЛ может как поступать с пищей, так
и синтезироваться в организме (главным образом в печени, синтез ХЛ проходит в цитоплазме).Слайд 22Синтез ХЛ
1. Образование мевалоновой кислоты.
2. Образование сквалена.
3. Конденсация сквалена.
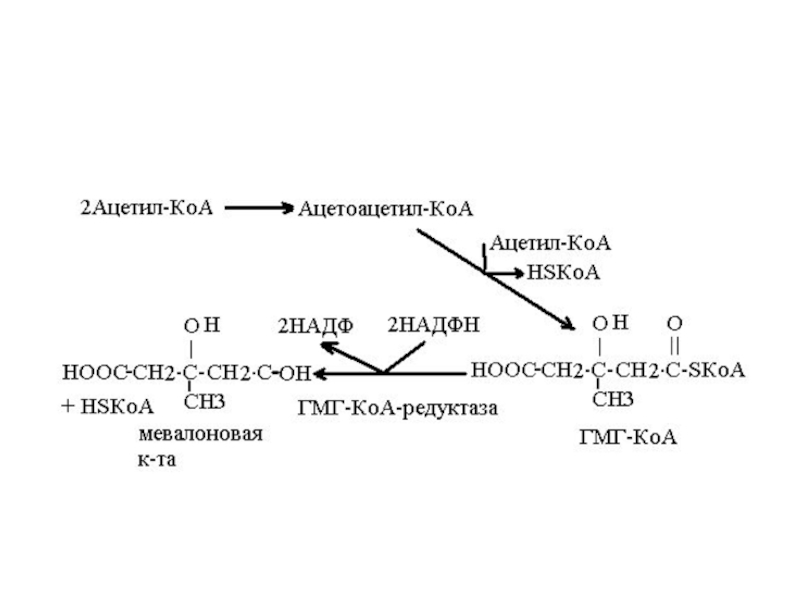
Слайд 23Образование мевалоновой кислоты.
1. Две молекулы ацетил-КоА превращаются в ацетоацетил-КоА. Фермент –
ацетоацетил-КоА-тиолаза;
2. Ацетоацетил-КоА принимает 3-й ацетильный остаток с ацетил-КоА, образуется 3-гидрокси-3-метил-глутарил-КоА (ГМГ).
Фермент – ГМГ-КоА-синтетаза;3. ГМГ-КоА восстанавливается 2-мя НАДФН, образуется мевалоновая к-та. Фермент – ГМГ-КоА-редуктаза.
Слайд 25Образование сквалена.
мевалоновая к-та фосфорилируется образуется 5-фосфомевалоновая к-та;
фосфорилируется еще раз
по С5 – образуется 5-пирофосфомевалоновая к-та;
фосфорилируется по С3 – 3-фосфо-5-пирофосмевалоновая
к-та;декарбоксилируется и дефосфорилируется образуется изопентилпирофосфат;
Слайд 26
часть изопентилпирофосфата изомеризуется в диметилалилпирофосфат;
изопентилпирофосфат вместе с диметил-алилпирофосфатом образуют геранилпирофосфат;
геранилпирофосфат
с изопентилпирофосфатом (или диметилалилпирофосфатом) образуют фарнезилпирофосфат;
две молекулы фарнезилпирофосфата образуют сквален.
Слайд 28Регуляция синтеза ХЛ
ГМГ-КоА-редуктаза ингибируется:
ХЛ (механизм отрицательной обратной связи)
Лекарственными препаратами (они
структурно похожи на мевалоновую кислоту – ловастатин, симвастатин и т.д).
Слайд 29Катаболизм ХЛ
Ферментов окисляющих ХЛ – нет.
Выводится в виде желчных
кислот.
Желчные кислоты (гликохолевая, таурохолевая) синтезируются в печени из ХЛ
(на МСГ). Существует печеночно-кишечная циркуляция желчи.
Потери желчи за сутки 0,5-1 гр.
Слайд 30Транспорт ХЛ
ХЛ из клеток в ЛПВП
В ЛПВП ХЛ этерифицируется
с помощью лецитин-холестерин-ацил-трансферазы (ЛХАТ), образуется эфир ХЛ (эХЛ)
Часть эХЛ в
составе ЛПВП поступает в печеньДругая часть эХЛ из ЛПВП передается ХМ, ЛПОНП, ЛППП, ЛПНП.
эХЛ в ХМ, ЛПОНП, ЛППП, ЛПНП поступает в ткани.
Слайд 31Нарушения
Нарушения ХЛ-го баланса приводит к отложению ХЛ на эндотелий сосудистой
стенки – атеросклероз, или отложению в ткани – ксантоматозу.
Одна из
причин возникновения атеросклероза – это изменение содержания ЛП в плазме крови – дислипопротеидемия. Слайд 32Гиперлипопротеидемии (ГЛП). (по классификации ВОЗ)
I. ↑ ХМ (↓ЛПЛ) – может
привести к о. панкреатиту, ожирению.
IIа- ↑ЛПНП (↓
рецепторы к ЛПНП) – приводит к атеросклерозу.IIб- ↑ ЛПОНП и ЛПНП (за счет пищи)
III. ↑ ЛПНП (нарушен синтез апо-белка) – приводит к атеросклерозу.