Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
1 Лекция Поверхностные явления. Адсорбция. Хроматография. Кафедра общей и
Содержание
- 1. 1 Лекция Поверхностные явления. Адсорбция. Хроматография. Кафедра общей и
- 2. Граф структуры
- 3. Адсорбция – процесс, самопроизвольного накопления одного вещества на поверхности другого (экзотермический)Обратный процесс – десорбция ( эндотермический)
- 4. Адсорбент – вещество, на поверхности
- 5. Хемосорбция – процесс сорбции
- 6. Причина адсорбции – уменьшение поверхностного натяжения (энергии)Поверхностное натяжение σ – величина, измеряемая энергией Гиббса.
- 7. σ численно равна работе,
- 8. Каждая из «глубинных» молекул жидкости притягивается друг
- 9. Каждая жидкость с поверхности как бы
- 10. Чем больше силы сцепления между молекулами, тем больше σ.
- 11. Значения σЭтанол – 22.75 эрг/см2Вода – 72.75 эрг/см2Ртуть – 480.3 эрг/см2
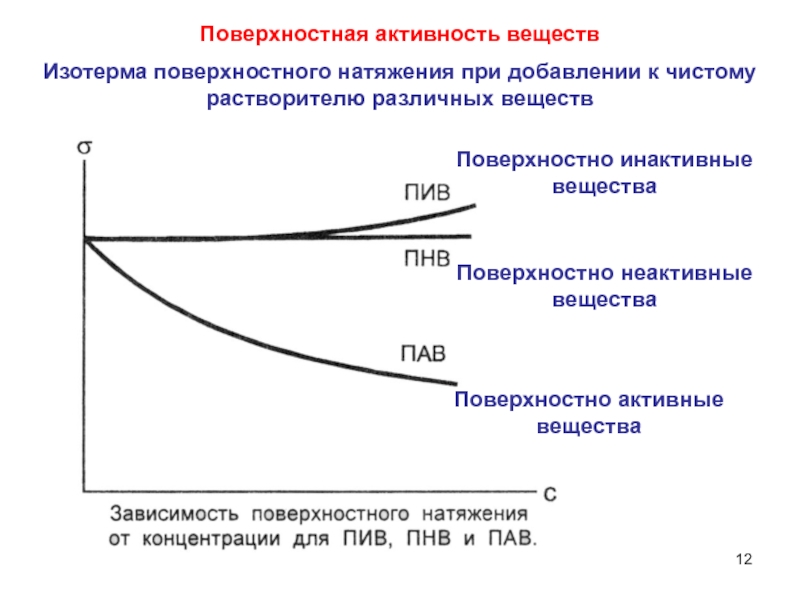
- 12. Поверхностная активность веществИзотерма поверхностного натяжения при добавлении
- 13. ПАВ ∆σ/∆С <
- 14. Модель молекулы поверхностно-активного вещества:а — строение гептановой
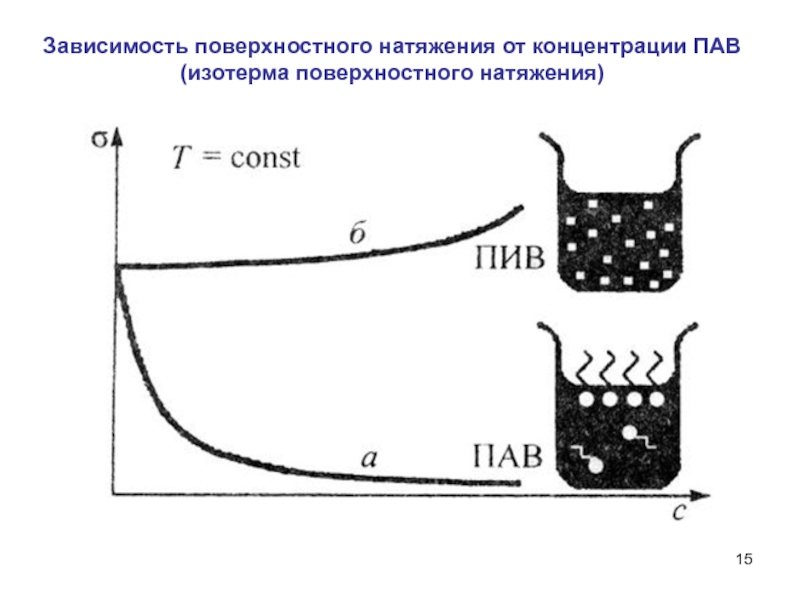
- 15. Зависимость поверхностного натяжения от концентрации ПАВ(изотерма поверхностного натяжения)
- 16. Антимикробное действие ПАВ связывают
- 17. Слайд 17
- 18. Слайд 18
- 19. Биологическая активность (наркотическое действие, бактерицидность) веществ одного
- 20. Правило Дюкло–Траубе. Увеличение радикала на одну
- 21. Связь σ с концентрацией.Уравнение ГиббсаМолекулы ПАВ на
- 22. Уравнение ГиббсаГИББС Джозайя Уиллард(11.02.1839-28.04.1903)Заложил основы термодинамики поверхностных явлений и электрохимических процессов, ввел понятие адсорбции.
- 23. С 1942 г. заведовал
- 24. Нобелевская премия по химии
- 25. гладкие адсорбенты; концентрации адсорбтива большие и
- 26. Изотерма Ленгмюра для границы раздела«твердое вещество-газ»Изотерма мономолекулярной адсорбции
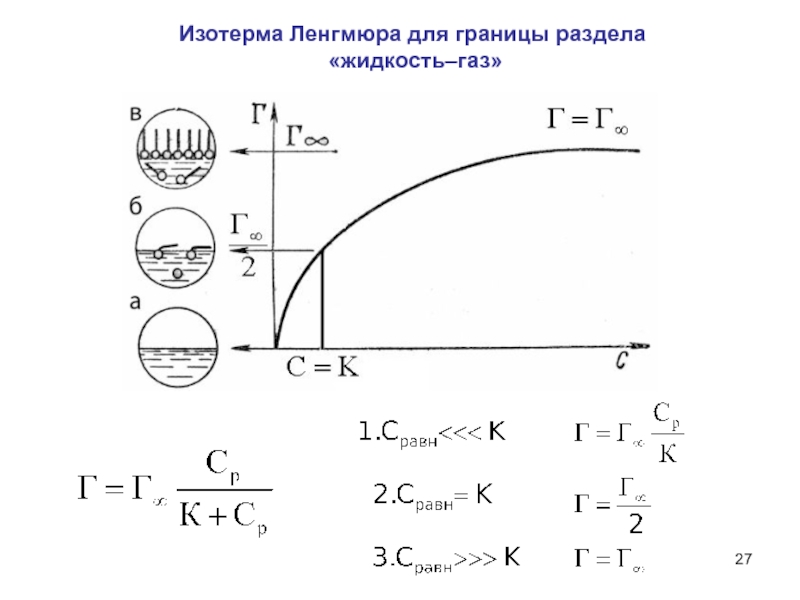
- 27. Изотерма Ленгмюра для границы раздела «жидкость–газ»
- 28. Определение констант изотермы адсорбции Ленгмюра→→
- 29. «Частокол» Ленгмюра. Определение длины молекул ПАВ.Представления об
- 30. В 1925 году Е.Горшнер и Г.Грендел установили,
- 31. 1 – липидный
- 32. Мозаичная модель биологической мембраныМакромолекулы интегральных белков, пронизывающих
- 33. 2. S-образная изотерма БЭТ (Брунауэр, Эммет, Теллер)
- 34. Пористые адсорбенты Николай Дмитриевич Зелинский(6.02.1861–31.07.1953)Русский советский химик.
- 35. Была весна 1915 года. 22
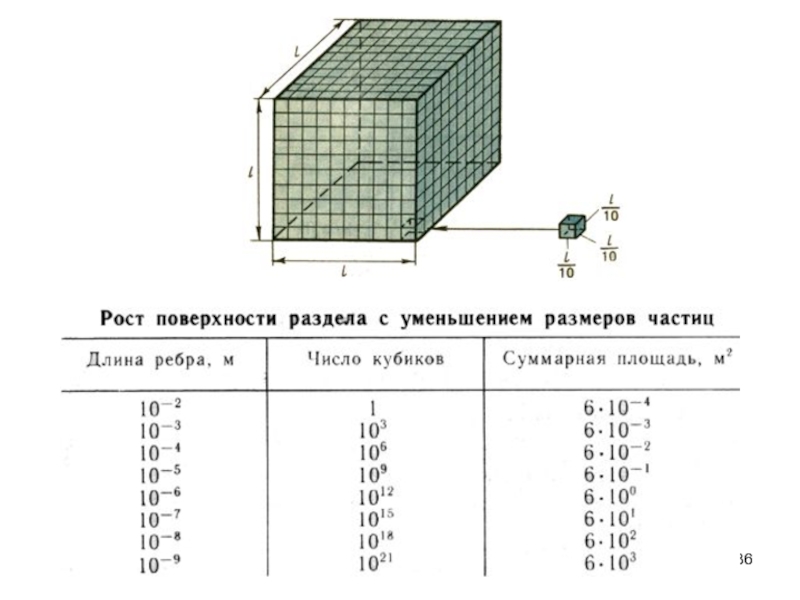
- 36. Слайд 36
- 37. Герберт Макс Фрейндлих(28.01.1880 – 30.03.1941)
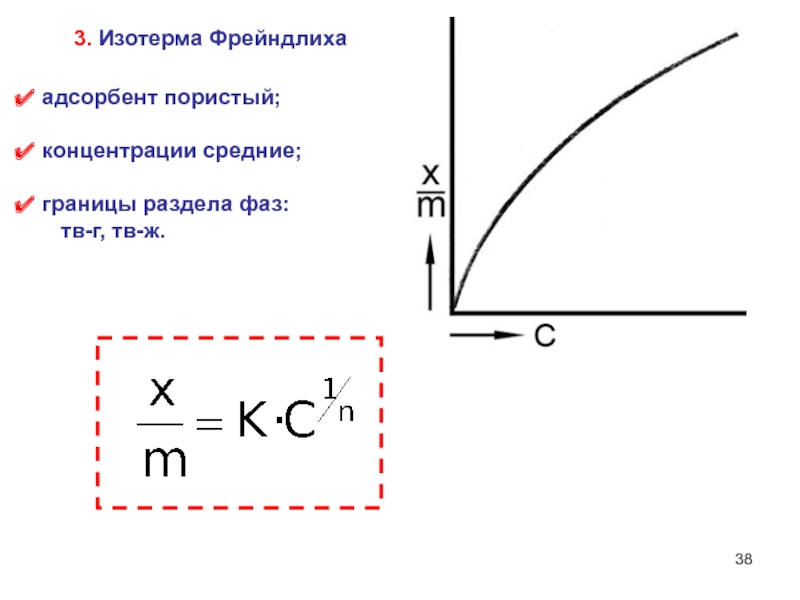
- 38. адсорбент пористый; концентрации средние; границы раздела фаз: тв-г, тв-ж.3. Изотерма Фрейндлиха
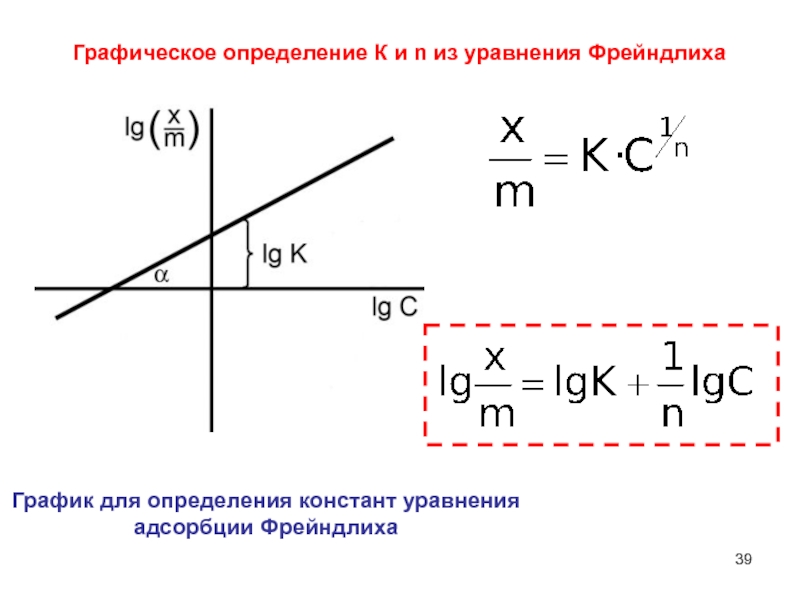
- 39. Графическое определение К и n из уравнения ФрейндлихаГрафик для определения констант уравнения адсорбции Фрейндлиха
- 40. Характеристики поверхностей в живых организмах
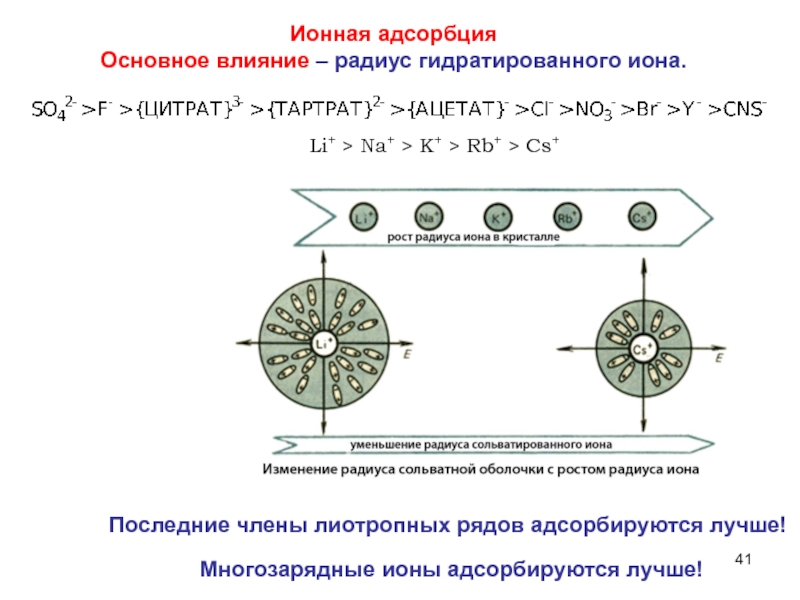
- 41. Li+ > Na+ > K+ > Rb+
- 42. В первую очередь из
- 43. Явление избирательной адсорбции токсинов
- 44. Ионообменная адсорбция- процесс, в котором адсорбент и
- 45. Весовая обменная емкость Гвес -
- 46. Определение динамической обменной емкости ионита(микроаналог схемы опреснения
- 47. Применение ионитов1. Разделение и очистка аминокислот и
- 48. норма††††††7.40некомпенсированныйацидозкомп.ацидозкомп.алкалознекомпенсированныйалкалознорма4. Лечение отеков и ацидоза
- 49. 5. Очистка сточных вод
- 50. 6. Удаление ионов металлов ( Fe3+, Cu2+ и Ca2+) , вызывающих помутнение вин
- 51. 7. Опреснение воды
- 52. Граф структурыХроматография
- 53. Хроматография - динамический метод анализа, основанный на
- 54. Михаил Семенович Цвет (1872-1919)Русский ботаник, физиолог,
- 55. Вещества распределяются по высоте колонки в зависимости
- 56. 1. Адсорбционная Основана на различии в адсорбционных
- 57. б) колоночная
- 58. в) тонкослойнаяХроматография на пластинке в тонком слое сорбента.
- 59. 2. Распределительная хроматография Основана на различной растворимости
- 60. 3. Молекулярно-ситовая хроматографи (гель-фильтрация, гель-хроматография)В качестве стационарной
- 61. Из гель-хроматограммы видно, что вещества из колонки
- 62. Слайд 62
- 63. Из анализируемой смеси с высокой степенью специфичности
- 64. Иммобилизация уреазы широко применяется при аналитическом
- 65. Клиренс - объем крови, полностью очищаемый в
- 66. Принцип афинной хроматографии в сочетании с абсорбцией используется в марлевых повязках
- 67. Современные активные медицинские сорбенты можно
- 68. 5. Ионообменная хроматография Разделение вещества связано с
- 69. Уравнение Б.П.Никольского:где x1 и x2 – количество
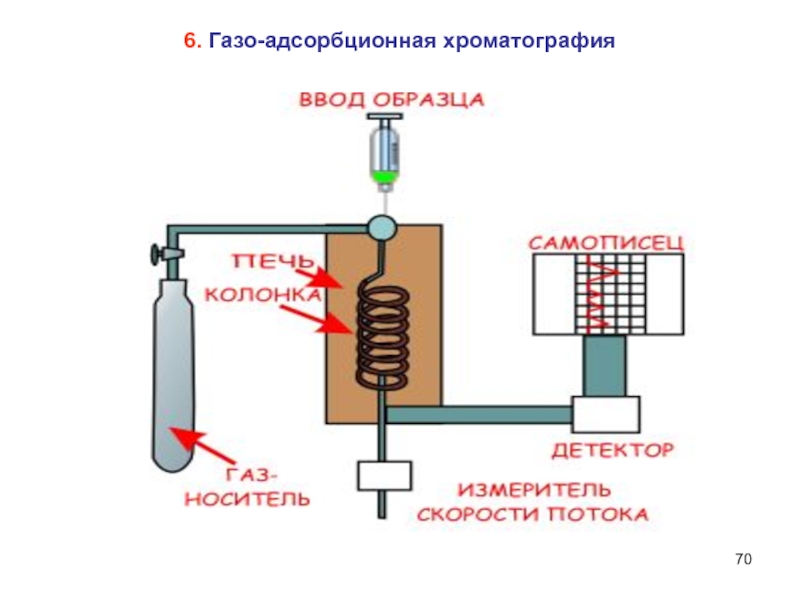
- 70. 6. Газо-адсорбционная хроматография
- 71. Степень разделения зависит от:длины колонки;природы адсорбента;природы адсорбтива;температуры.
- 72. Типичная запись показаний прибора при хроматографическом разделении
- 73. Слайд 73
- 74. На твердый адсорбент наносится тончайший слой растворителя, что позволяет разделять жидкие смеси7. Газо-жидкостная хроматография
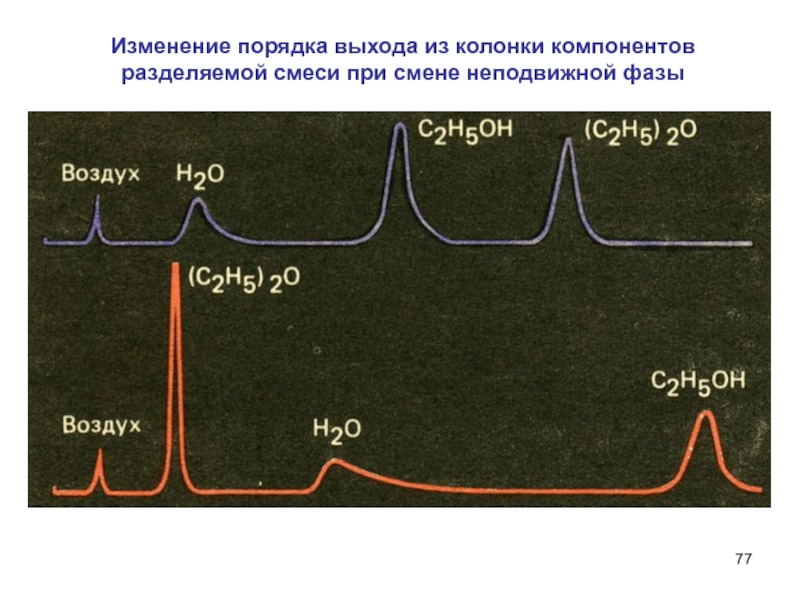
- 75. Первыми из колонки выходят плохо растворимые
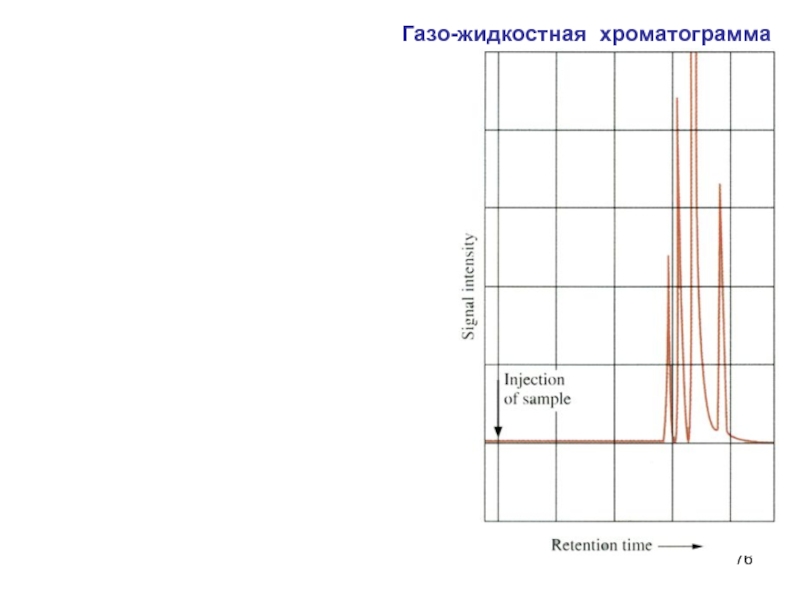
- 76. Газо-жидкостная хроматограмма
- 77. Изменение порядка выхода из колонки компонентовразделяемой смеси при смене неподвижной фазы
- 78. Каждый двадцатый раненый в годы второй
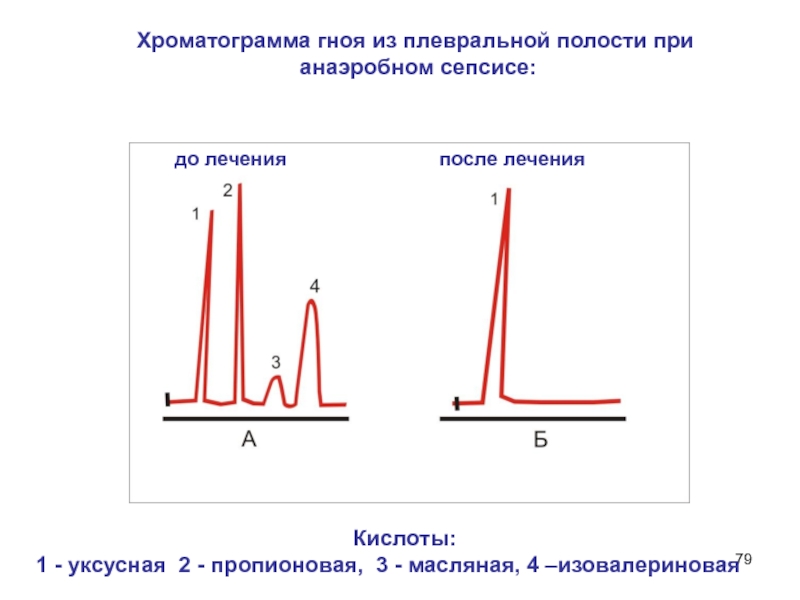
- 79. до леченияпосле лечения Хроматограмма гноя из
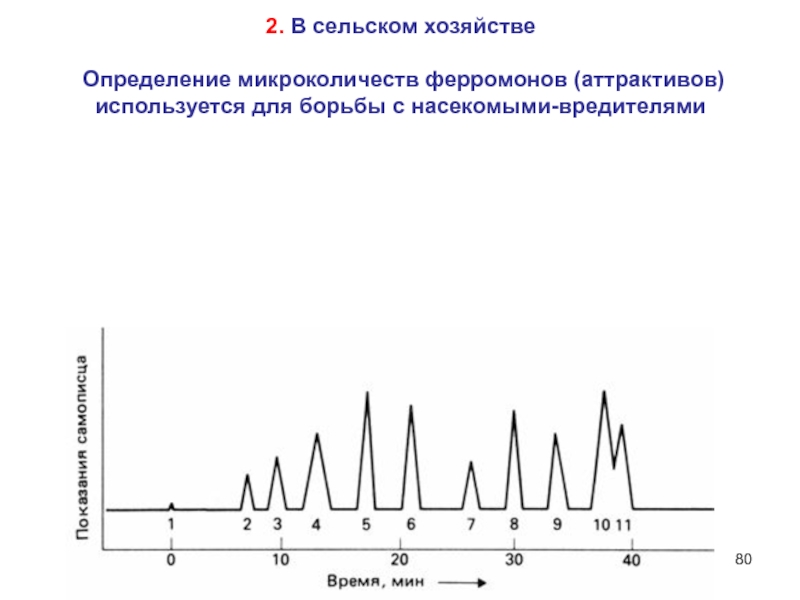
- 80. 2. В сельском хозяйстве Определение микроколичеств ферромонов (аттрактивов) используется для борьбы с насекомыми-вредителями
- 81. 3. В фармакологической промышленностиДля получения и очистки биологически активных веществ:витаминовферментовгормоновантибиотиков
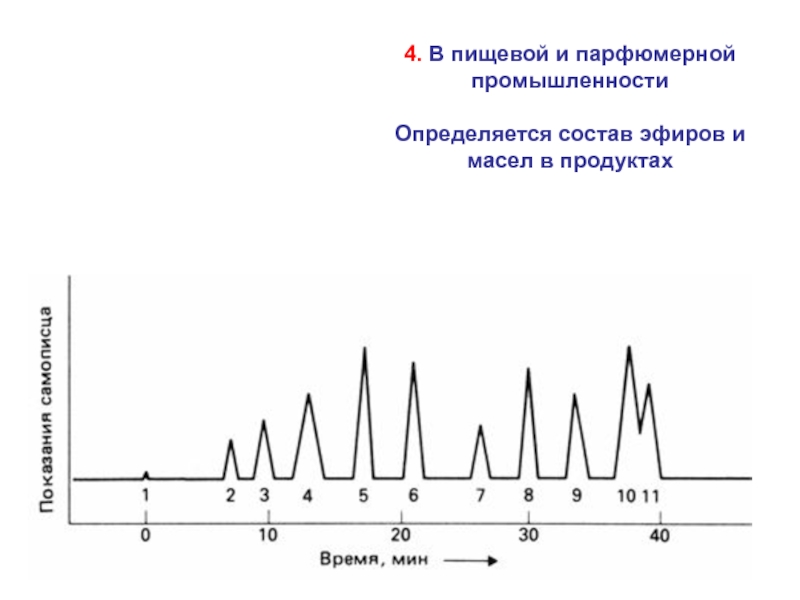
- 82. 4. В пищевой и парфюмерной промышленностиОпределяется состав эфиров и масел в продуктах
- 83. 5. При борьбе с воздушным терроризмом.
- 84. Спасибо за внимание!
- 85. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Адсорбция – процесс, самопроизвольного накопления
одного вещества на поверхности другого
(экзотермический)
Слайд 4 Адсорбент – вещество, на поверхности которого происходит адсорбция.
гидрофильные: силикагель, глины, пористое стекло
гидрофобные: активированный уголь, графит, тальк
Адсорбтив – вещество, которое накапливается
на поверхности.
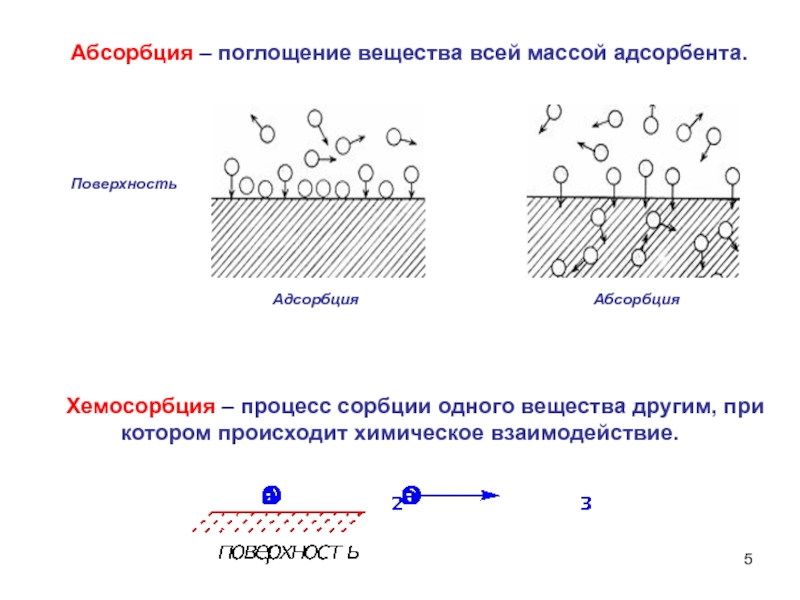
Слайд 5 Хемосорбция – процесс сорбции одного вещества другим,
при котором происходит химическое взаимодействие.
Абсорбция – поглощение вещества всей
массой адсорбента. Слайд 6Причина адсорбции
– уменьшение поверхностного натяжения (энергии)
Поверхностное натяжение σ –
величина, измеряемая энергией Гиббса.
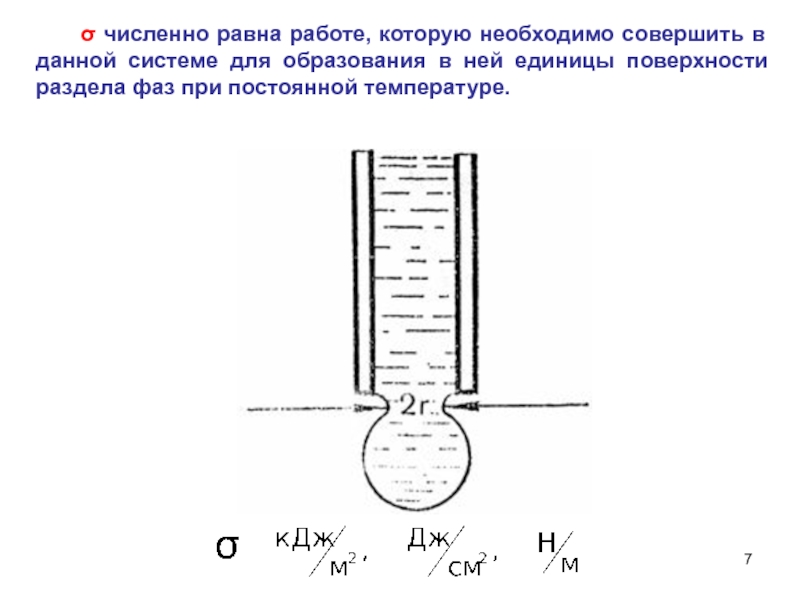
Слайд 7 σ численно равна работе, которую необходимо совершить
в данной системе для образования в ней единицы поверхности раздела
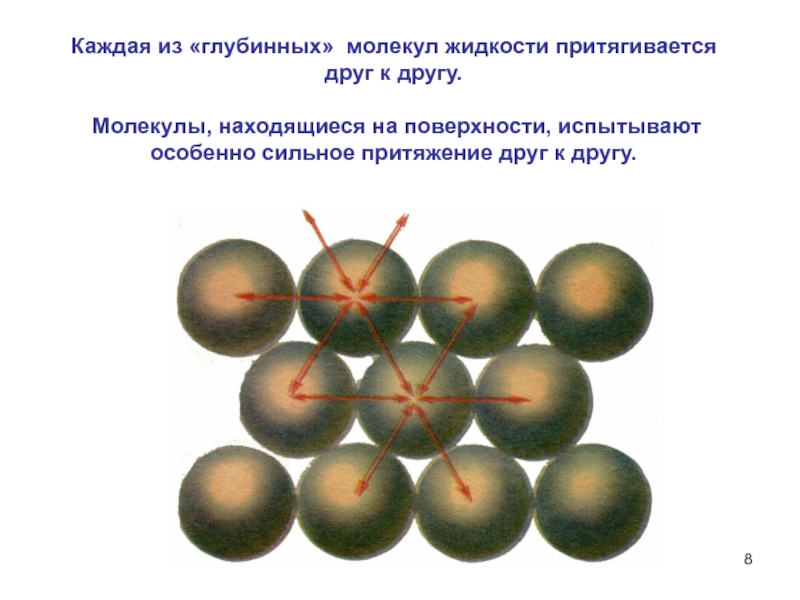
фаз при постоянной температуре.Слайд 8Каждая из «глубинных» молекул жидкости притягивается друг к другу.
Молекулы,
находящиеся на поверхности, испытывают особенно сильное притяжение друг к другу.
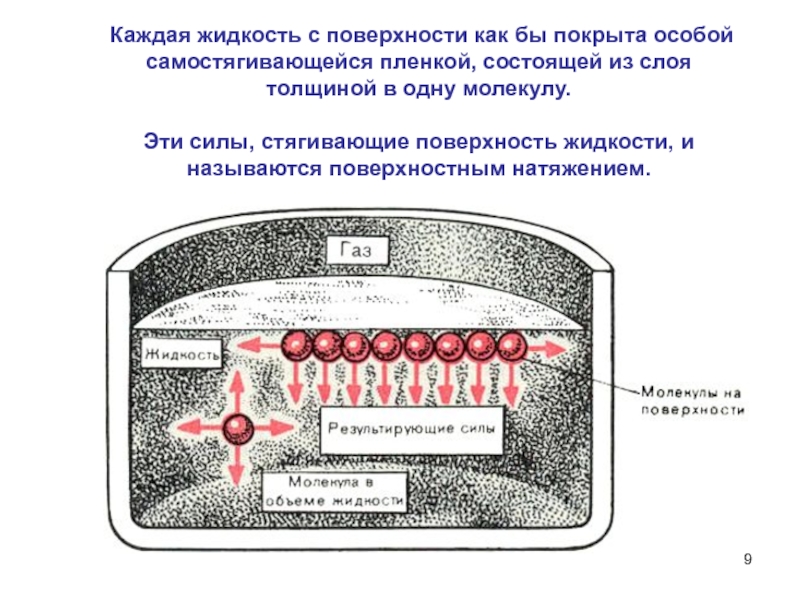
Слайд 9 Каждая жидкость с поверхности как бы покрыта особой самостягивающейся
пленкой, состоящей из слоя толщиной в одну молекулу.
Эти силы, стягивающие
поверхность жидкости, и называются поверхностным натяжением. Слайд 12Поверхностная активность веществ
Изотерма поверхностного натяжения при добавлении к чистому растворителю
различных веществ
Поверхностно активные
вещества
Поверхностно инактивные
вещества
Поверхностно неактивные
вещества
Слайд 13 ПАВ
∆σ/∆С < 0
- соли высших карбоновых кислот
(мыла),- высшие предельные спирты,
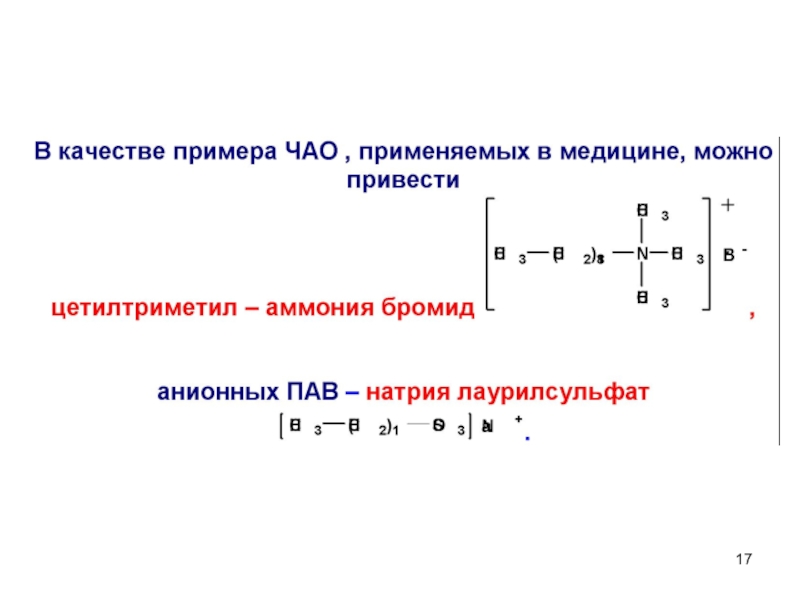
- ЧАО (четвертичные аммониевые основания ) -
основания тетраалкиламмония,
а также его соли
ПИВ ∆σ/∆С > 0
- кислоты, основания, соли
ПНВ ∆σ/∆С = 0
глюкоза, сахароза
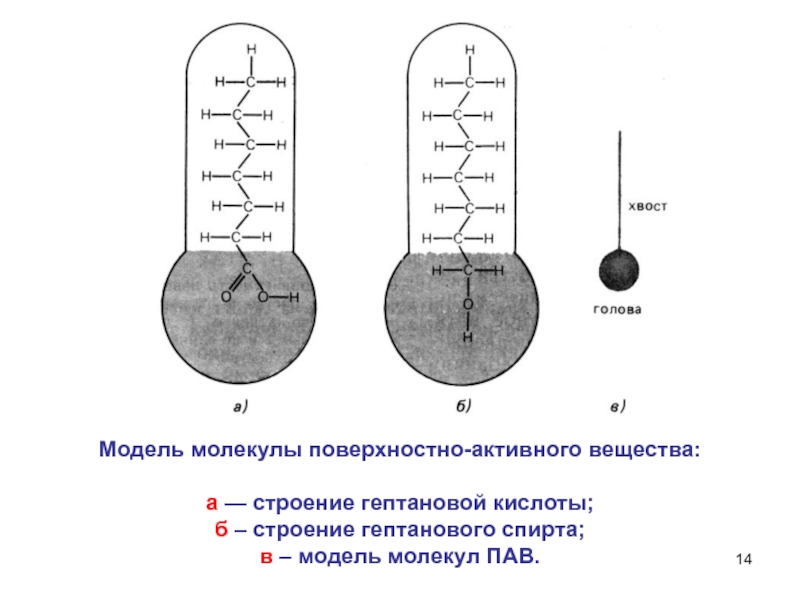
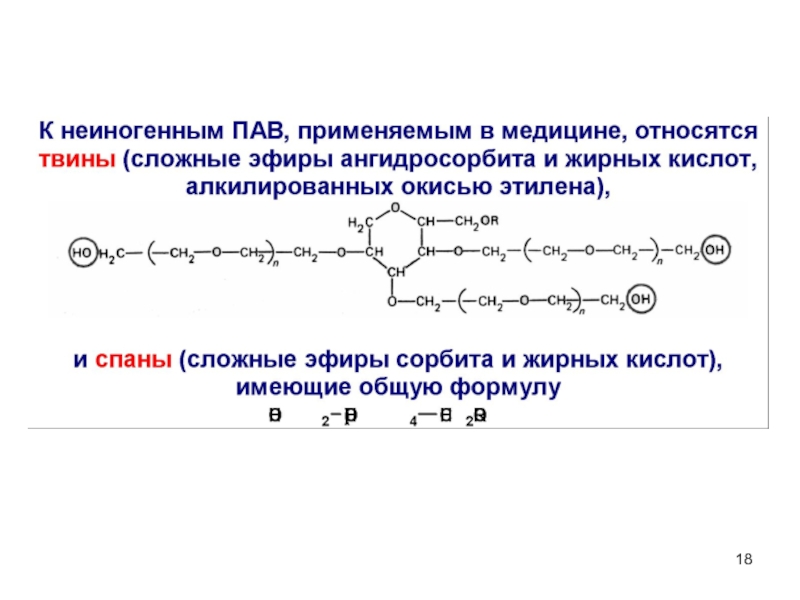
Слайд 14Модель молекулы поверхностно-активного вещества:
а — строение гептановой кислоты;
б –
строение гептанового спирта;
в – модель молекул ПАВ.
Слайд 16 Антимикробное действие ПАВ связывают с их влиянием
на проницаемость клеточных мембран, а также ингибирующим действием на ферментативные
системы микроорганизмов.Четвертичные аммониевые основания (ЧАО)
обладают ярко выраженной антифаговой активностью.
Они приблизительно в 300 раз эффективнее фенола по губительному действию в отношении микроорганизмов и применяются в в хирургии в качестве антисептиков.
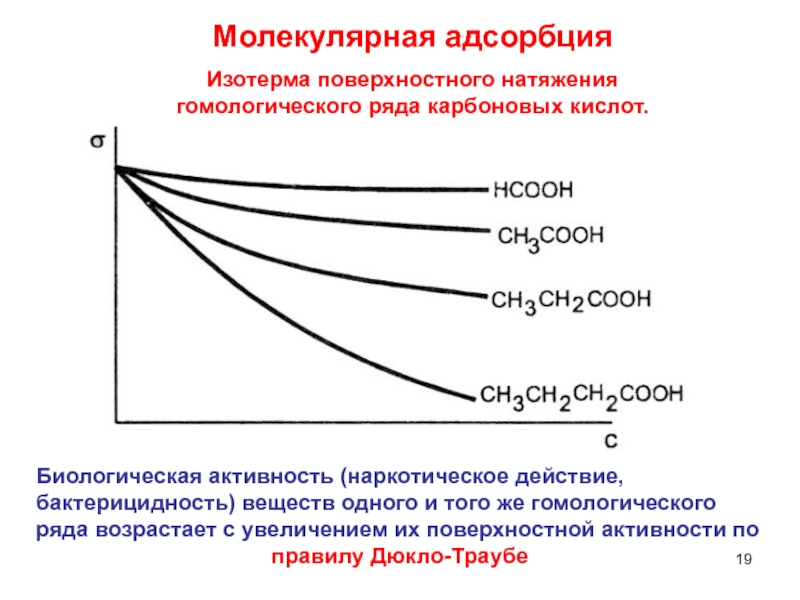
Слайд 19Биологическая активность (наркотическое действие, бактерицидность) веществ одного и того же
гомологического ряда возрастает с увеличением их поверхностной активности по
правилу Дюкло-Траубе
Молекулярная адсорбция
Изотерма поверхностного натяжения
гомологического ряда карбоновых кислот.
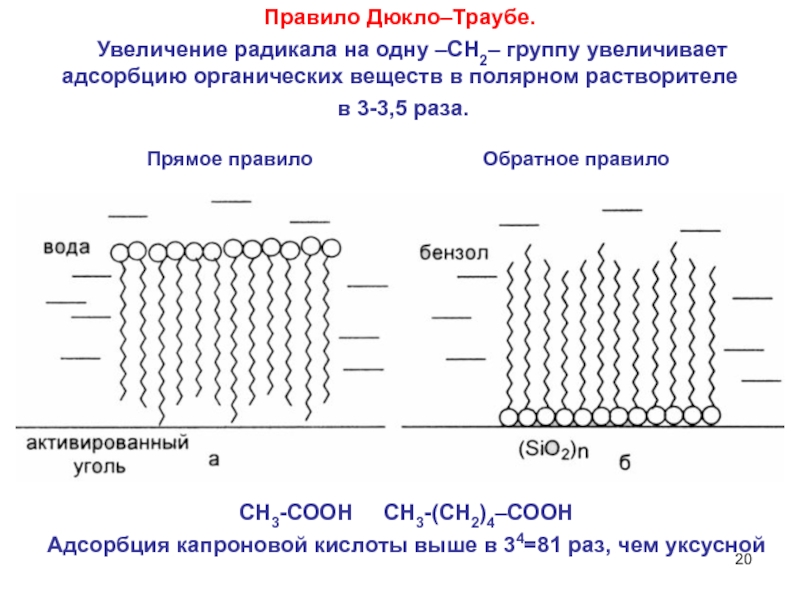
Слайд 20Правило Дюкло–Траубе.
Увеличение радикала на одну –СН2– группу увеличивает
адсорбцию органических веществ в полярном растворителе
в 3-3,5 раза.
Прямое правило
Обратное
правилоСН3-СООН СН3-(СН2)4–СООН
Адсорбция капроновой кислоты выше в 34=81 раз, чем уксусной
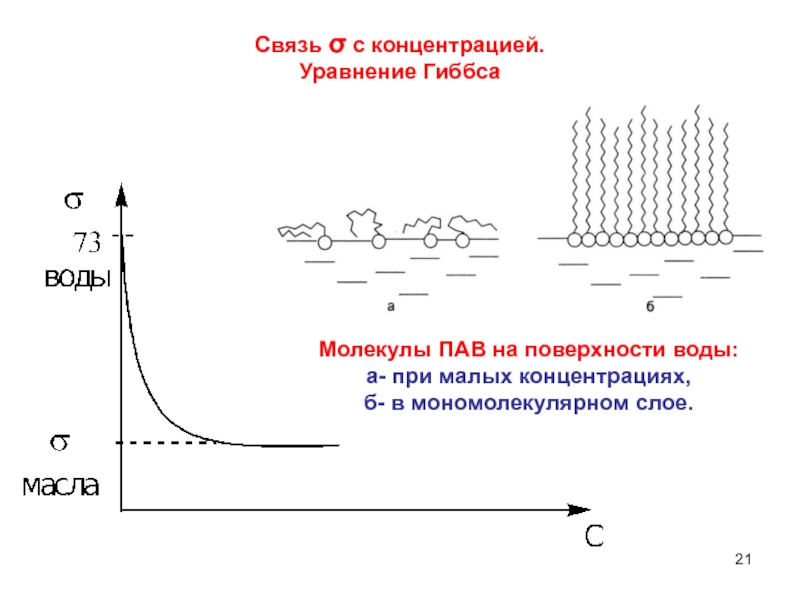
Слайд 21Связь σ с концентрацией.
Уравнение Гиббса
Молекулы ПАВ на поверхности воды:
а-
при малых концентрациях,
б- в мономолекулярном слое.
Слайд 22Уравнение Гиббса
ГИББС Джозайя Уиллард
(11.02.1839-28.04.1903)
Заложил основы термодинамики поверхностных явлений и электрохимических
процессов, ввел понятие адсорбции.
Слайд 23 С 1942 г. заведовал кафедрой коллоидной химии
Московского университета. Изучал влияние адсорбционных слоев на свойства дисперсных материалов,
явления смачивания, а также структурообразования. Исследовал ПАВ, закономерности образования и стабилизации пен и эмульсий. Правило Ребиндера
В первую очередь из растворов адсорбируются
вещества полярность которых ближе к полярности
адсорбента
(с наименьшей диэлектрической проницаемостью )
ε угля = 1 < ε уксусной к-ты = 6 < ε воды = 81
↓
Ребиндер Петр Александрович
(3.10.1898 – 12.07.1972)
Слайд 24 Нобелевская премия по химии (1932) «за открытия
и исследования в области химии поверхностных явлений».
Его именем названа
гора на Аляске, а также один из колледжей Нью-Йоркского государственного университета. Ирвинг Ленгмюр
(31.01.1881 – 16.08.1957)
1. Изотерма Ленгмюра
Изотермы адсорбции
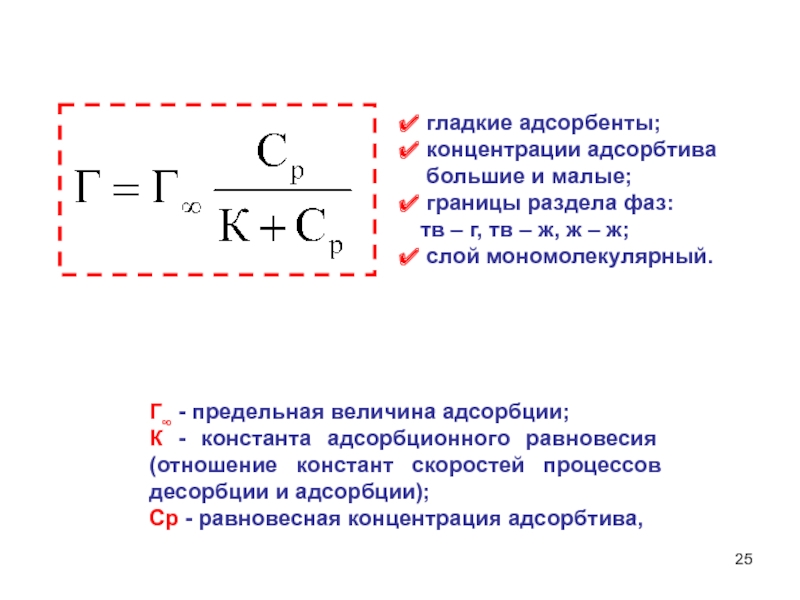
Слайд 25 гладкие адсорбенты;
концентрации адсорбтива
большие и малые;
границы раздела
фаз:
тв – г, тв – ж, ж – ж;
слой мономолекулярный.Г∞ - предельная величина адсорбции;
К - константа адсорбционного равновесия (отношение констант скоростей процессов десорбции и адсорбции);
Ср - равновесная концентрация адсорбтива,
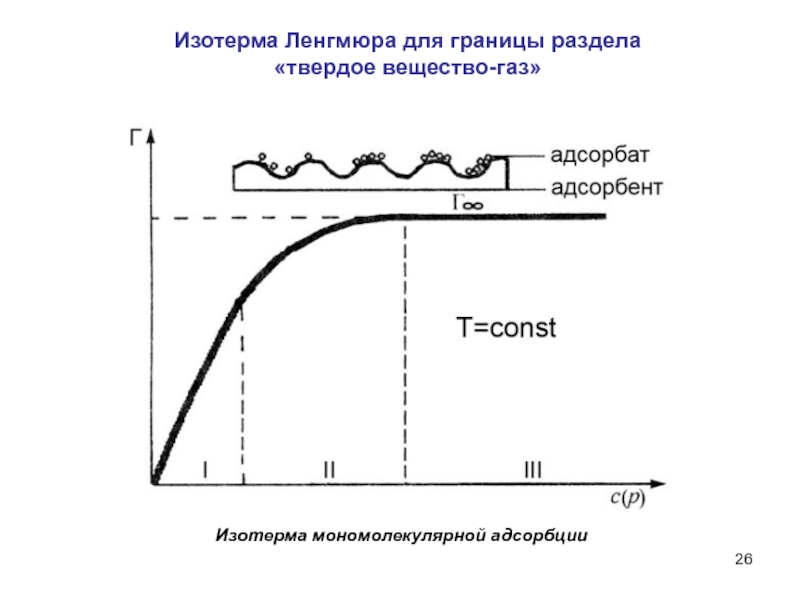
Слайд 26Изотерма Ленгмюра для границы раздела
«твердое вещество-газ»
Изотерма мономолекулярной адсорбции
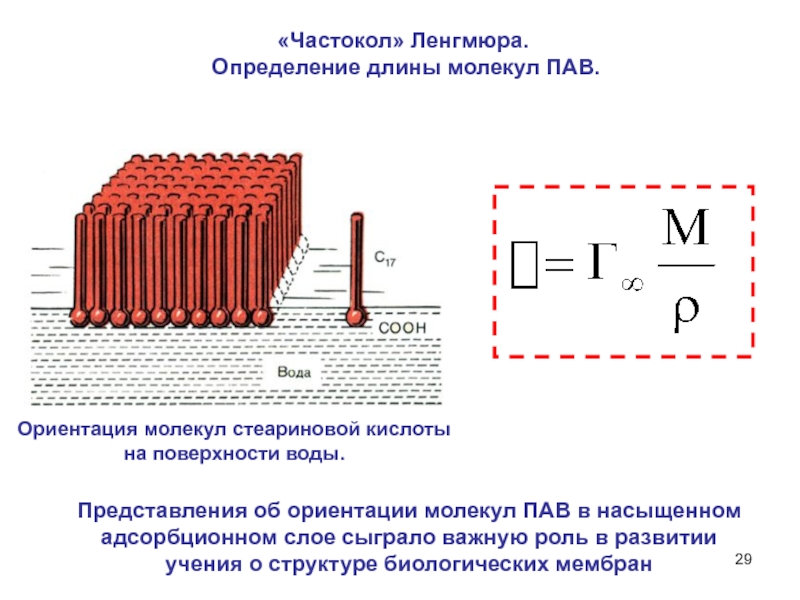
Слайд 29«Частокол» Ленгмюра.
Определение длины молекул ПАВ.
Представления об ориентации молекул ПАВ
в насыщенном
адсорбционном слое сыграло важную роль в развитии
учения о
структуре биологических мембранОриентация молекул стеариновой кислоты
на поверхности воды.
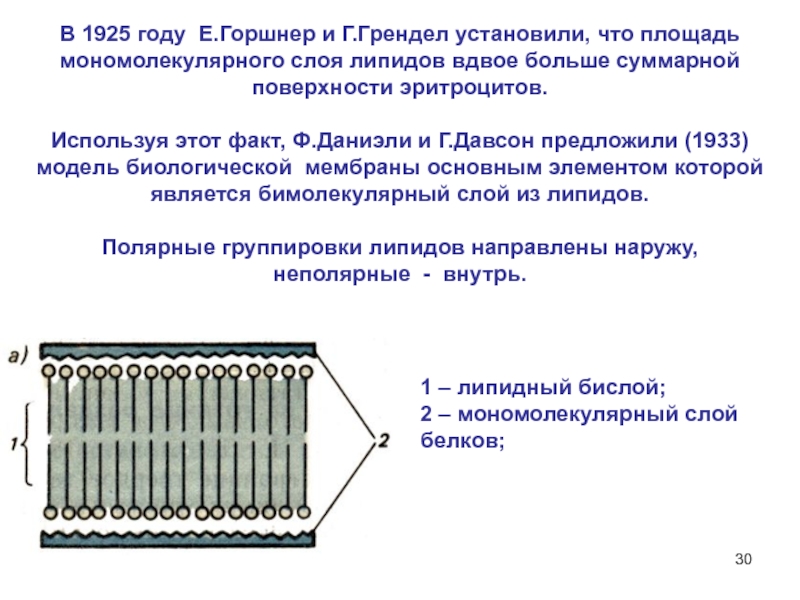
Слайд 30В 1925 году Е.Горшнер и Г.Грендел установили, что площадь мономолекулярного
слоя липидов вдвое больше суммарной поверхности эритроцитов.
Используя этот факт,
Ф.Даниэли и Г.Давсон предложили (1933) модель биологической мембраны основным элементом которой является бимолекулярный слой из липидов.Полярные группировки липидов направлены наружу, неполярные - внутрь.
1 – липидный бислой;
2 – мономолекулярный слой белков;
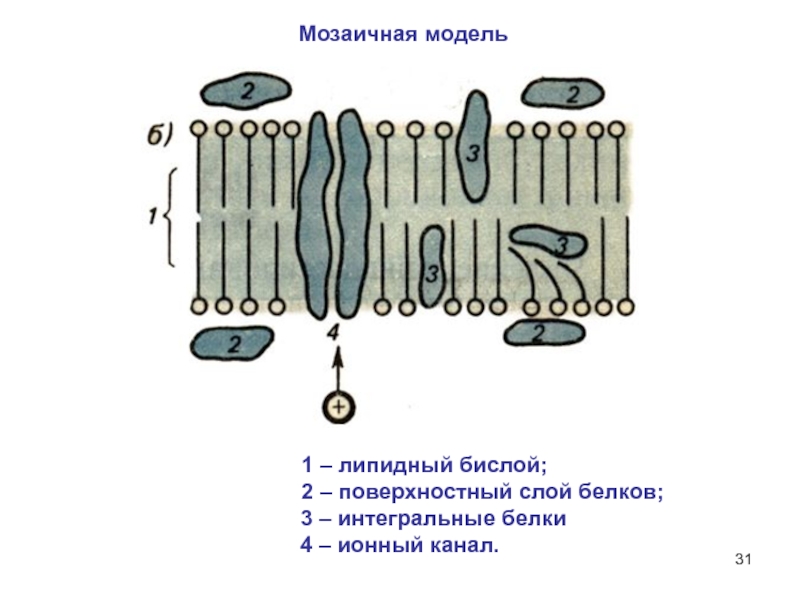
Слайд 31 1 – липидный бислой;
2 – поверхностный слой белков; 3 – интегральные белки
4 – ионный канал.
Мозаичная модель
Слайд 32Мозаичная модель биологической мембраны
Макромолекулы интегральных белков, пронизывающих мембрану, образуют ионные
каналы, обладающие избирательной проницаемостью для различных ионов.
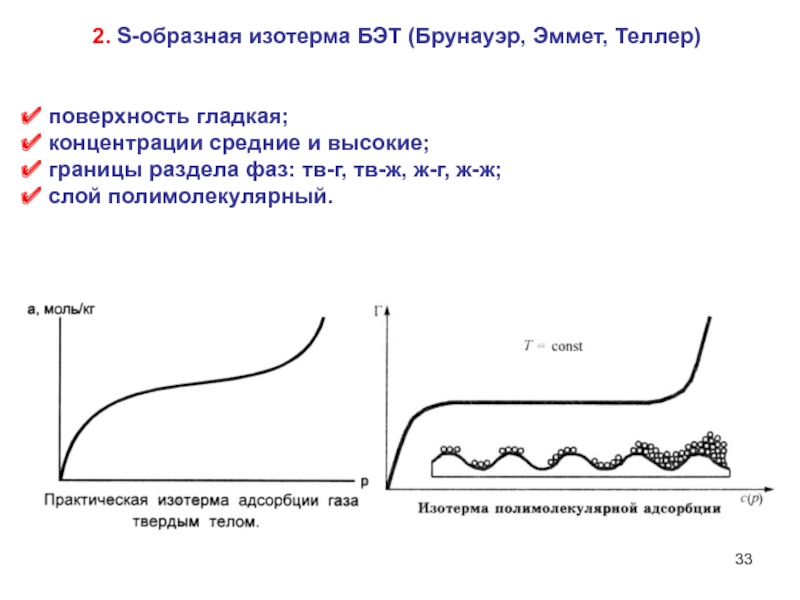
Слайд 332. S-образная изотерма БЭТ (Брунауэр, Эммет, Теллер)
поверхность гладкая;
концентрации
средние и высокие;
границы раздела фаз: тв-г, тв-ж, ж-г, ж-ж;
слой полимолекулярный.Слайд 34Пористые адсорбенты
Николай Дмитриевич Зелинский
(6.02.1861–31.07.1953)
Русский советский химик. Высшее образование получил
в Одесском университете, после чего стажировался в Геттингене. В 1915
г. он создал первый в мире противогаз, в котором отравляющие газы адсорбировались углем.Слайд 35 Была весна 1915 года. 22 апреля вечером на
реке Ипр немцы впервые в истории войн применили удушливый газ
хлор. Около 15000 канадских и французских солдат тяжело пострадало, а около 5000 погибло в ту же ночь.Слайд 37Герберт Макс Фрейндлих
(28.01.1880 – 30.03.1941)
Исследовал коагуляцию и
устойчивость коллоидных растворов.
Подтвердил уравнение изотермы адсорбции, выведенное в 1888
году Ван-Бемеленом (Голландия).Открыл явление тиксотропии.
Занимался коллоидно-химическими проблемами, связанными с биологией и медициной.
Слайд 38 адсорбент пористый;
концентрации средние;
границы раздела фаз:
тв-г,
тв-ж.
3. Изотерма Фрейндлиха
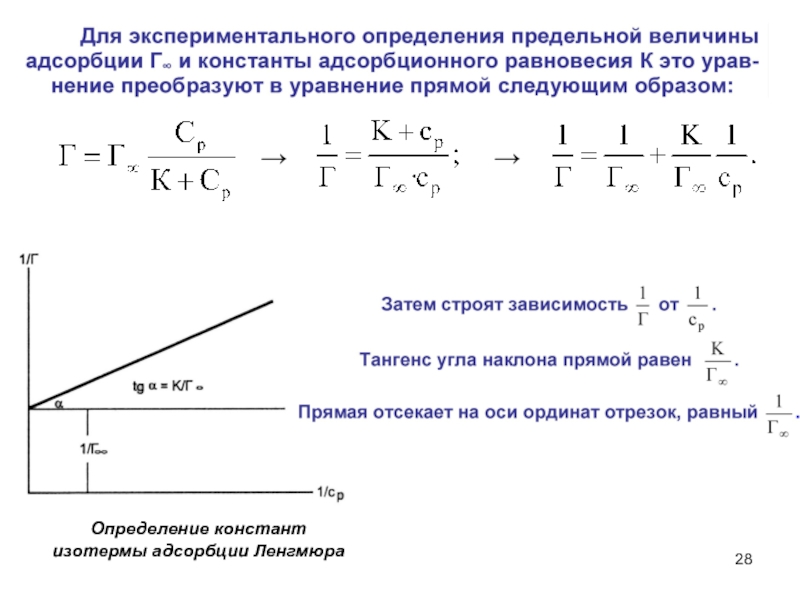
Слайд 39Графическое определение К и n из уравнения Фрейндлиха
График для определения
констант уравнения
адсорбции Фрейндлиха
Слайд 40Характеристики поверхностей в живых организмах
Живые организмы представляют
собой системы с очень развитыми поверхностями раздела, к которым относят
кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны, мембраны ядер, митохондрий, лизосом. Поверхность
кожи взрослого человека составляет ~ 2,0 м2,
эритроцитов ~ 2500—3800 м2,
капилляров печени ~ около 400 м2,
альвеол ~ около 90-120 м2,
скелета ~ около 2 тыс. км2.
Слайд 41Li+ > Na+ > K+ > Rb+ > Cs+
Многозарядные ионы
адсорбируются лучше!
Ионная адсорбция
Основное влияние – радиус гидратированного иона.
Последние члены
лиотропных рядов адсорбируются лучше!Слайд 42 В первую очередь из растворов адсорбируются те
ионы, которые входят в состав кристаллической решетки адсорбента
(или изоморфны
с ней - HS-, S2- на поверхность As2S3)Казимир Фаянс
(27.05.1887 – 18.05.1975)
Американский физико-химик. Определил взаимосвязь деформации электронных оболочек с химическими и оптическими свойствами неорганических соединений. Изучал сорбцию ионов и красящих веществ. Предсказал и открыл изотопы некоторых элементов. Сформулировал (1913) правило соосаждения радиоактивных элементов.
Правило Панета-Фаянса
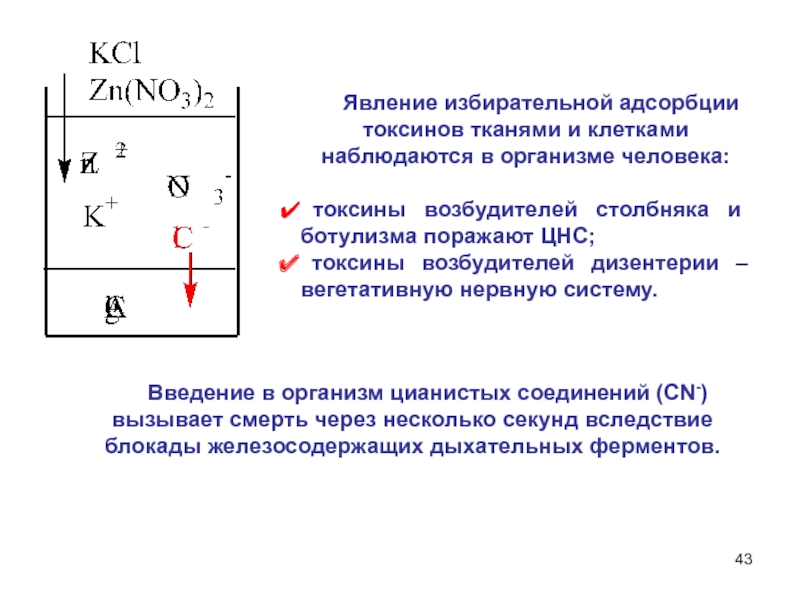
Слайд 43 Явление избирательной адсорбции токсинов тканями и клетками
наблюдаются в организме человека:
токсины возбудителей столбняка и ботулизма поражают
ЦНС;токсины возбудителей дизентерии – вегетативную нервную систему.
Введение в организм цианистых соединений (СN-) вызывает смерть через несколько секунд вследствие блокады железосодержащих дыхательных ферментов.
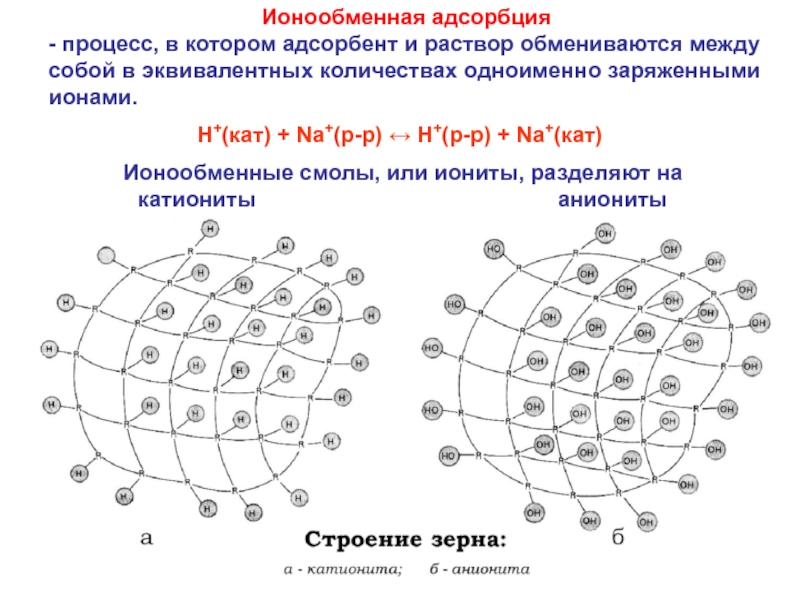
Слайд 44Ионообменная адсорбция
- процесс, в котором адсорбент и раствор обмениваются между
собой в эквивалентных количествах одноименно заряженными ионами.
Ионообменные смолы, или
иониты, разделяют накатиониты аниониты
Н+(кат) + Nа+(р-р) ↔ Н+(р-р) + Nа+(кат)
Слайд 45 Весовая обменная емкость Гвес - число ммоль-эквивалентов ионов,
поглощенных 1 г сухого ионита (ммоль-экв/г), находящимся в равновесии с
раствором определенной концентрации.Динамическая обменная емкость Гполн. – число ммоль-экв ионов, поглощенных 1 г сухого ионита при полном поглощении ионов в динамических условиях.
Н+(кат)+Nа+(р-р) ↔ Н+(р-р)+Nа+(кат)
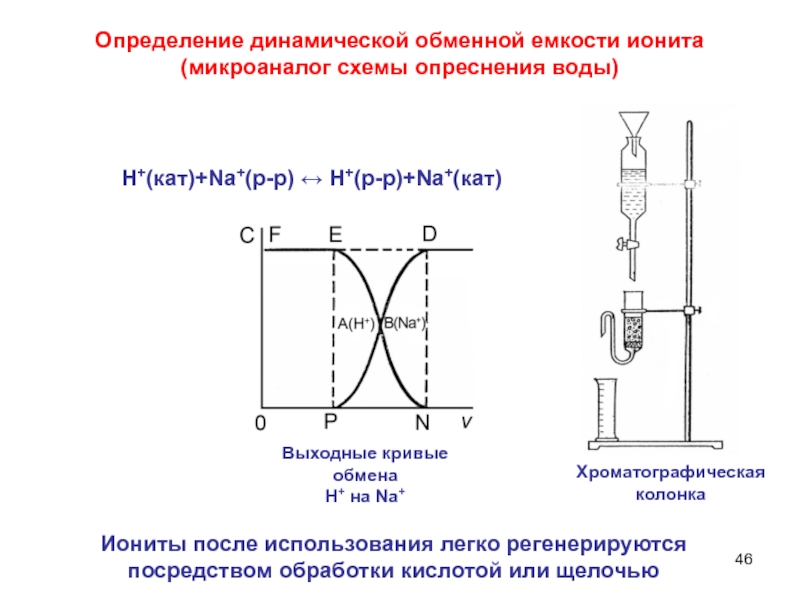
Слайд 46Определение динамической обменной емкости ионита
(микроаналог схемы опреснения воды)
Н+(кат)+Nа+(р-р) ↔ Н+(р-р)+Nа+(кат)
Иониты после использования легко регенерируются посредством обработки кислотой или щелочью
Выходные
кривые обмена
H+ на Na+Хроматографическая колонка
Слайд 47Применение ионитов
1. Разделение и очистка аминокислот и белков
(пепсин (рI=2), химотрипсин (рI=8.6) помещаются в аммиачный буфер с рН
= 8.4. Пепсин заряжается отрицательно (рН>рI) и при пропускании смеси через катионит не вступает в реакцию обмена. Положительно заряженный химотрипсин (рН<рI) будет адсорбироваться на катионите 3. Изменение солевого
состава молока
2. Консервирование крови
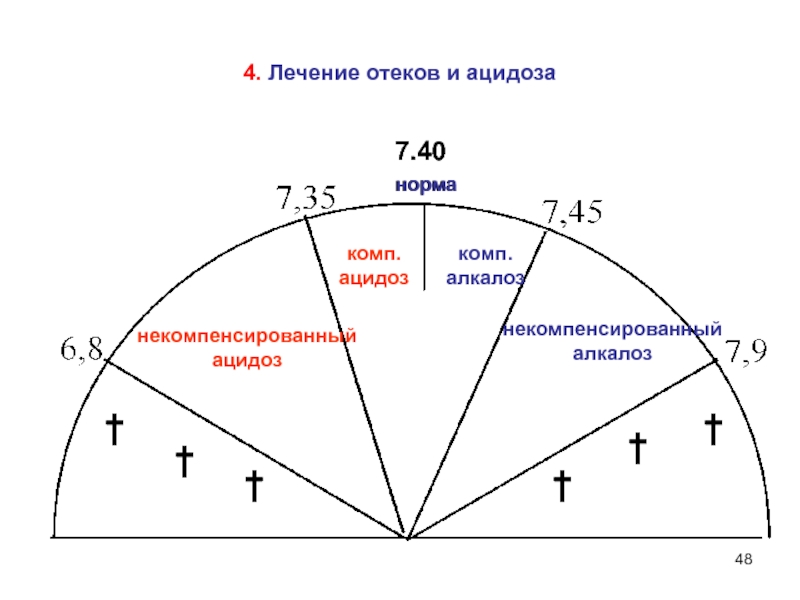
Слайд 48норма
†
†
†
†
†
†
7.40
некомпенсированный
ацидоз
комп.
ацидоз
комп.
алкалоз
некомпенсированный
алкалоз
норма
4. Лечение отеков и ацидоза
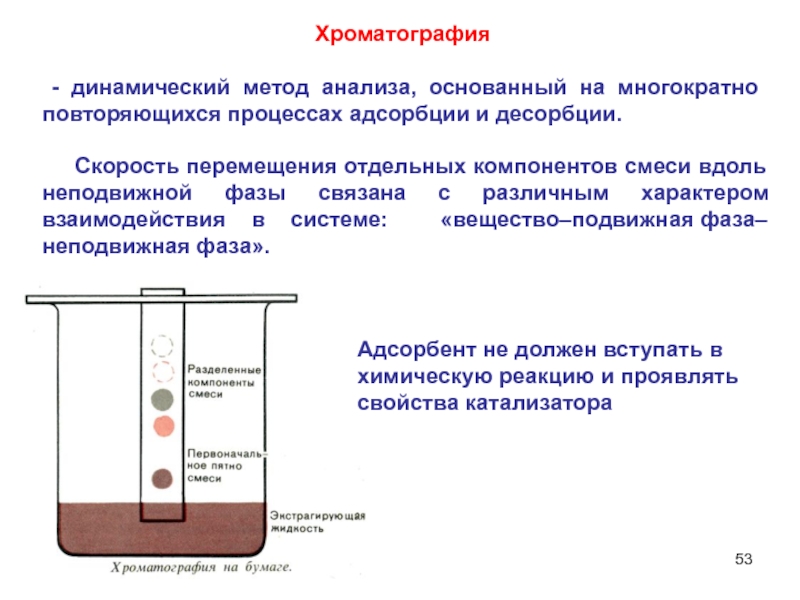
Слайд 53Хроматография
- динамический метод анализа, основанный на многократно повторяющихся процессах
адсорбции и десорбции.
Скорость перемещения отдельных компонентов смеси
вдоль неподвижной фазы связана с различным характером взаимодействия в системе: «вещество–подвижная фаза–неподвижная фаза».
Адсорбент не должен вступать в химическую реакцию и проявлять свойства катализатора
Слайд 54Михаил Семенович Цвет
(1872-1919)
Русский ботаник, физиолог, биохимик. Исследовал пигменты растений
и искал методы их разделения. Хроматографический метод описан был впервые
в статье «Об одной новой категории адсорбционных явлений и о их применении в биохимическом анализе», напечатанной в 1903 году. Принципы хроматографии М.С.Цвет изложил в книге «Хлорофилл в растениях и животных» (1910).Слайд 55Вещества распределяются по высоте колонки в зависимости от адсорбционных свойств:
плохо адсорбирующиеся вещества
выходят из колонки первыми.
Слайд 561. Адсорбционная
Основана на различии в адсорбционных свойствах разделяемых
веществ.
Хорошо адсорбирующиеся компоненты перемещаются с низкой скоростью.
а) бумажная
Хроматографическое разделение
чернил на компоненты в водно-метанольной смеси
Виды хроматографии
Слайд 592. Распределительная хроматография
Основана на различной растворимости вещества
в
неподвижной фазе (жидкость) и в подвижной фазе
(жидкость или газ)
Первыми
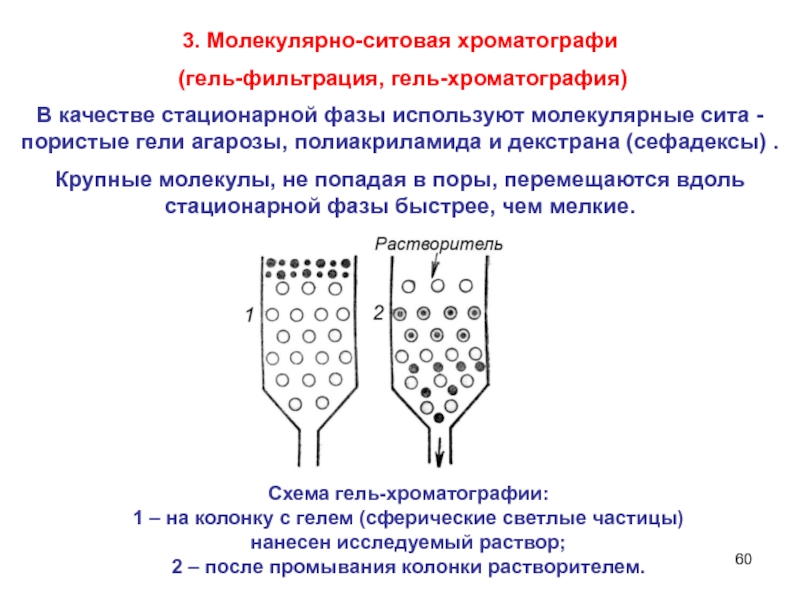
из колонки выходят плохо растворимые вещества!Слайд 603. Молекулярно-ситовая хроматографи
(гель-фильтрация, гель-хроматография)
В качестве стационарной фазы используют молекулярные
сита - пористые гели агарозы, полиакриламида и декстрана (сефадексы) .
Крупные молекулы, не попадая в поры, перемещаются вдоль стационарной фазы быстрее, чем мелкие.
Схема гель-хроматографии:
1 – на колонку с гелем (сферические светлые частицы)
нанесен исследуемый раствор;
2 – после промывания колонки растворителем.
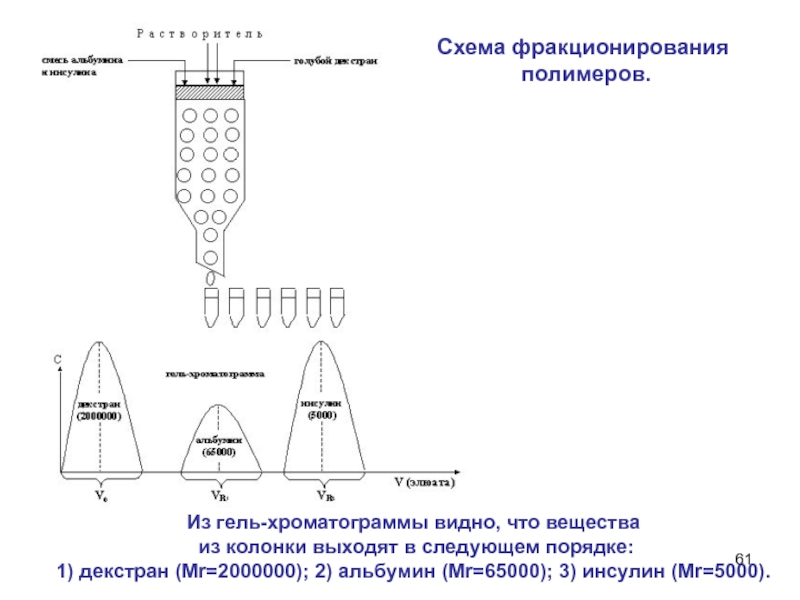
Слайд 61Из гель-хроматограммы видно, что вещества
из колонки выходят в
следующем порядке:
1) декстран (Мr=2000000); 2) альбумин (Мr=65000); 3) инсулин
(Мr=5000). Схема фракционирования
полимеров.
Слайд 62 4.
Афинная хроматография (биоспецифическая)
Основана на специфичности взаимодействия ферментов.
Стационарная фаза содержит
либо фермент, либо субстрат.Иммобилизация
закрепление веществ на твердой поверхности адсорбента-носителя (силикагели, силохромы)
Иммобилизованные ферменты можно многократно применять
в проточных системах и они не теряют активности при длительном хранении (до полугода)
Слайд 63Из анализируемой смеси с высокой степенью специфичности будет «вылавливаться» партнер
соответствующей
фермент-субстратной реакции.
Размеры каждого кармана и природа образующих его радикалов
определяют тип аминокислотной цепи, которую он удерживает лучше всего. Слайд 64 Иммобилизация уреазы широко применяется при аналитическом определении мочевины и
в аппарате «искусственная почка»
Для удаления токсических веществ из биологических жидкостей
через адсорбент пропускают:кровь – гемосорбция (гемоперфузия);
плазму – плазмосорбция (плазмоперфузия);
лимфу – лимфосорбция (лимфоперфузия).
Слайд 65Клиренс -
объем крови, полностью очищаемый в данном аппарате за
единицу времени при заданной объемной скорости крови или среды.
Слайд 67
Современные активные медицинские сорбенты можно разделить на четыре
группы:
1. Дренирующие сорбенты - обеспечивают отток раневого отделяемого и микрофлоры
со дна раны;2. Биологически активные сорбенты – содержат иммобилизованные в их структуре лекарственные вещества;
3. Избирательные сорбенты - необратимо адсорбируют микрофлору в пористой структуре;
4. Комбинированные сорбенты - это перевязочные средства, содержащие различные по механизму действия сорбенты.
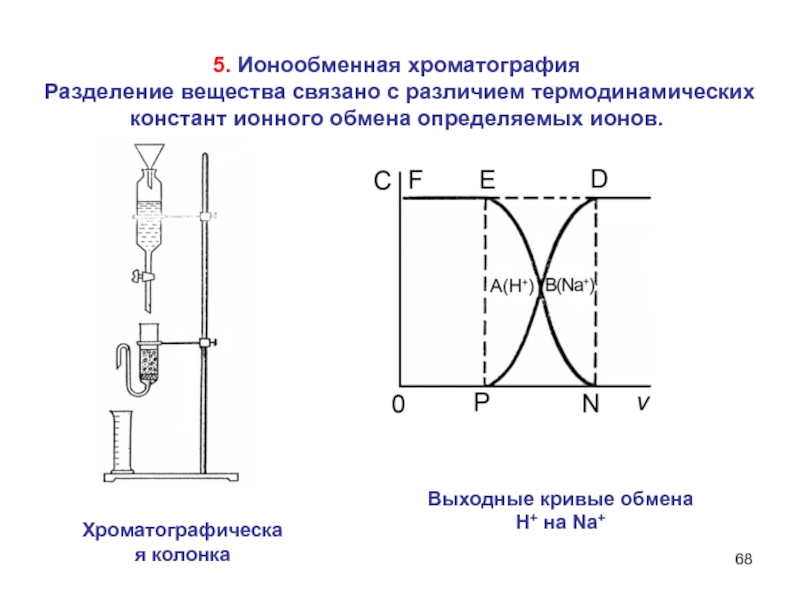
Слайд 685. Ионообменная хроматография
Разделение вещества связано с различием термодинамических констант
ионного обмена определяемых ионов.
Выходные кривые обмена
H+ на Na+
Хроматографическая колонка
Слайд 69Уравнение Б.П.Никольского:
где x1 и x2 – количество поглощенных ионов
(мг-экв/г);
a1 и a2 – активности ионов; z1 и z2 валентности
ионов; K – константа обмена.Слайд 71Степень разделения зависит от:
длины колонки;
природы адсорбента;
природы адсорбтива;
температуры.
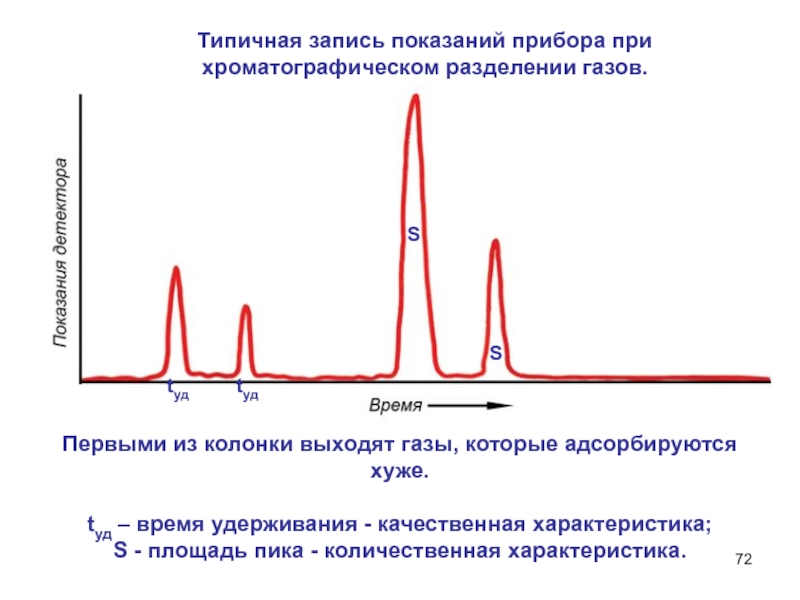
Слайд 72Типичная запись показаний прибора при хроматографическом разделении газов.
Первыми из колонки
выходят газы, которые адсорбируются хуже.
tуд – время удерживания - качественная
характеристика;S - площадь пика - количественная характеристика.
tуд
S
tуд
S
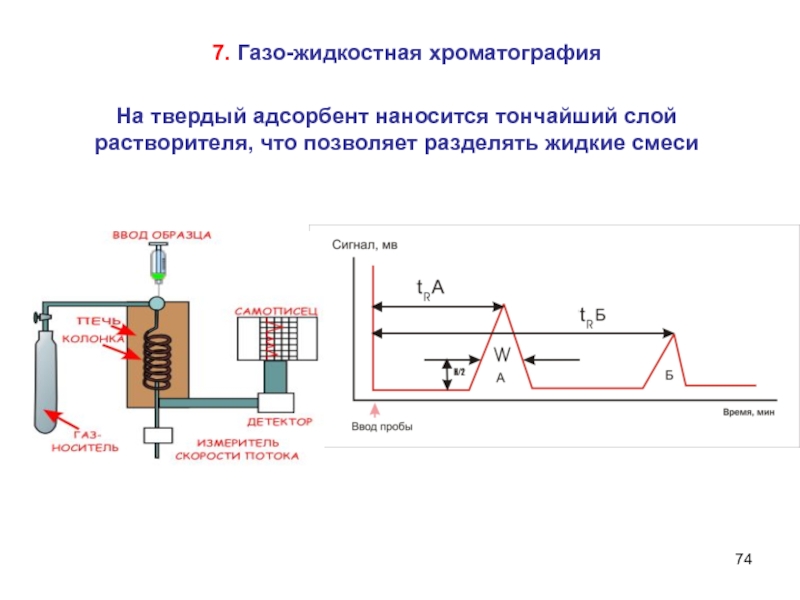
Слайд 74На твердый адсорбент наносится тончайший слой растворителя, что позволяет разделять
жидкие смеси
7. Газо-жидкостная хроматография
Слайд 75Первыми из колонки выходят плохо растворимые вещества
Хроматограмма смеси изомерных
ксилолов.
Разделение великолепное:
Пики, соответствующие изомерам, далеко отстоят друг от
друга.Слайд 78 Каждый двадцатый раненый в годы второй мировой войны страдал
от гнойно-септических осложнений, вызванных анаэробными бациллами – возбудителями газовой гангрены.
Применение хроматографических методов сделало возможным верификацию диагноза анаэробной инфекции в течение нескольких часов, что позволило снизить число осложнений, вызванных анаэробными микроорганизмами почти в 100 раз.
Применение хроматографии
1. В медицине