Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
279 химия 20.10
Содержание
- 1. 279 химия 20.10
- 2. Слайд 2
- 3. Слайд 3
- 4. Взаимодействие кислот с металлами2Al + 6HCl = 2AlCl3 + 3H2↑
- 5. Слайд 5
- 6. Взаимодействие концентрированной серной кислоты с медью2H2SO4 (конц.) + Cu = CuSO4 + SO2↑ + 2H2O
- 7. Слайд 7
- 8. Особенности взаимодействия азотной кислоты с металламиAl + 6HNO3(конц.) → Al(NO3)3 +
- 9. Концентрированная азотная кислота не взаимодействует с благородными
- 10. Особенности взаимодействия азотной кислоты с металламиNO, N2O,
- 11. Взаимодействие кислот с основными и амфотерными оксидамиH2SO4
- 12. Взаимодействие кислот с основаниями и амфотерными гидроксидамиHCl
- 13. Кислоты взаимодействуют с солями, в результате чего
- 14. Взаимодействие кислот с солямиAgNO3 + HCl =
- 15. Взаимодействие кислот с солями2HNO3 + Na2CO3 =
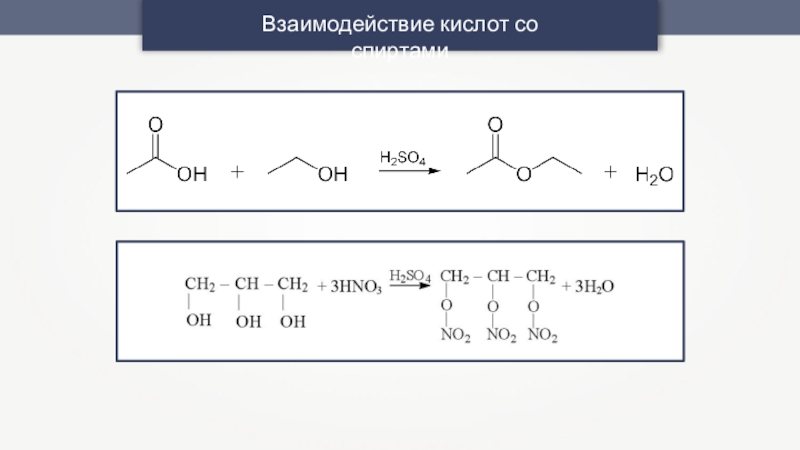
- 16. Взаимодействие кислот со спиртами
- 17. Скачать презентанцию
Слайды и текст этой презентации
Слайд 6Взаимодействие концентрированной
серной кислоты с медью
2H2SO4 (конц.) + Cu =
CuSO4 + SO2↑ + 2H2O
Слайд 8Особенности взаимодействия
азотной кислоты с металлами
Al + 6HNO3(конц.) → Al(NO3)3 + 3NO2↑ + 3H2O
Концентрированная
азотная кислота при взаимодействии с активными металлами образует нитрат металла,
оксид азота (IV) и воду:Ag + 2HNO3(конц.) → AgNO3 + NO2↑ + H2O
Концентрированная азотная кислота при взаимодействии с малоактивными металлами образует нитрат металла, оксид азота (IV) и воду:
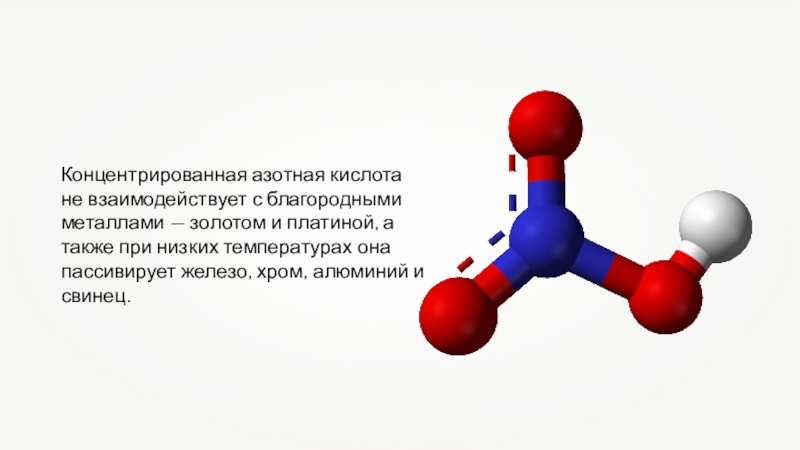
Слайд 9Концентрированная азотная кислота
не взаимодействует с благородными металлами — золотом
и платиной, а также при низких температурах она пассивирует железо,
хром, алюминий и свинец.Слайд 10Особенности взаимодействия
азотной кислоты с металлами
NO, N2O, N2, NH4NO3
Разбавленная азотная
кислота при взаимодействии
с активными металлами может давать разные продукты,
что зависит от степени разбавленности кислоты и температуры:3Cu + 8HNO3(разб.) → 3Cu(NO3)2 + 2NO↑ + 4H2O
Разбавленная азотная кислота при взаимодействии с металлами, стоящими после водорода, образует нитрат металла, оксид азота (II) и воду:
Слайд 11Взаимодействие кислот
с основными и амфотерными оксидами
H2SO4 + CaO =
CaSO4 + H2O
При взаимодействии серной кислоты с основным оксидом кальция
образуются сульфат кальция и вода:H2SO4 + Al2O3 = Al2(SO4)3 + H2O
При взаимодействии серной кислоты с амфотерным оксидом алюминия образуются сульфат алюминия и вода:
CH3COOH + CuO → (CH3COO)2Cu + H2O
При взаимодействии уксусной кислоты с оксидом меди образуются соль — ацетат меди и вода:
Слайд 12Взаимодействие кислот с основаниями
и амфотерными гидроксидами
HCl + KOH =
KCl + H2O
При взаимодействии соляной кислоты со щёлочью гидроксидом калия
образуются хлорид калия и вода: 3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 6H2O
При взаимодействии серной кислоты с амфотерным гидроксидом железа третьей валентности образуются сульфат железа третьей валентности и вода:
3HCOOH + Al(OH)3 → (HCOO)3Al + 3H2O
При взаимодействии органической муравьиной кислоты с амфотерным гидроксидом алюминия образуются формиат алюминия и вода:
Слайд 13Кислоты взаимодействуют с солями,
в результате чего образуются новая соль
и новая кислота. Однако для протекания реакции нужно, чтобы в
результате образовывался осадок или выделялся газ. Слайд 14Взаимодействие кислот с солями
AgNO3 + HCl = AgCl↓ + HNO3
При
взаимодействии нитрата серебра с соляной кислотой образуется белый творожистый осадок
хлорида серебра и азотная кислота:BaCl2 + H2SO4 = BaSO4↓ + 2HCl
Растворимые соли бария — реагенты для качественного определения серной кислоты или её солей, так как в результате образуется осадок сульфат бария белого цвета:
Слайд 15Взаимодействие кислот с солями
2HNO3 + Na2CO3 = 2NaNO3 + H2O
+ CO2↑
При взаимодействии азотной кислоты с карбонатом натрия образуются нитрат
натрия, вода и углекислый газ:2CH3COOH + CaCO3 = (CH3COO)2Ca + H2O + CO2↑
При взаимодействии уксусной кислоты с карбонатом кальция образуются ацетат кальция, вода и выделяется углекислый газ.