Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алкены
Содержание
- 1. Алкены
- 2. ПЛАНОпределение. Общая формула класса углеводородов.Гомологический ряд.Виды изомерии.Номенклатура.Строение молекулы.Физические свойства.Способы получения.Химические свойства.Применение.Задание
- 3. Алкены – ациклические углеводороды, в молекуле которых
- 4. Слайд 4
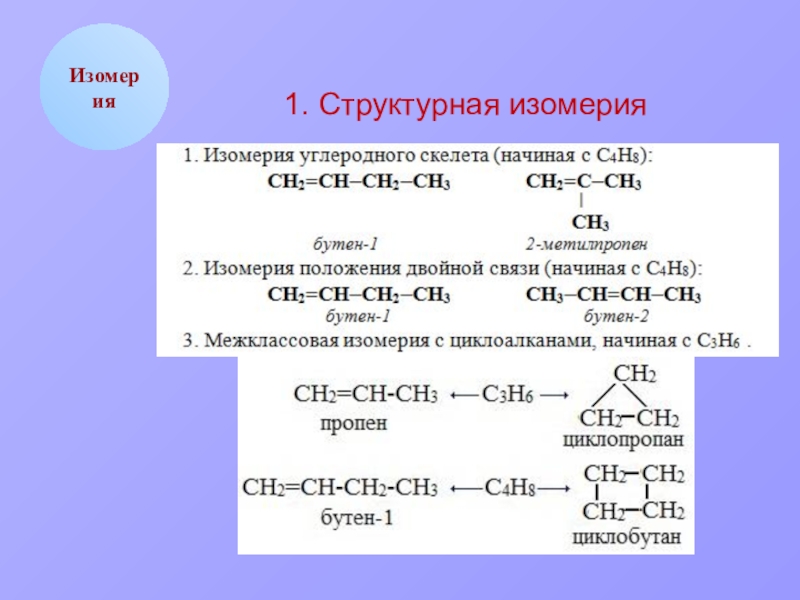
- 5. Изомерия1. Структурная изомерия
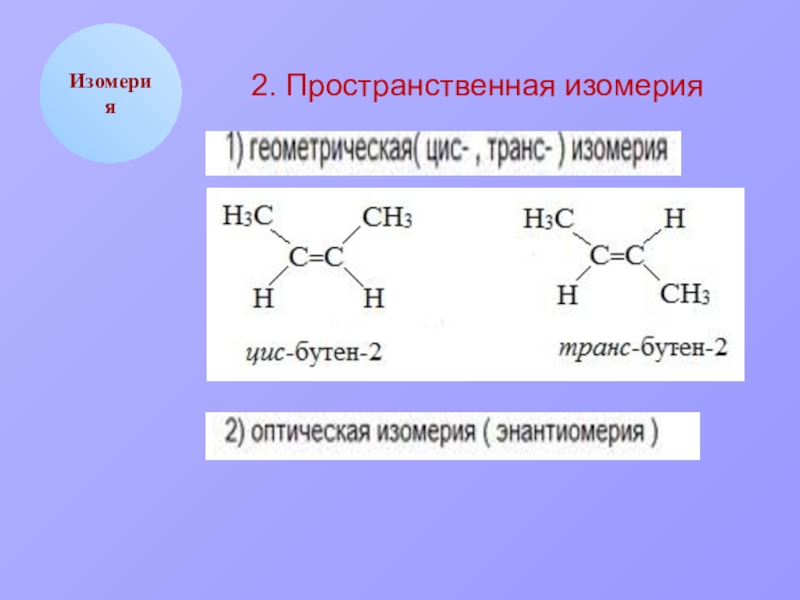
- 6. Изомерия2. Пространственная изомерия
- 7. НСНоменклатура1. Выбор главной цепи.НН3ССССССН3ННН32. Нумерация атомов главной цепи.НН3ССССССН3ННН3123453. Формирование названия.НН3СССССН3НН34 – метилпентен - 2
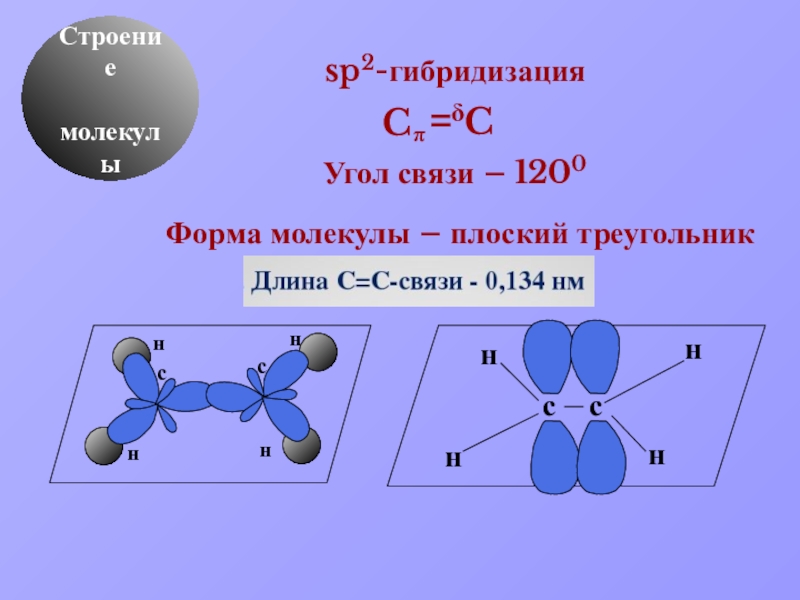
- 8. δ Строение молекулыsp2-гибридизацияУгол связи – 1200Форма молекулы – плоский треугольникC πC
- 9. Физические свойства
- 10. Химическиесвойства+ Н2, t0, Ni+ Hal2+ HHal+ H2O,
- 11. СНОН4. Гидратация:Pt, tХимические свойства алкенов1. Гидрирование:
- 12. Получение
- 13. Слайд 13
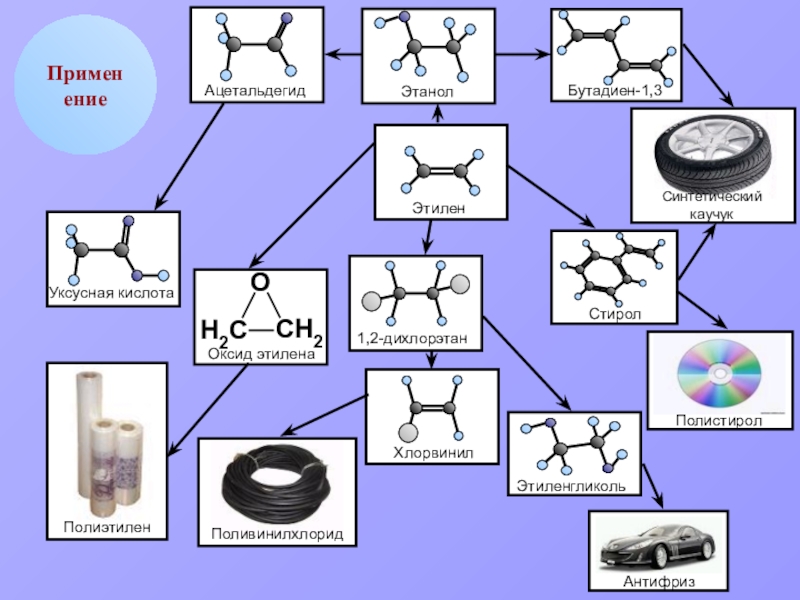
- 14. Применение
- 15. Задания1. Напишите структурные формулы соединений: а) 2,5-диметилгексен-1
- 16. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2ПЛАН
Определение. Общая формула класса углеводородов.
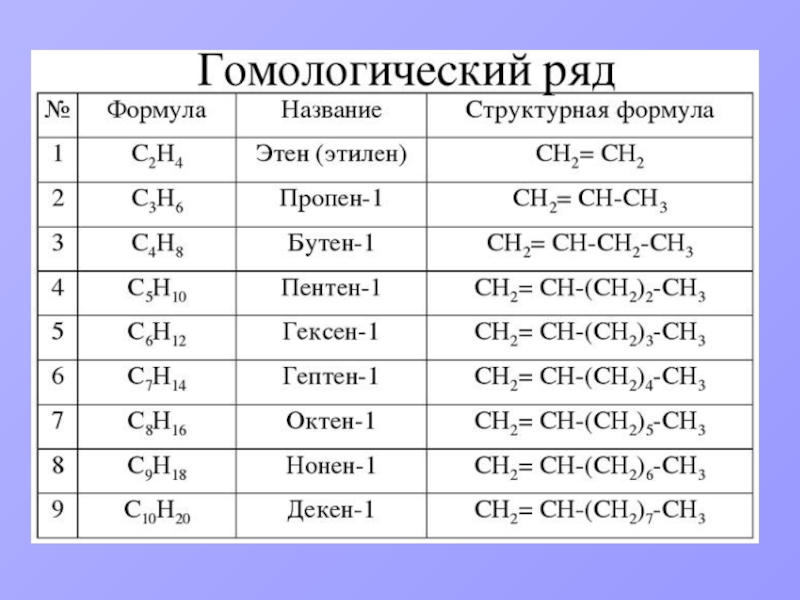
Гомологический ряд.
Виды изомерии.
Номенклатура.
Строение молекулы.
Физические свойства.
Способы получения.
Химические
свойства.
Слайд 3Алкены – ациклические углеводороды, в молекуле которых кроме одинарных связей
содержится одна двойная связь между атомами углерода.
Общая формула: СnH2n
CnH2n
Слайд 7Н
С
Номенклатура
1. Выбор главной цепи.
Н
Н3
С
С
С
С
С
СН3
Н
Н
Н3
2. Нумерация атомов главной цепи.
Н
Н3
С
С
С
С
С
СН3
Н
Н
Н3
1
2
3
4
5
3. Формирование названия.
Н
Н3
С
С
С
С
СН3
Н
Н3
4
– метилпентен - 2
Слайд 10Химические
свойства
+ Н2, t0, Ni
+ Hal2
+ HHal
+ H2O, t0, H+
+ H2O
+ [O]
+ O2, t0 (горение)
- H2, t0, Ni
+ nCnH2n
CnH2n+2
дигалогеналканы, СnH2nHal2
галогеналканы, СnH2n+1Hal
CnH2n+1OH
CnH2n(OH)2
CO2 + H2O
CnH2n-2
полимер
СnH2n
Слайд 11СН
ОН
4. Гидратация:
Pt, t
Химические свойства алкенов
1. Гидрирование:
СН2
СН2
+ Н2
СН3
СН3
2. Галогенирование:
СН2
СН2
+ Br2
СН2Вr
СН2Вr
3.
Гидрогалогенирование:СН2
СН2
+ НСl
CН3
СН2Сl
СН2
СН2
+ Н2О
t, Н3РО4
CН3
СН2ОН
5. Мягкое окисление:
СН2
СН2
+ [О] +Н2О
СН2
СН2
ОН
6. Горение:
СН2
СН2
+ 3О2
2СО2
2Н2О
7. Дегидрирование:
СН2
СН2
t, Ni
СН
+ Н2
8. Полимеризация:
nСН2
СН2
cat
( …
СН2
СН2
…)n
Для алкенов наиболее характерны реакции присоединения (1-4)
Учитывать правило Марковникова! (№ 3,4 )





![Алкены Химическиесвойства+ Н2, t0, Ni+ Hal2+ HHal+ H2O, t0, H++ H2O + Химическиесвойства+ Н2, t0, Ni+ Hal2+ HHal+ H2O, t0, H++ H2O + [O]+ O2, t0 (горение)- H2, t0,](/img/tmb/7/607796/a7ef4ce917f2d7810bcd6f33dc7b7f0e-800x.jpg)