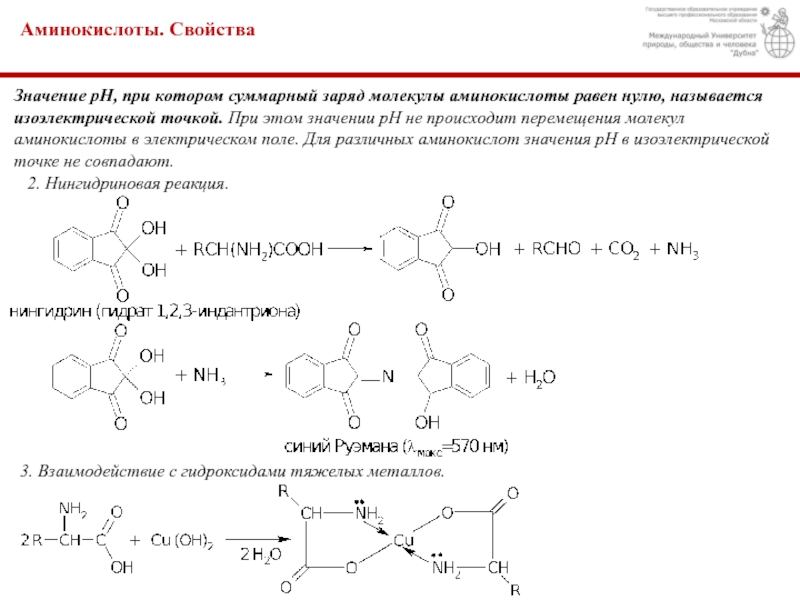
две
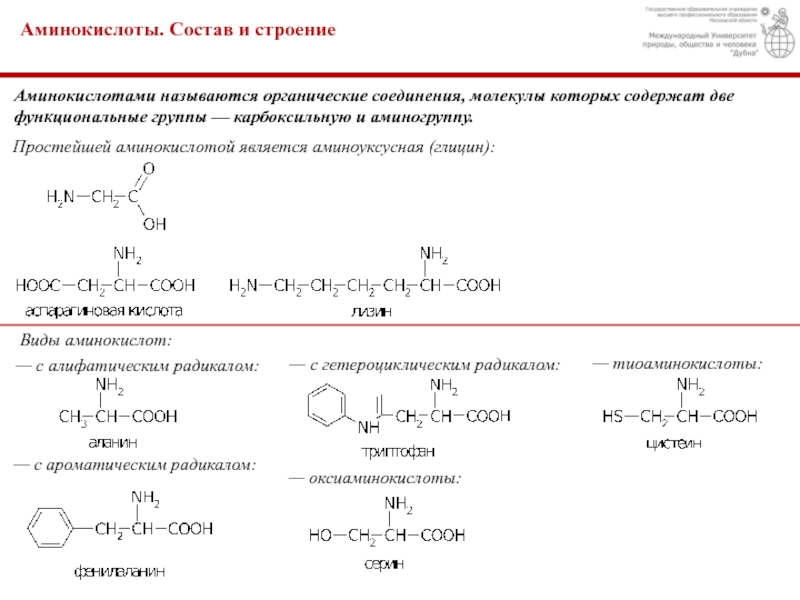
функциональные группы — карбоксильную и аминогруппу.
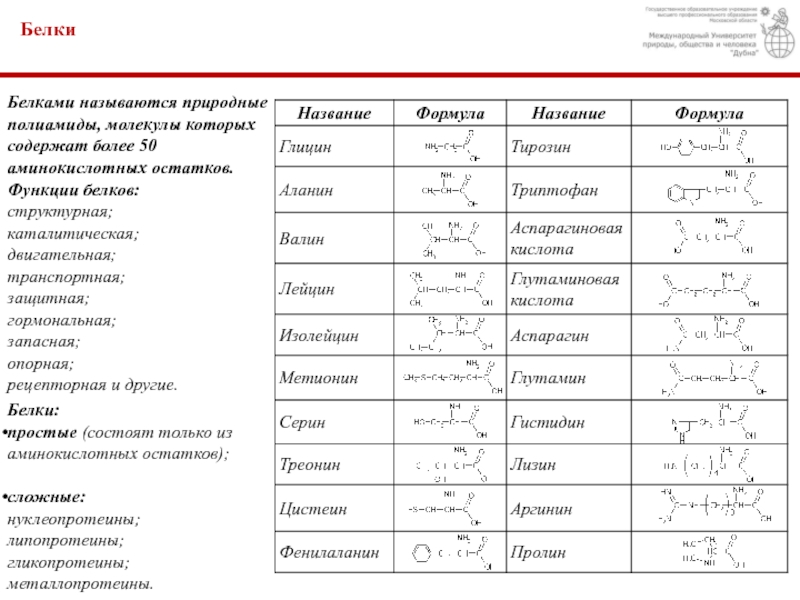
Простейшей аминокислотой является аминоуксусная (глицин):
Виды
аминокислот:— с алифатическим радикалом:
— с ароматическим радикалом:
— с гетероциклическим радикалом:
— оксиаминокислоты:
— тиоаминокислоты: