Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Асқазан обыры
Содержание
- 1. Асқазан обыры
- 2. Асқазан обыры — асқазанның шырышты қабатындағы эпителиальды
- 3. Дұрыс тамактанбауТемекі шегуХеликобактер пилориЭпштейн БарТұқым қуалаушылықРадиацияАсқазан рагының пайда болуына әкелетін септігін тигізетін факторлар:
- 4. Асқазан обыры мәселесінің маңыздылығы.
- 5. Слайд 5
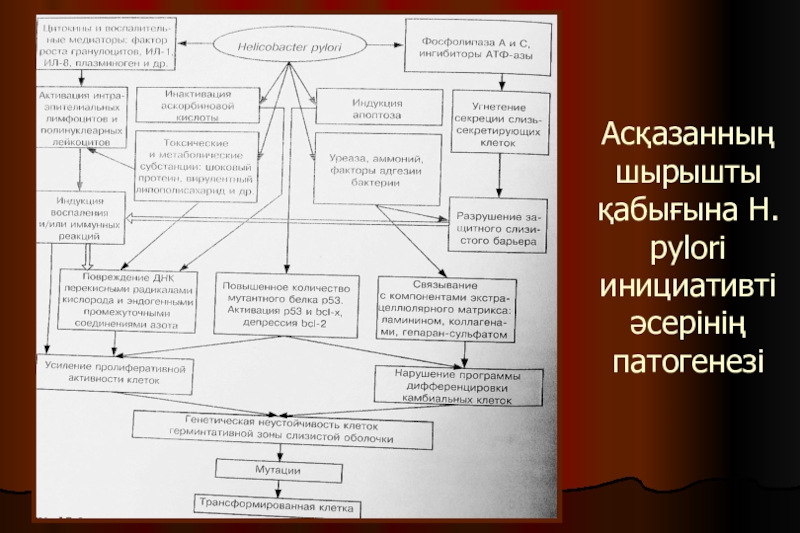
- 6. Асқазанның шырышты қабығына H. pylori инициативті әсерінің патогенезі
- 7. Асқазан ракалды аурулары:Атрофиялық гастритАхлоргидрия(4-5)Гипертрофиялық гастритІшектік метаплазияАденамотозды полиптерПернициоздық анемияСозылмалы ойық жара
- 8. Слайд 8
- 9. Слайд 9
- 10. Боррманның асқазан ісігінің түрлері Borrmann (1926): формы
- 11. Слайд 11
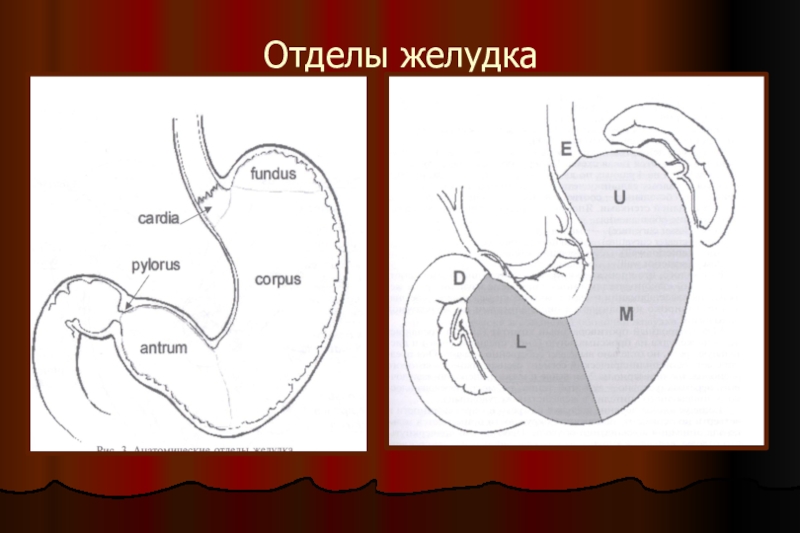
- 12. Отделы желудка
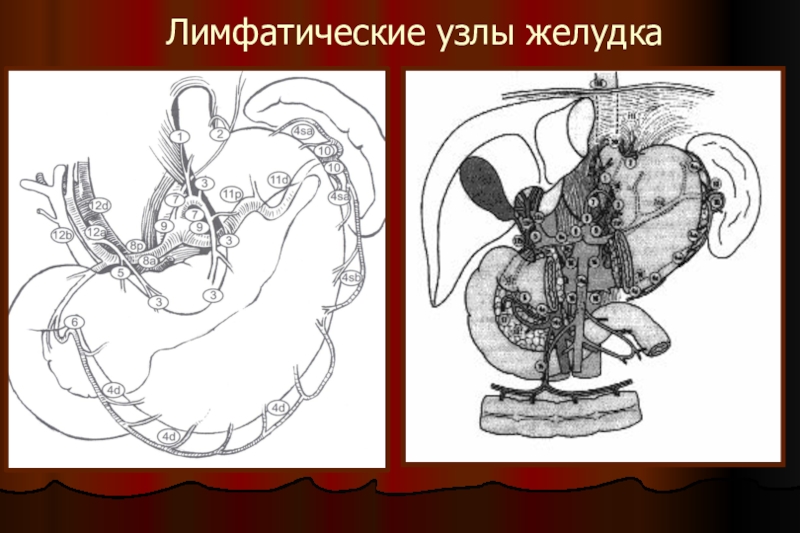
- 13. Лимфатические узлы желудка
- 14. Слайд 14
- 15. АО ның клиникалық көінісі
- 16. Клиническая картина РЖПризнаки запущенности болезни: 1) метастаз
- 17. Асқазан рагінің таралу жолдары
- 18. Диагностика РЖ-Эзофагогастродуоденоскопия с биопсией – является ведущим
- 19. Диагностика РЖ -Рентгеноскопия желудкапо данным японских авторов, ранний
- 20. ЛапароскопияЛапароскопия применяется тогда, когда есть подозрение на
- 21. Диагностика РЖУльтразвуковая томография органов брюшной полостиРентгеноскопия грудной
- 22. Рентгеноконтрастное исследование желудкаа Циркулярный стеноз антрального отдела
- 23. Лечение РЖХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕРАДИКАЛЬНАЯ ОПЕРАЦИЯ
- 24. Выбор объема хирургического вмешательства
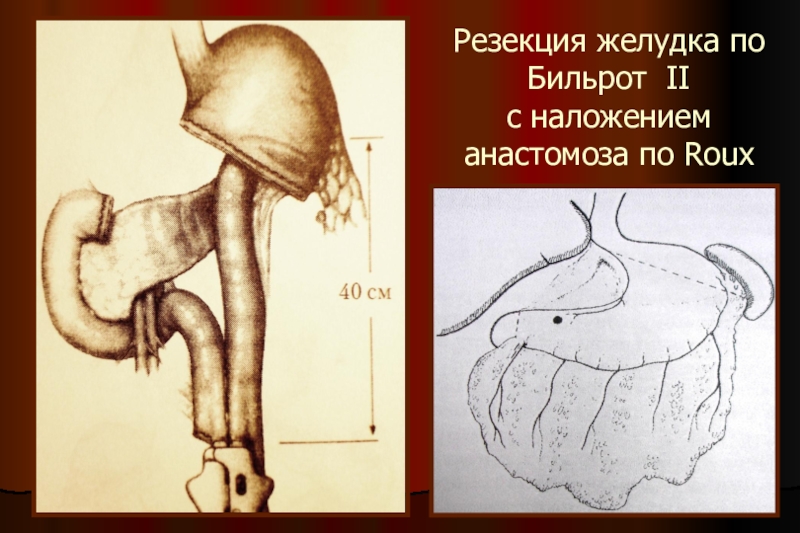
- 25. Резекция желудка по Бильрот II с наложением анастомоза по Roux
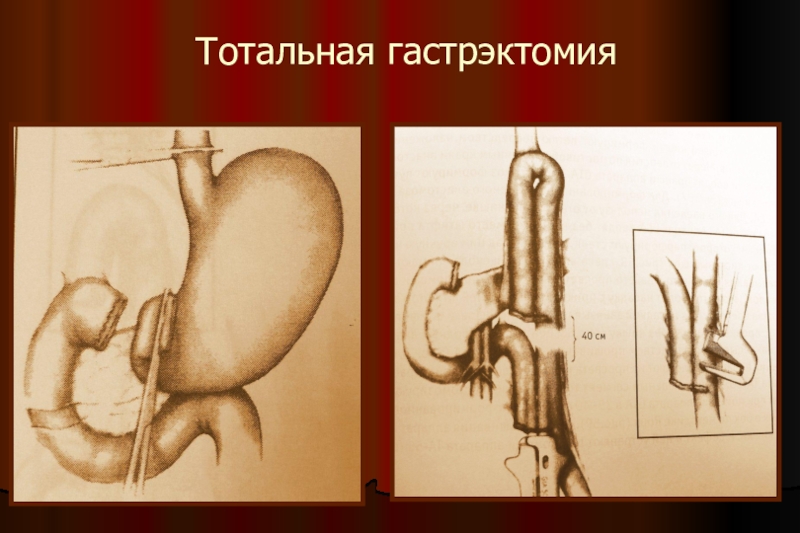
- 26. Тотальная гастрэктомия
- 27. Тип хирургического вмешательства на основании объема лимфодиссекцииD2 - удаление 15 л-узлов; D3 - удаление 25 л-узлов
- 28. Показатели 5-летней выживаемости, по результатамболее 60.000 операций
- 29. Результаты 5-летней выживаемости (в %) в зависимости
- 30. Гастрэктомия лимфодиссекция D2. 1.Культя пищевода2.Чревный ствол,
- 31. Мобилизация преаортальной клетчатки и скелетизация нижней брыжеечной артерииАортаНижняя полая венаНижняя брыжеечная артерия
- 32. Химиотерапия РЖРезультаты лекарственного лечения диссеминированного рака желудка
- 33. Современные режимы химиотерапии РЖОдним из перспективных кандидатов
- 34. Современные режимы химиотерапии РЖДоцетаксел завоевывает все большую
- 35. Результаты сравнения комбинаций с включением доцетаксела с комбинацией ECF (Швейцария, 2004)
- 36. Внутрибрюшная химиотерапияПоказана эффективность адъювантной внутрибрюшной химиотерапии при
- 37. Схема проведения ГИИХ
- 38. Выживаемость больных РЖ5-летняя выживаемость больных при РЖ
- 39. Скачать презентанцию
Асқазан обыры — асқазанның шырышты қабатындағы эпителиальды жасушалардан дамитын, қатерлі ісік. Обыр асқазанның әртүрлі аймақтарынан дамуы мүмкін.
Слайды и текст этой презентации
Слайд 2Асқазан обыры — асқазанның шырышты қабатындағы эпителиальды жасушалардан дамитын, қатерлі
ісік. Обыр асқазанның әртүрлі аймақтарынан дамуы мүмкін.
Слайд 3Дұрыс тамактанбау
Темекі шегу
Хеликобактер пилори
Эпштейн Бар
Тұқым қуалаушылық
Радиация
Асқазан рагының пайда болуына
әкелетін септігін тигізетін факторлар:
Слайд 4Асқазан обыры мәселесінің маңыздылығы. *Әлемде жыл сайын асқазан обыры
ауруының 1 млн- нан астам жаңа түрі диагностикаланады *ҚР асқазан
обыры онкологиялық сырқаттанушылық және өлімділік құрылымында екінші орында тұрСлайд 7Асқазан ракалды аурулары:
Атрофиялық гастрит
Ахлоргидрия(4-5)
Гипертрофиялық гастрит
Ішектік метаплазия
Аденамотозды полиптер
Пернициоздық анемия
Созылмалы ойық жара
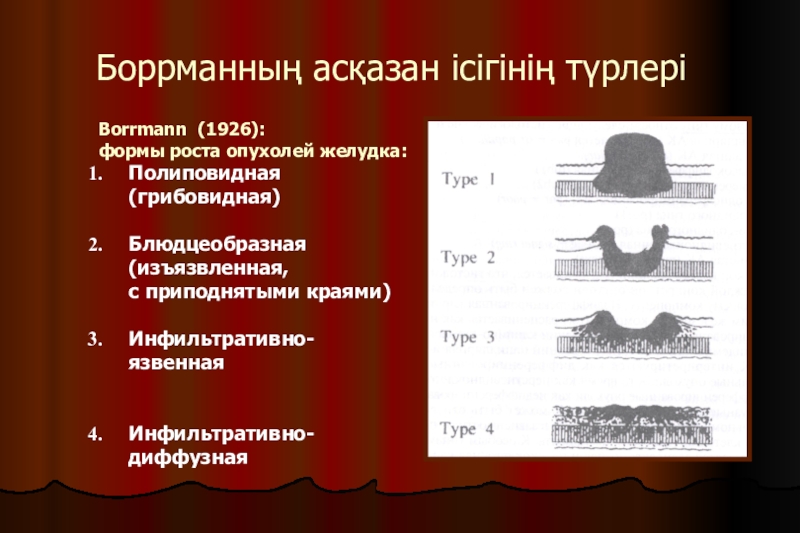
Слайд 10Боррманның асқазан ісігінің түрлері
Borrmann (1926):
формы роста опухолей
желудка:
Полиповидная (грибовидная)
Блюдцеобразная (изъязвленная,
с приподнятыми краями) Инфильтративно-язвенная
Инфильтративно-диффузная
Слайд 16Клиническая картина РЖ
Признаки запущенности болезни:
1) метастаз Вирхова – в
надключиный лимфоузел слева между ножками «кивательной» мышцы
2) метастаз Шницлера –
в парарактельную клетчатку3) метастаз Крукенберга – в яичник у женщин
4) метастаз Айриша – метастаз в подмышечный лимфоузел
5) метастаз сестры Джозеф – в пупок
Признаками неоперабельности являются также
асцит, желтуха, наличие пальпируемой опухоли в
эпигастрии.
Слайд 18Диагностика РЖ
-Эзофагогастродуоденоскопия с биопсией – является ведущим методом диагностики
В развитых
странах, и прежде всего в Японии, широко используется ультразвуковая эндоскопия,
позволяющая визуализировать 5 слоев стенки желудка и довольно точно определять индекс Т. Точность эндоскопического УЗИ приближается к 90%. Метод также применяется для определения прилежащих увеличенных лимфоузлов (чаще при раке пищевода).Слайд 19Диагностика РЖ
-Рентгеноскопия желудка
по данным японских авторов, ранний РЖ рутинным рентгенологическим
методом пропускается почти в 25%.
изучение распространения опухоли в области кардиоэзофагеального
соустья на пищевод и при распространении опухоли на 12– перстную кишку (что влияет на выбор оперативного доступа и планирование объема операции)точно оценивает распространение опухоли по подслизистому слою за счет видимой ригидности стенок органа (пищевода, желудка или 12–перстной кишки).
В случаях подслизистого роста опухоли («linitis plastica») рентгенологический метод может оказаться ведущим в установке диагноза.
-Компьютерная томография (КТ)
основная роль сводится к определению метастазов в печени и определению увеличенных лимфоузлов; достоверных признаков инвазии в прилежащие органы, в частности, в поджелудочную железу, не существует.
Слайд 20Лапароскопия
Лапароскопия применяется тогда, когда есть подозрение на наличие отдаленных метастазов,
не определяемых традиционными методами (УЗИ брюшной полости, клинический осмотр) –
при тотальном поражении желудка
подозрении (небольшое количество жидкости в малом тазу или боковых отделах живота) на асцит
при увеличенных яичниках у женщин (подозрение на метастазы Крукенберга)
Обязательно:
перитонеальный лаваж (цитологическое исследование обнаруженной в брюшной полости жидкости и смывы с брюшины),
осмотр печени, гепатодуоденальной связки, мезоколон, поперечноободочной кишки, пищеводного отверстия диафрагмы.
Как и при КТ, метод мало информативен при оценке задней стенки желудка
Слайд 21Диагностика РЖ
Ультразвуковая томография органов брюшной полости
Рентгеноскопия грудной клетки
В большинстве клиник
Японии перед операцией определяется сывороточный уровень раковоэмбрионального антигена (РЭА), карбогидратного
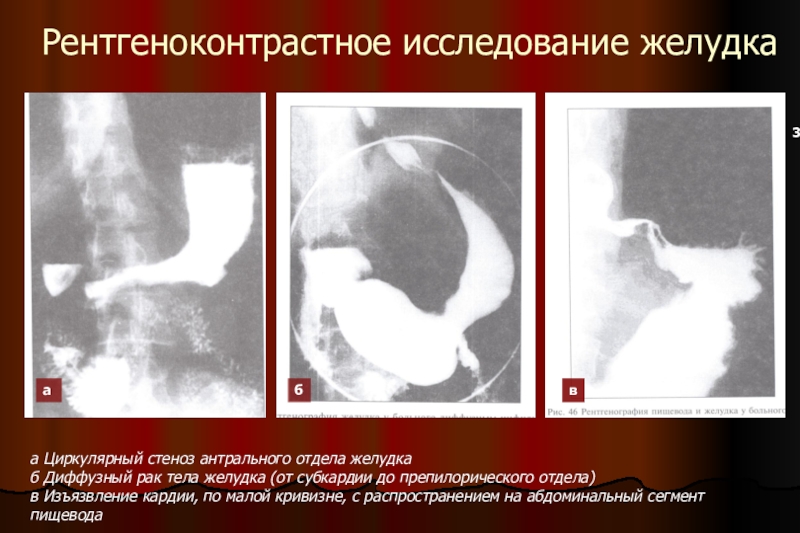
антигена СА19–9, при лапаротомии обязателен перитонеальный лаваж с цитологическим исследованием. По показаниям для обнаружения костных метастазов проводят трепанобиопсию.Слайд 22Рентгеноконтрастное исследование желудка
а Циркулярный стеноз антрального отдела желудка
б Диффузный рак
тела желудка (от субкардии до препилорического отдела)
в Изъязвление кардии, по
малой кривизне, с распространением на абдоминальный сегмент пищеводаа
б
в
3
Слайд 23Лечение РЖ
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
РАДИКАЛЬНАЯ ОПЕРАЦИЯ
-СУБТОТАЛЬНАЯ РЕЗЕКЦИЯ ЖЕЛУДКА
-ГАСТРЭКТОМИЯ
ПАЛЛИАТИВНАЯ ОПЕРАЦИЯ
-СУБТОТАЛЬНАЯ РЕЗЕКЦИЯ ЖЕЛУДКА
-ГАСТРЭКТОМИЯ
СИМПТОМАТИЧЕСКАЯ ОПЕРАЦИЯ
-ФОРМИРОВАНИЕ ОБХОДНОГО АНАСТОМОЗА
-ФОРМИРОВАНИЕ СТОМЫ
-РЕКАНАЛИЗАЦИЯ КАРДИО-ЭЗОФАГЕАЛЬНОЙ ЗОНЫ
ИНТРАОПЕРАЦИОННАЯ ГИПЕРТЕРМИЧЕСКАЯ ИНТРАПЕРИТОНЕАЛЬНАЯ ХИМИОТЕРАПИЯ
СИСТЕМНАЯ ПОЛИХИМИОТЕРАПИЯ
Слайд 27Тип хирургического вмешательства
на основании объема лимфодиссекции
D2 - удаление 15 л-узлов;
D3 - удаление 25 л-узлов
Слайд 28
Показатели 5-летней выживаемости, по результатам
более 60.000 операций (Конгресс JAGC, 1992):
Cтадия
I (T1-2N0) D2(3) – 92,4%. D1 -
74,0%.Cтадия II (T1-3N2-0) D2(3) – 76-75%. D1 – 52-66%.
Cтадия III (T2-4N2-0) D2(3) – 45-47%. D1 – 24,6%.
Расширенные операции улучшают результаты в стадии
II-IIIА, кроме случаев массивного прорастания серозной
оболочки и метастатического поражения
лимфоколлекторов N2.
Результаты радикальных операций
Слайд 29Результаты 5-летней выживаемости (в %) в зависимости от стадии расширенных
операций с D1 и D2-D3
F. Paccelli и соавт. (1993)
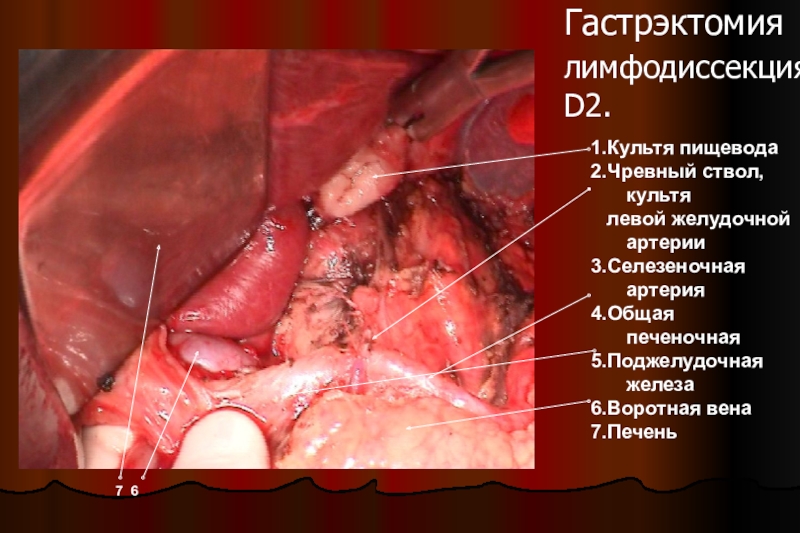
Слайд 30Гастрэктомия лимфодиссекция
D2.
1.Культя пищевода
2.Чревный ствол, культя
левой
желудочной артерии
3.Селезеночная артерия
4.Общая печеночная
5.Поджелудочная железа
6.Воротная вена
7.Печень
7 6
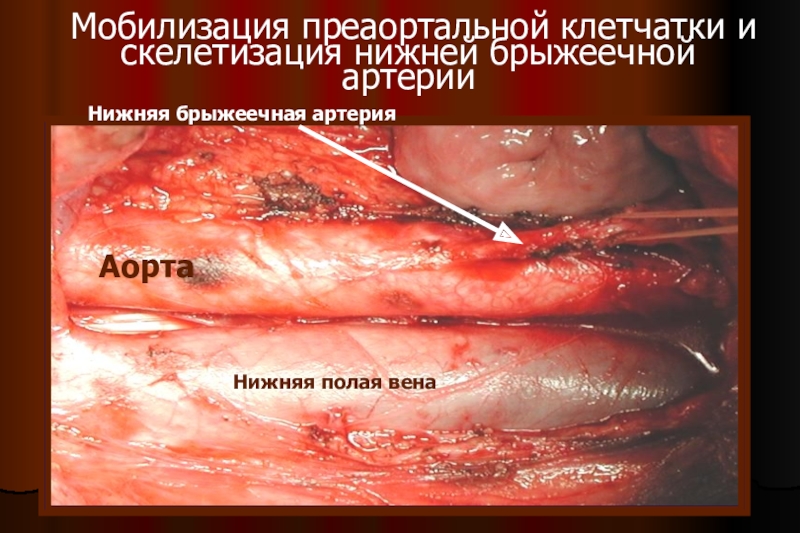
Слайд 31 Мобилизация преаортальной клетчатки и скелетизация нижней брыжеечной артерии
Аорта
Нижняя полая
вена
Нижняя брыжеечная артерия
Слайд 32Химиотерапия РЖ
Результаты лекарственного лечения диссеминированного рака желудка остаются крайне неудовлетворительными
и за последние 10 лет не отмечено улучшение результатов терапии.
Стандартной комбинацией в большинстве странах считается комбинацииPF (цисплатин и 5-фторурацил)
ELF (этопозид, лейковорин и 5-фторурацил)
ECF (эпидоксорубицин, цисплатин и 5-фторурацил)
Не отмечено преимущество какой либо из вышеперчисленных комбинаций. Частота объективного эффекта при их применении составляет 30-40%, а медиана продолжительности жизни 8-9 месяцев.
Слайд 33Современные режимы химиотерапии РЖ
Одним из перспективных кандидатов является доцетаксел, который
в проведенных исследованиях продемонстрировал эффективность при назначении как в монотерапии,
так и в комбинациях с цисплатином, иринотеканом, 5-фторурациломДругим перспективным препаратом для лечения рака желудка является иринотекан. Этот препарат также продемонстрировал способность индуцировать объективный противоопухолевый эффект при использовании в монотерапии. Интересным представляется создание комбинаций с включением иринотекана.
Слайд 34Современные режимы химиотерапии РЖ
Доцетаксел завоевывает все большую популярность при проведении
химиотерапии у больным РЖ.
Предварительные результаты исследования V 325 свидетельствуют о
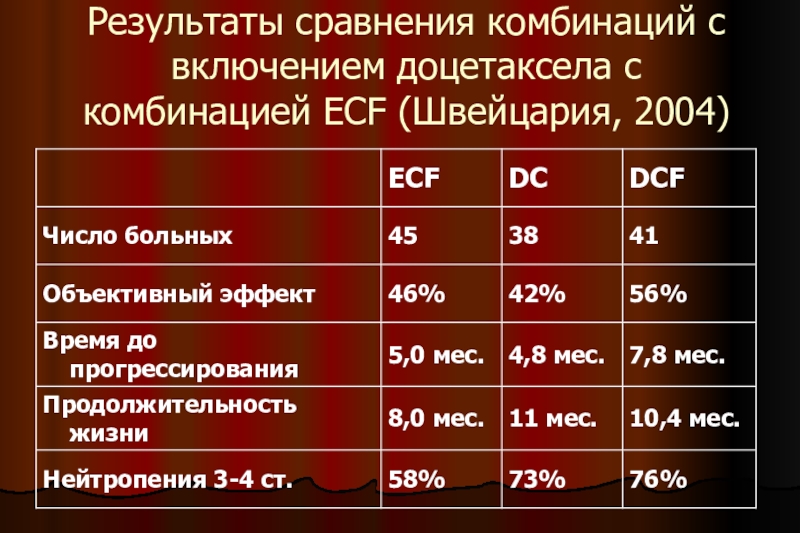
преимуществе комбинации DCF перед комбинацией PF в качестве химиотерапии первой линии у больных раком желудка. Швейцарские коллеги сравнили комбинации с включением доцетаксела с другой стандартной комбинацией – ECF: DC: доцетаксел 75 мг/м² и цисплатин 75 мг/м² каждые 3 недели;
DCF: доцетаксел 75 мг/м² 1 день, цисплатин 75 мг/м² 1 день и инфузия 5-ФУ в суточной дозе 300 мг/м² 1-14 дни каждые 3 недели;
ECF: эпирубицин 50 мг/м² и цисплатин 60 мг/м² каждые 3 недели, инфузия 5-ФУ в суточной дозе 200 мг/м² постоянно.
Слайд 35Результаты сравнения комбинаций с включением доцетаксела с комбинацией ECF (Швейцария,
2004)
Слайд 36Внутрибрюшная химиотерапия
Показана эффективность адъювантной внутрибрюшной химиотерапии при прорастании опухоли серозного
покрова.
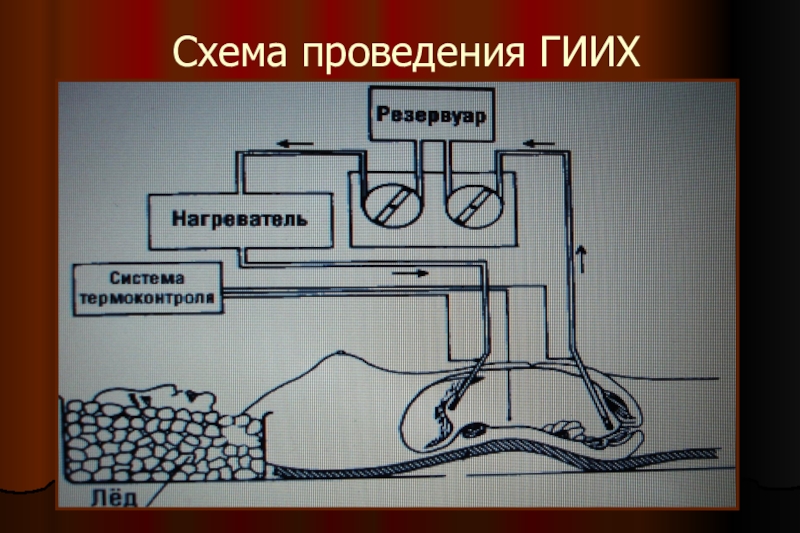
Как модификация указанного метода применяется внутрибрюшная гипертермическая химиотерапия. Эффективность метода
показана как при наличии метастазов на брюшине, так и с точки зрения профилактики последних. Слайд 38Выживаемость больных РЖ
5-летняя выживаемость больных при РЖ в Европе составляет
20% у мужчин и 25,4% - у женщин, в странах
западной Европы - 24%, в восточной Европе – 16%, в США – 33%, в Японии, стране, где внедрен масс-скрининг, – 52%. Увеличение выживаемости на 8% по сравнению с 1990 г. европейскими эпидемиологами объясняется не улучшением адъювантной химиотерапии и совершенствованием хирургической техники, а снижением послеоперационной летальности. Локорегиональные рецидивы наблюдаются после радикальной операции у 41% больных.Больные диссеминированным РЖ живут 5-6 мес. на поддерживающей терапии, при лечении с использованием режимов на основе Txt, FU, IRI – 8-9 мес