Слайд 1Биохимические аспекты биотрансформации лекарственных веществ
Слайд 2План лекции:
Этапы биотрансформации лекарственных веществ;
Реакции 1 фазы химической модификации лекарственных
веществ;
Характеристика микросомальной системы окисления. Функционирование цитохрома Р450
Вторая фаза биотрансформации лекарственных
веществ;
Изменение свойств лекарств при биотрансформации;
Факторы, влияющие на превращение лекарств в организме.
Слайд 3Этапы биотрансформации лекарств в организме:
Всасывание;
Связывание с белками и транспорт кровью;
Взаимодействие
с рецепторами;
Распределение в тканях;
Метаболизм;
Выведение из организма.
Слайд 4Всасывание лекарственных веществ
Этап зависит от физико-химических свойств лекарства
Гидрофобные (липофильные) соединения
(простая диффузия)
Гидрофильные (липофобные) соединения (трансмембранный перенос с участием ферментов –
транслоказ)
Крупные нерастворимые частицы (пиноцитоз)
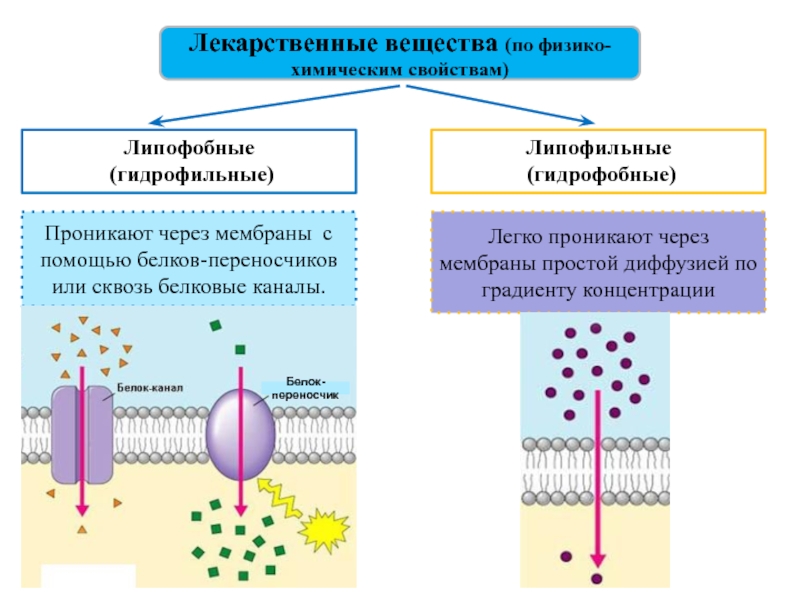
Слайд 5Лекарственные вещества (по физико-химическим свойствам)
Легко проникают через мембраны простой диффузией
по градиенту концентрации
Проникают через мембраны с помощью белков-переносчиков или сквозь
белковые каналы.
АТФ
Слайд 6Транспорт лекарств по крови
Альбумин
Кислый α1-гликопротеин
В составе липопротеинов
Гидрофобные
молекулы
Гидрофильные
молекулы
Транспортируются
самостоятельно
Слайд 7Характеристика фаз биотрансформации лекарственных веществ
I фаза – фаза модификации
II фаза – фаза конъюгации
I фаза – фаза модификации
Процесс химической модификации исходной структуры лекарственного вещества, в результате которой в молекуле:
А) образуются функциональные группы;
Б) освобождаются свои функциональные группы, заблокированные в начальном состоянии.
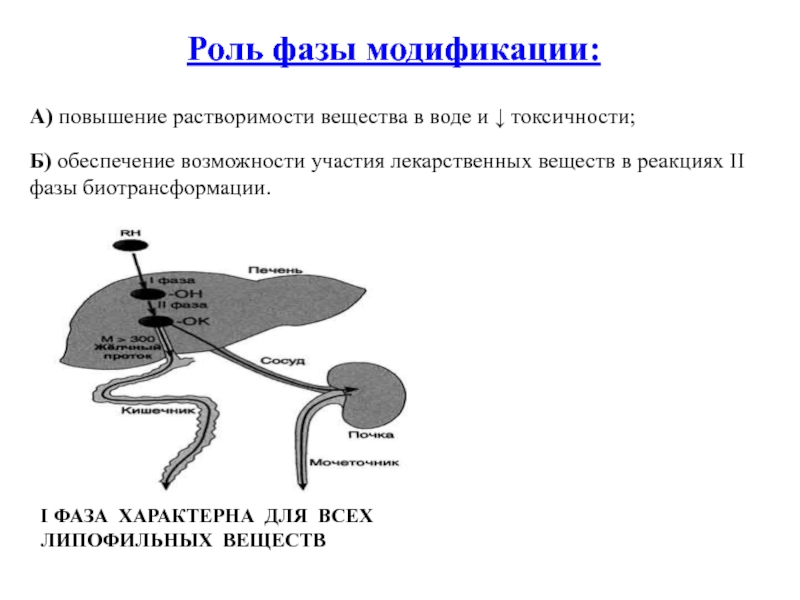
Слайд 8Роль фазы модификации:
А) повышение растворимости вещества в воде
и ↓ токсичности;
Б) обеспечение возможности участия лекарственных веществ в реакциях
II фазы биотрансформации.
I ФАЗА ХАРАКТЕРНА ДЛЯ ВСЕХ ЛИПОФИЛЬНЫХ ВЕЩЕСТВ
Слайд 9Система микросомального окисления
Микросомальная система – это комплекс мембранных белков
эндоплазматического ретикулума, образующих электронтранспортные цепи:
А). НАДФН-зависимая цепь микросомального окисления.
Б). НАДН-зависимая
цепь микросомального окисления.
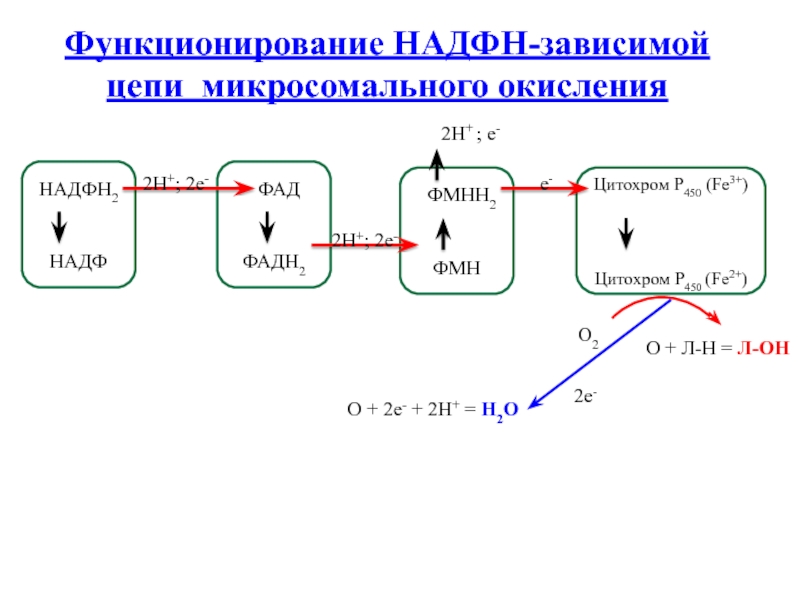
Слайд 10Функционирование НАДФН-зависимой цепи микросомального окисления
НАДФН2
НАДФ
ФАД
ФАДН2
2Н+; 2е-
ФМНН2
ФМН
2Н+; 2е-
Цитохром Р450 (Fe3+)
Цитохром Р450 (Fe2+)
е-
2Н+ ; е-
О2
2е-
О + 2е- +
2Н+ = Н2О
О + Л-Н = Л-ОН
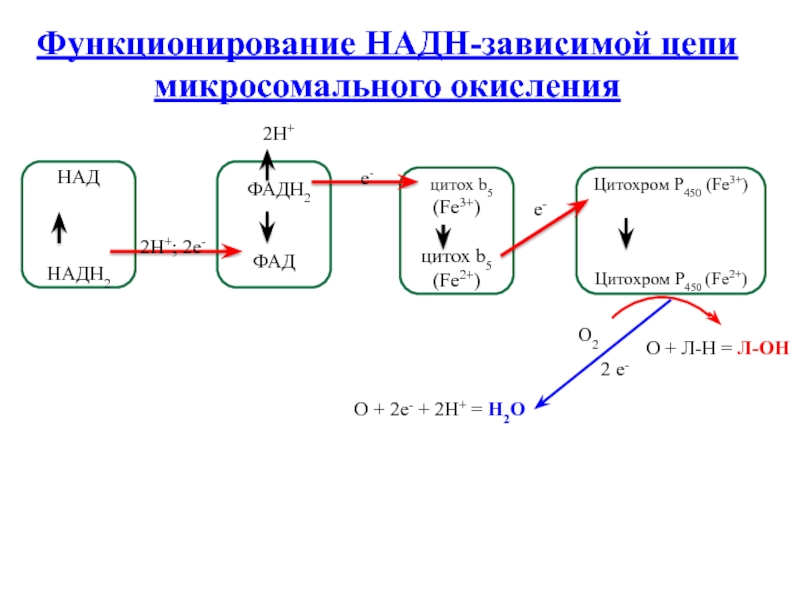
Слайд 11Функционирование НАДН-зависимой цепи микросомального окисления
НАД
НАДН2
ФАДН2
ФАД
2Н+; 2е-
цитох b5
(Fe3+)
цитох b5 (Fe2+)
е-
Цитохром Р450 (Fe3+)
Цитохром Р450 (Fe2+)
е-
2Н+
О2
2 е-
О
+ 2е- + 2Н+ = Н2О
О + Л-Н = Л-ОН
Слайд 12В результате микросомального окисления:
1). Один атом кислорода восстанавливается до
воды;
2). Второй атом кислорода внедряется в молекулу лекарственного вещества.
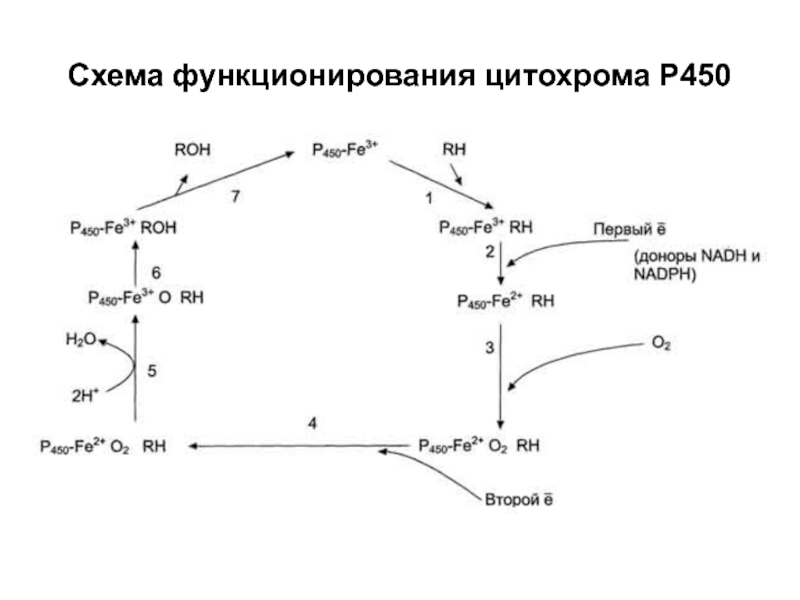
Слайд 131). Л-Н + окисленная форма цитохрома Р450 (Fe3+) = комплекс
Л-Н-цитохром Р450 (Fe3+)
2). Л-Н-цитохром Р450 (Fe3+) + е-, доставленный ФМНН2
= Л-Н-цитохром Р450 (Fe2+)
3). Л-Н-цитохром Р450 (Fe2+) + О2 = тройной комплекс
4). К тройному комплексу присоединяется второй электрон, доставленный цитохромом b5
5). Внутримолекулярные превращения тройного комплекса. Завершается его распадом с освобождением воды и гидроксилированного лекарственного вещества.
Стадии функционирования цитохрома Р450
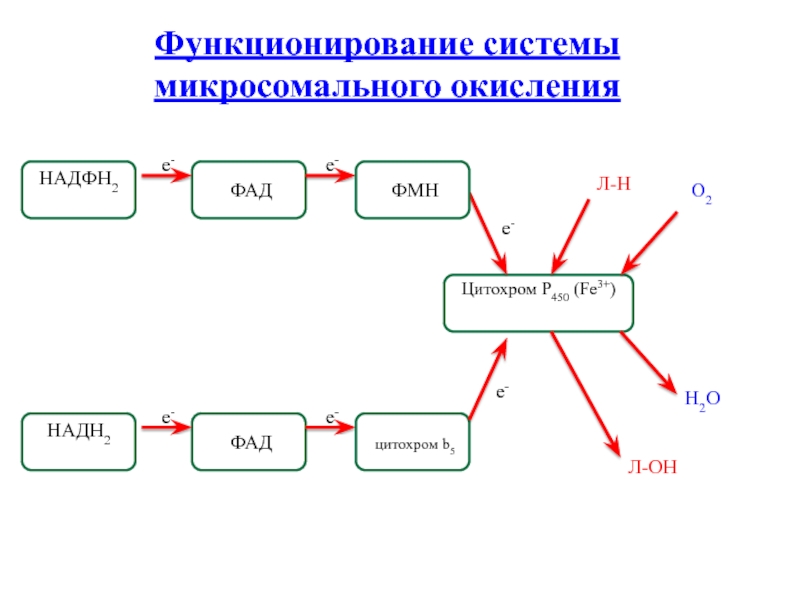
Слайд 14Функционирование системы микросомального окисления
НАДФН2
ФАД
е-
Цитохром Р450 (Fe3+)
е-
е-
ФМН
НАДН2
ФАД
е-
е-
цитохром b5
е-
Л-Н
О2
Л-ОН
Н2О
Слайд 15Схема функционирования цитохрома Р450
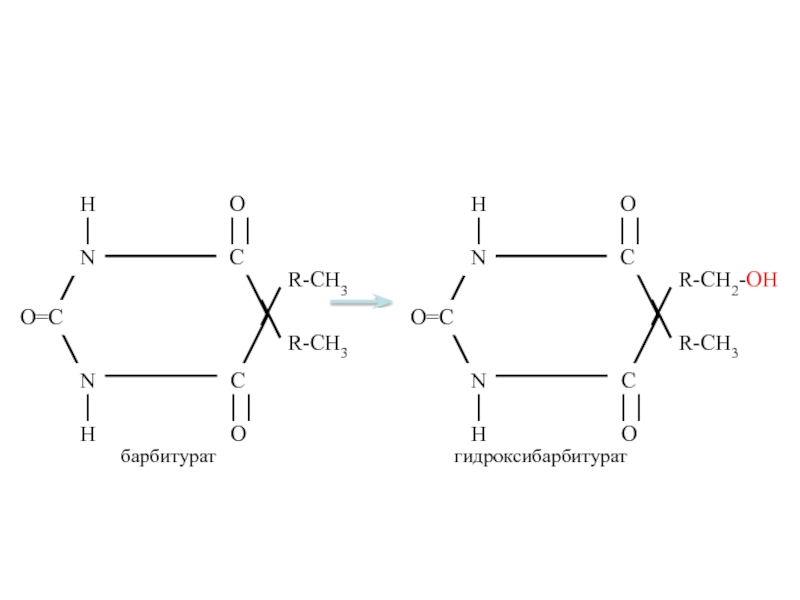
Слайд 16барбитурат
гидроксибарбитурат
R-CH3
R-CH3
O=C
H
│
N
N
│
H
O
││
C
C
││
O
R-CH2-OH
R-CH3
O=C
H
│
N
N
│
H
O
││
C
C
││
O
Слайд 17Свойства системы микросомального окисления:
1). Широкая субстратная специфичность
Описано ≈
150 вариантов гена цитохрома Р450 , кодирующих различные изоформы фермента.
Каждая из изоформ имеет много гидрофобных субстратов (эндогенные и экзогенные).
2). Регулируемая активность
Слайд 18 Активность микросомальных монооксигеназ не является строго постоянной и
зависит от режима питания, возраста, пола, функционального состояния организма,
но наиболее выраженное действие на функционирование систем, участвующих в модификации лекарств оказывают химические вещества, подразделяющиеся на 2 группы: индукторы и ингибиторы микросомальных монооксигеназ.
Слайд 19Индукторы (вещества, вызывающие активацию микросомальных ферментов) подразделяются на:
индукторы широкого
спектра действия (барбитураты, хлорированные углеводороды)
и индукторы узкого спектра действия
(полициклические ароматические углеводороды).
В основе действия индукторов лежит активация регуляторных элементов ДНК (энхансеров) и последующее увеличение количества белка.
Слайд 20Выделяют 4 группы ингибиторов микросомальных монооксигеназ:
Обратимые ингибиторы прямого действия (фенолы,
хиноны, оксигенированные стероиды);
Обратимые ингибиторы непрямого действия (производные бензола, ароматические амины).
Промежуточные продукты их метаболизма образуют комплексы с цитохромом Р450.
Необратимые ингибиторы (производные олефинов, полигалогенизированные алканы), вызывающие разрушение цитохрома Р450.
Ингибиторы, ускоряющие распад или тормозящие синтез цитохрома Р450.
Слайд 21Характеристика II фазы биотрансформации лекарственных веществ
Фаза конъюгации - присоединение к
функциональным группам, образующимся на первом этапе, других молекул, которые увеличивают
гидрофильность и уменьшают токсичность лекарств.
Слайд 22Ферменты, функционирующие во второй фазе, относятся к классы трансфераз.
глюкуронилтрансферазы,
сульфотрансферазы,
метилтрансферазы,
ацетилтрансферазы,
глутатионтрансферазы,
глицилтрансфераза.
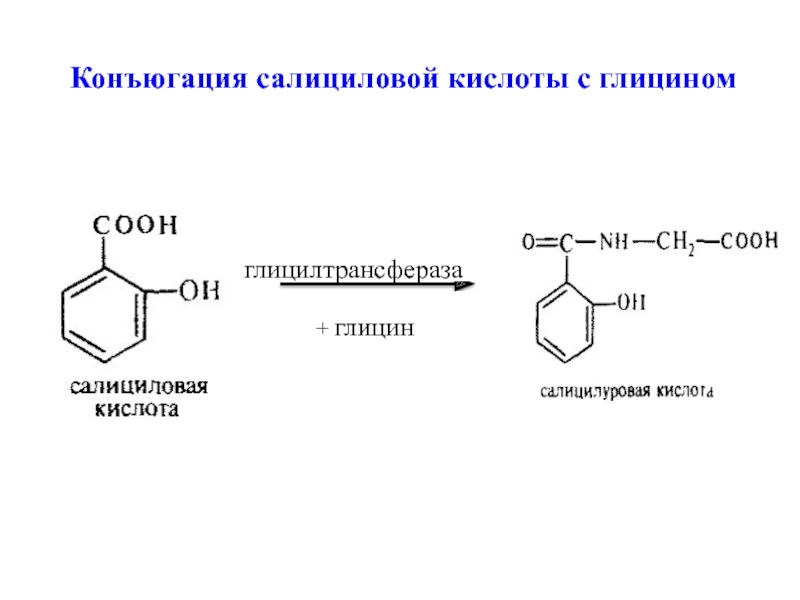
Слайд 23+ глицин
глицилтрансфераза
Конъюгация салициловой кислоты с глицином
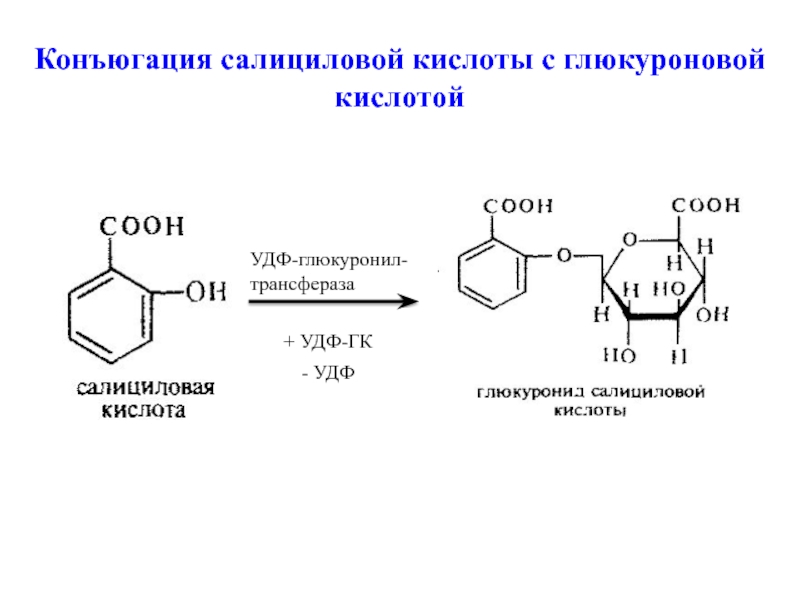
Слайд 24Конъюгация салициловой кислоты с глюкуроновой кислотой
+ УДФ-ГК
- УДФ
УДФ-глюкуронил-трансфераза
Слайд 25Изменение свойств лекарств при биотрансформации
1. Инактивация лекарственного вещества
2. Повышение активности
лекарственного вещества
3. Модификация основного эффекта
4. Образование токсичных продуктов
Слайд 26
Инактивация лекарственного вещества (инактивация фенобарбитала, которая заключается в приобретении им
гидрофильности, последующем связывании с глюкуроновой кислотой с образованием неактивного метаболита
- глюкуронида оксифенобарбитала);
повышение активности лекарства
(при деметелировании имипрамина - неактивного предшественника - происходит образование активного метаболита - дезметилимипрамина, обладающего антидпрессантным действием);
Слайд 27модификация основного эффекта (деметилирование кодеина с противокашлевым действием вызывает формирование
морфина, оказывающего анальгезирующий эффект);
образование токсичных продуктов
(отщепление уксусной кислоты от
фенацетина приводит к образованию парафенитидина, вызывающего формирование метгемоглобина и, соответственно, развитие гипоксии;
превращение парацетамола в бензохинонимин, может приводить к поражению клеток печени в результате связывания тиоловых остатков белков, интенсификации перекисного окисления липидов).
Слайд 28Выведение (элиминация)
Гидрофобные лекарственные вещества могут задерживаться в тканях, связываясь с
белками и липидами мембран, но приобретая гидрофильные свойства, они легче
выводятся из организма.
Гидрофильные вещества элиминируются в составе различных секретов.
Слайд 29Факторы, влияющие на биотрансформацию лекарственного вещества
Генетические факторы
Возраст
Заболевания печени
Прием лекарственных препаратов
Пол
Режим
питания
Внешние факторы
Слайд 30Генетические факторы
Индивидуальные различия в превращении
лекарств связывают с полиморфизмом генов ферментов биотрансформации.
Кроме того, отмечаются наследственные нарушения синтеза ферментов биотрансформации лекарственнных веществ
Пролонгирование действия миорелаксанта дитилина при дефекте синтеза фермента псевдохолинэстеразы, разрушающего ацетилхолин;
Развитие гипербилирубинемии при применении сульфаниламидных препаратов у пациентов с дефектом УДФ-глюкуронилтрансферазы).
Слайд 31Возраст
У новорожденных отмечается низкая, по сравнению со взрослыми, активность многих
ферментов биотрансформации лекарств (цитохрома Р450, УДФ-глюкуронилтранферазы).
В детском возрасте повышена проницаемость
гематоэнцефалического барьера, что проявляется большей чувствительностью к средствам, влияющим на центральную нервную систему.
В пожилом возрасте происходит снижение функциональной активности печени, что приводит к замедлению элиминации лекарственных веществ.
Слайд 32Заболевания печени
При патологии печени происходит снижение активности микросомальных ферментов, приводящее
к замедлению инактивации лекарств,
увеличению продолжительности их действия
и частоты
развития нежелательных эффектов.
Слайд 33Прием лекарственных препаратов
Прием препаратов, обладающих индуцирующим действием на микросомальные ферменты
(барбитураты), приводит к более быстрой инактивации лекарств, уменьшению выраженности фармакологического
эффекта.
Применение лекарственных средств, вызывающие ингибирование микросомальных ферментов (левомицетин, бутадион), ведет к замедлению инактивации лекарств, увеличению продолжительности их действия и частоты развития нежелательных эффектов
Слайд 34Половые различия биотранформации лекарств
связывают с различным действием половых гормонов на
активность ферментных систем превращений лекарств.
Андрогены, являясь индукторами ферментов микросомальной
системы, обеспечивают более быстрое, по сравнению с женщинами, превращение лекарств в мужском организме.
Отмечено, что эстрогены и прогестины могут угнетать гидроксилирование в микросомах и конъюгацию с глюкуроновой кислотой.
Слайд 35Режим питания
Голодание, недостаток белков в пищевом рационе приводит к снижению
активности микросомальных ферментов, большей вероятности развития нежелательных эффектов лекарства.
Недостаток в
пище витаминов (тиамина, рибофлавина) вызывает замедление гидроксилирования лекарственных веществ.
Слайд 36Внешние факторы
Увеличение продолжительности светового дня снижает активность ферментов микросом в
печени.
В ночное время активность микросомальных ферментов, напротив, увеличивается.
Воздействие стрессовых
факторов ведет к повышению выделения глюкокортикоидов, которые увеличивают активность ферментов биотрансформации лекарственных веществ.