Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биохимия крови
Содержание
- 1. Биохимия крови
- 2. Внутренняя среда организма формируется
- 3. Слайд 3
- 4. Химический состав плазмы
- 5. Функции крови Дыхательная -транспорт кислорода от
- 6. Химический состав кровиБольшую часть этих функций выполняют
- 7. Характеристика белков плазмы кровисодержатся в плазме кровисинтезируются
- 8. Состав белков плазмы кровиВ плазме обнаружено более
- 9. Остаточный азотВсе азотсодержащие вещества плазмы образуют общий
- 10. Состав ОАМочевина - 50% (главный компонент)АК -
- 11. Ds значение ОАУровень ОА зависит от:Интенсивности катаболизмаТравмы
- 12. Азотемия - повышение уровня ОА в крови
- 13. Общие понятия КОСКОС – система гомеостаза рН
- 14. рН – производное метаболизмаЗа сутки организм hs
- 15. Стабильный рН - необходимое условие метаболизма Изменение рН
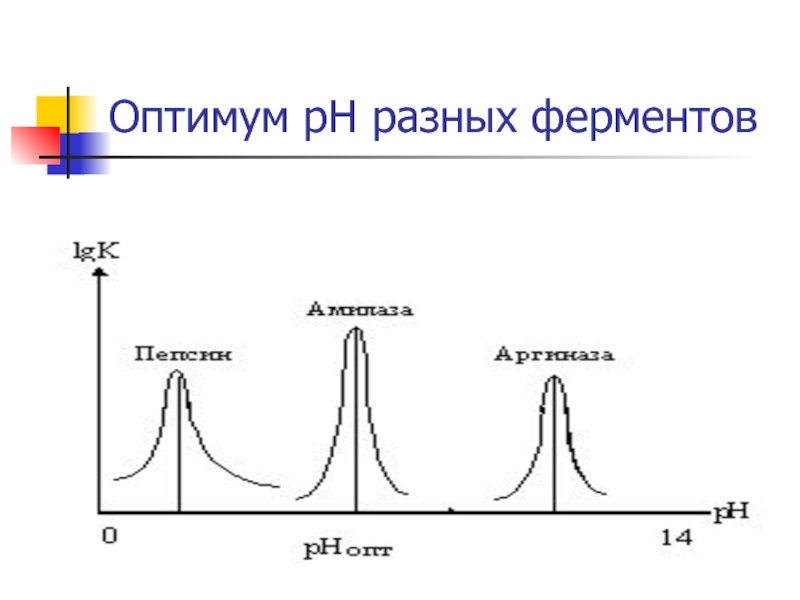
- 16. Оптимум рН разных ферментов
- 17. Изоосмолярность – осм. давление=310 осМ/л - const любые
- 18. Слайд 18
- 19. Механизмы регуляции КОСФизико-хим – действует в автоматическом
- 20. Классификация нарушений КОСрНО =7.40±0.04рН = 7.35 и
- 21. Механизм развития респираторных нарушений КОСацидоз СО2 + Н2О
- 22. Межорганное взаимодействие в регуляции рНЕсли этих респираторных
- 23. Слайд 23
- 24. Слайд 24
- 25. Эритропоэтин (Эпо) Эпо – цитокин, специфический
- 26. Э общий обзорКол-во Э у мужчин -
- 27. Цитоскелет Э
- 28. Структура цитоскелета Э Большинство мембран Э -
- 29. Метаболизм глюкозы в Э Глюкоза в
- 30. Особенности метаболизма Э (шунт Раппопорта)
- 31. Мет Hb редуктазная система ЭHb(Fe2+)Met-Hb(Fe3+)2 G-SHG-S-S-GNAD(P)H +
- 32. Синтез порфобилиногена и гемаПервая реакция б/с гема
- 33. Слайд 33
- 34. Синтез порфобилиногена и гема (прод)Затем следует этап
- 35. Б/с гема
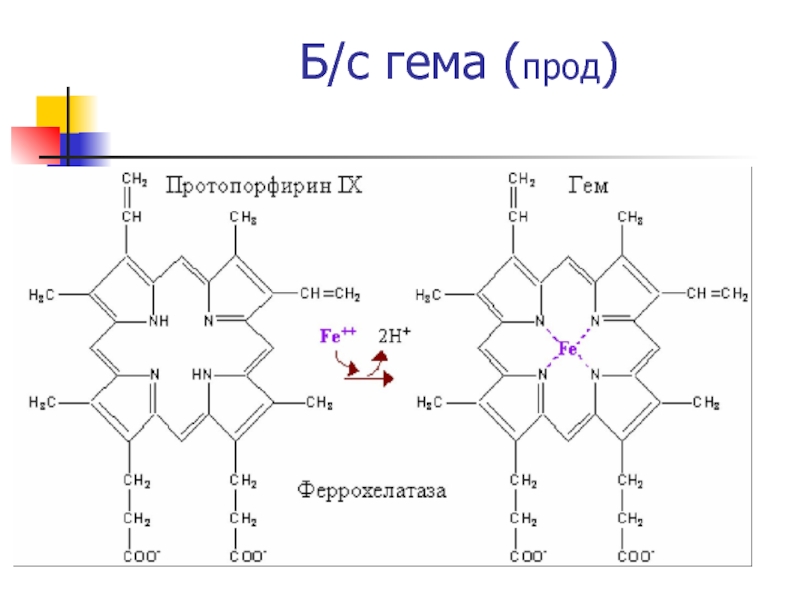
- 36. Б/с гема (прод)
- 37. SH-содержащие ферменты - Феррохелатаза, синтаза дАЛК и
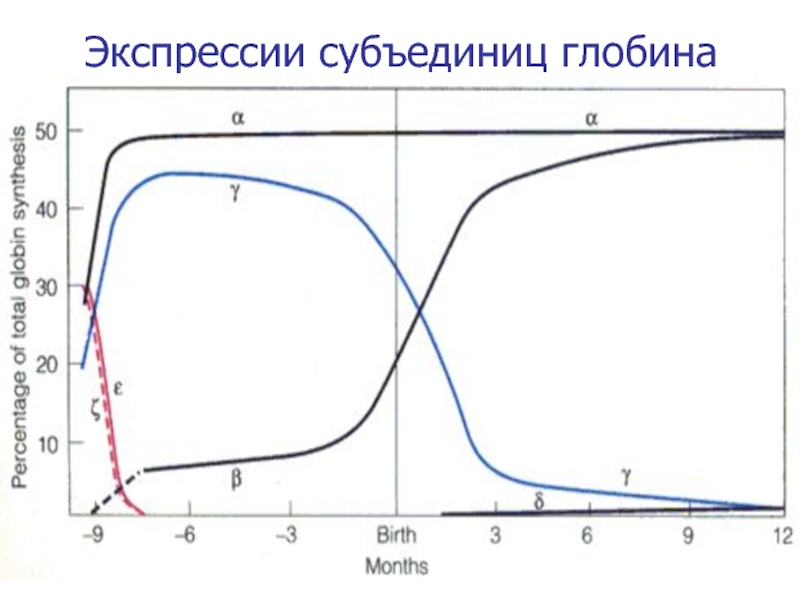
- 38. Экспрессии субъединиц глобина
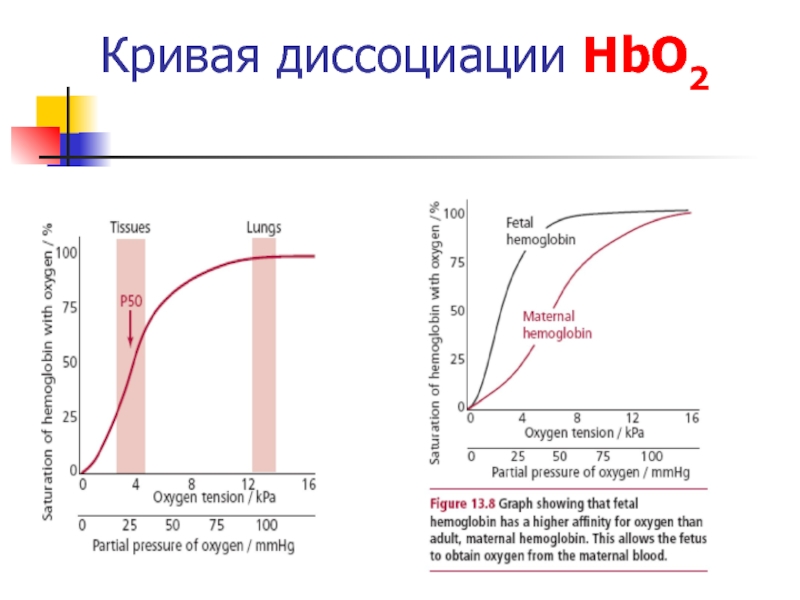
- 39. Кривая диссоциации HbО2
- 40. Распад гемаПродолжительность жизни Э ~120 дней, ежедневный
- 41. Образование билирубинаСледующий этап СН2 мост (между кольцами
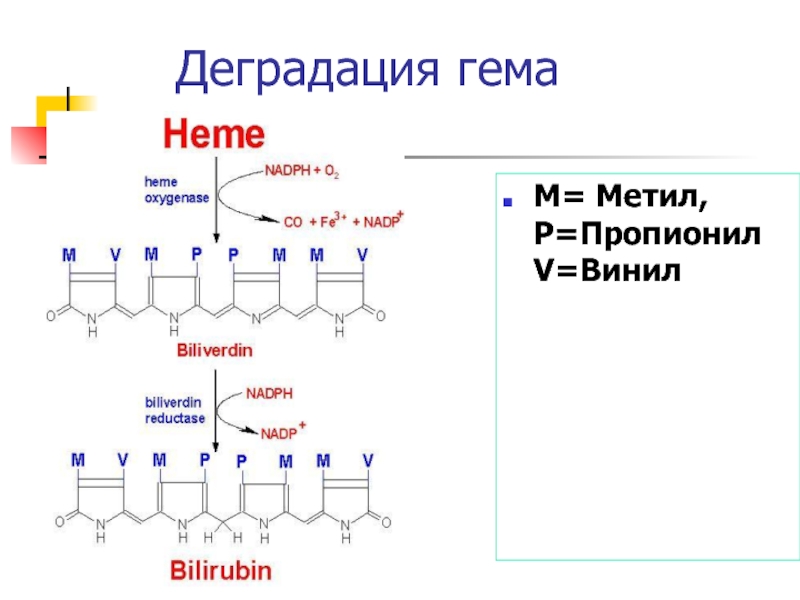
- 42. Деградация гемаM= Метил, P=Пропионил V=Винил
- 43. Билирубин-диглюкуронидВ гепатоцитах УДФ-глюкуронил трансфераза присоединяет 2 остатка
- 44. Клинические аспекты метаболизма гемапредставлены в виде:Дефектов ферментов
- 45. ЖелтухиГипербилирубинемия проявляется в виде желтух – желтой
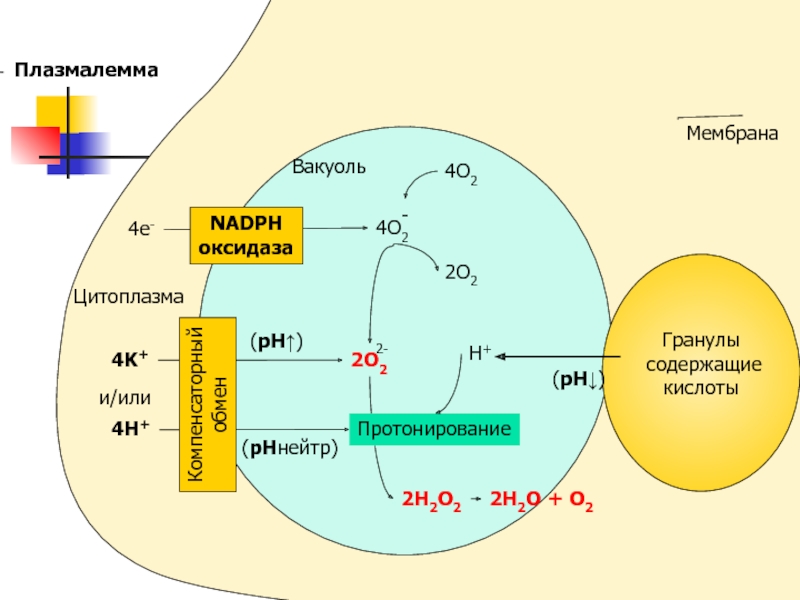
- 46. Нейтрофилы (гранулоциты) –полиморфноядерные лейкоциты: обладают выраженной способностью к
- 47. 4O22O2H+2H2O22H2O + O2(pH↓)Цитоплазма4e-Вакуоль4K+и/или4H+(pHнейтр)(pH↑)NADPH оксидазаКомпенсаторный обменПлазмалеммаМембранаПротонирование
- 48. Структура тромбоцитаТромбоцит имеет Мх (ЦТК, β-окисление ЖК,
- 49. Скачать презентанцию
Внутренняя среда организма формируется совокупностью биологических жидкостей (кровь, лимфа, тканевая жидкость), омывающих клетки и структуры тканей. Эти жидкости функционально тесно взаимосвязаны, они постоянно обмениваются между собой клетками и
Слайды и текст этой презентации
Слайд 5
Функции крови
Дыхательная -транспорт кислорода от легких к тканям и
CO2 от тканей к легким
Выделительная - транспорт конечных
продуктов метаболизма к органам выделения (почкам, легким, коже, потовым железам, кишечнику) для удаления.Защитная (иммунитет, гемостаз и др.)
Транспортная
Трофическая - транспорт субстратов (поступающих с пищей и метаболитов), обеспечивающих основные жизненные потребности клетки
Регуляторная (КОС, водно-электролитный баланс, t°, метаболизма – транспорт БАВ и др.).
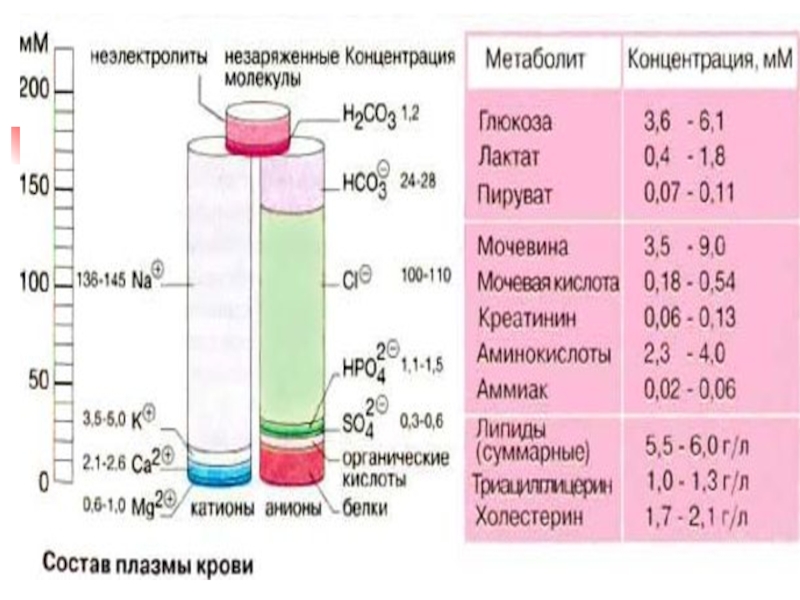
Слайд 6Химический состав крови
Большую часть этих функций выполняют компоненты плазмы крови.
Плазма крови состоит на 90-93% из воды и 10-7%. сухого
остатка – белки, углеводы, липиды,, органич. метаболиты и электролитыСухой остаток на 6,6-8,5% состоит из белков плазмы крови и 1,5-3,5% - органических метаболитов (углеводы, липиды, азотосодержащие продукты) и электролитов (Na+, K+, Ca2+ , Cl-, HCO3- и др.).
Водный и электролитный состав плазмы очень похож на состав др. внеклеточных биологических жидкостей.
Лабораторный мониторинг уровней Na+, K+, Са2+, Cl-, HCO3- и рН крови важны для оценки состояния метаболизма.
Слайд 7Характеристика белков плазмы крови
содержатся в плазме крови
синтезируются в печени или
РЭС (реже в специализированных тканях)
проявляют основную функцию в пределах сосудистой
системысекретируются в кровь, а не попадают в результате повреждения тканей
находятся в плазме в концентрации большей, чем в других биологических жидкостях
проявляют генетический полиморфизм, имеют вариантные формы, не связанные с тканевым происхождением
не являются продуктами катаболизма в плазме, но могут быть продуктами ограниченного протеолиза
имеют большее время биологического полураспада в плазме, чем время транспорта по крови.
Слайд 8Состав белков плазмы крови
В плазме обнаружено более 100 разных белков
соответствующих этим критериям, содержание которых колеблется в широких пределах
Изучение их
функций, содержания, состава при патологии — одна из важных задач клинической биохимии. Уровень ~10 белков составляющих 90 %, и называемых главными достигает высоких значений (альбумин – 40 г/л).
Остальные 10 % минорные, следовые белки.
приходится свыше 100 различных белков, содержание которых может быть в пределах 50 – 200 мкг/л. Это
Слайд 9Остаточный азот
Все азотсодержащие вещества плазмы образуют общий пул азота, состоящий
из:
Азота белкового – осаждаемого кислотами
Азота небелкового (остаточного) (ОА), представленного конечными
продуктами обмена АК, ФЛ, АО, Амины и др. азотсодержащих в-в, которые остаются после осаждения белковСлайд 10Состав ОА
Мочевина - 50% (главный компонент)
АК - 25% (~ 10%
ГЛУ и ГЛН)
Ураты - 8%
Креатинин - 2.5%
NH3 и индикан -
0.5%билирубин, нуклеотиды, биогенные амины, метаболиты АК, АО, холин, олигопептиды и др
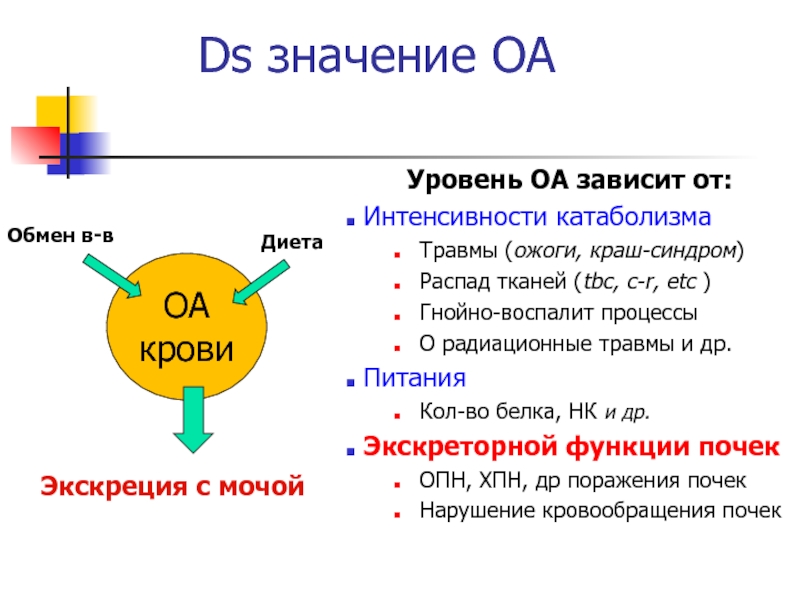
Слайд 11Ds значение ОА
Уровень ОА зависит от:
Интенсивности катаболизма
Травмы (ожоги, краш-синдром)
Распад тканей
(tbc, c-r, etc )
Гнойно-воспалит процессы
О радиационные травмы и др.
Питания
Кол-во белка,
НК и др.Экскреторной функции почек
ОПН, ХПН, др поражения почек
Нарушение кровообращения почек
ОА
крови
Экскреция с мочой
Обмен в-в
Диета
Слайд 12Азотемия - повышение уровня ОА в крови
Ретенционная – задержка
компонентов ОА в организме из-за нарушения экскреторной функции почек
Почечная азот
мочевины составляет 90% ОА крови (норма 50%) (ОПН, ХПН – отравления, травмы, гломерулонефриты, пиелонефриты и др поражения почек) Внепочечная азотемия возникает при снижения почечного кровотока из-за недостаточности кровообращения, снижения АД (шок, коллапс, большая кровопотеря)
Продукционная – увеличение продукции ОА за счет катаболизма
Комбинированная
Слайд 13Общие понятия КОС
КОС – система гомеостаза рН внутри- и внеклеточной
среды организма.
Единицы измерения :рН = -lg [H+],
сдвиг рН:
на 1ед соответствует 10 кратному изменению [H+] на 2ед соответствует 100 кратному изменению [H+]
рН внутри клеток рНi ~ 6.9 – 7.0
рН вне клеток рНО =7.40±0.04 [H+] ~ 40 ±0.5 нМ/л
Кислоты – доноры H+
Основания – акцепторы H+
Щелочи - доноры ОН -
Буфер система состоит из слабой кислоты и ее соли, образованной сильным основанием, стабилизирует рН,
Слайд 14рН – производное метаболизма
За сутки организм hs образует 50-100 мМ
[Н+] на 15-20л ВКЖ.
Весь метаболизм представлен преимущественно обменом кислот
(Г6Ф, ЖК, АК и др.): Распад 100г Б дает ~ 30 мМ Н2SO4 и 100 мМ Н2РО4-
Распад 100 г Л дает ~ 17 мМ Н2РО4-
постоянно образуется ПВК, лактат, ацетат и др.
накопление оснований идет значительно меньше: ОН-, NH3, основных АК, креатинина и др, которые вместе с буферами стабилизируют рН
Слайд 15Стабильный рН - необходимое условие метаболизма
Изменение рН приводит к изменению:
заряда
и функции белков (ферментов, каналов, рецепторов и др.), что обуславливает:
рН зависимость всех б/х реакций и многих физиологических процессов в организме
Наличие мощной гомеостатической системы
стабилизации рН
Слайд 17
Изоосмолярность – осм. давление=310 осМ/л - const
любые изменения должны поддерживать
эту константу
Электронейтральность – (по 155 мМ- катионов и анионов)
Постоянство рН
Принципы
организации КОС
Слайд 19Механизмы регуляции КОС
Физико-хим – действует в автоматическом режиме и представлен:
разбавлением
т.е. выходом Н+ или др. иона из одного компартмента в
др. (из клетки в МКЖ или наоборот)активность буферных систем (см типы, мех-мы действия БС
Физиологические – функция экскреторных органов (выделение или задержка Н+ или др. иона ) – легкие, почки, ЖКТ и др.
Слайд 20Классификация нарушений КОС
рНО =7.40±0.04
рН = 7.35 и ниже – ацидоз
рН
= 7.45 и выше – алкалоз
По этиологии:
Респираторный (дыхательный, газовый)
Метаболический
Выделительный
Смешанный
По степени
компенсации:Компенсированный
Декомпенсированный (выраженное истощение буферных систем и сдвиг значений рН)
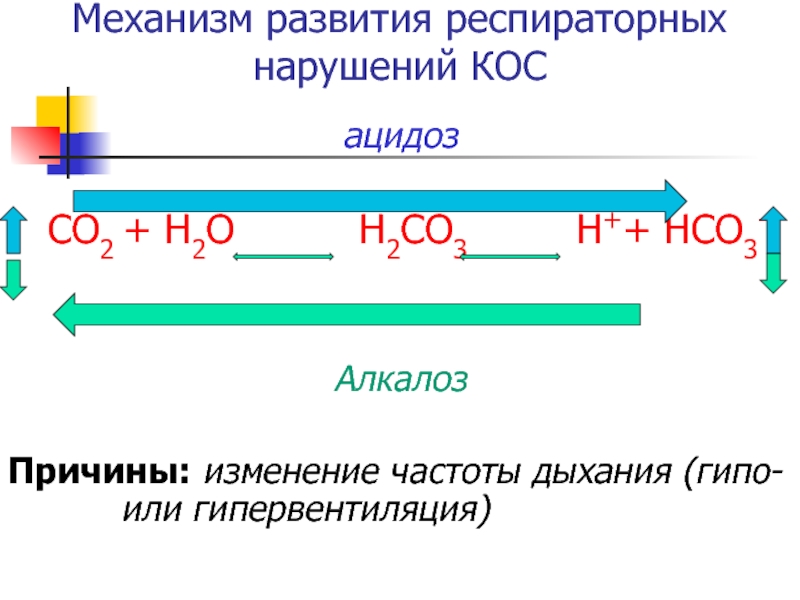
Слайд 21Механизм развития респираторных нарушений КОС
ацидоз
СО2 + Н2О
Н2СО3 Н++ НСО3-
Алкалоз
Причины:
изменение частоты дыхания (гипо- или гипервентиляция)
Слайд 22Межорганное взаимодействие в регуляции рН
Если этих респираторных механизмов недостаточно, то
активируются др.экскреторные системы.
В печени снижение рН ингибирует биосинтез
мочевины.NH3 + HCO3- ---? мочевина
В почках – ацидо- и аммониогенез – подкисление мочи и одновременно «подщелачивание» крови (за счет поступления НСО3- в плазму). Детоксикация NH3 происходит путем аммониогенеза
Слайд 25Эритропоэтин (Эпо)
Эпо – цитокин, специфический регулятор эритропоэза в
костном мозге
Эпо человека – гликопротеид, состоит из 193
АК (ММ -21,28 kDa), синтезируется почками и печенью, скорость его секреции в кровоток возрастает при гипоксии. Эпо взаимодействует в костном мозге с клетками-мишенями при участии рецептора со свойствами тирозинкиназы способствуя их пролиферации и дифференцировке. Тип вторичного посредника и специфичные гены к настоящему времени точно не установлены.
Действие Эпо усиливается другими факторами (ИЛ-3 и ИПФР).
Рекомбинантный Эпо используется в лечении анемий.
Слайд 26Э общий обзор
Кол-во Э у мужчин - 4.6-6.2 млн/мкл крови,
а у женщин - 4.2-5.4 млн/мкл. Общее количество Э в
кровотоке ~2.5 x 1013.Продолжительность жизни Э - 120 суток.
Ежедневно обновлняется ~1 % популяции Э кровеносного русла (200 млрд клеток или 2 млн/сек).
«Старые» Э разрушаются клетками РЭС (селезенка, костный мозг и печень). Образующиеся при распаде гема желчные пигменты выделяются, а Fe и АК глобина используются повторно.
Увеличение кол-ва Э в крови называют полицетемией, снижение – анемией.
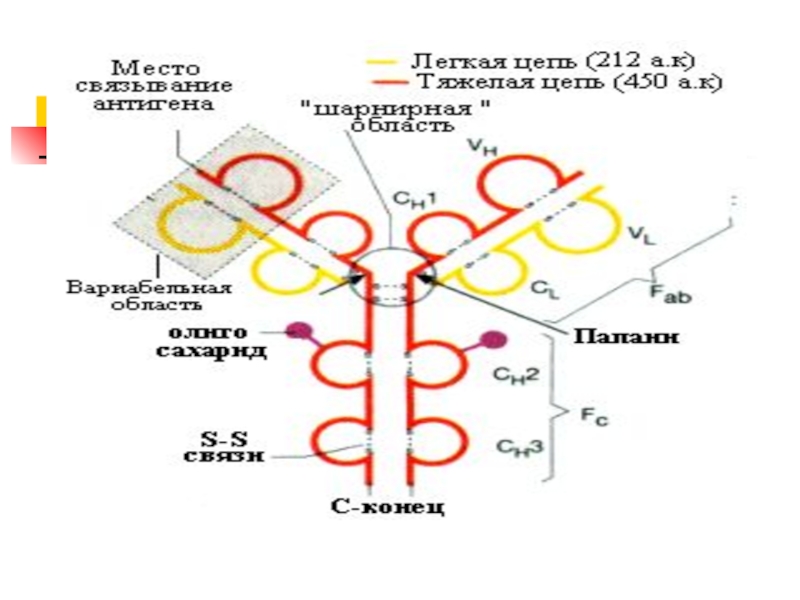
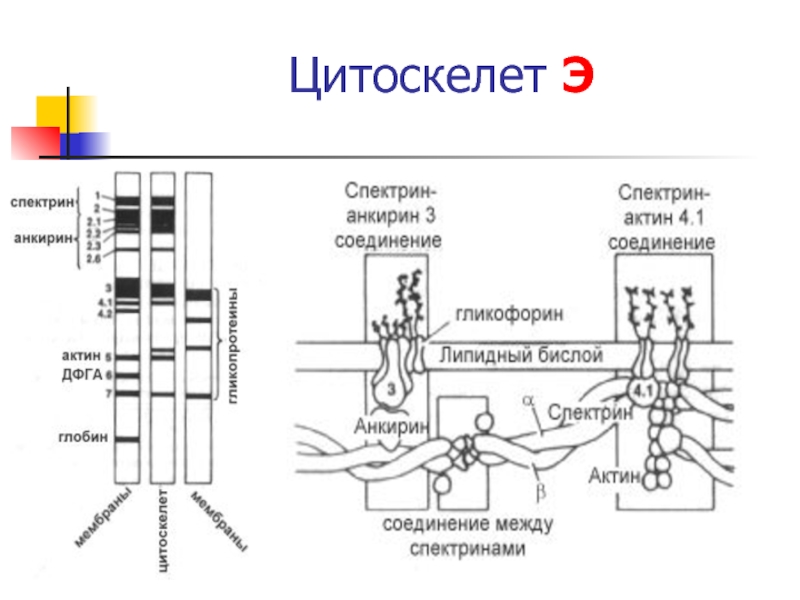
Слайд 28Структура цитоскелета Э
Большинство мембран Э - интегральные Б, гликопротеиды.
Б без углеводной части находятся на внутренней поверхности:
Ферменты -
3ФГА ДГ, структурные белки (спектрин или актин) и Hb.
анкирин 3 обеспечивает, связь спектрина с цитозольном концом белка полосы 3 с бислоем ФЛ
актиновые филаменты взаимодействуют с несколькими молекулами спектрина , формируется единая молекулярная сеть в мембране эритроцита.
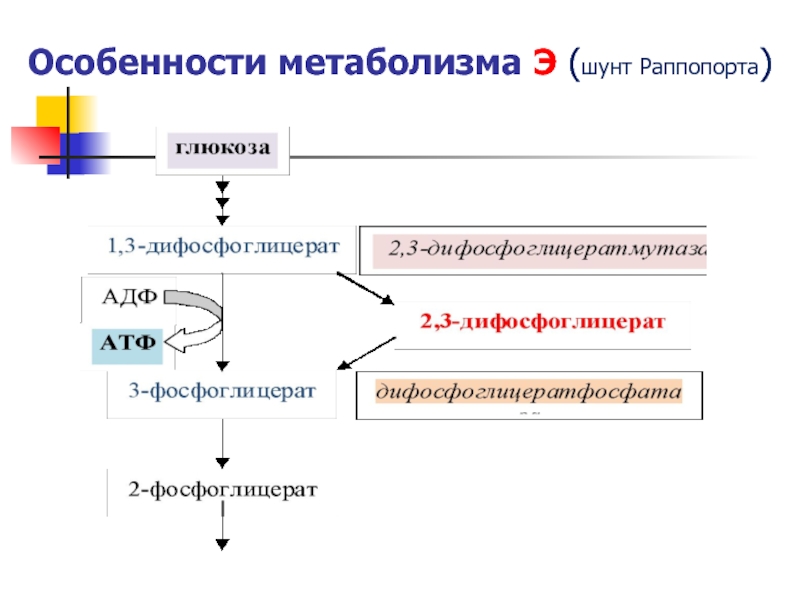
Слайд 29Метаболизм глюкозы в Э
Глюкоза в Э используется в:
Гликолизе
(90-95%) – образование АТФ
ПФП (10-5%) - образование NADPH (АОЗ)
Особенностью обмена
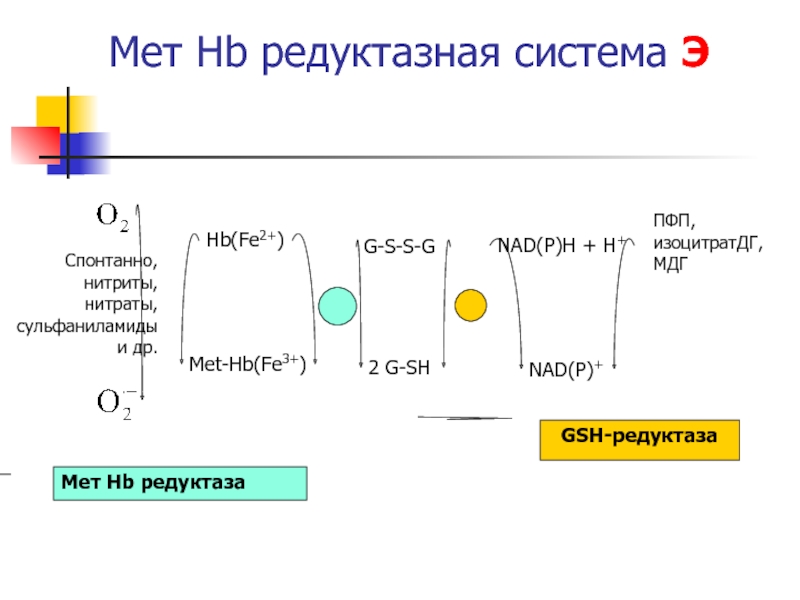
в Э является боковой путь, ответвляющийся на уровне 1.3-ди ФГК (шунт Раппопорта). Слайд 31Мет Hb редуктазная система Э
Hb(Fe2+)
Met-Hb(Fe3+)
2 G-SH
G-S-S-G
NAD(P)H + H+
NAD(P)+
Мет Hb редуктаза
GSH-редуктаза
ПФП,
изоцитратДГ,
МДГ
Спонтанно,
нитриты, нитраты, сульфаниламиды и др.
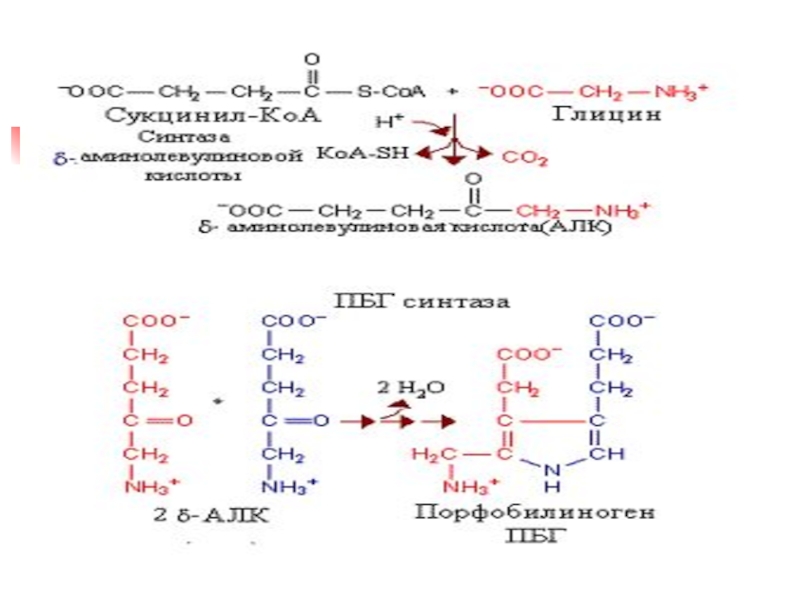
Слайд 32Синтез порфобилиногена и гема
Первая реакция б/с гема происходит в Мх
и происходит путем конденсации гли и сукцинил-КоА при участии пиридоксаль-фосфат
содержащего фермента – синтазы d-аминолевулиновой кислоты (дАЛК).Эта реакция регуляторная и скорость-лимитирующая в синтезе гема
Из Мх дАЛК транспортируется в цитозол, где дАЛК дегидратаза (синтаза порфобилиногена) димеризует 2 молекулы дАЛК с образованием пиррольного кольца порфобилиногена
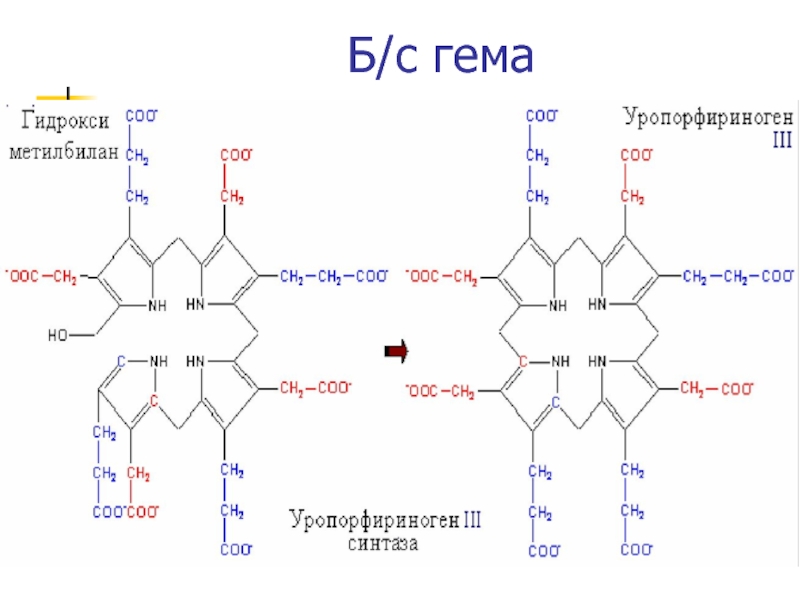
Слайд 34Синтез порфобилиногена и гема (прод)
Затем следует этап конденсации (голова-хвост) 4
молекул порфобилиногена с образованием линейного тетрапиррола – гидроксиметилбилана при участии
фермента порфобилиноген деаминаза (уропорфирин I синтаза)Гидроксиметилбилан превращается в
Уропорфириноген III и далее в гем (фермент уропорфириноген синтаза)
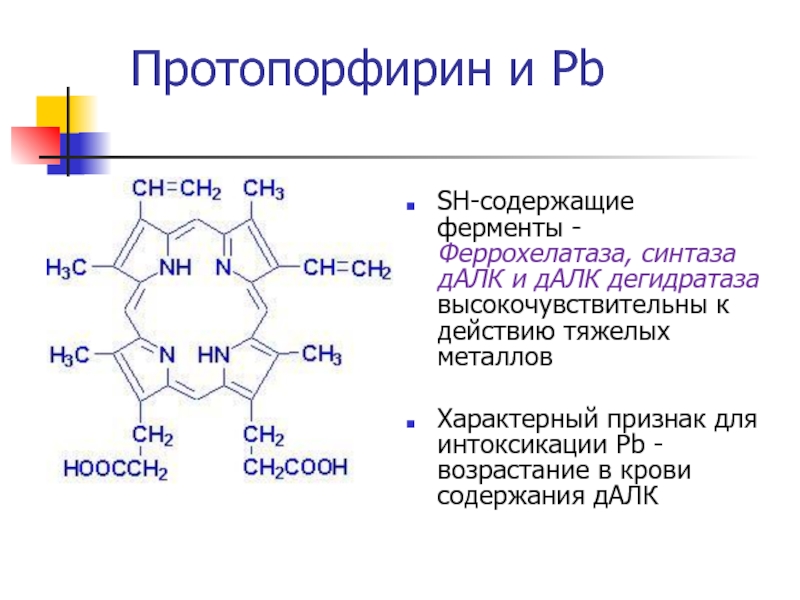
Слайд 37SH-содержащие ферменты - Феррохелатаза, синтаза дАЛК и дАЛК дегидратаза высокочувствительны
к действию тяжелых металлов
Характерный признак для интоксикации Pb - возрастание
в крови содержания дАЛКПротопорфирин и Pb
Слайд 40Распад гема
Продолжительность жизни Э ~120 дней, ежедневный оборот Hb ~6
г/день.
Гем из старых Э и др источников (цитохромы и др.
гем-содержащие ферменты) освобождаются в РЭС. Глобин деградирует обычным путем и АК реутилизируются.
Гем окисляется в ЭПС гем оксигеназой с разрывом цикла и образованием линейного тетрапиррола – биливердина, выделения Fe3+ и СО .
Стадия окисления The oxidation step requires heme as a substrate, and any hemin (Fe3+) is reduced to heme (Fe2+) prior to oxidation by heme oxygenase. The oxidation occurs on a specific carbon producing the linear tetrapyrrole biliverdin, ferric iron (Fe3+), and carbon monoxide (CO).
CO выделяется легкими и его количество является показателем активности гем оксигеназы l.
Слайд 41Образование билирубина
Следующий этап СН2 мост (между кольцами III и IV)
биливердина восстанавливается биливердин редуктазой до билирубина, с соответствующим изменением цвета
Деградация
гема отражается при прогрессирующем «цветении» гематом-синяков темно-синий →красно-желтый → желтый. Билирубин гидрофобен поэтому транспортируется в виде комплекса с альбумином в печень, где подвергается дальнейшей деградации путем коньюгации с глюкуронидами.
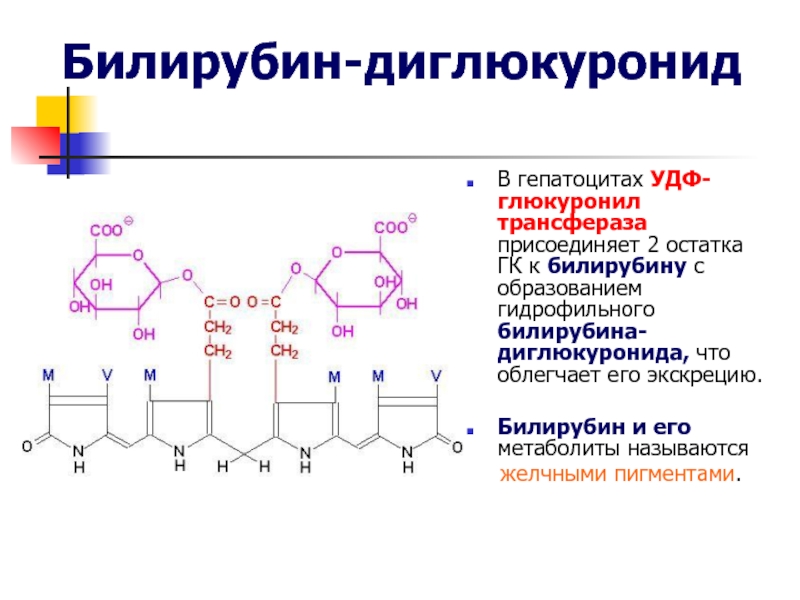
Слайд 43Билирубин-диглюкуронид
В гепатоцитах УДФ-глюкуронил трансфераза присоединяет 2 остатка ГК к билирубину
с образованием гидрофильного билирубина-диглюкуронида, что облегчает его экскрецию.
Билирубин и
его метаболиты называютсяжелчными пигментами.
Слайд 44Клинические аспекты метаболизма гема
представлены в виде:
Дефектов ферментов и нарушения б/с
гема – порфирий, которые сопровождаются увеличением содержания в крови и
моче интермедиатов б/с гема .Врожденные и приобретенные нарушения метаболизма и экскреции билирубина – гипербилирубинемии (желтухи).
Слайд 45Желтухи
Гипербилирубинемия проявляется в виде желтух – желтой пигментации кожи и
слизистых.
В норме в кишечнике билирубин при участии бактерий превращается в
уробилиноген (мезобилиноген), который выделяется с фекалиями. Bilirubin and its catabolic products are collectively known as the bile pigments.
Слайд 46Нейтрофилы (гранулоциты) –полиморфноядерные лейкоциты:
обладают выраженной способностью к фагоцитозу,
Хорошо развитый,
подвижный цитоскелет,
Активное Мх и Мс - окисление
Систему продукции NADPH (ПФП
и др.)Систему генерации АФК
Богаты гранулами (определяющие название), в состав которых входят гидролазы - протеазы: эластаза, коллагеназа или катепсин G и гликозидазы: лизоцим (мураминидаза), лизирующие бактерии
Слайд 47
4O2
2O2
H+
2H2O2
2H2O + O2
(pH↓)
Цитоплазма
4e-
Вакуоль
4K+
и/или
4H+
(pHнейтр)
(pH↑)
NADPH
оксидаза
Компенсаторный
обмен
Плазмалемма
Мембрана
Протонирование
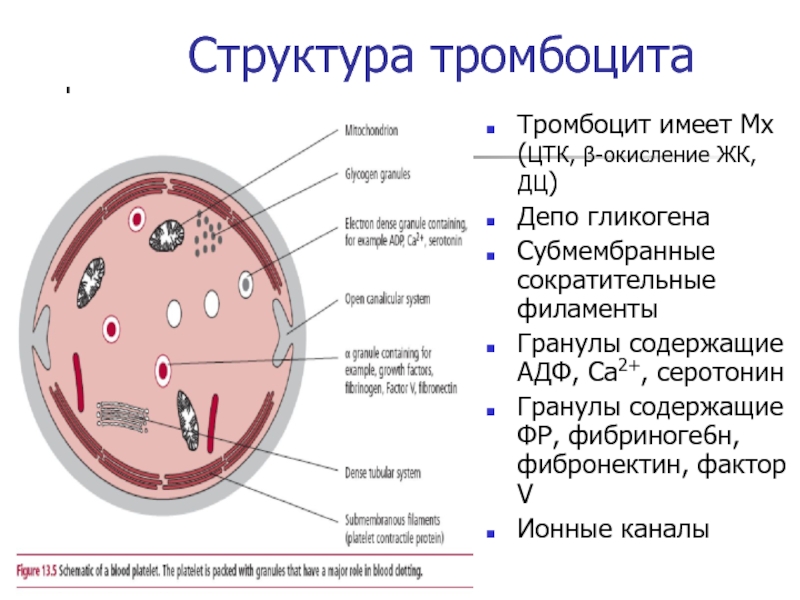
Слайд 48Структура тромбоцита
Тромбоцит имеет Мх (ЦТК, β-окисление ЖК, ДЦ)
Депо гликогена
Субмембранные сократительные
филаменты
Гранулы содержащие АДФ, Са2+, серотонин
Гранулы содержащие ФР, фибриноге6н, фибронектин, фактор
VИонные каналы










![Биохимия крови Общие понятия КОСКОС – система гомеостаза рН внутри- и внеклеточной среды Общие понятия КОСКОС – система гомеостаза рН внутри- и внеклеточной среды организма. Единицы измерения :рН = -lg [H+],](/img/thumbs/1199b20f51983792ea3692c942a791bb-800x.jpg)
![Биохимия крови рН – производное метаболизмаЗа сутки организм hs образует 50-100 мМ [Н+] рН – производное метаболизмаЗа сутки организм hs образует 50-100 мМ [Н+] на 15-20л ВКЖ. Весь метаболизм представлен](/img/thumbs/9854a7cc6d78d425ee52170a62f1e89d-800x.jpg)