Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Будова атомів і молекул
Содержание
- 1. Будова атомів і молекул
- 2. План лекціїКвантові постулати Бора. Випромінювання і поглинання світла атомами. Спектри та їх види. Спектральний аналіз.
- 3. Перший постулат (положення) Бора у стійкому атомі
- 4. Постулати Бора написані для атома воднюПерший постулат
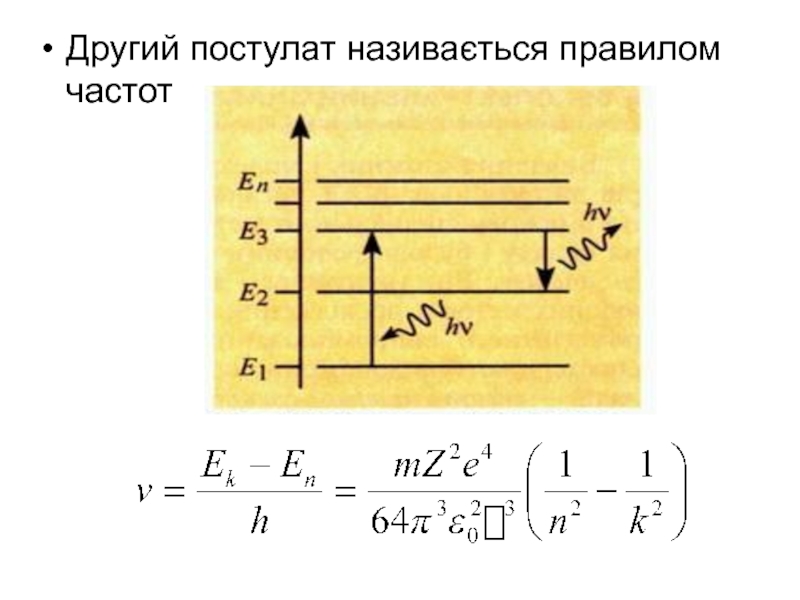
- 5. Другий постулат атом може, переходити із
- 6. Другий постулат називається правилом частот
- 7. Третій постулату стаціонарному стані атома електрон, рухаючись
- 8. Третій постулат називається правилом квантування орбіт. Виявилося,
- 9. Спектральні серії
- 10. Слайд 10
- 11. Недоліки теорії Бора: 1.
- 12. Слайд 12
- 13. Спектральним аналізом називається метод вивчення хімічного складу речовини, заснований на дослідженні його спектрів.
- 14. Найбільш прості спектральні прилади — призма та
- 15. У 1860 році німецькі вчені Г. Кірхгоф
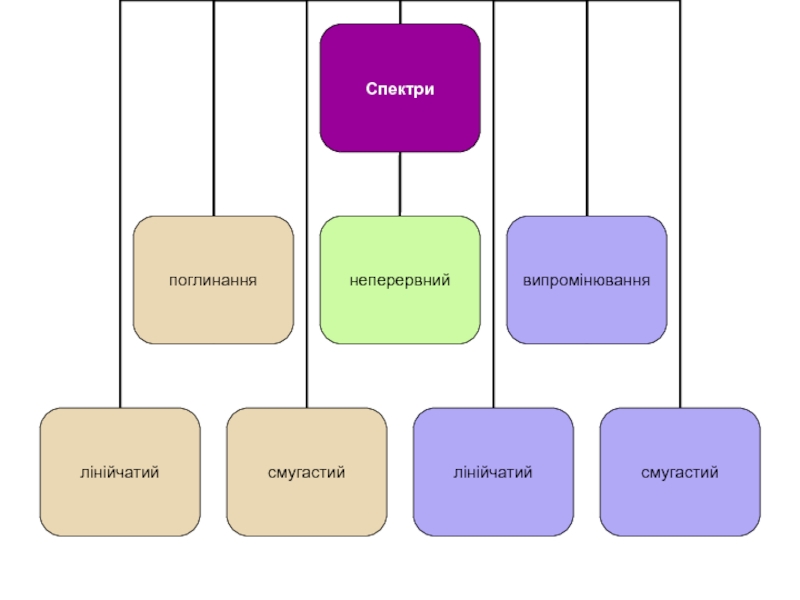
- 16. Спектр — послідовність монохроматичних випромінювань,
- 17. Лінійчатий спектр випромінювання - воденьЛінійчаті спектри дають
- 18. Смугастий спектрсмугасті спектри створюються не атомами, а
- 19. Слайд 19
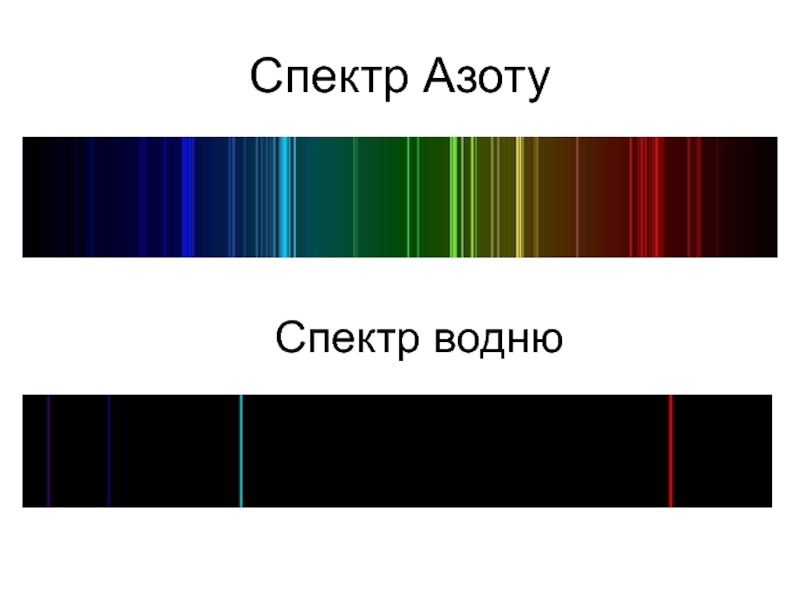
- 20. Спектр АзотуСпектр водню
- 21. Спектр Гелію
- 22. Спектр Неону
- 23. Слайд 23
- 24. Слайд 24
- 25. Слайд 25
- 26. Слайд 26
- 27. Слайд 27
- 28. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2План лекції
Квантові постулати Бора.
Випромінювання і поглинання світла атомами.
Спектри
та їх види. Спектральний аналіз.
Слайд 3Перший постулат (положення) Бора
у стійкому атомі електрон може рухатися
лише по особливих, стаціонарних орбітах, не випромінюючи при цьому електромагнітної
енергії;Слайд 4Постулати Бора написані для атома водню
Перший постулат називається постулатом стаціонарних
станів. Цей постулат суперечить класичній механіці та електродинаміці Максвелла.
Слайд 5Другий постулат
атом може, переходити із одного стаціонарного стану
до іншого. Під час переходу атома зі стаціонарного стану з більшою
енергією до стану з меншою енергією атом випромінює квант енергії, якому відповідає частотаСлайд 7Третій постулат
у стаціонарному стані атома електрон, рухаючись по коловій орбіті,
повинен мати дискретні, квантові значення моменту імпульсу
Слайд 8Третій постулат називається правилом квантування орбіт. Виявилося, що можна одержати
низку дискретних розділених стаціонарних станів тільки за того, припущення, що
момент імпульсу електрона квантується. Звідси дістаємо вираз для радіусів орбіт
Слайд 11Недоліки теорії Бора:
1. Внутрішня суперечливість, непослідовність
(поєднання класичної фізики та квантово-механічних постулатів).
2. Ніяк не пояснювалося
відмінність інтенсивностей спектральних ліній випромінювання, тобто не було пояснення тому, що деякі енергетичні переходи виявляються більш вірогідними, ніж інші. 3. Не дозволяла створити теоретичні моделі більш складних атомних систем, наприклад, гелію всього з двома електронами в атомі.
Теорія Бора була замінена послідовної квантової теорії, що враховує хвильові властивості мікрочастинок, що отримала назву квантова (хвильова) механіка.
Слайд 13Спектральним аналізом називається метод вивчення хімічного складу речовини, заснований на
дослідженні його спектрів.
Слайд 14Найбільш прості спектральні прилади — призма та дифракційна решітка. Більш
точні — спектроскоп і спектрограф.
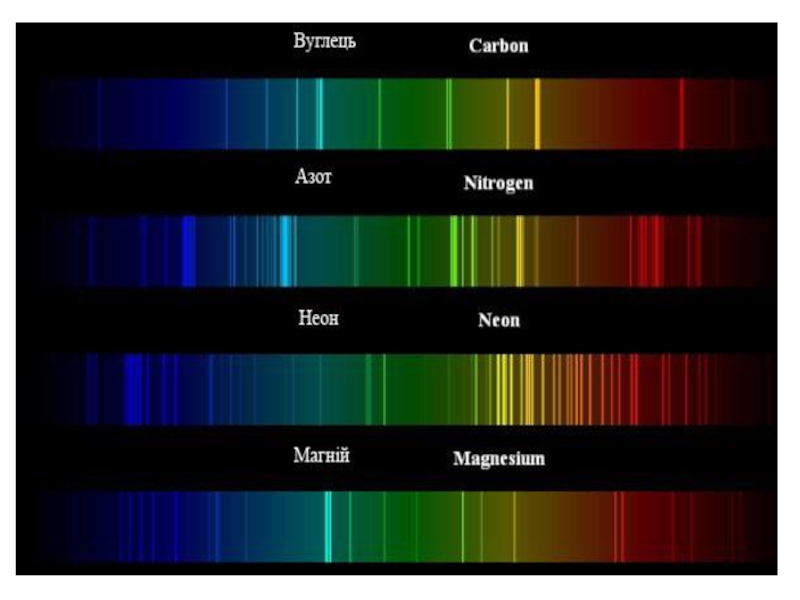
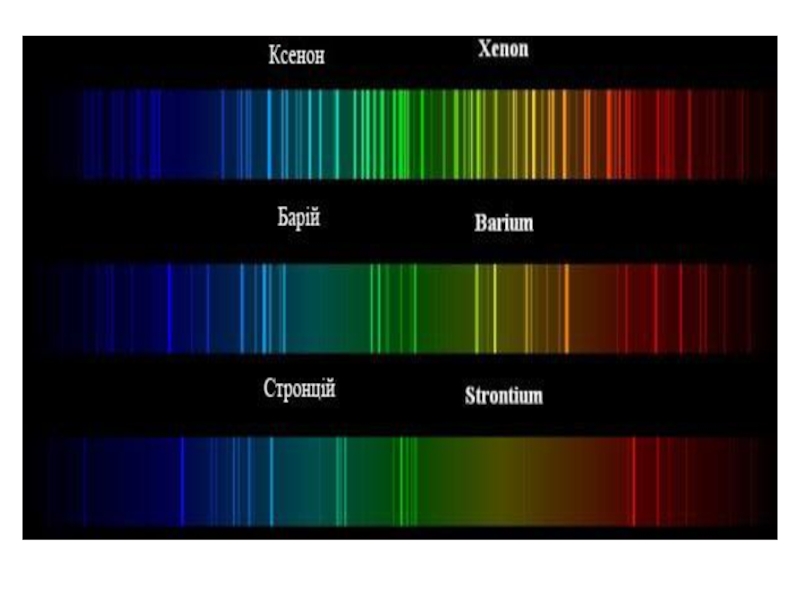
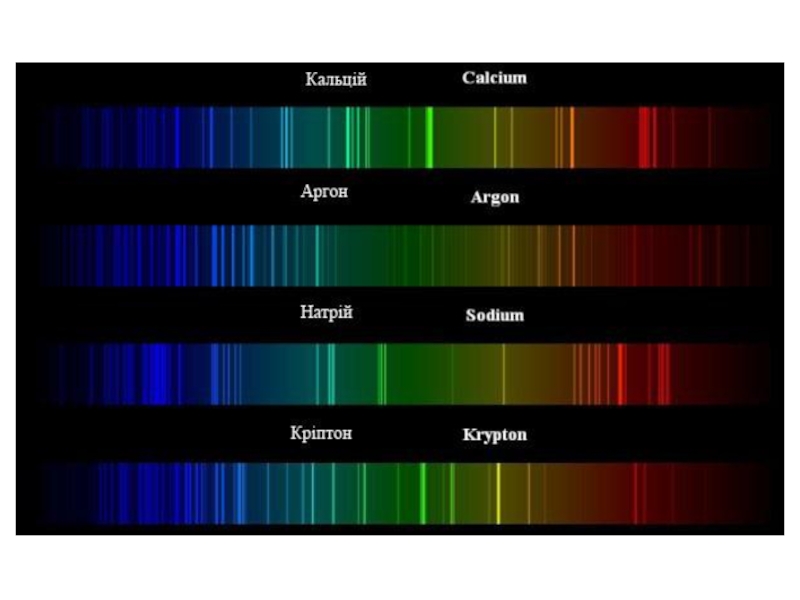
Слайд 15У 1860 році німецькі вчені Г. Кірхгоф і Р. Бунзен,
вивчаючи спектри металів, установили такі факти:
кожний метал мас свій спектр;
спектр
кожного металу суворо постійний;введення в полум'я пальника будь-якої солі одного й того самого металу завжди приводить до появи однакового спектра;
у разі внесення в полум'я суміші солей декількох металів у спектрі одночасно з'являються всі їхні лінії;
яскравість спектральних ліній залежить від концентрації елемента в даній речовині.
Слайд 16Спектр — послідовність монохроматичних випромінювань,
кожному з яких відповідає певна
довжина хвиліелектромагнітного коливання
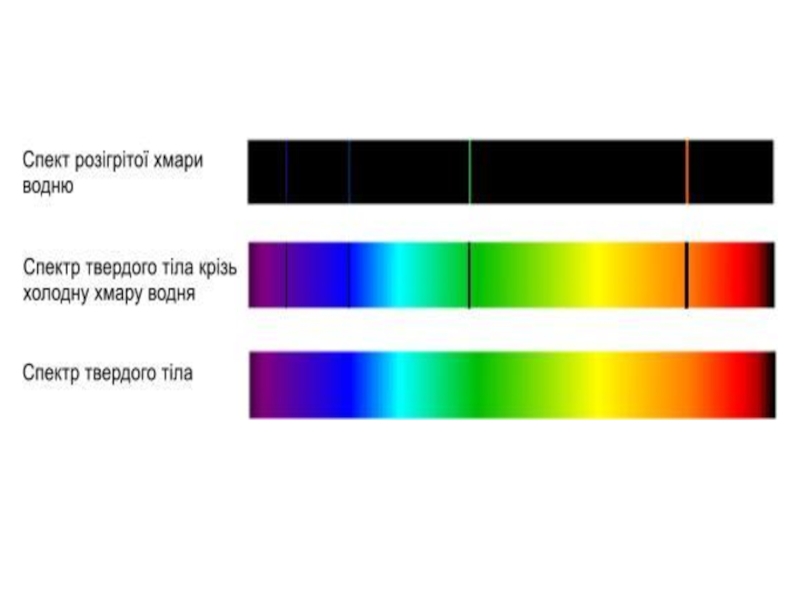
Безперервні (або суцільні) спектри дають тіла,
що перебувають у твердому або рідкому стані,
а також сильно стиснені гази. Для одержання
безперервного спектра потрібно нагріти тіло до
високої температури. (плазма)
390—440 – фіолетовий
440—480 - синій
480—510 – блакитний
510—550 – зелений
550—575 - жовто-зелений
575—585 - жовтий
585—620 – жовтогарячий
630—770 – червоний
Слайд 17Лінійчатий спектр випромінювання - водень
Лінійчаті спектри дають всі речовини в
газоподібному
атомарному (але не молекулярному) стані.
Ізольовані атоми хімічного елемента
випромінюютьстрого певні довжини хвиль.