Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Cr Mo W
Содержание
- 1. Cr Mo W
- 2. Слайд 2
- 3. FeO·Cr2O3 – хроміт (хромистий залізняк)PbCrO4 - крокоїтMoS2
- 4. Добування: FeO·Cr2O3+ 4C → Fe +
- 5. Cr2O3 + 2Al → 2Cr + Al2O3
- 6. СаWO4 + Na2CO3 → CaCO3 + Na2WO4
- 7. Mo і W отримують у вигляді порошків,
- 8. Cr
- 9. Cr + 2HCl
- 10. W + HF +HNO3 → H2[WF8] +
- 11. Cr + O2 → Cr2O3
- 12. Cr +2 Сполуки Cr(ІІ) в
- 13. Cr +3
- 14. Cr2O3 – амфотерний Cr2O3 +
- 15. Солі Cr(IІI) існують у водних розчинах у
- 16. Отримати безводні солі Cr(ІІІ) зневодненням гідратів неможливо
- 17. У розчині солі Cr(ІІІ) гідролізують [Cr(H2O)6]3++H2O
- 18. Cr3+ + 3OH-→ Cr(OH)3↓[Cr(H2O)6]3++3OH-→[Cr(OH)3(H2O)3]+3H2O
- 19. Cr(OH)3 має амфотерні властивості Cr(OH)3
- 20. Під дією сильних окисників Cr +3
- 21. Cr2O3 + 3KNO3 + 4KOH → 2K2CrO4
- 22. CrO4 +
- 23. Слайд 23
- 24. xCrO3·H2O
- 25. Cr +6 – сильний окисник Cr2O7
- 26. Взаємодія Cl- і Cr2O7 залежить від умов
- 27. CrO3 + 2HCl → CrO2Cl2 + H2O
- 28. Порівняння властивостей сполук Cr, Mo,
- 29. CrO3
- 30. MoO3 + 2NaOH → Na2MoO4 + H2O
- 31. H2EO4 мають амфотерні властивості H2MoO4
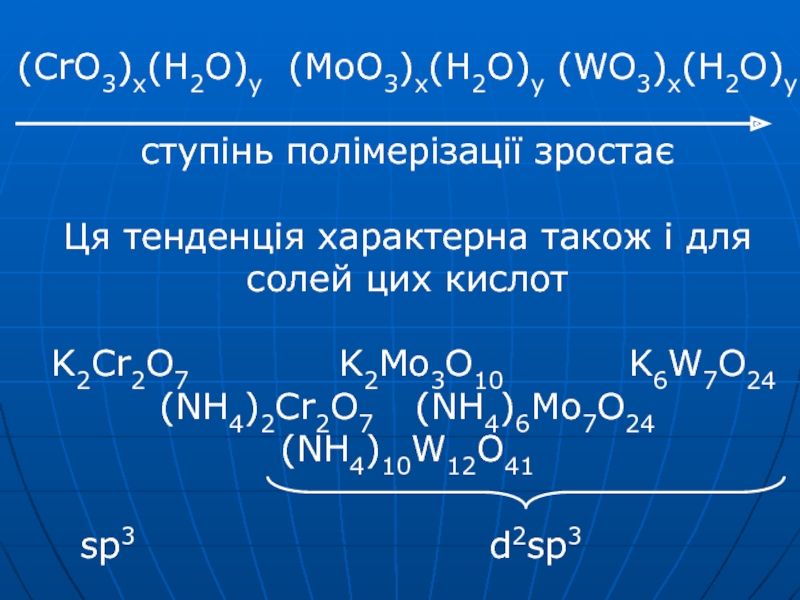
- 32. (СrO3)x(H2O)y (MoO3)x(H2O)y (WO3)x(H2O)y ступінь полімерізації
- 33. (NH4)6Mo7O24 → 7MoO3 + 6NH3 + 3H2O
- 34. Застосування Cталі, що не іржавіють містять
- 35. Хромування деталейЕлектроліз СrO3 в H2SO4
- 36. Mo, W надзвичайно підвищують твердість і міцність
- 37. Електрична лампа1 – нитка розжарювання із
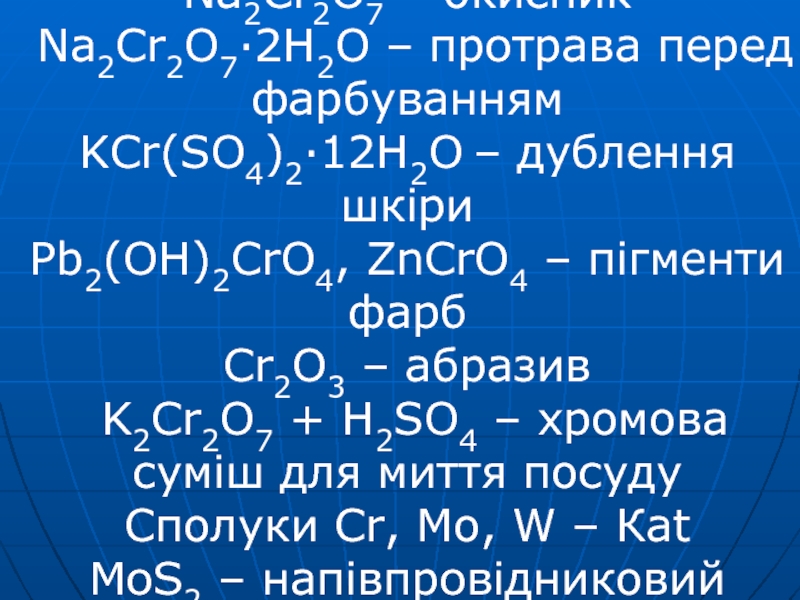
- 38. Na2Cr2O7 – окисник Na2Cr2O7·2H2O – протрава
- 39. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3FeO·Cr2O3 – хроміт
(хромистий залізняк)
PbCrO4 - крокоїт
MoS2 – молібденіт
Мо
– в поліметалічних рудах
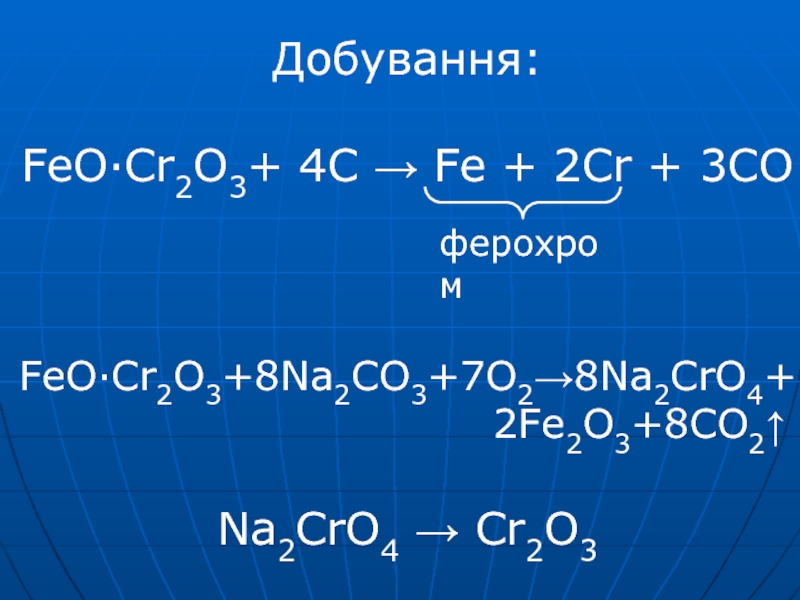
Слайд 4Добування: FeO·Cr2O3+ 4C → Fe + 2Cr + 3CO
FeO·Cr2O3+8Na2CO3+7O2→8Na2CrO4+ 2Fe2O3+8CO2↑ Na2CrO4 → Cr2O3
ферохром
Слайд 5Cr2O3 + 2Al → 2Cr + Al2O3 2Cr2O3 +3Si + 3CаO
→ 4Cr +3CaSiO3 2MoS2 +7O2 → 2MoO3 + 4SO2 MoO3 попередньо очищують
MoO3 + 3H2 → Mo + 3H2OСлайд 6СаWO4 + Na2CO3 → CaCO3 + Na2WO4 4FeWO4 + 4Na2CO3 +
O2 → 4Na2WO4
+ 2Fe2O3 + 4CO2 Na2WO4 → WO3 WO3 + 3H2 → W + 3H2OСлайд 7Mo і W отримують у вигляді порошків, потім їх переробляють
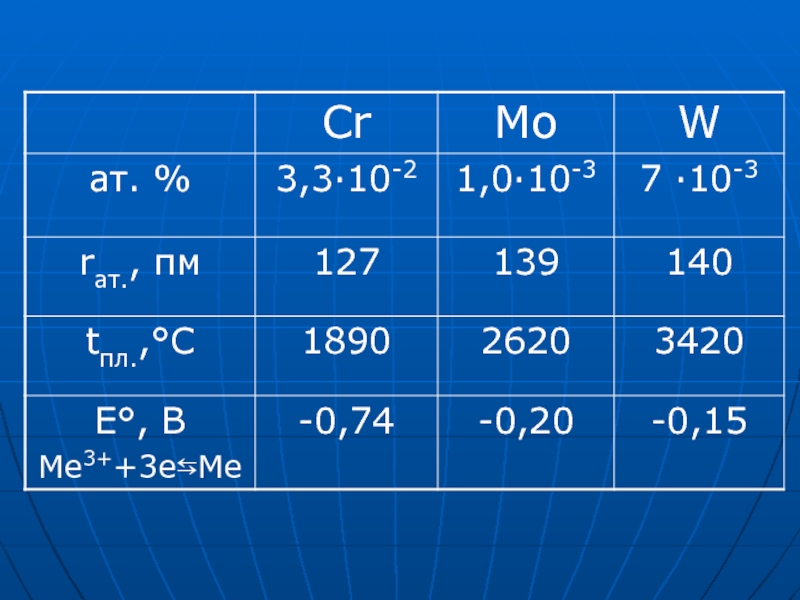
методами порошкової металургії Cr, Mo, W – сріблясто-білі метали, тверді,
тугоплавкі Cr, Mo, W мають високу корозійну стійкість через утворення на їх поверхні інертних оксидних плівокСлайд 8Cr
Mo W 3d54s1
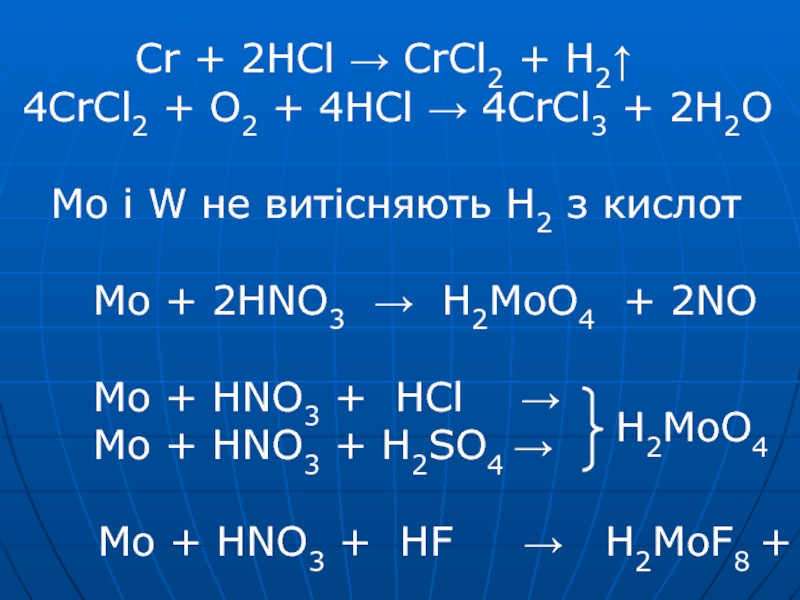
4d55s1 5d46s2 хімічна активність зменшується (+2), +3, +6 +6 +6 Cr має значення Е0 між Zn і Fe Азотною кислотою пасивується Розчиняється в HCl і розведеній H2SO4Слайд 9 Cr + 2HCl → CrCl2 +
H2↑ 4CrCl2 + O2 + 4HCl → 4CrCl3 + 2H2O Mo
і W не витісняють Н2 з кислот Mo + 2HNO3 → H2MoO4 + 2NO Mo + HNO3 + HCl → Mo + HNO3 + H2SO4 → Mo + HNO3 + HF → H2MoF8 +H2MoO4
Слайд 10W + HF +HNO3 → H2[WF8] + ... 2Mе
+ 4KOH + 3O2 → 2K2MеO4 + 2H2O
Me+3KNO3+Na2CO3→Na2MeO4+3KNO2+CO2
Слайд 11Cr + O2 → Cr2O3
Mo(W) + O2 → MeO3 Cr, Mo, W реагують з
галогенами З N, C, Si, B ці метали утворюють сполуки нестехіометричного складу з металічним зв’язком, дуже тверді, тугоплавкі, хімічно інертніСлайд 12Cr +2 Сполуки Cr(ІІ) в звичайних умовах не існують CrO,
Cr(OH)2 мають основні властивості, дуже сильні відновники Cr3+ + 1e ⇆ Cr2+,
E0 = -0,41B 2CrCl2 + 2H2O → 2CrOHCl2 + H2+2
+3
Слайд 13Cr +3 4Cr + 3O2 → 2Cr2O3 (NH4)2Cr2O7
→ N2 + Cr2O3 + 4H2O Cr2O3 – зелений колір, висока
твердість tпл. = 2275°С Cr2O3 + H2O →t
t
Слайд 14Cr2O3 – амфотерний Cr2O3 + 2NaOH → 2NaCrO2 +H2O Cr2O3 + 3K2S2O7
(K2SO4·SO3) → Cr2(SO4)3
+ 3K2SO4t
t
Слайд 15Солі Cr(IІI) існують у водних розчинах у вигляді аквакомплексів, а
кристалізуються разом з кристалізаційною водою CrCl3·6H2O [Cr(H2O)6]Cl3⇆[Cr(H2O)5Cl]Cl2·Н2О⇆
⇆[Cr(H2O)4Cl2]Cl·2Н2Офіолетовий
кристалізується
з холодних
розчинів
жовто-зелений кристалізується з гарячих розчинів
світло-зелений
Слайд 16Отримати безводні солі Cr(ІІІ) зневодненням гідратів неможливо 2CrCl3·6H2O → Cr2O3 +
6HCl + 3H2O
Cr2O3 + 3C + 3Cl2 →2CrCl3 + 3CO
t
Слайд 17У розчині солі Cr(ІІІ) гідролізують [Cr(H2O)6]3++H2O ⇆ [CrOH(H2O)5]2+ + H3O+ Cr(ІІІ)
утворює галуни XCr(SO4)2·12H2O, де X – іони лужних металів або іон
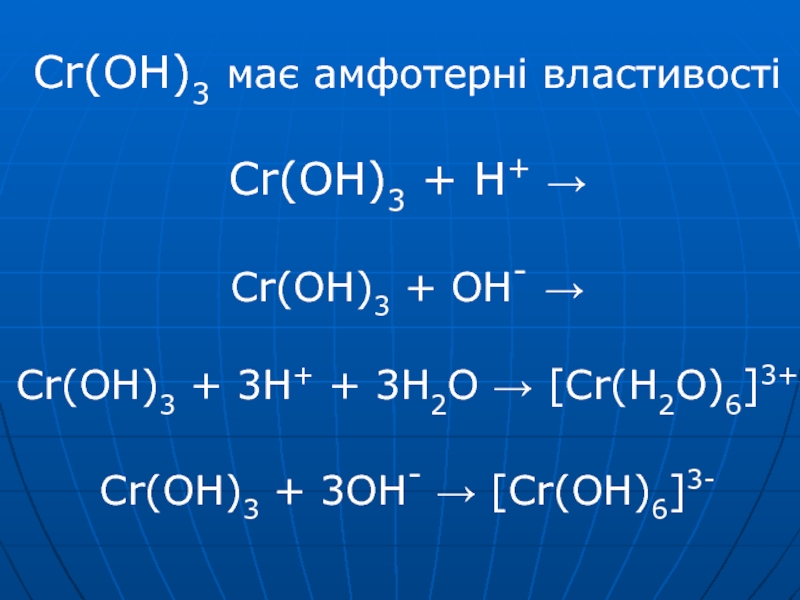
амонію Cr(ІІІ) утворює чисельні комплекси [Cr(NH3)6]Cl3 [CrEn3]Cl3 K3[Cr(CN)6]Слайд 19Cr(OH)3 має амфотерні властивості Cr(OH)3 + H+ → Cr(OH)3 + OH-
→ Cr(OH)3 + 3H+ + 3H2O → [Cr(H2O)6]3+ Cr(OH)3 + 3OH- →
[Cr(OH)6]3-Слайд 20Під дією сильних окисників Cr +3 → Cr +6 2Cr2O3+ 4Na2CO3+ 3O2→4Na2CrO4+
4CO2 2K3[Cr(OH)6] + 3Br2 + 4KOH → 2K2CrO4 +
6KBr + 8H2O 2Cr(NO3)3 + 3K2S2O8 + 7H2O → H2Cr2O7 + 3K2SO4 + 3H2SO4 + 6HNO3Слайд 21Cr2O3 + 3KNO3 + 4KOH → 2K2CrO4 +
+ 3KNO2 + 2H2O Cr2(SO4)3 + 3H2O2 + 10KOH → → 2K2CrO4 + 3K2SO4 + 8H2O
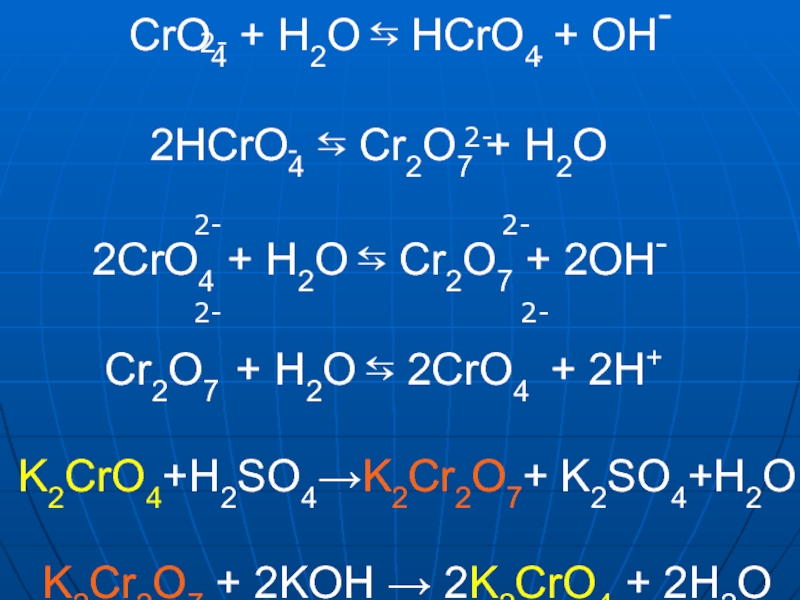
Слайд 22 CrO4 + H2O ⇆ HCrO4
+ OH-
2HCrO4 ⇆ Cr2O7 + H2O 2CrO4 + H2O ⇆ Cr2O7 + 2OH- Cr2O7 + H2O ⇆ 2CrO4 + 2H+ K2CrO4+H2SO4→K2Cr2O7+ K2SO4+H2O K2Cr2O7 + 2KOH → 2K2CrO4 + 2H2O2-
-
-
2-
2-
2-
2-
2-
Слайд 23
Cr +6 CrO3
– хромовий ангідрид K2Cr2O7 + H2SO4 → H2Cr2O7 + K2SO4 H2Cr2O7 2CrO3 K2Cr2O7 + H2SO4(конц.) → 2CrO3 + K2SO4 + H2O CrO3 – дуже сильний окисник 4CrO3 → 2Cr2O3 + 3O2H2SO4
-H2O
Червоні голчасті
кристали
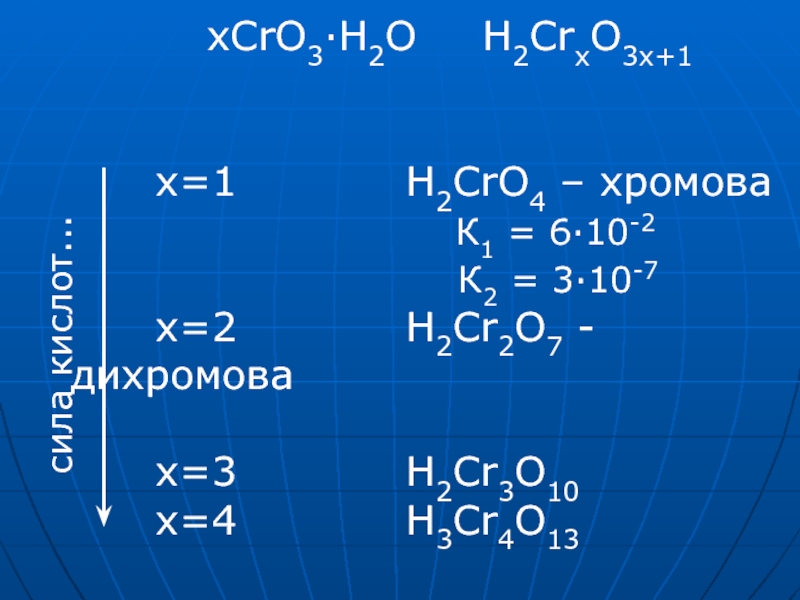
Слайд 24 xCrO3·H2O
H2CrxO3x+1 x=1
H2CrO4 – хромова К1 = 6·10-2 К2 = 3·10-7 x=2 H2Cr2O7 - дихромова x=3 H2Cr3O10 x=4 H3Cr4O13cила кислот...
Слайд 25Cr +6 – сильний окисник Cr2O7 + 14H+ + 6e ⇆
2Cr + 7H2O Е0 = 1,33 B Окиснює Cl-, Br-, J-,
H2S, Fe2+ K2Cr2O7 + відновник + H2SO4 →2-
3+
Слайд 26Взаємодія Cl- і Cr2O7 залежить від умов На холоді K2Cr2O7 +
2HCl → 2KCrO3Cl + H2O При нагріванні K2Cr2O7 + 6HCl →
2CrO2Cl2 + 2KCl + 3H2O K2Cr2O7+14HCl→2CrCl3+3Cl2+2KCl+7H2O2-
Слайд 27CrO3 + 2HCl → CrO2Cl2 + H2O CrO2Cl2 – хлористий
хроміл
диоксохлорид хрому (VІ)
2CrO2Cl2 + 3H2O → H2Cr2O7 + 4HCl
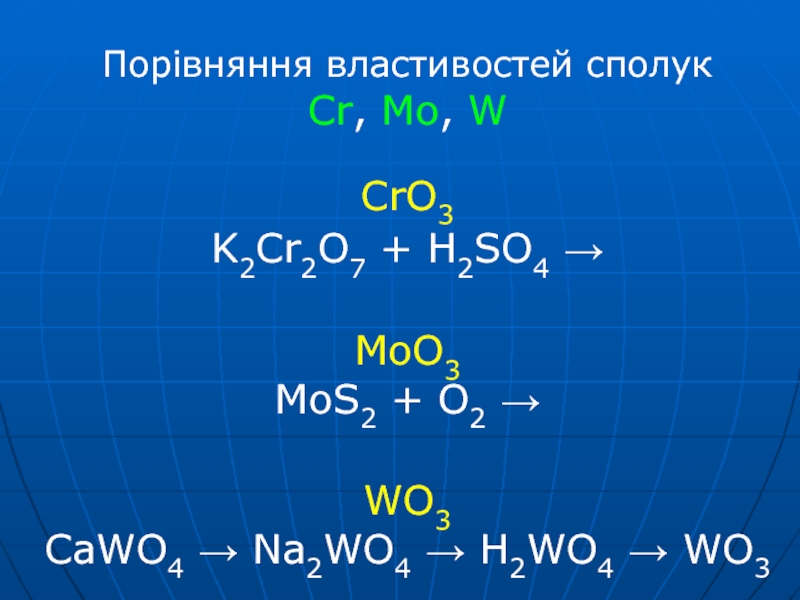
Слайд 28 Порівняння властивостей сполук Cr, Mo, W CrO3 K2Cr2O7 + H2SO4 → MoO3 MoS2
+ O2 →
WO3
CaWO4 → Na2WO4 → H2WO4 → WO3
Слайд 29CrO3
MoO3
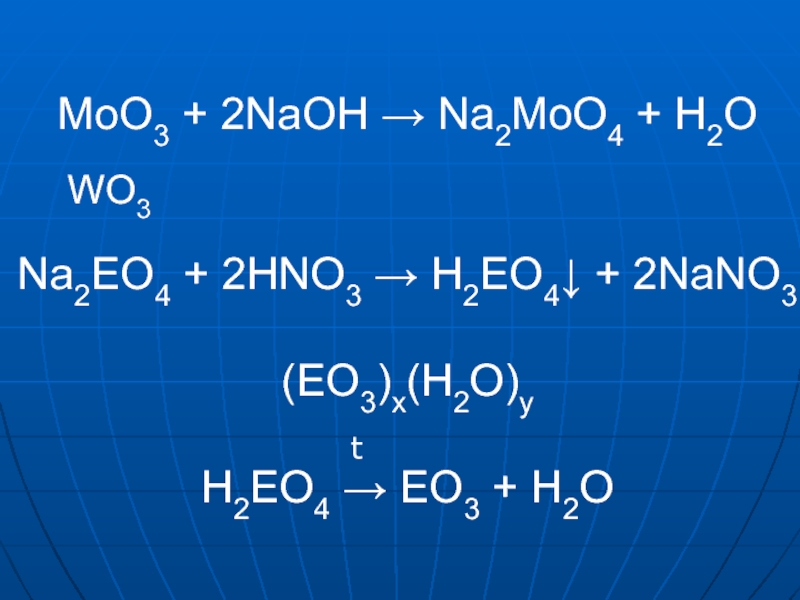
WO3 62%(15°C) 0,4г/л (20°C) 0,02 г/л (20°C) збільшується стійкість зменшується розчинніть зменшуються кислотні властивості зменшуються окисні властивостіСлайд 30MoO3 + 2NaOH → Na2MoO4 + H2O Na2EO4 + 2HNO3
→ H2EO4↓ + 2NaNO3
(EO3)x(H2O)y
H2EO4 → EO3 + H2O
WO3
t
Слайд 31H2EO4 мають амфотерні властивості H2MoO4 + 2NaOH → Na2MoO4 +
2H2O H2MoO4 + 2HCl → MoO2Cl2 + 2H2O H2WO4 розчиняється в
більш концентрованих лугах та кислотах Mo(W)O2Cl2+H2O → H2Mo(W)O4+2HClСлайд 32(СrO3)x(H2O)y (MoO3)x(H2O)y (WO3)x(H2O)y ступінь полімерізації зростає Ця тенденція характерна також і
для солей цих кислот K2Cr2O7
K2Mo3O10 K6W7O24 (NH4)2Cr2O7 (NH4)6Mo7O24 (NH4)10W12O41sp3
d2sp3
Слайд 33(NH4)6Mo7O24 → 7MoO3 + 6NH3 + 3H2O (NH4)10W12O41 → 12WO3 +
10NH3 + 5H2O (NH4)2EO4 → EO3 + 2NH3 + H2O (NH4)2Cr2O7 →
Cr2O3 + N2 + 4H2Ot
t
t
t






![Cr Mo W W + HF +HNO3 → H2[WF8] + ... 2Mе + W + HF +HNO3 → H2[WF8] + ... 2Mе + 4KOH + 3O2 →](/img/thumbs/b6b2ce726e635f370b5f0048cb3c7c12-800x.jpg)






![Cr Mo W У розчині солі Cr(ІІІ) гідролізують [Cr(H2O)6]3++H2O ⇆ [CrOH(H2O)5]2+ + H3O+ У розчині солі Cr(ІІІ) гідролізують [Cr(H2O)6]3++H2O ⇆ [CrOH(H2O)5]2+ + H3O+ Cr(ІІІ) утворює галуни](/img/thumbs/d00e97c30246150dcca4bfc34332a020-800x.jpg)
![Cr Mo W Cr3+ + 3OH-→ Cr(OH)3↓[Cr(H2O)6]3++3OH-→[Cr(OH)3(H2O)3]+3H2O Cr3+ + 3OH-→ Cr(OH)3↓[Cr(H2O)6]3++3OH-→[Cr(OH)3(H2O)3]+3H2O](/img/thumbs/1d29ad4bc859fd6acff9715c5b03f303-800x.jpg)
![Cr Mo W Під дією сильних окисників Cr +3 → Cr +6 2Cr2O3+ 4Na2CO3+ Під дією сильних окисників Cr +3 → Cr +6 2Cr2O3+ 4Na2CO3+ 3O2→4Na2CrO4+ 4CO2 2K3[Cr(OH)6]](/img/thumbs/d8c8e4e69a42035913305e653ce645e3-800x.jpg)